Na ĆW. 6
(część: Badanie właściwości fizycznych i składu moczu)
obowiązuje:
Znajomość zagadnień zawartych w materiałach „Fizjologia układu wydalniczego” w szczególności:
funkcje układu wydalniczego i nerek
procesy zachodzące w nefronie i kanaliku zbiorczym
skład moczu prawidłowego i krótka charakterystyka składników
składniki patologiczne moczu i przyczyny ich obecności w moczu
zasady wykrywania składników nieorganicznych i organicznych moczu
zasada działania testów paskowych oraz sposób wykonania badania moczu przy ich użyciu
sposób odczytu i interpretacji wyników analizy moczu
właściwości fizyczne moczu prawidłowego i patologicznego
składniki osadu moczu
prawidłowe wartości diurezy dobowej, odczynu, ciężaru właściwego i osmolalności moczu oraz przyczyny zmian tych wartości
znajomość pojęć: nefron, kłębuszek, kanaliki nefronu, kanaliki nerkowe, mocz pierwotny/filtrat, mocz ostateczny, klirens nerkowy, GFR, diureza, anuria, oliguria, poliuria, glukomocz/cukromocz, białkomocz, związki ketonowe, ketonuria, urobilinogen, urobilinogemia, bilirubina
FIZJOLOGIA UKŁADU WYDALNICZEGO
Najważniejszą funkcją układu wydalniczego jest: wydalenie produktów przemiany materii, utrzymywanie i regulowanie bilansu wodno-elektrolitowego oraz równowagi kwasowo-zasadowej organizmu. Funkcjonowanie nerek, jako głównych narządów tego układu, zapewnia utrzymanie prawidłowego składu i objętości płynów ustrojowych (homeostazy) pomimo bardzo zmieniających się warunków, w jakich znajduje się organizm. Homeostaza zależy od właściwego uwodnienia, odpowiedniego stężenia elektrolitów i innych substancji osmotycznie czynnych oraz niezmiennego stężenia jonów wodorowych i jest niezbędnym warunkiem do prawidłowego przebiegu procesów metabolicznych w tkankach.
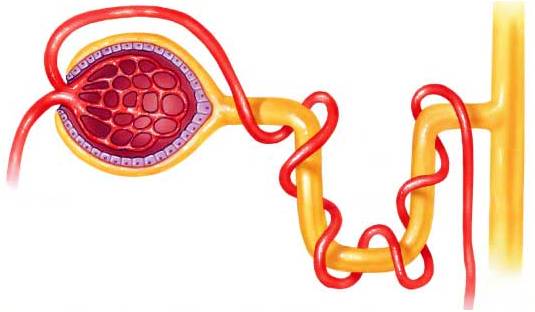
Nerki wytwarzają płyn - mocz ostateczny, w którym usuwane są z organizmu zbędne metabolity oraz nadmiar wody i elektrolitów. Mocz ostateczny powstaje na drodze trzech fizycznych procesów wymiany zachodzących pomiędzy kanalikami nerkowymi a naczyniami krwionośnymi (rycina 1):
filtracji - biernego przesączania ok. 20% osocza przepływającego przez nerkę ze światła naczyń krwionośnych (kapilar) kłębuszka do torebki Bowmana i światła kanalików krętych I rzędu, w wyniku którego powstaje mocz pierwotny, różniący się od osocza nieobecnością białka (globulin)
resorpcji - biernego lub czynnego wchłaniania zwrotnego składników filtratu i płynu kanalikowego (wody, elektrolitów, glukozy, aminokwasów i mocznika) ze światła kanalików nefronu (kanalików I i II rzędu, pętli Henlego) oraz kanalika zbiorczego do światła naczyń krwionośnych (kapilar) otaczających kanaliki nerkowe
sekrecji - biernego lub czynnego transportu substancji (wydzielanych przez ściany kanalika jonów NH4+ i H+ oraz substancji obcych) ze światła naczyń krwionośnych (kapilar) otaczających kanaliki nerkowe do światła kanalików nefronu (kanalików I i II rzędu, pętli Henlego) oraz kanalika zbiorczego.
Do oceny sprawności wydalniczej nerek służą badania czynnościowe o charakterze ilościowym i jakościowym. Wiele z tych prób opiera się na oznaczeniu klirensu nerkowego dla różnych substancji. Klirens nerkowy (wskaźnik oczyszczenia nerkowego) danej substancji jest to objętość osocza, wyrażona w ml, którą nerki w ciągu minuty oczyszczają całkowicie z tego składnika, wydalając go w moczu ostatecznym. Klirens substancji, która uległa przesączeniu, ale nie wchłania się zwrotnie i nie jest wydzielana przez kanaliki, jest równy przesączaniu kłębuszkowemu i wynosi ok. 120 ml/min. Do substancji takich należy egzogenny cukier - inulina lub endogenna kreatynina powstająca z fosfokreatyny mięśni. Substancje, które nie pojawiają się w moczu mają klirens =0, te które ulegają zwrotnemu wchłanianiu - <120 ml/min., a wydzielane dodatkowo przez kanaliki nerkowe - >120 ml/min.
Klirens nerkowy może więc służyć do oznaczenia wielkości przesączania kłębuszkowego (GFR), czyli wielkości filtracji kłębuszkowej, zachodzącej dzięki istnieniu ciśnienia hydrostatycznego krwi w naczyniach włosowatych kłębuszka. Wartość GFR u mężczyzn wynosi 125±15 ml/min/1,75m2 powierzchni ciała, a u kobiet 110±15 ml/min/1,75 m2 powierzchni ciała.
SKŁAD I WŁAŚCIWOŚCI MOCZU
Skład i objętość moczu ostatecznego, powstającego w nerkach w wyniku filtracji, resorpcji i sekrecji, waha się w szerokich granicach. Zależnie od bilansu wodnego różne substancje są wydalane w małej lub dużej ilości wody (mocz hipertoniczny lub hipotoniczny w stosunku do osocza).
Podstawowym badaniem, wstępnie oceniającym stan układu wydalniczego, jest ogólne badanie moczu. W analizie moczu bada się jego:
cechy fizyczne (objętość, barwę, przejrzystość, zapach, odczyn i ciężar właściwy)
skład chemiczny (składniki organiczne i nieorganiczne)
osad (krwinki białe, krwinki czerwone, komórki nabłonka i wałeczki powstające z komórek nabłonka i krwinek, kryształy kwasu moczowego, szczawianów, moczanów, fosforanów, węglanów i siarczanów oraz bakterii i śluzu)
WŁAŚCIWOŚCI FIZYCZNE MOCZU
Dobowa ilość moczu (diureza)
Dobowa diureza u ludzi zdrowych wynosi 1000-1500 ml, co stanowi około 60% przyjętej wody. Kobiety wydalają mniej moczu niż mężczyźni.
Zmniejszenie ilości wydalanego moczu (oliguria - skąpomocz) obserwuje się przy obniżonej podaży płynów, w odwodnieniu organizmu, przy obfitym poceniu się, po biegunkach, w ostrych zapaleniach nerek i w stanach gorączkowych. Całkowite zahamowanie wydalania moczu nazywane jest anurią (bezmoczem).
Zwiększenie ilości wydalanego moczu (poliuria - wielomocz) następuje po wypiciu dużej ilości wody, oraz występuje w cukrzycy, w moczówce prostej i po podaniu środków moczopędnych.
Barwa moczu
Barwa moczu zależy od następujących barwników: urochromu, urobiliny, uroerytryny, kwasu ksanturenowego i porfiryn. Mocz prawidłowy jest jasnożółty, ale może być jasnobursztynowy. Barwa zależy nie tylko od wymienionych barwników, ale i od zagęszczenia moczu (ilości przyjętych płynów), rodzaju pożywienia (betacyjaniny), wydalanych składników patologicznych i przyjmowanych leków. Mocz ciemny może wskazywać na żółtaczkę lub kamicę nerek i pęcherza moczowego.
Przejrzystość moczu
Mocz świeżo oddany powinien być przejrzysty. Po pewnym czasie w moczu pojawia się obłoczkowe zmętnienie pochodzące od niewielkiej ilości białka, śluzu, leukocytów i komórek nabłonkowych. Mocz świeży może być mętny z powodu wytrącenia się różnych soli, obecności bakterii, ropy i tłuszczów. Mocz mętny może wskazywać na stany zapalne dróg moczowych.
Stopień zmętnienia moczu określa się jako: przejrzysty, lekko mętny, mętny, silnie mętny.
Zapach (woń) moczu
Mocz ma swoisty zapach, który zmienia się po spożyciu np. chrzanu, czosnku, szparagów. Woń owocowa jest skutkiem obecności acetonu, gnilna - siarkowodoru (rozkładu ropy). Zapach amoniaku świadczy o rozkładzie moczu, woń kałowa - o zanieczyszczeniu kałem lub pałeczką okrężnicy.
Odczyn moczu (pH)
U ludzi zdrowych, pozostających na przeciętnej diecie mieszanej, odczyn moczu jest lekko kwaśny i wynosi średnio 6,2. Zmiana odczynu związana jest zazwyczaj z dietą i może mieścić się w granicach 4,5-8,2. Do obniżenia pH dochodzi podczas stosowania diety bogatobiałkowej (mięsnej), spożywania dużej ilości potraw zbożowych i w głodzeniu. Zmiana odczynu w kierunku zasadowym może wynikać ze stosowania diety owocowo-warzywnej (jarskiej) oraz może świadczyć o stanach zapalnych i kamicach.
Odczyn kwaśny moczu zależy od zawartości wydalanych w nim wodorofosforanów(V) i kwasów. Kwasowość moczu wzrasta również w przebiegu cukrzycy, gdy ustrój wydala kwasy organiczne (acetooctowy i β-hydroksymasłowy).
Ciężar właściwy (gęstość względna) moczu
Ciężar właściwy moczu zależy od stanu uwodnienia organizmu i jest wprost proporcjonalny do ilości rozpuszczonych składników stałych, a odwrotnie - do ilości wydalonej wody. Gęstość względna moczu może wynosić od 1,001 do 1,035 g/ml, a najczęściej waha się w granicach 1,015 - 1,025 g/ml. Wartość ta wzrasta przy zmniejszaniu się diurezy i może świadczyć o zagęszczeniu moczu. Niższa gęstość względna moczu związana jest ze zwiększoną diurezą i świadczy zazwyczaj o rozcieńczeniu moczu. Wyjątek stanowią: ciężkie uszkodzenie nerek, w którym oligurii towarzyszy niska gęstość względna i cukrzyca, w której poliurii towarzyszy wysoki ciężar właściwy moczu, z powodu dużej zawartości glukozy.
Oznaczanie ciężaru właściwego przeprowadza się najczęściej specjalnym areometrem zwanym urometrem o rozpiętości podziałki od 1,000 do 1,040 g/ml.
Na podstawie ciężaru właściwego moczu, z dużym przybliżeniem można obliczyć jego osmolalność (Uosm), posługując się wzorem:
Uosm = (gęstość względna - 1) x 26 x 1000 [mOsm/l]
Osmolalność moczu świadczy o bieżącym udziale nerek w regulacji gospodarki wodnej organizmu. Osmolalność osocza wynosi 300 mOsm/l. Wyższa od niej osmolalność moczu ostatecznego świadczy o nadmiarze zwrotnie wchłanianej wody (zwiększenie zagęszczenia moczu), a niższa od tej wartości wskazuje na wydalenie dodatkowej ilości wody (zmniejszenie zagęszczenia moczu).
SKŁAD CHEMICZNY MOCZU PRAWIDŁOWEGO
Z moczem ostatecznym wydalane są woda, sole mineralne, kwasy, zasady, substancje toksyczne, produkty przemiany materii, detoksykacji, leki i inne związki.
Składniki chemiczne moczu można podzielić na następujące grupy:
składniki organiczne
związki azotowe
związki nieazotowe
składniki nieorganiczne (sole mineralne)
Prawidłowy skład chemiczny moczu człowieka przedstawia tabela 1.
Tabela 1. Skład chemiczny moczu prawidłowego (g/dobę).
Woda |
1000 - 1500 |
ZWIĄZKI ORGANICZNE NIEAZOTOWE |
|
Substancje stałe |
50 - 70 |
Eterosiarczany |
0,2 -0,3 |
ZWIĄZKI ORGANICZNE AZOTOWE |
Siarka obojętna |
0,2 - 0,4 |
|
Mocznik |
25 - 35 |
SOLE MINERALNE |
|
Kreatynina |
1 - 1,8 |
Chlorki |
6 - 9 |
Kwas moczowy |
0,4 - 1 |
Sód |
3 - 5 |
Amoniak |
0,4 - 1 |
Potas |
1,5 - 3,5 |
Kwas hipurowy |
0,2 - 1 |
Wapń |
0,1 |
Aminokwasy |
0,2 - 0,4 |
Magnez |
0,1 |
Zasady purynowe |
0,01 - 0,06 |
Żelazo |
0,001 |
Indykan |
0,01 - 0,03 |
Fosforany |
1 - 1,5 |
Fenole |
0,1 - 0,2 |
Siarka całkowita |
2 - 3,4 |
Kwas szczawiowy |
0,01 - 0,02 |
Siarczany nieorganiczne |
1,6 - 2,7 |
Składniki organiczne moczu
Spośród substancji organicznych dominującą rolę odgrywają związki azotowe, będące odpowiednikami azotu niebiałkowego krwi. Główną część azotu moczu stanowi azot mocznika (ok. 80-90% przy przeciętnej diecie mieszanej). Ważną pozycję zajmują również: amoniak, kreatynina i kwas moczowy. W moczu występują ponadto niewielkie ilości kwasu hipurowego, różnych aminokwasów oraz innych związków azotowych uwzględnionych w tabeli 1.
Mocznik
Mocznik jest produktem rozpadu białek w organizmie. Jego stężenie w moczu uzależnione jest od zawartości białka w diecie, przemian metabolicznych białka oraz od wydolności nerek i wątroby. Ilość tego związku jest tym większa, im większe jest spożycie białka lub większy katabolizm białek i im gorsza jest wydolność nerek. Obniżenie stężenia mocznika w moczu świadczy o gorszej wydolności wątroby.
Amoniak
Amoniak jest jednym z końcowych produktów przemiany białek. Jest on wytwarzany w nerkach w ilości zależnej od równowagi kwasowo-zasadowej, ale jego wydalana ilość jest bardzo mała ze względu na silne właściwości toksyczne tego związku dla komórek zwierzęcych. U ssaków amoniak zostaje przekształcony w mocznik w wyniku procesów zachodzących w wątrobie (cykl mocznikowy). Część wytworzonego w nerkach amoniaku dostaje się do płynu kanalikowego i po połączeniu z jonami wodorowymi ulega przekształceniu w jony amonowe (NH4+), które są wydalane w moczu. Zwiększenie wydalania jonów amonowych w moczu może świadczyć o kwasicy metabolicznej będącej efektem niewydolności nerek lub zaburzeń metabolizmu węglowodanów i tłuszczów.
Kreatynina
Kreatynina jest bezwodnikiem kreatyny i charakteryzuje się małymi wahaniami w wydalaniu dobowym. Stopień jej wydalania związany jest z wielkością masy mięśniowej organizmu.
Kwas moczowy
Kwas moczowy jest końcowym produktem przemian puryn pokarmowych i kwasów nukleinowych. W moczu występuje w postaci wolnej lub w formie soli (moczanów sodu i potasu w moczu kwaśnym oraz rzadziej moczanów amonu w moczu zasadowym). Zwiększenie ilości wydalanego w moczu kwasu moczowego świadczy o zwiększonym katabolizmie zasad purynowych (np. po chemioterapii nowotworów) lub o zwiększonej biosyntezie kwasu moczowego (np. w cukrzycy). Stany takie mogą sprzyjać powstawaniu kamieni moczanowych.
Do najważniejszych nieazotowych związków organicznych w moczu należą:
glukuronidy - połączenia kwasu glukurunowego ze związkami tj.: fenole, kwasy organiczne, steroidy, niektóre leki, hormony płciowe i bilirubina;
związki siarki - eterosiarczany (związki siarki z fenolem, krezolem i indoksylem, które w postaci wolnej są toksyczne) i siarka obojętna (aminokwasy siarkowe, tauryna, tiocyjaniany i kwas tarocholowy).
Z innych związków organicznych wydalane są nieduże ilości kwasu szczawiowego, mlekowego (którego ilość wzrasta w czasie natężonej pracy), różnych barwników, witamin i hormonów. W prawidłowym moczu w śladowych ilościach występują również glukoza oraz ciała ketonowe. Ilości te jednak są tak małe, że nie dają się wykryć stosowanymi metodami, wobec tego mówi się, że glukozy i związków ketonowych nie ma w moczu prawidłowym.
Składniki nieorganiczne moczu
Związki nieorganiczne występują w moczu jako jony. Z kationów ustrój wydala najwięcej jonów sodowych i potasowych, w mniejszej ilości - jony wapnia i magnezu, a z anionów - jony chlorkowe, siarczany, fosforany(V), a w moczu zasadowym również wodorowęglany.
SKŁAD MOCZU PATOLOGICZNEGO
Oprócz badania właściwości fizycznych i składu chemicznego moczu, opisanego powyżej, wykrywa się w nim następujące składniki: białko i glukozę, związki ketonowe, krew (erytrocyty i hemoglobinę), barwniki żółciowe (bilirubinę i urobilinogen) oraz azotyny i leukocyty.
Białko
Mocz prawidłowy może zawierać tylko znikome ilości białka (do kilkudziesięciu mg / dobę) ponieważ globuliny nie podlegają filtracji, a przefiltrowane albuminy są usuwane z płynu kanalikowego w procesie resorpcji zwrotnej. Te małe ilości białka nie dają wykryć się stosowanymi metodami laboratoryjnymi i dlatego mówi się, że mocz prawidłowy nie zawiera białka. W stanach patologicznych ilość białka wydalanego z moczem zwiększa się (białkomocz patologiczny) i może dochodzić do kilkudziesięciu g / dobę.
Białkomocz patologiczny (proteinuria) może być pochodzenia nerkowego i pozanerkowego (np. z dróg moczowych). Największy białkomocz występuje w nerczycy. Białkomocz może wskazywać również na kamicę nerek i stan zapalny. Śladowe ilości białka w moczu pojawiają się w czasie gorączki i podczas intensywnego wysiłku fizycznego.
Mocz zawierający składniki komórkowe (nabłonki, leukocyty lub bakterie) może dawać dodatnie odczyny na białko. W związku z tym mocz badany na obecność białka musi być przezroczysty, a ponadto mieć odczyn kwaśny.
Glukoza
Mocz prawidłowy zawiera tylko śladowe ilości cukrów (glukozy), niewykrywalne zwykłymi metodami chemicznymi. W warunkach prawidłowych cała ilość glukozy moczu pierwotnego jest wchłaniana zwrotnie w kanalikach nerkowych. W stanach patologicznych dochodzi do utraty glukozy przez nerki (cukromocz / glukomocz / glikozuria). Glukoza może być wydalana w moczu po przekroczeniu progu nerkowego, który wynosi 180 mg/100ml (wydalenie nadmiaru niewchłonietej glukozy) oraz przy upośledzonym wchłanianiu zwrotnym, kiedy zawartość glukozy we krwi jest mniejsza lub prawidłowa.
Duża utrata glukozy przez nerki świadczy o cukrzycy lub złym jej prowadzeniu. W zaawansowanej cukrzycy ilość glukozy wydalana z moczem może sięgać kilkudziesięciu g / dobę.
Związki ketonowe
Do grupy związków ketonowych zaliczamy: kwas acetooctowy, aceton i kwas β-hydroksymasłowy. Wśród nich centralnym związkiem jest kwas acetooctowy, który w procesie dekarboksylacji przechodzi w aceton, a przez uwodornienie - w kwas β-hydroksymasłowy. Normalnie ilość związków ketonowych w ustroju jest niewielka. Znacznemu zwiększeniu ulega głównie w cukrzycy, podczas głodzenia i podczas stosowania diety wysokotłuszczowej. Wykrywalne ilości związków ketonowych mogą pojawić się w moczu w okresie ciąży lub podczas wysiłku fizycznego.
Produkcja kwasu acetooctowego w wątrobie zwiększa się wtedy, gdy dochodzi do upośledzenia spalania lub syntezy kwasów tłuszczowych. W cukrzycy zaburzenia gospodarki węglowodanowej powodują zaburzenia w przemianie tłuszczowej, prowadzące do powstania związków ketonowych. Wydalanie związków ketonowych z moczem w cukrzycy jest bardzo duże (ketonuria) - nawet do kilkudziesięciu g / dobę.
Krew
W warunkach prawidłowych w osadzie moczu można znaleźć pojedyncze erytrocyty (1-3 w polu widzenia, w średnim powiększeniu mikroskopu). Przyczyną obecności krwi w moczu są choroby nerek (np. kamice, nowotwory), układu moczowo-płciowego, niektóre choroby krwi i zatrucia. Mikroskopowy krwiomocz u osób starszych jest wynikiem miażdżycy naczyń nerkowych, a u młodych może być następstwem wysiłku fizycznego. Pojawienie się krwi w moczu może świadczyć nie tylko o uszkodzeniu nerek, ale również dróg moczowych. U kobiet należy brać pod uwagę możliwość obecności w moczu krwi menstruacyjnej.
Małe ilości krwi dają lekkie zmętnienie i zabarwienie moczu, natomiast duże ilości barwią go na czerwono. W moczu starym może powstać zabarwienie ciemnobrunatne wskutek powstającej methemoglobiny. Mocz zawierający hemoglobinę (hemoglobinuria) ma barwę czerwoną, a w jego osadzie nie stwierdza się krwinek czerwonych. W przypadku dużych krwawień pojawienie się hemoglobiny w mocze może być spowodowane jej uwolnieniem z krwinek czerwonych (hemolizą). Natomiast mocz zawierający erytrocyty (hematuria) jest czerwony i mętny, a po odwirowaniu staje się klarowny i ma barwę moczu normalnego oraz w osadzie badaniem mikroskopowym stwierdza się obecność krwinek.
Występowanie hemoglobiny w moczu jest najczęściej skutkiem zwiększonego jej stężenia w osoczu. Hemoglobina łatwo ulega filtracji w kłębuszkach nerkowych, a następnie podlega wtórnej resorpcji w kanalikach nefronu i w moczu ostatecznym pojawia się wówczas, gdy jej stężenie w osoczu przekroczy wartość progową.
Barwniki żółciowe
Bilirubina
Bilirubina jest podstawowym barwnikiem żółciowym. Powstaje ona w szpiku kostnym czerwonym, śledzionie i wątrobie w wyniku fizjologicznego rozpadu krwinek czerwonych. W osoczu bilirubina wiąże się z białkami osocza i w formie nierozpuszczalnej w wodzie (bilirubina pośrednia) transportowana jest do wątroby, gdzie staje się rozpuszczalna (bilirubina bezpośrednia).
W moczu prawidłowym bilirubina nie występuje. Natomiast w stanach patologicznych (żółtaczce miąższowej lub mechanicznej), kiedy stężenie bilirubiny bezpośredniej we krwi znacznie zwiększa się, towarzyszy temu pojawienie się bilirubiny w moczu. W żółtaczce hemolitycznej mimo dużego stężenia bilirubiny pośredniej, nie przechodzi ona do moczu, jeżeli nie ma uszkodzenia nerek. Bilirubina barwi mocz na kolor ciemnobrunatny lub żółtozielony oraz pianę na kolor żółty. Bilirubina bardzo łatwo utlenia się do zielonej biliwerdyny, co wykorzystuje się w próbach wykrywania tego barwnika żółciowego.
Urobilinogen
Urobilinogen jest barwnikiem żółciowym powstającym z bilirubiny. Po dostaniu się bilirubiny wraz z żółcią do jelita następuje jej przemiana do urobilinogenu z udziałem flory bakteryjnej. Powstały urobilinogen może utlenić się do pomarańczowej urobiliny.
W prawidłowym moczu zarówno urobilinogen, jak i urobilina występują w małej ilości. Barwniki te zostają częściowo wchłonięte do krwi i wracają do wątroby, gdzie ulegają dalszym przemianom. Niewchłonięte związki są wydalane z kałem. W zdrowym organizmie tylko nieznaczna część urobilinogenu nie ulega przemianie i jest wydalona z moczem, będąc przyczyną fizjologicznej urobilinogemii.
Badanie moczu na zawartość urobilinogenu jest bardzo ważne, ponieważ zwiększenie jego zawartości jest charakterystyczne dla wielu schorzeń i pozwala stwierdzić niewielkie zmiany w czynności wątroby. Nieznaczne uszkodzenie tkanki wątrobowej lub tylko silne obciążenie czynnościowe wątroby hamuje zamianę urobilinogenu w bilirubinę, co prowadzi do nagromadzenia się urobilinogenu we krwi i wydalenia go z moczem w zwiększonych ilościach. Podobnie jest, gdy wzrasta stężenie bilirubiny (np. w żółtaczce hemolitycznej) i wątroba nie może przerobić całości wchłoniętego urobilinogenu. Wzmożone wydalanie urobilinogenu w chorobach zakaźnych powodowane jest zwykle upośledzeniem czynności wątroby.
Azotyny
W moczu prawidłowym nie wykrywa się azotynów. Azotyny wytwarzane są w moczu przez bakterie, głównie Gram ujemne z azotanów pochodzenia pokarmowego. Wykrycie azotynów w moczu świadczy o bakteryjnym zapaleniu dróg moczowych. Infekcje dróg moczowych powodowane są najczęściej przez mikroorganizmy, które zawierają reduktazę zdolną do redukcji azotanów do azotynów.
Leukocyty
W prawidłowym moczu nie wykrywa się zazwyczaj leukocytów, chociaż wydalane są z moczem w ilości od 3 do 3000 na 1 mililitr. Odpowiada to kilku (0-5) krwinkom białym w polu widzenia, w średnim powiększeniu mikroskopu. W stanach chorobowych liczba leukocytów może ulegać bardzo znacznemu zwiększeniu, ale nie zawsze jest proporcjonalna do ciężkości choroby. Obecność leukocytów w moczu świadczy zazwyczaj o bakteryjnym zapaleniu dróg moczowych.
ANALIZA MOCZU LUDZKIEGO
Celem ćwiczenia będzie zbadanie właściwości fizycznych oraz składu moczu, ocena działania / stanu układu wydalniczego oraz określenie prawidłowości przebiegu procesów metabolicznych u badanych osób.
Do badania będzie używany mocz pobrany wcześniej do czystych i suchych pojemników, po które prosimy zgłaszać się do pokoju 2101. Jeżeli badanie nie będzie przeprowadzone w ciągu 1 godziny od pobrania moczu, należy go szybko schłodzić do temperatury 2-8° C (w lodówce na sali ćwiczeń 2088). Próbki takie przed oznaczeniem należy doprowadzić do temperatury pokojowej i dobrze wymieszać.
Zadania do wykonania:
1. BADANIE WŁAŚCIWOŚCI FIZYCZNYCH MOCZU
Ćwiczenia będą polegały na określeniu barwy i przejrzystości moczu oraz pomiarze, przy użyciu testu paskowego (Combur10-Test®M) odczynu i ciężaru właściwego moczu badanej osoby
Zasada oznaczania odczynu moczu bazuje na metodzie podwójnego wskaźnika pH, w której reagenty zmieniają wyraźnie barwę powyżej odpowiedniego pH w zakresie 5 - 9.
Zasada oznaczania ciężaru właściwego bazuje na widocznej, w postaci zmiany zabarwienia, zmianie stałej dysocjacji określonych polielektrolitów w zależności od stężenia jonów.
Dokładną instrukcję do wykonania oznaczeń z użyciem testów paskowych zamieszczono w punkcie 2 materiałów.
Na podstawie zmierzonych wartości ciężaru właściwego należy obliczyć osmolalność moczu korzystając ze wzoru podanego na str. 4 materiałów.
2. BADANIE SKŁADU CHEMICZNEGO I OBECNOŚCI KRWINEK W MOCZU
Ćwiczenie będzie polegało na:
analitycznym oznaczeniu obecności składników nieorganicznych (Cl- i PO43-) i organicznych (kwas moczowy, kreatynina)
wykonaniu przy użyciu testu paskowego (Combur10-Test®M), półilościowych i jakościowych oznaczeń w moczu osoby badanej: leukocytów, azotynów, białka, glukozy, związków ketonowych, urobilinogenu, bilirubiny i krwi (erytrocytów i hemoglobiny)
Zasada wykrywania składników nieorganicznych:
Cl-
Zasada metody: strącenie chlorków roztworem AgNO3 i rozpuszczenie wytrąconego AgNO3 w amoniaku z wytworzeniem kompleksowego jonu Ag(NH3)2+
Wykonanie: do 2 ml moczu zakwaszonego HNO3 (0,5 ml) dodać 0,5 ml 0,1M roztworu AgNO3. Wytrącony osad rozpuścić po dodaniu roztworu amoniaku (NH4OH)
PO43-
Zasada metody: reakcja z molibdenianem (VI) amonu w środowisku kwaśnym z wytworzeniem żółtego osadu lub zabarwienia pochodzącego od fosforomolibdenianu amonowego
Wykonanie: do 3 ml moczu dodać 1 ml stężonego HNO3 i 3 ml 5% roztworu molibdenianu amonu. Ogrzewać przez kilka minut.
Zasada wykrywania składników organicznych:
Kwas moczowy
Zasada metody: kwas moczowy redukuje kwas fosforowolframowy z wytworzeniem błękitu wolframowego - mieszaniny tlenków wolframowych oraz alantoiny.
Wykonanie: do 2 ml moczu dodać 0,5 ml roztworu kwasu fosforowolframowego, a następnie ok.1 ml 10% roztworu NaOH (do odczynu zasadowego)
Kreatynina
Zasada metody: reakcja Jaffe'go - redukcja przez kreatyninę (w środowisku zasadowym) kwasu pikrynowego do pomarańczowo zabarwionego kwasu pikraminowego
Wykonanie: do 1 ml moczu dodać 2 ml nasyconego roztworu kwasu pikrynowego i 0,5 ml 10% roztworu NaOH
Testy paskowe
Zasada działania testów paskowych polega na swoistej reakcji określonego (badanego) składnika chemicznego moczu z substancjami chemicznymi (wskaźnikami) znajdującymi się na odpowiednim polu paska testowego. W wyniku zachodzących reakcji chemicznych dochodzi do zmiany zabarwienia pól testowych paska w zależności od obecności / ilości danego składnika w moczu.
Podczas wykonywania badania należy postępować w następujący sposób (rycina 2):
pobrać jednorazową pipetką 10 ml moczu do szklanej probówki (1)
z pojemnika wyjąć tylko jeden pasek testowy (2), a po jego wyjęciu szczelnie zamknąć pojemnik (3)
zanurzyć całkowicie pasek testowy w moczu (4) i natychmiast go wyjąć, aby nie doszło do rozpuszczenia reagentów (5)
usunąć nadmiar moczu z krawędzi wyjętego paska (6)
dokonać odczytu uzyskanych wyników porównując zabarwienie pól na pasku ze skalą barwną umieszczoną na etykiecie pojemnika z paskami, uwzględniając odpowiadające poszczególnym parametrom czasy czytania - leukocyty po 3 min., pozostałe parametry po 1-2 min. (7).
Uzyskane wyniki oznaczenia jakościowego należy odczytać jako:
prawidłowe
ujemne (negatywne): „-” - jeżeli nie wykryto obecności danego składnika w moczu
w normie: „n” - jeżeli wykryto obecność danego składnika w moczu i jego ilość mieści się w zakresie wartości prawidłowych
nieprawidłowe (pozytywne / dodatnie): w skali 1+ - 4+, gdzie: 1+ - ilość niewielka; 2+ - ilość umiarkowana; 3+ - ilość duża; 4+ - ilość bardzo duża - jeżeli wykryto obecność danego składnika w moczu i składnik ten nie powinien występować w moczu prawidłowym
Dokonać półilościowego odczytu wyników z uwzględnieniem jednostek poszczególnych parametrów!
W obserwacjach należy uwzględnić również barwę obserwowanych pół testowych na pasku.
Sposób ODCZYTU I OMÓWIENIA WYNIKÓW aNALIZY MOCZU
DOKONANEJ przy użyciu testów paskowych Combur10-Test®M
BADANY PARAMETR |
JEDNOSTKI |
WYNIK |
|||||
|
|||||||
Właściwości fizyczne |
WARTOŚĆ OCZEKIWANA |
NIEPRAWIDŁOWY |
|||||
Ciężar właściwy |
g/ml |
1,015 - 1,025 |
<1,001 lub >1,035 |
||||
Odczyn (pH) |
- |
4,8 - 7,4 |
<4,5 lub >8,2 |
||||
|
|||||||
Skład chemiczny i obecność krwinek |
PRAWIDŁOWY |
NIEPRAWIDŁOWY* |
|||||
|
|
1+ |
2+ |
3+ |
4+ |
||
Obecność leukocytów |
ilość/μl |
ujemny <10 |
10-25 |
75 |
500 |
- |
|
Obecność azotynów |
mg/dl |
ujemny <0,075 |
dodatni ≥0,075 = ≥105 organizmów / 1 ml moczu |
||||
Zawartość białka |
mg/dl |
ujemny <10 |
30 |
100 |
500 |
- |
|
|
g/l |
ujemny <0,1 |
0,3 |
1 |
5 |
- |
|
Obecność glukozy |
mg/dl |
w normie <30 |
50 |
100 |
300 |
1000 |
|
|
mmol/l |
w normie <1,7 |
2,8 |
5,5 |
17 |
55 |
|
Obecność związków ketonowych |
mg/dl |
ujemny <5 |
15 |
50 |
150 |
- |
|
|
mmol/l |
ujemny <0,5 |
1,5 |
5 |
15 |
- |
|
Obecność urobilinogenu |
mg/dl |
w normie <1 |
1 |
4 |
8 |
12 |
|
|
μmol/l |
w normie <17 |
17 |
70 |
140 |
200 |
|
Obecność bilirubiny |
mg/dl |
ujemny <0,2 |
1 |
3 |
6 |
- |
|
|
μmol/l |
ujemny <3,4 |
17 |
50 |
100 |
- |
|
Obecność krwi |
erytrocytów |
ilość/μl |
ujemny <0,5 |
5-10 |
25 |
50 |
250 |
|
hemoglobiny |
|
|
10 |
|
|
|
* Sposób OMÓWIENIA WYNIKÓW półilościowej aNALIZY MOCZU
1+ - ilość niewielka
2+ - ilość umiarkowana
3+ - ilość duża
4+ - ilość bardzo duża
TĘTNICZKA
DOPROWADZAJĄCA
TĘTNICZKA
ODPROWADZAJĄCA
TOREBKA
BOWMANA
KŁĘBUSZEK
KANALIK
ZBIORCZY
PĘTLA HENLEGO
KAPILARY
OKOŁOKANALIKOWE
KANALIK I RZĘDU (PROKSYMALNY)
KANALIK II RZĘDU (DYSTALNY)
F
R
R
R
R
R
S
S
S
W
Rycina 1. Procesy zachodzące w nefronie i kanaliku zbiorczym.
Objaśnienia: F - filtracja, R - resorpcja, S - sekrecja, W - wydalanie
MOCZ
OSTATECZNY
FILTRAT = MOCZ PIERWOTNY
woda,
jony (Na+, Cl-, HCO3-), mocznik,
glukoza,
aminokwasy
Rycina 2. Sposób wykonania analizy moczu przy użyciu testów paskowych Combur10-Test®M.
1
2
3
4
6
pasek testowy
z 10 polami testowymi
pasek
testowy
skala barwna
NEFRON
7
ręcznik papierowy
5
KANALIKI NERKOWE
10 ml
1 - ciężar właściwy (g/ml)
2 - pH
3 - leukocyty (ilość leukocytów/μl)
4 - azotyny (mg/dl)
5 - białko (mg/dl lub g/l)
6 - glukoza (mg/dl lub mmol/l)
7 - związki ketonowe (mg/dl lub mmol/l )
8 - urobilinogen (mg/dl lub μmol/l)
9 - bilirubina (mg/dl lub μmol/l)
10 - krew (ilość erytrocytów/μl)
1
2
3
4
5
6
7
8
9
10
hemoglobina
erytrocyty
1
10
pojemnik
z moczem
badana próbka moczu
pojemnik
z paskami
Wyszukiwarka
Podobne podstrony:
FIZJOLOGIA UKŁADU ODDECHOWEGO - laborki, ZDROWIE, MEDYCYNA, Anatomia i fizjologia człowieka, Anatomi
Fizjologia mięśni szkieletowych - laborki, ZDROWIE, MEDYCYNA, Anatomia i fizjologia człowieka, Anato
Fizjologia mięśni gładkich - laborki, ZDROWIE, MEDYCYNA, Anatomia i fizjologia człowieka, Anatomia i
Choroby układu moczowo- płciowego, ZDROWIE-Medycyna naturalna, 3-Medycyna chińska, MEDYCYNA CHIŃSKA-
BUDOWA I FUNKCJE UKŁADU WYDALNICZEGO I ROZRODCZEGO U PTAKÓW, weterynaria, I semestr, Anatomia i fizj
Fizjologia 8.03.12 Fizjologia wysilku – repetytorium, MEDYCYNA ZDROWIE LECZENIE, anatomia, Fizjologi
31 FIZJOLOGIA UKŁADU WYDALNICZEGO
ANATMONIA I FIZJOLOGIA SERCA, MEDYCYNA, Anatomia, Notatki, tablice
Kolokwium Fizjologia ukladu wydalniczego, Dietetyka CM UMK, Fizjologia
Budowa i fizjologia narządu ruchu, Medycyna, Anatomia
Biologia część I, Budowa układu wydalniczego człowieka i fizjologia powstania
Kolokwium Fizjologia ukladu wydalniczego, II rok, II rok CM UMK, Giełdy, 2 rok, II rok, giełdy od Nu
Fizjologia Układu Wydalniczego
Choroby układu nerwowego, ZDROWIE-Medycyna naturalna, 01-Do uporządkowania, ZIOŁA
Choroby układu nerwowego, ZDROWIE-Medycyna naturalna, 01-Do uporządkowania, ZIOŁA
Koncepcja zdrowia w medycynie
OUN pytania, medycyna, anatomia, OUN
więcej podobnych podstron