POLITECHNIKA WROCŁAWSKA INSTYTUT FIZYKI
|
Sprawozdanie z ćwiczenia nr 24 |
|
TEMAT: Wyznaczanie ciepła topnienia lodu. |
|
DATA: OCENA: |
Cel ćwiczenia:
Zapoznanie się z techniką pomiarów kalometrycznych oraz ocena dokładności tych pomiarów.
Część teoretyczna ( opis zjawiska fizycznego ).
Mierzeniem ilości ciepła zajmuje się dział nauki o cieple, zwany kalorymetrią. Kalorymetria opiera się na kilku zasadach, które można wyrazić następująco:
- ilość ciepła ![]()
oddana przez ciało badane jest równa ilości ciepła ![]()
pobranej przez ciała otaczające;
- ilość ciepła pobrana przez ciało podczas ogrzewania jest równa ilości ciepła oddanej podczas ostygania w tym samym zakresie temperatur jeśli ciało przechodzi w odwrotnym porządku przez te same stany pośrednie;
- ilość ciepła Q oddana bądź pobrana przez ciało jednorodne jest proporcjonalna do jego masy, a przy niewielkich zmianach temperatury - do przyrostu temperatury ![]()
.
Ciepłem topnienia nazywamy ilość ciepła potrzebną do zamiany 1 kg ciała stałego
o temperaturze topnienia na ciecz o tej samej temperaturze.
Ilość ciepła Q potrzebna do stopienia masy m ciała o temperaturze topnienia wyraża się wzorem ![]()
, gdzie ![]()
- ciepło topnienia.
Temperatura topnienia T zależy od ciśnienia, przy którym zachodzi przemiana ciała stałego
w ciecz.
Część doświadczalna (pomiary dokonano 2x):
Kalorymetr wodny:
- Po zważeniu na wadze laboratoryjnej pustego suchego naczynia kalorymetrycznego wraz
z mieszadłem, napełniono 2/3 obj. wodą destylowaną i ponownie zważono.
- Po wstawieniu naczynia do kalorymetru i zanurzeniu termometru, przez ok. 5min odczytywano temperaturę.
TABELA 1 (pomiar1)
czas[min] |
temp.[C] |
1 |
23,5 |
2 |
23,5 |
3 |
23,6 |
4 |
23,5 |
5 |
23,45 |
- Po otworzeniu kalorymetru, wsypaniu drobno potłuczonego lodu (1/4 obj.), mieszając wodę odczytywano temperaturę co 1015s.
TABELA 2 (pomiar1)
czas[s] |
temp.[C] |
15” |
18 |
30” |
17 |
45” |
16,1 |
1'00” |
14,8 |
1'15” |
13,3 |
1'30” |
12,6 |
1'45” |
12,2 |
2'00” |
12,1 |
2'15” |
11,95 |
3'15” |
12,15 |
4'15” |
12,6 |
5'15” |
12,8 |
6'15” |
13 |
7'15” |
13,2 |
- Zważono naczynie kalorymetryczne.
TABELA 3 (pomiar1)
masa naczynia |
130,65g |
masa naczynia z woda |
192,2g |
masa wody |
61,55g |
masa naczynia z wodą+lód |
206,7g |
masa lodu |
14,5g |
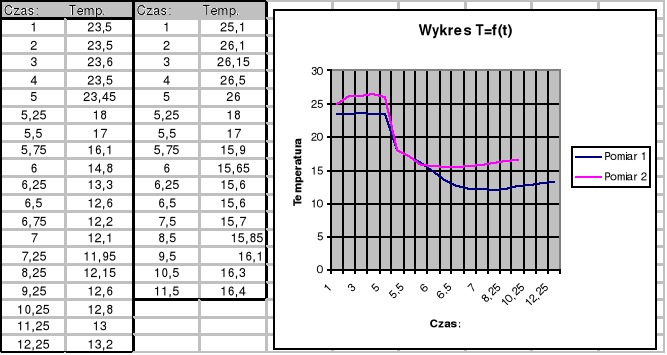
Sporządzenie wykresu T=f(t):
Pomiar 1 : Pomiar 2 :
Część obliczeniowa :
Wartości stałe:
Oznaczenia jakie przyjąłem:
CX ciepło topnienia lodu
mL masa lodu
CW ciepło właściwe wody
mW masa wody w kalorymetrze
CK ciepło właściwe kalorymetru
mK masa kalorymetru z mieszadełkiem
R objętościowe ciepło właściwe szkła i rtęci
V objętość zanurzonej części termometru
TW temperatura początkowa wody w kalorymetrze
TK temperatura końcową układu
TT temperatura topnienia lodu równa 273.15 K
Wyznaczenie ciepła topnienia lodu z równania bilansu cieplnego:
Po podstawieniach:
![]()
![]()
![]()
![]()
![]()
Otrzymałem:
![]()
Teraz mogę wyliczyć ciepło topnienia lodu Cx :
![]()
Błąd Cx obliczę z różniczki zupełnej:
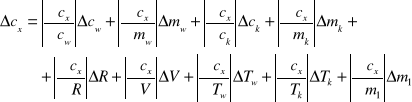
Wartości jakie przyjąłem do obliczeń:
mL = 0,0145 kg mL = 0.000 02 kg
CW= 4185 J/kg K CW = 8 J/kg K
mW = 0,06155 kg mW = 0.000 02 kg
CK = 879 J/kg K CK = 1 J/kg K
mK = 0,13065 kg mK = 0.000 01 kg
R = 1 930 000 J/m3 K R = 80 000 J/m3 K
V = 0.000 000 25 m3 V = 0.000 000 02 m3
TW = 296,5 K TW = 0.2 K
TK = 286,2 K TK = 0.2 K
Tt = 273.15 K
Z obliczeń:
Cx = 320 541.7584 J/kg
Cx = 12 453.92341 J/kg
Ostatecznie Cx=(320 500 +-12 500) J/kg
Błąd względny : ![]()
Wnioski :
Celem ćwiczenia było zmierzenie ciepła topnienia lodu. Pomiary dały wynik 320500 J/kg. Wartość ciepła topnienia podawana w tablicach fizycznych wynosi 340000 J/kg. Błąd bezwzględny wyniku to 12453 J/kg co jest spora wartością, lecz jako błąd względny daje ostatecznie 3.88 % (myślę, ze jest to nieźle).
Na wykresie topnienia (na papierze milimetrowym) widać, ze charakterystyka jest "zaokrąglona", nie ma tam kątów ostrych (teoretycznie - bez uwzględniania warunków praktycznych pomiaru powinny być ostre). Wynika to z bezwładności cieplnej wszystkich elementów biorących udział praktycznie w wymianie ciepła, wiec : kalorymetr, woda, termometr, mieszadełko kalorymetru, powietrze w kalorymetrze i poza nim, stół na którym stal kalorymetr. Największy wpływ na zaokrąglenie charakterystyki miały czynniki bezpośrednio stykające się z lodem. Pomiar ciepła topnienia lodu był pośredni (nie można zmierzyć tego bezpośrednio - należy wyliczyć ze wzoru). W związku z tym, że wzór był dość rozbudowany i składał się z wielu zmiennych. Na błąd pomiaru wpływało wiele czynników takich jak :
dokładność pomiaru mas (kalorymetru, kalorymetru z woda, kolorymetru z woda i lodem)
dokładność pomiaru objętości pojemniczka z rtęcią w termometrze
dokładność pomiaru temperatury w rożnych chwilach
Spośród tych rożnych przyczyn największy wpływ na błąd miały : dokładność pomiaru temperatury końcowej całego układu i dokładność pomiaru temperatury początkowej wody w kalorymetrze. Generalnie na błędy najbardziej wpłyną pomiar temperatury.
2
ciepło właściwe wody Cw=
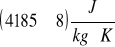
pojemność cieplna właściwa zbiornika z rtęcią termometru
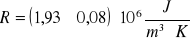
ciepło właściwe kalorymetru:
aluminiowego
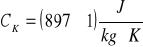
mosiężnego
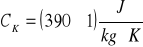
miedzianego
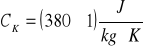
szklanego
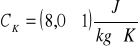
Wyszukiwarka
Podobne podstrony:
9465, materiały PWr, LPF
2588, materiały PWr, LPF
4263, materiały PWr, LPF
1794, materiały PWr, LPF
5262, materiały PWr, LPF
1866, materiały PWr, LPF
4731, materiały PWr, LPF
8606, materiały PWr, LPF
549, materiały PWr, LPF
3093, materiały PWr, LPF
6413, materiały PWr, LPF
160, materiały PWr, LPF
6721, materiały PWr, LPF
6341, materiały PWr, LPF
1317, materiały PWr, LPF
5036, materiały PWr, LPF
więcej podobnych podstron