WSTĘP.
Od dłuższego czasu walka ze szkodnikami polega głównie na stosowaniu różnego typu związków chemicznych jak np.: herbicydów czy insektycydów. Ma to jednak niekorzystny wpływ na całe środowisko i człowieka, gdyż są to środki nie działające w sposób wybiórczy, a częste ich stosowanie powoduje uodpornienie się na nie szkodników. W związku z tym dąży się do wprowadzania i udoskonalania metod nie chemicznych, bardziej ekologicznych w walce ze szkodnikami.
W metodach tych coraz większe zastosowanie znajdują feromony, czyli związki charakteryzujące się wysoką selektywnością, działaniem już w niskich stężeniach oraz szybkim zanikiem w środowiskiem. Substancje te działają na zmysł węchu. Mogą one być wydzielane przez organizmy zwierzęce, różnego rodzaju rośliny, a także otrzymywane w sposób syntetyczny. Niekiedy związki syntetyczne mają dużo większą aktywność od związków naturalnych. Do najbardziej znanych należą: feromony płciowe, ścieżkowe, agregacyjne, rozpraszające, zniechęcające i znaczące.
Ze względu, iż mogą one zapewnić zwalczanie określonego gatunku szkodnika, czy nawet kontrolować jego występowanie na danym obszarze, stosuje się różnego rodzaju pułapki z wykorzystaniem feromonów. Mają one za zadanie np.: zwabić, odstraszyć, zdezorientować lub przy zastosowaniu feromonu z preparatami owadobójczymi -zabić dane gatunki szkodników.
Celem opracowania jest przygotowanie opracowania monograficznego na temat semiozwiązków ze szczególnym uwzględnieniem feromonów.
Zakres pracy obejmuje następujące zagadnienia:
Sposób oddziaływania feromonów
Charakterystykę wybranych grup feromonów
Przykłady syntez
Zastosowanie feromonów w pułapkach na szkodniki.
WPŁYW PESTYCYDÓW NA SZKODNIKI I ŚRODOWISKO.
„Szkodniki”, to według Leksykonu biologicznego, organizmy wpływające ujemnie na rozwój i zdrowie człowieka oraz roślin i zwierząt, których prosperowaniem człowiek jest zainteresowany; niszczące wytwory gospodarki ludzkiej lub w jakikolwiek sposób odczuwane jako uciążliwe czy nieprzyjemne. 1
Do zwalczania szkodników używa się wielu metod z grubsza podzielonych na: metody zapobiegawcze (kwarantanna, różne metody uprawne, itp.), metody bezpośredniego zwalczania (mechaniczne, biologiczne i chemiczne).
Niestety, jeszcze do tej pory zwalczanie szkodników oparte jest przed wszystkim na stosowaniu syntetycznych środków chemicznych, między innymi pestycydów. Już sama nazwa -pestycydy, mówi coś o tych związkach, gdyż została ona utworzona z dwóch łacińskich słów tj.: „pestis „ -co znaczy „morowe powietrze” oraz „ caedo” -zabijam. Jednak większości ludzi nazwa ta nie przeraża, gdyż do tej pory prześcigali się oni w wytwarzaniu coraz to nowych preparatów chemicznych do zwalczania szkodników, a mówiąc bardziej otwarcie -do „zabijania” różnych roślin i zwierząt. Spoglądając na kierunek zastosowania oraz sposobu działania pestycydów to rośliny możemy zabić herbicydami, grzyby -fungicydami, bakterie -bakteriocydami, a wreszcie i zwierzęta -zoocydami. Potrafimy również niszczyć tylko wybrane grupy zwierząt: na owady stosujemy insektycydy, na gryzonie rodentycydy, na ślimaki moluskocydy, roztocza zwalczamy okarycydami, nicienie -nematocydami, mszyce -aficydami. Jeśli jakiś środek nie jest skuteczny na dorosłe formy owadów, możemy spróbować niszczyć ich jaja za pomocą owicydów. 2
W większości są to wszystko preparaty o szerokim spektrum działania, działające równocześnie na wiele różnych grup owadów zarówno szkodliwych jak i pożytecznych w tym także na pszczoły oraz drapieżce i pasożyty szkodników. Jak donoszą statystyki to z reguły niewielka ilość pestycydu osiada na opryskiwanej roślinie (10 -20 %), reszta natomiast paruje lub spływa do gleby. Zaś na ciało owadów, które zamierza się zwalczyć dostaje się jedynie 0,1 % zastosowanego insektycydu. Kłopot w tym, że pestycydy odznaczają się dużą rakotwórczością, mutagenicznością oraz toksycznością. Wiele z nich, po dostaniu się do środowiska przekształca się w substancje jeszcze bardziej niebezpieczne, a co gorsza przemieszcza się w ekosystemie, a nawet w całej biosferze. A więc zatruwając glebę, powietrze i wodę, zatruwają człowieka i zwierzęta. Jednym słowem ich stosowanie przyczynia się do zakłócenia równowagi biologicznej oraz skażenia środowiska.
Do związków najbardziej groźnych zalicza się tzw.: substancje perystentne -to znaczy takie, które w związku ze swoją trwałością długo pozostają w obiegu. Do nich zalicza się osławione już DDT i jego analogi. Obecnie związki zawierające w swym składzie DDT zostały wycofane z użycia i produkcji, jednak będą one wykrywalne przez wiele lat, czego przyczyną jest skażenie gleby, wody, a tym samym mięsa zwierząt hodowlanych, itp. Insektycydami bardzo toksycznymi dla fauny pożytecznej są wszystkie preparaty z grupy pyretroidów, a w naszym kraju prawie wszystkie preparaty fosforoorganiczne. Zdarza się, że stosuje się związki stosunkowo nietrwałe i co większość przez to rozumie -mniej szkodliwe, np.: pestycyd tiofos. Jest to jednak źle rozumiane, gdyż jest on wiązany z cząsteczkami próchnicy. Próchnica rozkładana jest następnie przez grzyby, a uwalniana substancja jest bardzo szkodliwa i zaczyna niekorzystnie oddziaływać na wszystkie organizmy w otoczeniu jej „promieniowania”.
Okazało się również, że subtelne dawki niektórych pestycydów mogą wręcz nawet przyśpieszać rozrodczość szkodników. W jednym z doświadczeń wykazano, iż subtelne dawki, przecież tak toksycznego DDT, parationu czy nawet dieldryny zwiększyły ilość składanych przez stonkę ziemniaczaną jaj i to od 33 % w przypadku dieldryny, do 65 % po zastosowaniu parationu, a w przypadku DDT nastąpił wzrost o 50 %. 3
Jednym z poważnych problemów, jakie napotkano w ostatnich latach, jest wytworzenie przez wiele gatunków odporności na pestycydy. Powodowało to iż dawki pestycydów były sukcesywnie zwiększane.
Do roku 1980 zidentyfikowano aż 428 gatunków uodpornionych stawonogów. Wśród nich znalazły się min.: wołek zbożowy (Calandra granaria), prusak (Blotella germanica) i korczan wschodni (Blatta orientalis). Naukowcy przypuszczają, że organizmy żywe są w stanie wykształcić odporność na wszystkie środki chemiczne, które obecnie stosowane są do ich unieszkodliwiania. Odporność najszybciej wykształca się u gatunków mających krótki cykl rozwojowy i dużo potomstwa, gdyż wtedy więcej osobników ma możliwość zetknięcia się z pestycydem. Populacje owadów są z reguły heterogeniczne, to znaczy że w populacji znajduje się zarówno osobniki mało odporne, jak i bardziej odporne na działanie danej substancji. Podczas zastosowania pestycydów giną jedynie osobniki nieodporne. Pozostałe (odporne) krzyżują się, dając odporny biotop. Co ciekawe, podczas zastosowania danego preparatu w dawkach powodujących wysoką śmiertelność, następuje szybsze uodpornienie się populacji, gdyż intensywniej eliminowane są osobniki wrażliwe. Jako przykład takich szkodników (szybko się uodparniający) można podać organizmy zasiedlające np. sady. Należą do nich przede wszystkim: przędziorki, mszyce i miodówka na gruszach. Do tej pory wśród przędziorków występujących na drzewach i krzewach owocowych znaleziono populację odporną na około 10 różnych związków chemicznych. Uważa się, że wystarczy aby preparat oddziaływał na 30 -40 generacji przędziorków, aby doszło do wyselekcjonowania się populacji odpornej. Jednym z ostatnich przykładów jest uodpornienie się przędziorków w Hiszpanii na bardzo skuteczny na początku preparat -Apollo. W kraju tym przędziorki były na tyle groźnymi, że Apollo stosowany był w sadach kilka razy w ciągu roku. W związku z tym po kilku latach preparat przestał całkowicie je ograniczać. W Polsce Apollo stosowany jest dopiero od niedawna więc nadal jest jeszcze skuteczny. Również obrazowym przykładem mogą być Stany Zjednoczone, gdzie na preparaty fosforoorganiczne całkowicie już uodporniły się takie szkodniki, jak: szrotówek, białaczek, mszyca jabłoniowo -babkowa, bawełnica królewska, przegibki i skoczki. W Polsce prawdopodobnie w niektórych sadach pojawiają się już mszyce tolerancyjne na toksyczny preparat -Pirimor. 4
Aby przeciwdziałać zjawisku „uodpornienia” specjaliści zalecają zmniejszenie dawek pestycydów do najmniejszych skutecznych, ograniczenie częstości zabiegów, nie używanie substancji perystentnych, zmienianie stosowanych pestycydów co pewien okres czasu. Jednak mimo takich zabiegów, średnio co 6 lat podwaja się ilość owadów odpornych na ich działanie, a do biosfery wciąż dostają się ogromne ilości trucizn -coraz to nowych i toksycznych.
Do tej pory skupiałam się głównie na kosztach środowiskowych, które wynikają ze stosowania związków chemicznych, ale niekorzyści płynące z ich używania są też widoczne na podstawie kosztów społeczno -ekonomicznych. Pełne koszty użycia pestycydów tylko w Stanach Zjednoczonych przedstawił David Dimentel, profesor ekologii owadów i nauk rolniczych w Uniwersytecie Cornella. Oszacował on, że koszty bezpośrednie ponoszone przez użytkowników tych związków wynoszą 3,092 miliardów dolarów rocznie, natomiast koszty pośrednie to jest: środowiskowe i ochrony zdrowia, aż 5 miliardów dolarów rocznie. 2
W związku z tak przerażającymi faktami z roku na rok dąży się do udoskonalenia i wprowadzania metod niechemicznych w zwalczaniu szkodników, a także bardziej selektywnych.
SEMIOZWIĄZKI.
Można się spodziewać, że z niechemicznych metod zwalczania coraz większe zastosowanie znajdują tzw. semiozwiązki. Semiozwiązki są to substancje chemiczne, które emitowane lub rozpraszane przez jedne organizmy żywe wpływają na zachowanie się innych organizmów. Charakterystyczną rzeczą jest, że semiozwiąki wydzielane do środowiska w minimalnych ilościach wywołują zdecydowane reakcje innych organizmów w niektórych przypadkach oddalonych nawet o kilka kilometrów. Zaletą semiozwiązków jest też ich wysoka selektywność oraz szybkie zanikanie w środowisku. 4
Najbardziej powszechnymi semiozwiązkami są feromony, działające w niskich stężeniach i najczęściej nieszkodliwe dla większości organizmów. Feromony były prawdopodobnie pierwszą formą komunikowania się najprostszych organizmów. Ich nazwa pochodzi z połączenia greckich słów pherein (przekazywać) i hormon ( pobudzać). Stosowanie feromonów stwierdzono, jak dotychczas u ponad 1500 gatunków zwierząt (głównie owadów -1100 gatunków), kilkudziesięciu roślin, a także szeregu bakterii i drożdży. 1
Typowe przykłady oddziaływania feromonów na zachowanie się organizmów to:
oddziaływanie wabiące
oddziaływanie zatrzymujące
oddziaływanie odpychające
oddziaływanie odstraszające
oddziaływanie stymulujące jedzenie
oddziaływanie stymulujące zakładanie gniazda, składanie jaj
oddziaływanie stymulujące ośrodek nerwowy, itp. 5
ROLA ZAPACHU.
Rozwój badań nad tymi silnie działającymi i wysoce specyficznymi wabikami jest nierozerwalnie związany z reagowaniem i kierowaniem się zapachem przez różnego rodzaju organizmy. Ogólnie rzecz biorąc, zapach jest bardzo ważny przede wszystkim dla owadów latających, ale najprawdopodobniej jest w jakiś sposób związany z życiem większości owadów. Ze wszystkich narządów zmysłów, bardzo małe organizmy nie mają najmniejszych trudności z oceną wrażeń odbieranych przez zmysł węchu, gdyż reagują one już na pojedyncze cząsteczki. W rzeczywistości u owadów tylko trzy podstawowe funkcje życiowe mają istotne znaczenie. Są to: jedzenie, kopulacja oraz składnie jaj. A więc interesujące jest zbadanie substancji zapachowych, które byłyby związane z powyższymi czynnościami. Miałoby to duże znaczenie w walce ze szkodnikami, bez negatywnego wpływu na środowisko i zdrowie człowieka.
Jeśli chodzi o zapachy, które zwabiają owady do pożywienia, pochodzą w zasadzie ze źródła pokarmu, a nie są wytwarzane przez owada. Na przykład muszki owocowe, żywią się przejrzałymi owocami i nie zwracają uwagi na owoce gdy są one zielone. Mówiąc ściślej nie są one wabione przez tę część owocu, którą się zazwyczaj odżywiają tzn. przez sok, lecz przez związki chemiczne wytwarzane przez inne organizmy w procesie psucia się owocu.
Jeśli zaś chodzi o składanie jaj, to poszukiwanie miejsca odpowiedniego dla danego, bezpiecznego rozwoju potomstwa należy do tego samego rodzaju czynności, co i zwykłe poszukiwanie pożywienia. Tutaj również substancja kierująca wytwarzana jest niezależnie od owada. Nawet wówczas gdy jaja są rozsiewane, zapach może mieć znaczenie. Przykładem tego mogą być komary, które składają o wiele więcej jaj w zagłębieniach z wodą zawierającą takie substancje jak: siarkowodór, wyciąg z drożdży lub mocz bydlęcy, niż na powierzchni wody wodociągowej. Innym a jednocześnie jednym z najbardziej osobliwych i zadziwiających przykładów tego rodzaju są toczące drewno chrząszcze (np.: Melenophilia consputa i M. Atropurpurea). Występują one w niewielkich ilościach na terenach zniszczonych przez pożary. Owady te są silnie przyciągane przez dym. Widuje się je biegające po gorącej powierzchni spalonych drzew, prawdopodobnie w poszukiwaniu miejsca do złożenia jaj. Kiedy drzewo obumiera, większość owadów i pasożytów pod działaniem ognia ginie, tak że pierwsze przybywające pasożyty mają wolne pole do działania. Jednak nie tylko palące się drzewo działa na nie przyciągająco, ale również dym tytoniowy, a nawet paląca się ropa naftowa. Wynika z tego, że nie sam powstający dym działa na nie przyciągająco, ale określony związek znajdujący się w nim, który przypomina substancję normalnie karmiącą te owady.
Zazwyczaj można łatwo rozstrzygnąć czy owady zbliżają się dlatego, że wyczuwają substancję wabiącą do pożywienia czy też do składanie jaj. Substancja wabiąca do pożywienia na ogół gromadzi jednocześnie samców i samice, a często również dorosłe lub larwalne postacie. Natomiast substancja wskazująca miejsce składania jaj gromadzi prawie wyłącznie samice, a te z kolei wabią samców. Również często można spotkać substancję wabiącą wyłącznie samca. Wzbudza ona szczególne zainteresowanie. Substancja chemiczna wabiąca samce jest normalnie wydzielana przez samice i jest produktem metabolizmu owada, a nie jak substancje wskazujące pożywienie lub miejsce składania jaj, które powstają w środowisku zewnętrznym. Budowa chemiczna tzw. wabika seksualnego -substancji, która powstaje w samych owadach, może rzucić pewne światło na cały proces odczuwania zapachów przez owady, a nawet i przez zwierzęta wyższe. 6
SPOSÓB ODDZIALYWANIA FEROMONÓW.
Wiemy już, że substancje chemiczne (feromony) wydzielane przez organizmy działają na zmysł węchu, gdyż przejawiają swe właściwości w minimalnych stężeniach, wystarczających jednakże do wywołania gwałtownej reakcji samca. Można więc oczekiwać wywołania określonego zachowania nawet pod wpływem pojedynczej cząsteczki feromonu. W praktyce jest jednak wymagany kontakt z kilkoma cząsteczkami, co zabezpiecza przed przypadkowym uruchomieniem określonych reakcji. Jednymi z bardziej aktywnych są feromony płciowe karaluchów -perifanon i supelapyron, które uaktywniają samce nawet ze znacznej odległości. Stężenie feromonu może mieć też wpływ na rodzaj przekazywanej informacji, tak jak jest to w przypadku feromonu mrówek (Pogonomyrmex bodius) -4-metyloheptan -3-onu. Przy niskich stężeniach zachęca on robotnice do posłuszeństwa królowej, do wydajnej pracy, utrzymuje porządek w kolonii. Przy większych stężeniach staję się dla nich poleceniem do kopania podziemnych korytarzy -kryjówek.
Feromony, związki które są zdolne do wywołania określonych i tak gwałtownych reakcji, już w minimalnych ilościach są produkowane najczęściej w gruczołach zewnętrznych np.: owadzie, żeńskie atraktanty płciowe wytwarzane są często w gruczołach umieszczonych w membranach pomiędzy ostatnimi segmentami odwłoku. Samce wielkiej ćmy woskowej mogą wytwarzać je w gruczołach umieszczonych w skrzydłach. Mrówka posiada, aż ok. 50 zewnętrznych gruczołów produkujących związki semiochemiczne. Gruczoły te zostały podzielone na dwie grupy ze względu na rodzaj komórek, z których są zbudowane. Do tej grupy należą gruczoły nabłonkowe produkujące i wydzielające substancje bezpośrednio do otaczającego je nabłonka. Do drugiego typu, bardziej zróżnicowanego, należą gruczoły zawierające wiele wyspecjalizowanych komórek wydzielniczych i kanałowych. Produkty tych gruczołów mogą być wydzielone bezpośrednio na zewnątrz lub gromadzone przejściowo w specjalnych zbiornikach. Gromadzony w zbiorniczku jad mrówkowy, którego stężenie dochodzi do 65 % może stanowić aż 22 % wagi mrówki. Do wywołania jednak pożądanego efektu musi nastąpić kontakt związku z częścią ciała, w której znajdują się receptory. U owadów odbiornikiem feromonów lotnych są najczęściej czułki zawierające setki tysięcy komórek receptorowych. Zaadsorbowane na powierzchni czółek cząsteczki feromonu wnikają na zasadzie dyfuzji do ich wnętrza, gdzie poprzez system kanalików docierają do receptorów. Tam następuje ich rozpoznanie i przekształcenie chemiczne, czego rezultatem jest wytworzenie sygnału elektrycznego przesyłanego do mózgu. Mózg pod wpływem tego sygnału uruchamia skomplikowany proces, w tym syntezę lub uwalnianie enzymów, hormonów, czy przekaźników. Proces ten wywołuje specyficzne zachowanie odbiorcy zgodne z przesłaniem, którego treść zakodowana była w cząsteczce feromonu.
WYBRANE GRUPY FEROMONÓW I ICH RODZAJE.
Treść informacji zakodowana w wydzielonym związku chemicznym może być różnorodna. W zależności od pełnionych funkcji feromony podzielono na ok. 30 grup. Do najbardziej znanych należą tzw.: feromony płciowe, oprócz nich bardzo ważne są też feromony ścieżkowe, agregacyjne, rozpraszające, zniechęcające czy znaczące.
Feromony płciowe- jako najlepiej poznane są związkami chemicznymi wykorzystywanymi w procesie nawiązywania z partnerem wstępnej gry prowadzącej do parzenia się i zapłodnienia. Feromonami płciowymi mogą być różne związki chemiczne, w tym kwasy karboksylowe, węglowodory, związki aromatyczne i alifatyczne. Często przedstawiciele przeciwnej płci żyją osobno, niejednokrotnie okres płodny samic jest krótki i to utrudnia proces kojarzenia. Feromony mają na celu pokonanie tych utrudnień poprzez kojarzenie partnerów, synchronizację czynności prowadzących do zapłodnienia. 7
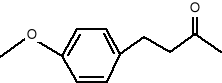
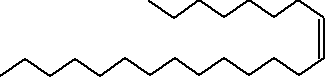
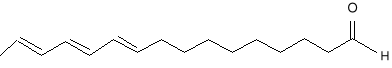
Pierwszym odkrytym feromonem płciowym był „bombykol” (1), związek wydzielony z gruczołów samic jedwabnika Bombyx mori, zdolny do zwabiania samców z odległości 11 km. O trudnościach związanych z izolacją i identyfikacją jego świadczą wysiłki zespołu A. Butenanda, który podejrzewając istnienie feromonów, poszukiwał ich przez 30 lat, zanim wyizolował „bombykol”. Do otrzymania kilkunastu mg tego związku zużył aż 500 000 gruczołów wyizolowanych z samic jedwabnika. Wyizolowanie wabika seksualnego wczystej formie było tylko początkiem na drodze do ustalenia jego budowy chemicznej. W wyniku przeprowadzonych badań ustalono strukturę tego związku, która jednak mogła mieć co najmniej cztery możliwości konfiguracji, wynikające z faktu, że dwie pary atomów węgla połączone były podwójnymi wiązaniami. Dopiero po otrzymaniu wszystkich struktur na drodze syntetycznej, sprawdzono która z nich ma własności biologiczne „bombykolu”, a jego budowę przedstawiono następującym wzorem 1:
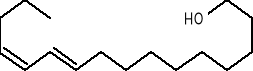
1.
Jak widać wyizolowanie substancji chemicznej wabika seksualnego, wydzielanej przez samiczki jest pracą długą i żmudną. Można to również uczynić metodą „prób i błędów” wybierając przypadkowe związki chemiczne i sprawdzając czy któryś z nich nie wykazuje właściwości wabiących.
W ten sposób odkryto, że olejek z nasion arcydzięgla ma silne działanie przyciągające samiczki śródziemnomorskiej muszki owocowej (Ceratitis capitata). Ponieważ owad ten jest szkodnikiem owoców cytrusowych, rozpoczęto na szeroką skalę program wyłapania tych owadów wykorzystując możliwość zastosowania wabika seksualnego. Wykorzystano wówczas całą światową produkcję olejku arcydzięglowego. Rozpoczęto więc poszukiwanie środków zastępczych. Środkiem takim okazał się związek nazwany Siglure, o budowie (2).
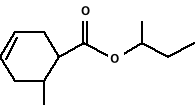
2.
Trudno przypuszczać, aby budowa chemiczna odpowiadała strukturze wabika naturalnego, ale z praktycznego punktu widzenia nie miało to znaczenia. Działał on na owady równie skutecznie. Jak już wspomniałam wcześniej, tak jak i w przypadku „bombykolu” mogą istnieć inne możliwości ułożenia, np.: węgli w związku. Otrzymano produkt Medlure (3), który był bardziej aktywny i trwalszy od preparatu Siglure.
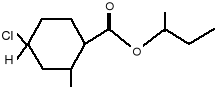
3.
Jednak po podjęciu dalszych prób zmian w łańcuchu bocznym otrzymano, aż czterdzieści sześć odmian. Jedna z nich okazała się lepsza od Medlure ze względu na właściwości wabiące, a jednocześnie była mniej trwała. Nazwano ją Trimedlure (4).
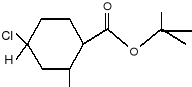
4.
Innym poważnym szkodnikiem jest muszka melonowa (Dacus cucurbitae) żyjąca między innymi na Hawajach. W tym przypadku również przebadano wiele związków i najlepsze działanie wabiące samce tej muszki wykazały dwa związki, tj.:
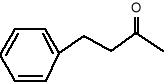
Benzyloaceton (5)
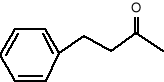
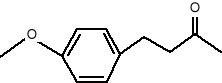
Anizyloaceton (6)
Kolejną substancją wabiącą, którą badano z dobrymi wynikami jest substancja wydzielana przez brudnice nieparkę (Porthetria dispar). Jest to szkodnik z rodziny brudnicowatych, występujący powszednie również w naszym kraju. Występuje on na drzewach liściastych, głównie w sadach, zadrzewieniach śródpolnych, przydrożnych lub w parkach. Wyjątkowo żeruje też na sośnie. Rozpiętość skrzydeł dorosłego owada wynosi 35 -65 mm u samic. Samce są mniejsze, o skrzydłach brązowych z odcieniem brunatnym i pierzastymi czółkami. Motyl ten składa jaja na korze, gałązkach pokrywając je włoskami z odwłoka. Gąsienice są silnie owłosione, szare z sześcioma rzędami niebieskich i czerwonych brodawek, na których znajdują się pęczki długich włosków. Gąsienice te w czasie rozwoju zjadają liście, powodują również ogołocenie kory drzew.
Jak stwierdzono oznakowane samczyki odnajdują samiczki oddalone o ponad trzy kilometry, a więc wabiący zapach jest bardzo silny. Budowę tego wabika opisano zastępującym wzorem: (7).
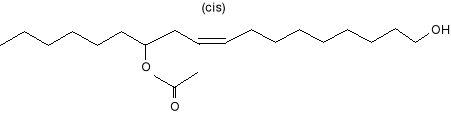
7.
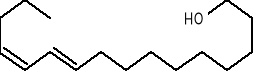
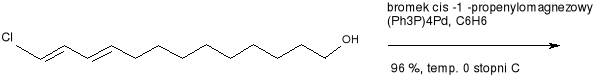
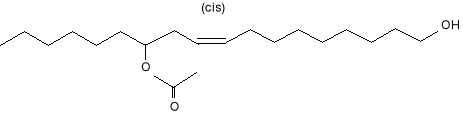
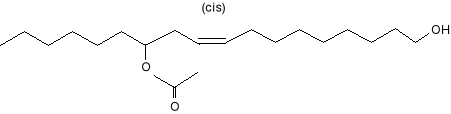
Jednak z chwilą kiedy zakończono pracę nad tym związkiem, okazało się, że substancję o podobnej budowie można otrzymać za pomocą syntezy.6 Produktem wyjściowym był kwas rycynolowy {CH3[CH3]5CH(OH)CH2-CH=CH[CH2]7COOH}, ponieważ ulegał łatwo przekształceniu w czystą formę był idealnym materiałem początkowym. Został on ilościowo redukowany wodorkiem litowo- glinowym [AlLiH4] do odpowiadającego alkoholu, następnie był acetylowany z 62 % -wydajnością z acetylochlorkiem, w schłodzonym benzenie do 1,12 -dioctanu. Po poddaniu go dodatkowym syntezom otrzymano (+) -12 -acetoksy -cis -9 -octadekan -1 -ol (Gyplure), (8), którego wydajność wynosiła aż 90 %. Po poddaniu go fluorescencji w świetle ultrafioletowym, okazał się on wabikiem stabilnym, nierozkładającym się w czasie przechowywania w temperaturze pokojowej nawet przez kilka lat.
Po doświadczeniach przeprowadzonych w terenie okazało się, że wykazuje on aktywność przy zastosowaniu już w ilości 10-5 [μg], zaś w warunkach laboratoryjnych w ilości 10-12[μg]. Dlatego w porównaniu z aktywnością naturalnego wabika okazał się on bardzo korzystny. Naturalny związek wykazuje aktywność w terenie przy 10 -7[μg], natomiast w laboratorium w ilości 10-12[μg].
Podjęto się również otrzymania trans -izomeru Gyplure. Jednak izomeryzacja została uzyskana w 28 % wydajności, przy potraktowaniu związku mieszaniną azotanu (III) sodu i kwasu azotowego (V), stosowanych według określonej procedury Kass and Radlove. Po badaniach okazało się, że w porównaniu z cis -izomerem, trans -izomer był mniej atrakcyjny dla samców ćmy, (Porthetria dispar), w terenie potrzebna ilość tego związku była >2,5 *105[μg], zaś w warunkach laboratoryjnych 104[μg].
Również propoksy i butoksy jako analogii Gyplure, przygotowane w czasie podobnej procedury były zupełnie nieaktywne w stosunku do samczyków ćmy.
Badania prowadzono również z kwasem [(+)-14-hydroksy -cis -11 -arachidowym], który użyto do przygotowania preparatu [(+) -14 -acetoksy -cis -11 -eikozan -1 -olu], jako atraktanta płciowego. Jednak i ten związek okazał się mniej aktywny niż Gyplure, gdyż w terenie wykazywał on aktywność przy zastosowaniu 10 [μg] zaś w laboratorium 10-2[μg]. 8
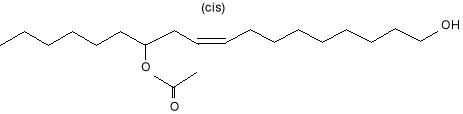
8.
Jednym ze zidentyfikowanych wabików seksualnych i również zasługujących na szczególną uwagę jest substancja wydzielana przez królową pszczół (Apis mellifera). W przeciwieństwie do samiczki brudnicy, która nie może latać i musi oczekiwać na przybycie samca, królowa pszczół dokonuje lotu godowego i w locie spotyka trutnia. Problem jaki stoi przed tymi owadami -to przebycie znacznej odległości w trójwymiarowej przestrzeni, sięgającej nawet do ok. 1 km . Trudność ta zostaje przezwyciężona właśnie dzięki wydzieleniu wabiącej substancji zapachowej, w której skład wchodzi głownie, chociaż nie jedynie związek o następującej budowie: (9). 6
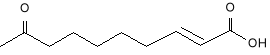
9.
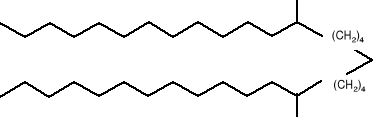
Uwagę moją zwróciły również następujące feromony płciowe: 13,23 -dimetylopentatriakontan (10) wydzielony przez samicę muchy tse -tse (Glosina pallialipes)
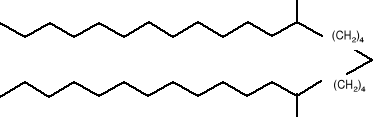
Feromon samicy muchy domowej (Musce domestica) zwany Z-9 -dokozen (11).
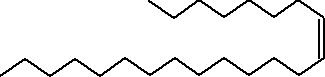
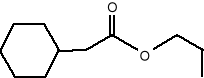
Feromon prusaka (Blattalla germanica) o nazwie Cykloheksylooctan propylu (12).
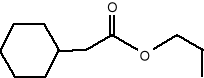
Jak już wiadomo owady przeciwnych płci odnajdują się i przywabiają w celu kopulacji za pomocą tzw. feromonów płciowych. Przykładem wykorzystania innych feromonów w procesie rozmnażanie mogą być mrówki, których samce z różnych kolonii gromadzą się w jednym miejscu tworząc rój, do którego zlatują się samice. W tym przypadku rolę wabika odgrywa feromon agregacyjny. Zaś samice innego gatunku (Megaponera foetus) podążają do gniazda ścieżką zaznaczoną przez robotnice i do parzenia dochodzi wewnątrz gniazda. Tym razem funkcję wabika spełniają tzw. feromony ścieżkowe.
Jak widać tak samo jak feromony płciowe, na uwagę zasługują również i inne związki chemiczne wydzielane przez owady, które tak samo są ważne w ich życiu.
Feromony ścieżkowe -wydzielane są z odwłoka owada i celowo rozsmarowywane przez osobnika mającego za zadanie zaznaczyć drogę. Są one często złożoną mieszaniną, a ich skład zależy nie tylko od gatunku ale również od rodzaju pożywienia, jego zasobów, a także i od przynależności do rodziny, podrodziny, czy nawet kolonii. Feromonami ścieżkowymi znaczony jest wąski pasek w terenie, który łatwo rozpoznają i mogą wzdłuż jego podążać osobniki tworzące wspólnotę. Tego typu chemiczny sposób zaznaczania ścieżek stosują często termity, mrówki czy gąsienice. Ścieżki takie prowadzą do źródła pożywienia, miejsca kopulacji, składania jaj czy założenia kolonii. Stwierdzono, że niektóre gatunki bez żądłowych pszczół stosują substancję tego typu do znakowania korytarzy powietrznych.
Feromony znaczące -są stosowane do oznakowania granic miejsca zamieszkania lub polowania. Pośród owadzich feromonów znaczących odkryto węglowodory alifatyczne i terpenoidy.
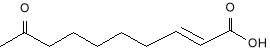
Jednym z bardziej znanych feromonów śladu jest wydzielany przez termita (Zootermopsis neradensis) kwas kapronowy (13).
![]()
Feromony alarmowe -są wydzielane w przypadku zagrożenia koloni, czy gniazda, wywołują przy tym całą gamę zachowań u odbiorcy. Taką reakcją na ten feromon może być ucieczka, bezruch, szukanie schronienia, agresja. Rolę feromonów alarmowych mogą pełnić różnorodne związki, jak: alifatyczne i cykliczne alkohole, aldehydy, ketony, estry, węglowodory, heterocykle, sulfidy, terpenoidy i wiele innych w zależności od rodzaju i gatunku osobnika.
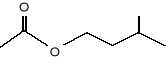
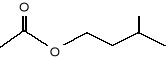
Feromon alarmowy, który wzywa do żądlenia np.: w obronie ula, wydziela pszczoła miodna (Apis mellifera) i jest to octan izopentylu (14).
Feromony agregacyjne -powodują gromadzenie się osobników jednego gatunku w miejscu, w którym ten feromon został wydzielony przez przedstawiciela lub przedstawicieli tego samego gatunku w celu zwabienia partnerów seksualnych, przekazania informacji o znalezionym obfitym źródle żywności, czy też o odkryciu miejsca do założenia kolonii. Feromony tego typu mają długą trwałość. Na przykład Undekan wydzielony przez robotnice jednego gatunku mrówek, zachowuje aktywność przez 12 godzin.
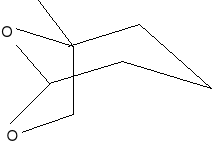
Jako przykład feromonu agregacyjnego można podać tzw.: Frontalinę (15) feromon ten wydzielany jest przez kornika (Dendroctonus frontalis).
Feromony rozpraszające- mają za zadanie utrzymanie osobników tego samego gatunku w określonej odległości od siebie w celu ograniczenia rywalizacji wewnątrzgatunkowej, w tym walki o żywność, partnerów płciowych, miejsca składania jaj, zakładania gniazd, itp.
Feromony dyskryminujące -powodują, najczęściej we wczesnym stadium rozwoju, hierarchiczny (kastowy), podział osobników. Tego typu podział stosują owady społeczne, np. pszczoły, mrówki i termity. Samice pszczół mogą być robotnicami stanowiącymi zdecydowaną większość kolonii lub królową -matką. Ten podział, będący swego rodzaju dyskryminacją, odbywa się pod wpływem mieszaniny ośmio -i dziewięciowęglowych kwasów karboksylowych. Mieszanina kwasów utrzymująca status robotnic nie jest typowym feromonem, gdyż jest wytwarzana przez ich gruczoły szczękowe. Pełni jednak rolę feromonów, gdyż służy jako dodatek konserwujący pożywienie larw, a przede wszystkim powstrzymuje rozwój larw żeńskich w kierunku królowej. Kwasy karboksylowe wytwarzane przez królową wchodzą w skład szczękowego feromonu królowej (QMP). Są one więc silnymi atraktantami wymuszającymi posłuszeństwo wobec królowej, tworzenie wokół niej orszaku, skłaniają do pracy. Feromon ten tłumi zdolność do składania jaj przez robotnice, ale po 2 -3 tygodniach niepłodności królowej, uzyskują zdolność składania jaj. W gruczołach robotnic i królowej znaleziono też śladowe ilości składników feromonu o przeciwnym działaniu co świadczy, że ich gruczoły zachowują zdolność obu feromonów. Wytwarzane są one z tego samego substratu, jakim jest kwas stearynowy. U mrówek (Solenopsis invicta) zapłodniona królowa produkuje feromon uznający królową, który czyni ją atrakcyjną dla robotnic i motywuje do służby. Aktywnym składnikiem tego feromonu jest mieszanina nienasyconego cyklicznego ketonu.
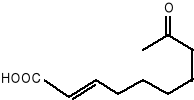
Za feromon, który przywabia robotnice i hamuje rozwój ich jajników, uważa się tzw. Substanję Królowej (Queen substation) (9) pszczoły miodnej, czyli:
Feromony obronne -oraz jad wytwarzane i wydzielane są w celach obronnych lub ułatwiających zdobycie pożywienia, są związkami wywołującymi odczucie nieprzyjemnego bólu, podrażnienia a nawet śmierci. Związki te, kiedy nie są przeznaczone dla osobników tego samego gatunku, nie są zaliczane do klasycznych feromonów. Dobrze znany jest jad obronny mrówek. Skład tego jadu jest zróżnicowany. Głównym składnikiem jadu mrówek (Formicidae) jest kwas mrówkowy. Oprócz kwasu mrówkowego, w jadzie tym znajdują się krótkie peptydy i wolne aminokwasy w stężeniu nie przekraczającym 5 %. Jad mrówek nie należących do (Formicidae) zawiera dużo białek -enzymów, wśród nich fosfolipazy i hialuronidazę. Niektóre gatunki mrówek, np.: (myrmicine), produkują alkaloidy. Robotnica (S. geminata) może zgromadzić w swoim ciele 19 mg alkaloidów. Jad fire ants, wywołujący miejscowe zapalenie w okolicy użądlenia, zawiera 2 -alkilo -6 -piperydyny. Ćmy (Utytheisa ornatrix), ich jaja oraz larwy są niejadalne dla większości zwierząt, ponieważ zawierają alkaloid odstraszający potencjalnych amatorów. 7
Dla przedstawionych grup feromonów ,o tak specyficznych oddziaływaniach można obliczyć ilość minimalnego stężenia jaki potrzebny jest by wywołały one właściwe reakcje organizmów. Można tego dokonać posługując się zależnościami ,które zostały ujęte we wzorze matematycznym na szybkość rozchodzenia się związków chemicznych w powietrzu.
Wzór taki wyprowadzony na podstawie prawa dyfuzji, uwzględniający lotność feromonu, pozwala obliczyć czas, po jakim wymagane stężenie substancji znajdzie się w określonej odległości od źródła. Dla niektórych feromonów ścieżkowych promień działania wynosi 0,6 cm, a pewnych feromonów płciowych nawet 600 m i więcej. Własności poszczególnych feromonów zależą od ich przeznaczenia, np.: ścieżka zaznaczana feromonem ścieżkowym powinna być wąska, a czas jego aktywności stosunkowo długi, rzędu godzin. Natomiast feromon alarmowy powinien działać szybko, ale krótko. Nie może on pozostać długo w powietrzu, żeby nie utrzymywać kolonii niepotrzebnie przez dłuższy czas w stanie gotowości bojowej. Promień działania feromonu alarmowego pewnego gatunku mrówek wynosi 10 cm, a po dwóch minutach jego stężenie spada poniżej stężenia aktywnego.
3. WYBRANE SYNTEZY FEROMONÓW.
Prace nad identyfikacją feromonów zaczynają się od wydobycia ich z materiału biologicznego. Dokonuje się tego poprzez izolacje ich z całych, homogenizowanych organizmów, ekstrahując skomplikowaną mieszaninę wielu związków. W trakcie oczyszczania tej mieszaniny następują jednak ogromne straty, a to z kolei wymaga zabijania znacznej ilości organizmów. Jak np.: podczas izolowania jednego z pierwszych feromonów bombykolu (1), kiedy to zabito aż 500 000 osobników. Obecnie jednak wraz z rozwojem techniki, można wyekstrahować potrzebną ilość feromonów z gruczołów pobranych zaledwie od kilku osobników. Zostały również już opracowane techniki pobierania feromonów bezpośrednio z gruczołów lub ze zbiorników, w których się znajdują. Identyfikacja składników feromonów za pomocą metod spektralnych wymaga potwierdzenia ich budowy poprzez porównywanie związków naturalnych z substancjami otrzymanymi na drodze syntezy chemicznej.
Wyizolowanie odpowiedniego związku wabiącego dla określonego gatunku, nie musi jednak być związana z ekstracją związku naturalnego. Można dokonać tego metodą prób, wybierając wiele grup związków organicznych i sprawdzając ich właściwości wabiące.
Obecnie jest już znanych wiele związków feromonowych oraz ich syntez.
Jedna z nich to: wysoce steroselektywna synteza składników feromonu płciowego u południowego Green Stink Bug (Nezara viridula) (L.) i Green Stink Bug (Acrosternum hilare) (Sag.).
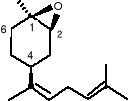
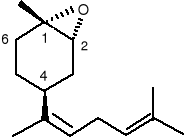
Nazara viridula (L.) -to notoryczny szkodnik upraw rolniczych, rozpowszechniony na całym świecie. Atakuje on wiele gatunków warzyw, owoców i plony zbóż. Polifagowa natura i ruchliwość robaka czynią go wyjątkowo trudnym do kontrolowania. Często spotykany z N. Viridula, jest spokrewniony z nim Acrosternum hilare .Tworzą one kompleksy rojące się w strąkach soji i innych strączkowatych, bawełnie i lucernie. Feromony płciowe u obu gatunków, wydzielone przez samców, przyciągają samice danego gatunku. Mieszanka feromonowa produkowana przez A. hilare składa się głównie z cis (Z) -(1R, 2S,4S)-epoksybisabolenu (16)
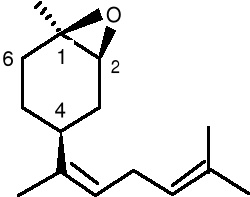
zmieszanego z mniejszą ilością odpowiedniego trans -izomeru (17), podczas gdy mieszanka wabiąca N. viridula składa się z przeciwnego stosunku z trans -izomeru (17)
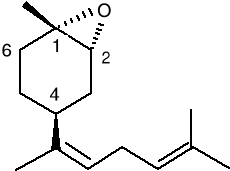
jako głównego i cis (Z) -(1R, 2S, 4S) -epoksybisabolenu (16) jako drugorzędnego składnika.
Ze względu na rolę tych owadów jako szkodników rolniczych i ważną rolę feromonów jaką mogą pełnić w rozwoju opartych na substancjach wabiących metod monitorowania i kontrolowania tych robaków, związki (16), (17) wzbudziły szerokie zainteresowanie chemików. Celem ich stało się opracowanie odpowiedniej metody dla syntetyzowania docelowego związku o wysokiej chemicznej i izomerycznej czystości, aby dostarczyć wystarczające ilości czystych materiałów do laboratoryjnych bioanaliz i testów na polach.
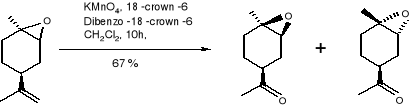
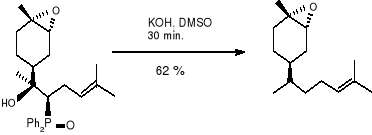
Dogodne syntezy związków (16), (17) przeprowadzono w trzech etapach z dostępnego w handlu tlenku (-) -limonenu, SCHEMAT 1. Największym wyzwaniem w budowie obu związków (16), (17) było kontrolowanie sterochemii trójpodstawionego podwójnego wiązania. Aby ustalić wymaganą Z- sterochemię opracowano alternatywny szlak, który wykorzystał stabilność półproduktów utworzonych w reakcji Hornera -Wittinga. Syntezę rozpoczęto od tlenku limonenu (18) dostępnego w handlu jako 42: 58 mieszaniny α i β -epoksydów. Jej utlenienie w obecności katalizatora międzyfazowego przeniesienia dało epoksyketony (19a), (19b). W przypadku gdy katalizatory zostały użyte samodzielnie, powodowały niecałkowitą konwersję. Jednakże, gdy użyto mieszaninę 18 -crown -6 i dibenzo -18 -crown -6 utlenienie było całkowite dając (19a) i (19b). (58: 42) z całkowitą wydajnością 67 %. Powstała mieszanina związków została następnie rozdzielona metodą chromatografii, a każdy izomer został z osoba poddany analitycznej reakcji, co można przedstawić w następujący sposób:
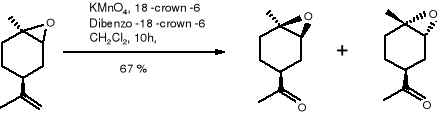
(18) (19a) (19b)
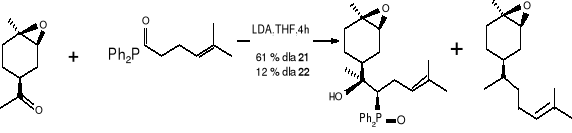
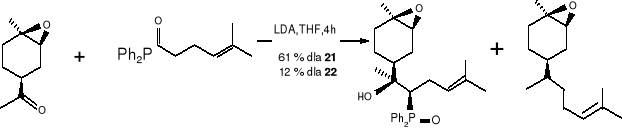
(19) (20) (21) (22)
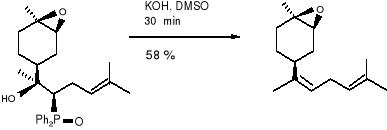
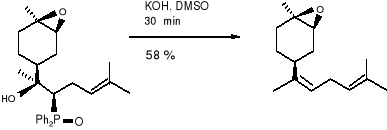
(21) (16)
SCHEMAT 1.
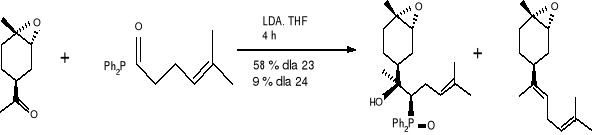
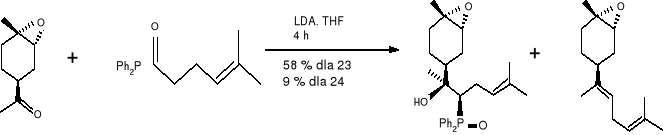
(19) (20) (23) (24)
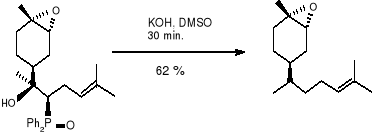
(17)
Otrzymany (E) -(1R, 2S, 4S) -epoksybisabolenen (22) okazał się produktem drugorzędnym. Jednakże wybór zasady był bardzo istotny, gdyż z n -butylliten wydajność była słabsza i większość przereagowanego ketonu (19a) była receniczna przy C -4. Następnie katalizowana zasadą (KOH) eliminacja kwasu olifenylofosfanowego z (21) była wysoce steroselektywna. Reakcja ta była bardzo wrażliwa na zastosowane warunki, ze względu na możliwość tworzenia się nieporządanych izomerów. Tak więc po długich doświadczeniach z różnymi zasadami, temperaturami, określono optymalne warunki dla eliminacji. Są to: szybkie dodawanie sproszkowanego (KOH) do roztworu (21) w DMSO, w temperaturze pokojowej i chłodzenie reakcji poprzez dodawanie lodowatej wody gdy tylko wszystkie materiały początkowe zostały zużyte (ok. 30 minut). W tych oto warunkach czysty cis (Z) -epoksybisabolen (16) został uzyskany przy 58 % wydajności, wolny od niepożądanych cis- (E)- izomerów, czy innych diasteroizomerów.
W analogiczny sposób trans -(Z) -epoksybisabolen (17) i jego (E) -izomer (23) były przygotowywane z α -epoksy ketonu (19b) - co przedstawiłam również na schemacie. 9
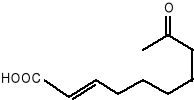
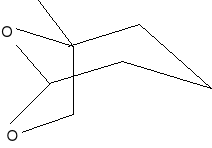
Kolejną syntezą, którą przedstawię będzie synteza (-)-Serricorninu.
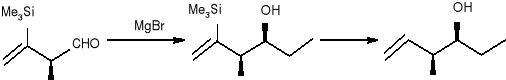
Ten atraktant seksualny wyizolowano z wnętrza żuka (Lasioderma, serricorne F.), który jest głównym szkodnikiem liści tytoniu. Całkowita sterochemia została ustalona jako (4S, 6S,7S) -izomer (25) o łańcuchu otwartym. Obecnie w skutek handlowego znaczenia serricorninu obserwuje się wiele jego syntez. Jedna z nich rozpoczyna się od czynnego optycznie aldehydu (26), który może być otrzymać metodą Sharplesa, reagującą następnie z odczynnikiem Grinarda dając syn- alkohol (27), który może być łatwo skonwertowany do (28): 9
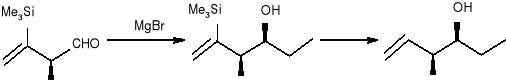
(26) (27) (28)
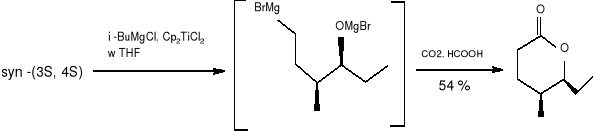
Następnie ten optycznie czysty związek (27), [syn- (3S, 4S)] poddano dalszej transformacji:
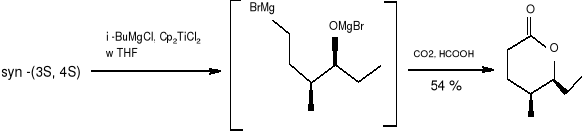
(29)
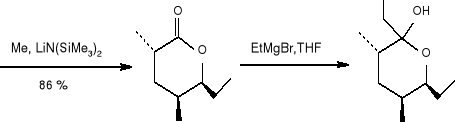
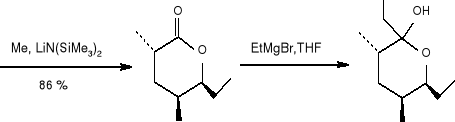
(30) (31)
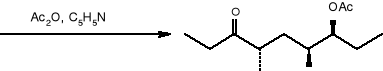
(25)
Jeżeli Ac=H to jest to 4,6 -dimetylo -7 -hydroksynona -3-on.
Nie tylko działają na owady, związki chemiczne wydzielone przez nie same. Również przyciągająco na nie mogą działać substancje pochodzące np.: z kwiatów, owoców, grzybów, itp.
Z tego względu chciałabym przedstawić: Enancjoselektywną syntezę każdego steroizomeru piranowych tlenków linalolu: szlak geraniolu.
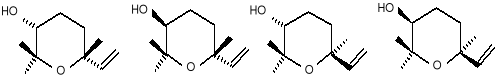
Cztery tlenki linalolu (32) (3R, 6R), (33) (3S, 6R), (34) (3R,6S), (35) (3S,6S) tj.:
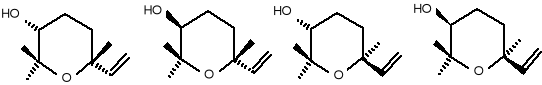
(32) (33) (34) (35)
Te różne mieszaniny steroizomerów stwierdzone zostały jako składniki wielu zapachów kwiatów i owoców, takich jak winogrona i owoce Carica papaya. Nawet jako niewielkie składniki tych aromatów, uważa się, że związki chemiczne (32 -35) są ważnymi elementami dla szczególnego „charakteru” lub „nuty” danego zapachu. Dodatkowo, mają one prawdopodobnie duże znaczenie biologiczne w określonych systemach zapylania, działając przyciągająco na owady. Interesujące jest też, że 2,2 , 6,6 -czteropodstawiony pierścień piranowy jest także spotykany w kilku naturalnych produktach morskich jak również w naziemnych metabolitach grzybów.
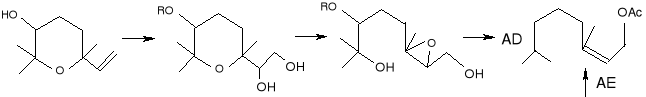
Opierając się o ogólną retrosyntetyczną analizę pokazaną na schemacie:
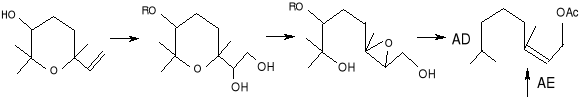
(36) (37)
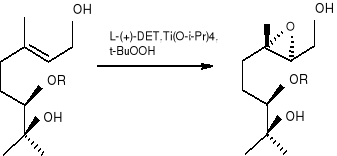
każdy steroizomer piranowych tlenków linalolu (32-35) może stać się osiągalny poprzez sterospecyficzny 6 -exo- tet hydroksyepoksydowe otwarcie odpowiedniego półproduktu (36). Podejście do związku (36) zostało oparte na tzw. „nagiej” strategii szkieletu węglowego, np.: selektywne umieszczanie sterochemicznie określonych funkcji tlenu na nagim nienasyconym szkielecie węgla. Dla uzyskania tego celu użyto Sharpless katalityczną, asymetryczną dihydroksylację (AD) i asymetryczną epoksydację (AE) reakcji, które pozwoliły na sterokontrolowaną funkcjonalizację prostereogenicznych olefin w wysoce przewidywalny sposób, zależąc od użytej chiralnej ligandy.
Korzystając z tego samego związku wyjściowego, np.: „nagiego” szkieletu węgla octanu geranylu (37), który już zawiera wszystkie atomy węgla docelowych produktów. Najpierw reakcja (AD)została wykorzystana, aby dlihydroksylować odległe podwójne wiązanie (38) i potem reakcja (AE) została użyta by epoksydować alliliczne podwójne wiązania.
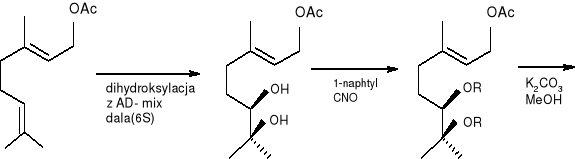
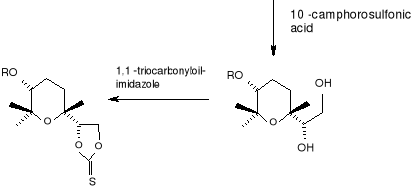
Uproszczoną ścieżkę syntezy tlenu linalolu (32) można przestawić następująco: 11
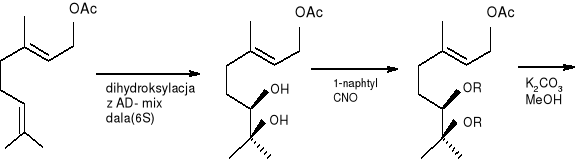
(6R) (38) (6R) (39)
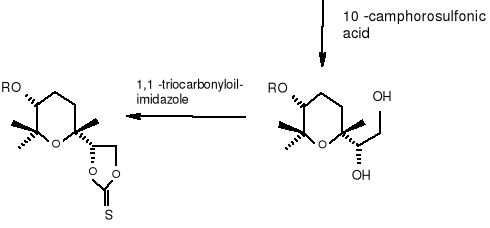
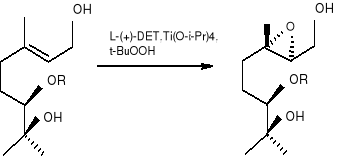
(6R)(40) (2S, 3S, 6R) (36)
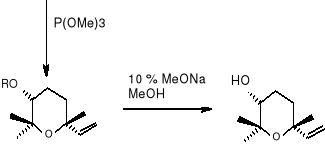
(3R, 6R, 1S) (42) (3R, 6R, 1S) (41)
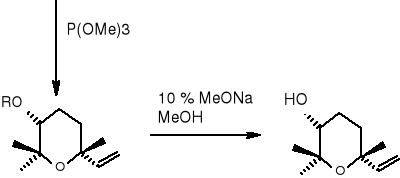
(3R, 6R) (43) (3R, 6R) (32)
Tlenek linalolu.
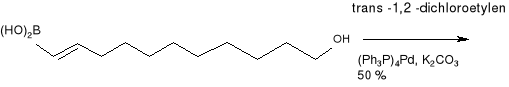
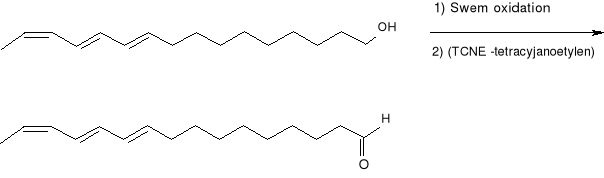
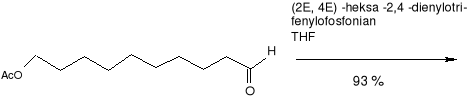
Innym przykładem może być: Preparatywna synteza izomerycznie czystego (10E, 12E,14Z) -i -(10e,12e, 14e) -heksadeka 10, 12, 14 -trienalu, Feromonu płciowego (Manduca Sexta).
Rogatek tytoniowy ćmy, Manduca sexta (Lapidoptera: Sphingidae) jest szkodnikiem tytoniu i innych psiankowatcych. Pierwsze lata badań nad atraktantem płciowym tego szkodnika przyniosły wiele trudności, wskutek dużej liczny składników tych gruczołów feromonowych (12 nasyconych i jedno- ,dwu- i trzy nienasyconych aldehydów). Jednak wskutek wielu syntez odkryto, że istnieją dwa związki o właściwościach wabiących, są to: (10E, 12E, 14Z) -heksadeka -10, 12, 14 -trienal (44) i jego (10E, 12E, 14E) -izomer (45). Kiedy poznano struktury tych związków, rozpoczęto ich syntezy, które miały na celu zdobycie bardzo wysokiej chemicznej i izomerycznej czystości tych związków o działaniu selektywnym, w celu dostarczenia czystych materiałów do opracowania pełnej mieszanki feromonów dla M. Sexta.
Syntezy tych związków można przedstawić w prosty sposób na poniższych schematach:
SCHEMAT 2.
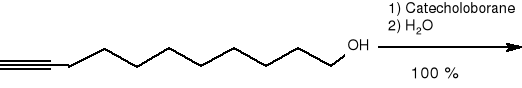
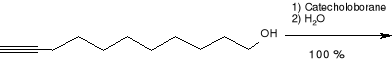
Synteza (10E, 12E, 14Z) -heksadeka -10, 12, 14 -trienalu (44)
10- undecyno -1 -ol.
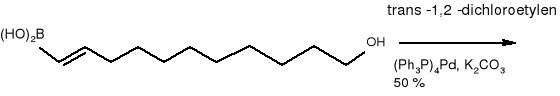
Kwas (E) -11 -hydroksy -1 -undecyloborowy.
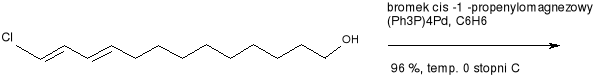
Chlorodienol
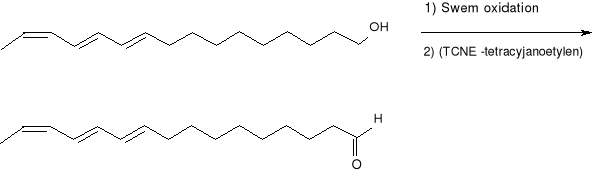
(44) (10E, 12E, 14Z)- heksadeka -12, 10, 14- trienal
(czystość izomeryczna >99 %)
SCHEMAT 3.
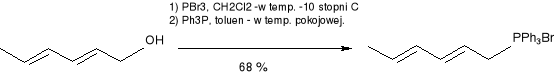
Synteza (10E, 12E, 14E) -heksadeka -10, 12, 14 -trienalu (45)
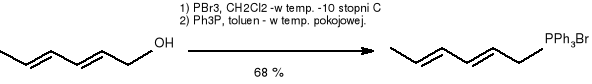
(2E, 4E) -heksa -2,4 -dien -1 -ol bromek -(2E, 4E) -heksa -
(alkohol sorbionowy) 2, 4- dienylotrifenylofosfonianu
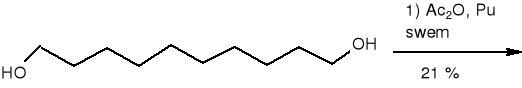
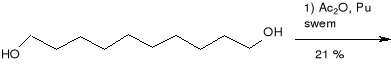
1,10 -dekandiol
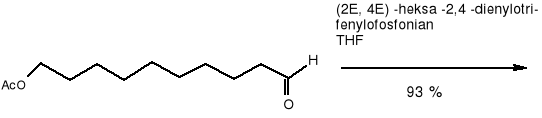
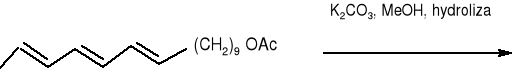
octan -10, 12, 14 -heksadekatrienylu
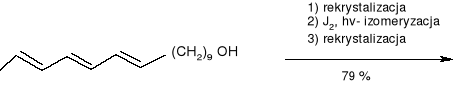
(EEE: ZEE=64: 39)
(10E,12E, 14E) -heksadeka- 10, 12, 14- trienol
(alkohol surowy)
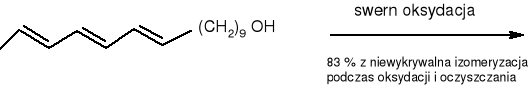
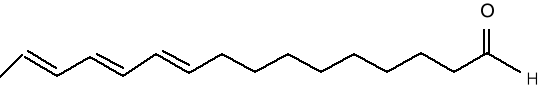
(45) (10E, 12E, 14E) -heksadeka -10, 12, 14- trienal.
Syntezy te świadczą o tym, że obydwa związki, cechują się wysoką czystością sterochemiczną, są one również łatwo rozdzielane od wszystkich steroizomerów i składników chemicznych.. 12
FEROMONOWE PUŁAPKI NA SZKODNIKI.
Ludzie starają się zmniejszyć straty żywności, stosując między innymi insektycydy, które niestety często są toksyczne nie tylko dla owadów -szkodników ale i dla owadów pożytecznych, a także dla organizmów wyższych, łącznie z ludźmi. Dlatego dużą nadzieją w walce ze szkodnikami pokłada się feromonach działających w niskich stężeniach, najczęściej nieszkodliwych dla środowiska i większości organizmów. Mogą one zapewnić zwalczanie ściśle określonego gatunku owadów, w wybranej fazie rozwoju, w dowolnym czasie, a więc korzystnie już na początku sezonu ich występowania, co zapewnia zwalczanie szkodników jeszcze przed stadium rozrodczym i intensywnym żerowaniem. Stosowane związki feromonowe są tak specyficzne, że za ich pomocą można też sprawdzić, czy na danym obszarze występują określone gatunki owadów, a nawet i w jakich ilościach.
Stężenia feromonów w pułapkach są na ogół większe niż w naturze, co powoduje zagłuszenie źródeł naturalnych, dezorientację odbiorców i kierowanie ich do pułapek nawet ze znacznych odległości. O skuteczności takich pułapek decyduje przede wszystkim właściwe dozowanie feromonów, gdyż zbyt małe czy duże stężenia mogły by wywołać niepożądane reakcje odbiorców. Urządzenie dozujące (dyspenser) powinno wiec zapewniać określone, stałe stężenie feromonu w pobliżu pułapki oraz długi czas jej działania. Do najczęściej stosowanych dozowników należą elementy o mikroporowej strukturze, np.: wiązki kapilar, włókna kapilarne, laminowane krążki, pakunki bibułowe, plastykowe porowate opaski lub ziarna, bądź pojemniki zamknięte porowatymi błonami o różnej przepuszczalności. Budowa pułapek zależy też od ich przeznaczenia, wielkości i czasu działania. Najprostsze przypominają znane lepy na muchy, a więc są taśmami lub opaskami pokrytymi substancjami klejącymi zawierającymi feromon. Bardziaj skomplikowane są urządzeniami przestrzennymi (np.: puszkami) o różnej pojemności z wejściem w kształcie lejka uniemożliwiającym wyjście. 7
Obecnie można wyróżnić wiele pułapek feromonowych o różnej specyfice działania.
Coraz bardziej powszechne stają się feromony umieszczone w specjalnych pułapkach z klejem w celu przywabienia i zatrzymania samców określonego gatunku. Dzięki tej metodzie można stosunkowo wiarygodnie ocenić wielkość populacji szkodnika na danym terenie. Przykładem tej metody może być doświadczenie jakie przeprowadzili naukowcy z Uniwersytetu z Wisconsin. Zastawili oni pułapki z drutu posmarowanego gęstym klejem. W każdej z nich umieścili jako przynętę samiczkę owada (Diprion similis). Do pułapek, w których samiczki wydzielały wabik (po jednej samiczce w każdej pułapce) przyleciało przeciętnie po tysiąc samców do każdej pułapki. Jedna wyjątkowa samiczka przywabiła aż jedenaście tysięcy samców w ciągu ośmiu dni, przy czym ostatnie trzy dni była martwa.
Innym sposobem wykorzystania feromonów jest metoda polegająca na dezorientacji samców szkodnika, w okresie w którym starają się odnaleźć samice w celu kopulacji. Na obszarach chronionych tą metodą tuż przed wylotem określonego szkodnika np.: w sadach, owocówki jabłkóweczki, zawiesza się na gałęziach drzew w podobnych odległościach bardzo dużo -ok. 500 szt. emiterów z feromonami samic. Feromony te powinny być równomiernie wydzielane do środowiska przez cały okres lotu owada. Na skutek tego samce wyczuwając wszędzie obecność samic nie potrafią ich zlokalizować. Nie dochodzi do kopulacji i składania jaj przez samice. W roku 1996 po zastosowaniu tej metody w południowym Tyrolu we Włoszech ilość robaczywych owoców w sadach nie przekroczyła 1 %.
Wysoce selektywną metodą jest połączenie feromonów z preparatami owadobójczymi. Pułapki takie najpierw szkodnika przywabiają, a następnie zabijają. Z metody tej skorzystała firma Ciba -Geigy, która wyprodukowała do zwalczania owocówki jabłkóweczki preparat o nazwie handlowej Sirene C. M., który w swym składzie zawiera oprócz feromonu także insektycyd. Preparat ten nanoszony jest na liście jabłoni przy pomocy specjalnego dozownika, w postaci pojedynczych kropel (trzy krople na drzewo w sadzie składającym się z tysiąca drzew). Wysoka skuteczność tego preparatu utrzymuje się przez 5 -6 dni. Poleca się go stosować dwukrotnie w sezonie.
Podobna metoda selektywnego zwalczania przy pomocy feromonów opracowana została niegdyś w Czechach. Do pułapek z feromonami, bez podłogi klejowej dodawane są preparaty wirusowe. Samce przylatujące do pułapek zostają zarażone i rozprowadzają je wśród innych osobników własnej populacji. Wstępne wyniki badań wskazują, że skuteczność tej metody wynosi 40 -85 %. 4
Wyłoniła się jeszcze jedna interesująca możliwość. Wykryto substancje chemiczne mające zdolność sterylizowania owadów bez ich zabijania. Jak stwierdzono substancje te mają bardzo silne działanie, dużo silniejsze od wielu stosowanych środków owadobójczych, a przy tym nie muszą być one rozpylane wszędzie, jak to ma miejsce w przypadku insektycydów. Gdy do tych środków wprowadzi się, np.: wabik seksualny, owady zostaną zwabione do pułapek, a po uwolnieniu nawet gdy spotkają samiczkę nie będą w stanie jej zapłodnić. Metoda ta nie tylko jest bardziej skuteczna ale i bezpieczna dla środowiska. 6
W trakcie badań nad feromonami w celu wykorzystania ich do zwalczania szkodników, okazało się, że wydzielane przez nie substancje w celu komunikowania się osobników tego samego gatunku, często przywabiają ich naturalnych wrogów. Substancje takie zsyntetyzowane w laboratoriach mogą więc zwiększyć skuteczność zwalczania biologicznego, umieszczenie ich na obszarach zagrożonych w celu sprowadzenia gatunków, które nie są szkodnikami dla upraw, a skutecznie eliminują szkodniki.
Owady wydzielają również feromony znaczące, np.: w celu zabezpieczenia jaj. W Szwajcarii stwierdzono, że nasionica trześniówki po złożeniu jaj w dojrzewające czereśnie wydziela substancję chemiczną informującą inne samice tego samego gatunku, że ten owoc jest już zajęty i nie należy składać w niego innych jaj bo to groziłoby, że ich wylęgnięte larwy nie będą mogły zakończyć swojego rozwoju. Substancję tą udało się zidentyfikować i wyprodukować. Na drzewach opryskanych tą substancją tuż przed lotem nasionicy samice nie składały jaj. Znacznik ten działał więc jako pewnego rodzaju pożyteczny repelent, nie szkodliwy dla środowiska i fauny. 4
ZAKOŃCZENIE.
Jak widać z wyżej przytoczonych przykładów już obecnie semiozwiązki w postaci feromonów znajdują praktyczne zastosowanie w wielu krajach. Jednak rozwój badań nad tymi silnie działającymi i wysoce specyficznymi wabikami jest w pewnym stopniu hamowany właśnie przez fakt, że działają one tak silnie. Tak mało wystarcza na tak wiele. Na przykład Departament of Agriculture w USA zużywa tylko ok. 500 kg substancji wabiącej „Medfly” w ciągu roku, a 50 kg syntetycznego środka wabiącego brudnicę wystarcza do obsłużenia 30 000 pułapek rocznie. Znaczy to, że popyt na te środki jest bardzo niewielki. Przemysł bardzo niechętnie traci wielki sumy na rozwój badań dotyczących związków chemicznych, na które nie ma zapotrzebowania w tonach lub cysternach. Stąd większość badań prowadzi się w laboratoriach państwowych dla „celów czysto naukowych”. 6
Myślę jednak, że stan taki chyba dość prędko ulegnie zmianie. Nastąpi to zapewne z chwilą, gdy zaczniemy traktować własności wabiące tych substancji jako cechę drugorzędną, a zwrócimy uwagę przede wszystkim na ich znaczenie jako środków rozpoznawczych. Dopiero wtedy ukażą się nowe możliwości wykorzystania tych związków. Należy również przekonać producentów rolnych do zalet feromonów jako skutecznych środków pielęgnacji upraw i roślin, a przede wszystkim nie zagrażających środowisku naturalnemu i co za tym idzie również człowiekowi.
LITERATURA.
R. W. Mysłajek, Odporne szkodniki, Zielone Brygady -Pismo Ekologów 1998, nr 4, 106 -(internet).
Odporne szkodniki, Zielone Brygady -Pismo Ekologów 1996, nr 3, 87. -(internet).
W. Seńczuk, Toksykologia, Państwowy Zakład Wydawnictw Lekarskich, Warszawa 1990.
E. Niemczyk, Przyszłość w ochronie sadów przed szkodnikami, Agrosan 1995- (internet).
E. Acree, M. Soderlund, Semiochemistry Flavors and Pheromones, Walter de Grugter -Berlin -New York 1985.
R. H. Wright, Nauka o zapachu, PWN, Warszawa 1972.
A. Kołodziejczyk, Feromony 1998 -(internet).
M. Jacobson, W. A. Jones, J. Org. Chem. 1962, 27, 2523- 2524.
G. Millar, Synthesis 2000, 269 -272.
B. Ferreira, J. Tercio, A. Marques, Tetrahedron: Asymmetry 1994, Vol. 5, 641 -648.
G. Vidari, A. Rosa , F. Castronovo, G. Zanomi, Tetrahedron: Asymmetry 2000, 11, 981 -989.
G. Millar, Synthesis 2000, 113 -118.
S. Kuwahara, W. S. Leal, O. Kodama, Tetrahedron 1986, 54, 11421 -11430.
M. Mori, T. Chuman, M. Kohno, M. Noguchi, Tetrahedron Letters 1982, Vol. 23, 667 -670.
B. Snider, D. Rodini, Tetrahedron Letters 1978, 16, 1399 -1400.
K. Mori, H. Nomi, Tetrahedron Letters 1981, Vol. 22, 1127 -1130.
F. Sato, Y. Takeda, Y. Kobayashi, Tetrahedron 1986, Vol. 42, 2937 -2943.
T. Umiński, Ekologia -środowisko -przyroda, PWN, Warszawa 1996.
B. Nogy'e, Atlas szkodników i chorób roślin sadowniczych, Państwowe Wydawnictwo Rolnicze i Leśne, Warszawa 1972.
9
![]()
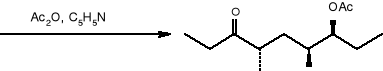
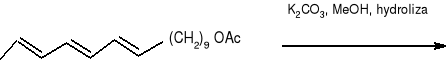
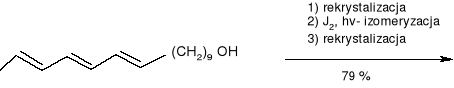
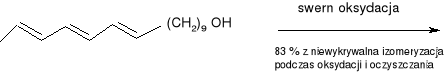
Wyszukiwarka
Podobne podstrony:
Ochrona Środ. Biochemia, Ekologia
Cykle biochemiczne, Studia, 1-stopień, inżynierka, Ochrona Środowiska, Ekologia
Zarys Ekologii biochemicznej, Ekologia
Ekologia biochemiczna częściowe opracowanie na koło, Studia, Ochrona środowiska
Różnorodność biologiczna, bio-chem-eko, Ekologia biochemiczna
Podstawy ekologii biochemicznej
Czynnik środowiskowy, a czynnik ekologiczny
Pedagogika ekologiczna z uwzględnieniem tez raportów ekologicznych
Określenie terminu ekologia Podział ekologii z uwzględnieniem
EkologiaIOchronaSrodowiska Wyklad 2
Wykład 3 polityka ekologiczna
6Hydrobiologia Formacje ekologiczne
EKOLOGIA!
pojazdy ekologiczne(1)
Wielkie katastrofy ekologiczne
więcej podobnych podstron