chemia cw3 3

Zmierzoną w doświadczeniu objętość wodoru należy traktować orientacyjnie. W dokładniejszych pomiarach powinno się uwzględnić prężność pary wodnej nad roztworem w biurecie oraz hydrostatyczne ciśnienie słupa cieczy w biurecie.
Ćw. 2. - Pomiar SEM stężeniowego ogniwa korozyjnego.
|
Qg |
niwo |
SEM [VI |
|
Fe 1NaCI |
Fe |
\WkO |
|
Fe I NaCI |
CN O ef Li. |
• Określić wpływ doprowadzonego powietrza (tlenu) na SEM ogniwa.............................................
jftjjjjj PjŁMsT*.....u jdlfelfg/'......
• Określić, która elektroda jest katodą, a która anodą ogniwa korozyjnego......................................
-łoftojm-................ **fGP*'
• Podać różnice w wyglądzie katody i anody ogniwa korozyjnego....................................................
AfĄ yy.p.7 iirLL ^ Stf ^DZ>f
Ćw. 3. - Ochrona protektorowa.
• Na podstawie zabarwienia roztworu określić w którym przypadku szybkość korozji żelaza jest największa?
• W toku badania można także zaobserwować wydzielanie się gazu (wodoru) - na którym metalu zachodzi reakcja wydzielania wodoru i z jaką szybkością?
• Który metal jest protektorem w przypadku b) i c)?
|
metale |
Intensywność barwy |
Szybkość korozji |
Wydzielanie wodoru |
Protektor |
|
Fe |
nA-tB | |||
|
Fe-Zn | ||||
|
Fe-Cu |
Pu 2 A |
-fe |
Ćw. 4. - Cynkowanie elektrolityczne
• Obliczyć teoretyczny przyrost masy cynku na precie stalowym po cynkowaniu ze wzoru:
mz» = k ■ i • t=........................
gdzie: k = 1,22 [g/Ah]
I - natężenie prądu [A]
T - czas cynkowania [h]
• Obliczyć wydajność prądową procesu cynkowania w % jako stosunek przyrostu masy próbki cynkowanej do teoretycznej ilości wydzielonego cynku obliczonej z I prawa Faraday'a.
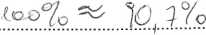
W = (Am/ mz„) 100% =
O O £2«3
|
Pow. elektrody |
Czas |
Masa przed |
Masa po |
Am |
mzn obi. z |
Wydajność | |
|
s |
cynkowania t |
cynkowaniem |
cynkowaniu |
[g] |
prawa Faradaya |
procesu | |
|
[dm2] |
[h] |
mi [g] |
m2 [g] |
[g] |
[%] |
Wyszukiwarka
Podobne podstrony:
chemia cw3 3 Zmierzoną w doświadczeniu objętość wodoru należy traktować orientacyjnie. W dokładniejs
chemia cw3 3 Zmierzoną w doświadczeniu objętość wodoru należy traktować orientacyjnie. W dokładniejs
0000027 (7) towych (utrzymanie siły) około 20%. Wymienione proporcje należy traktować orientacyjnie
08 09 4. Do pomiaru osnowy należy zastosować sprzęt o dokładnościach pomiaru odleg
IMG585 (3) 272 (De)Konstrukcje kobiecości przychylny stosunek do marksizmu. Uważa raczej, że należy
IMG762 W istocie rzeczy, celu tego nie należy traktować jako jeszcze jednej zdobyczy, którą chcemy w
skanowanie0056 Ćwiczenie statyczne - należy traktować jako formy pozycji wyjściowych do ćwiczeń dyna
Egzamin maturalny z chemii Poziom podstawowyZadanie 20. (2 pkt) Oblicz, jaką objętość wodoru, w prze
Zgodnie § 271.13 Rozporządzenia [1] Otwarte składowisko, ze względu na usytuowanie, należy traktować
IMGP0663 Glebę należy traktować nie tylko jako podłoże wzrosn rozwoju roślin, ale przede wszystkim j
Przykłady ćwiczeń umieszczone w poszczególnych działach tematycznych programu należy traktować jako
więcej podobnych podstron