PrepOrg II048 (2)

50
rze 204-207°. Wydajność 6,1 g (80% ilości teoretycznej). Pozostawiony po ekstrakcji eterem roztwór wodny benzoesanu potasu wlewa się do mieszaniny 40 cm* stężonego kwasu solnego, 40 cm* wody i 50 g drobno pokruszonego lodu. Wytręcony osad kwasu benzoesowego odsącza się na lejku sitowym, przemywa małę ilościę wody i krystalizuje z wrzącej wody. Otrzymuje się 8,6 g (około 100% ilości teoretycznej) produktu o temperaturze topnienia 121°.
Uwagi;
Sposób oczy
1. Aldehyd benzoesowy nie może zawierać kwasu benzoesowego.
szczania handlowego aldehydu benzoesowego: 30 g aldehydu przemywa się w rozdzielaczu kilkoma porcjami po 10 cm'* 10% roztworu węglanu sodowego, aż do zaprzestania wydzielania się dwutlenku węgla, następnie przemywa się wodę i suszy bezwodnym siarczanem magnezowym (3 g), dodaje się około 0,1 g hydrochinonu (dla zabezpieczenia przed samoutlenieniem aldehydu benzoesowego). Surowy aldehyd sączy się przez mały sęczek karbowany do kolby Claisena 1 destyluje zbierajęc frakcję w temperaturze 79°/25 mm Hg (69°/15 mm Hg, 62°/10 mm Hg, 17B°/760 mm Hgf.
13. ALKOHOL o-NITROBENZYLOWY
Sprawdził: R. Mazurkiewicz
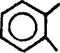
H + ((CH3)2CH0)3A1 + 3NaOH
NO'-
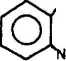
,CH20H
+ 3CH3-(i-CH3+Na3A103
li
W kolbie o pojemności 250 cnr zaopatrzonej w kolumnę Vigreux o długości 40 cm lub innę o podobnej sprawności i chłodnicę Liebiga umieszcza się roztwór izopropanolanu glinu w izopropanolu otrzymany z 2 g glinu (uwaga l) oraz 20 g aldehydu o-nitrobenzoeśowego. Mieszaninę reakcyjnę ogrzewa się z takę lntensywnościę, by temperatura destylujących par nie przekroczyła 60°. w clęgu 3-4 godzin oddestylowuje aię w ten sposób znacz-nr część powstającego w reakcji acetonu."
Po oddestylowaniu acetonu usuwa aię kolumnę rektyfikacyjną 1 oddeaty-lowuje się nadmiar lzopropanolb' ogrzewając kolbę w łaźni wodnej pod zmniejszonym ciśnieniem.
Pozostałość wylewa się do 100 cm* wody 1 alkalizuje 10% roztworem wodorotlenku sodowego do rozpuszczenia związków glinu, przy czym wydziela
'l mm Hg - 1,332 hPe.
Wyszukiwarka
Podobne podstrony:
22687 PrepOrg II068 (2) 70 trzu. Otrzymują się 14,0 g (78,0% ilości teoretycznej) benzylidenoaniliny
115/50 » "Roczn. Tow. Nauk. Warsz.", s. 204 - 207. - Z. LICHNIAK. "Dziś i Jutro"
ptaki I Perkoz dwuczubyPodiceps cristatus, C Perkoz len ma około 50 cm długości, rozpiętość skrzydeł
66481 P6150210 Typowe parametry respiratora Częstotliwość oddechów 5-50 c/min Ciśnienie oddechowe ~
nie substancji w eluacie, można uzyskać ponad 50-cio krotny wzrost wydajności kolumny). Ograniczenie
100 § 50 5 30 20 10 90 80 70 ^ 60 Rysunek 2 Przykładowa charakterystyka
termo Do reaktora uprowadza sic 50 moli mm mieszanin;, o ■** • ■! z i J" ‘ benzenu i 80 % molow
PrepOrg II078 (2) - 80 - kładnie wodę i odciska. Po krystalizacji z rozcieńczonego wodę metanolu (2:
i L DKRES DO II LATA 50-TE LATA 70-TE I 80-TE LATA 80-TE I 90-TE WOJNY ŚW. I
Wydruk programu z tej wizyty 150 140 130 120 110 100 90 80 70 60 50 40 30 20 1041.80 -Ji
DSC01274 - Wydajność • 80% redukcji zawiesin w procesie osadu czynnego (~ 10 -25 m
więcej podobnych podstron