skan0275
278 Elektrochemia
*i_ 1000
x2 m Mi
więc
ln
a2(B)
02(4)
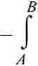
1000
mM\
d\nai = S.
Całkowanie wykonujemy graficznie, metodą trapezów w arkuszu kalkulacyjnym (zob. tab. 6.3). Znaleziona stąd wartość S wynosi 10,1754.
Tabela 6.3
|
m |
x2 |
Ap |
o\ |
ln z/! |
x\lx2 |
Z |
|
0,506 |
9,033 • 10“3 |
17 |
0,977632 |
-0,02262 |
109,7 |
- |
|
1,027 |
1,817 • 10-2 |
39,8 |
0,947632 |
-0,05379 |
54,05 |
-2,55184 |
|
2,114 |
3,669 • 10-2 |
95,3 |
0,874605 |
-0,13398 |
26,26 |
-3,22007 |
|
3,296 |
5,605 • 10-2 |
166,6 |
0,780789 |
-0,24745 |
16,84 |
-2,44518 |
|
4,555 |
7,584 • 10“2 |
241,5 |
0,682237 |
-0,38238 |
12,19 |
-1,95835 |
|
wartość całki = |
-10,1754 | |||||
Zależność funkcji podcałkowej xx/x2 od In^j przedstawiono na rys. 6.2.
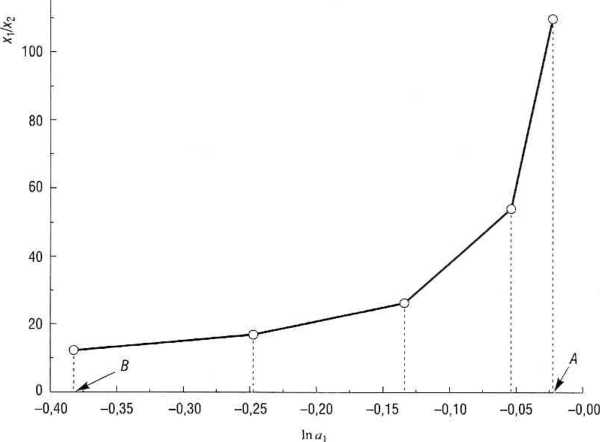
Rys. 6.2
Wyszukiwarka
Podobne podstrony:
skan0265 268 Elektrochemia A = K 1000 c [S - cm2 ■ mol *]. (6.12) Obecnie spotyka się równolegle obi
skan0284 287 Elektrochemia Jeśli zapisać E°(T) = a0 + axT + a2T2 + a2T3, to (dE°\~w)p = a +2aiT+^T =
skan0297 300 Elektrochemia 300 Elektrochemia ^nh4oh aNH4 pA b = pOH + lg skąd, po uwzględnieniu (6.6
skan0299 302 Elektrochemia ba rodzajów cząstek, które należy wziąć pod uwagę, wynosi 5 (ET, OH-, HA-
39748 skan0283 286 Elektrochemia Poza stanami równowagi 286 Elektrochemia oraz AG = -nFE, dE dT ,p A
skan0281 284 Elektrochemia dla kilku molalności m w temperaturze 25°C wynosi m ■ 103 [mol • kg
skan0289 292 Elektrochemia Tabela 6.9 i /[M] Ig y± y± c [M] A ■, = C/_! - Ci 1 1,889 •
skan0277 280 Elektrochemia z którego można łatwo obliczyć wartość A. Dla wody w 25°C statyczna przen
skan0279 282 Elektrochemia -Pt, H2(l bar)
więcej podobnych podstron