skan0310

Elektrochemia 313
skąd otrzymujemy
«a
8,314-298,15 96485 • 0,04136
0,621.
Z kolei
RT
aaF
ln j0 = -0,0857 V.
Zatem mamy
, . 0,0857 ^ _
lnjo~ 0,04136 _2’07-’
jo = 7,94 A - m-2. ■
W metodach elektrochemicznych stosowanych w dyfuzyjnej kinetyce elektrodowej ważne są procesy dyfuzji jonów opisane równaniami Ficka.
I prawo Ficka
^Ox(*, 0 = -D -^- (6.99)
określa, że przepływ substancji Ox, ./0x(x, /) jest proporcjonalny do gradientu jej stężenia.

Rys. 6.6
W warstwie dyfuzyjnej o grubości ó (zob. rys. 6.6) gradient ten możemy określić wyrażeniem
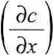
c(0, t)-c0
r
(6.99a)
Wyszukiwarka
Podobne podstrony:
66861 skan0052 Termodynamika chemiczna 55 W = -nRTl ln P Pl = -3-8,314-298,15- In 100 120 = 1355,83
63960 skan0295 298 Elektrochemia a stąd (6) _ (^soli (-H+) aAc~~ ę ® );± •>
skan0300 Elektrochemia 303 Wykorzystując warunek elektroobojętności (5) oraz równania (3) i (7), otr
84590 skan0304 Elektrochemia 307 otrzymamy całkowite stężenie ołowiu c c = [Pb2+] + [PbCl+] + [PbCl2
img014 (13) El. Wyznaczanie oporu elektrycznego metodą mostka Wheatstone ’a 1/3 El. Wyznaczanie opor
Toruń : Zakład Energetyczny Toruń SA, 1998. - 298 s.: il.; 29 cm 621.311(438)(091) ELEKTROWNIE; HIST
Skąd otrzymujemy dU = kxdx. Korzystając ze wzoru xdx = d(x2)/2, znajdujemy dU = d(-kx2). 2 A zatem (
skan0289 292 Elektrochemia Tabela 6.9 i /[M] Ig y± y± c [M] A ■, = C/_! - Ci 1 1,889 •
więcej podobnych podstron