80821 skanuj0005

Oksydazy fenolowe - przenoszą elektrony i protony z orto- lub para-dwufenoli na tlen. Oksydaza o-dwufenolwa poza utlenianiem o-dwufenolu katalizuje także reakcję hydroksylacji
Oksydaza cytochromowa_(EC 1.93.1) - końcowe ogniwo łańcucha transportu elektronów zlokalizowanego w wewnętrznej błonie mitochondriów
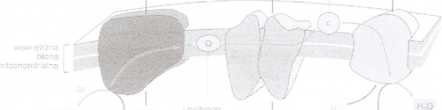
Łańcuch oddechowy katalizuje transport elektronów z NADH-H+ lub zredukowanego ubichi-nonu na tlen cząsteczkowy. Ubichinon może być redukowany enzymatycznie w reakcjach, w których np. utleniany jest bursztynian bądź flawoproteina (ETF) redukowana przez dehydrogenazę acy-lo-CoA, dehydrogenazę 3-fosfoglicerynianu lub dehydrogenazy utleniające cholinę czy dihydrooro-tan. Większa część energii towarzysząca reakcjom redoks wykorzystywana jest do formowania w poprzek wewnętrznej błony mitochondrialnej gradientu protonowego, który z kolei napędza syntezę ATP katalizowaną przez syntazę ATP. Łańcuch oddechowy obejmuje 3 białkowe kompleksy (kompleks 1, HI i IV) oraz dwie cząsteczki przenośnikowe: ubichinon (Q) i cytochrom c (Ryc. 3). Poza tym, z błoną wewnętrzną związana jest dehydrogenaza bursztynianowa (kompleks II) oraz inne dehydrogenazy przekazujące elektrony na ubichinon (Q) (nie pokazano na Ryc. 3 ).
MIĘDZY BŁONOWA
HKS issa }
Ryc. 3. Transport elektronów w łańcuchu oddechowym utworzonym przez trzy kompleksy białkowe i dwa ruchome nośniki (ubichinon i cytochrom c) przenoszące elektrony z utlenianego substratu na tlen. Transportowi elektronów wzdłuż łańcucha oddechowego towarzyszy wektorowe pompowanie protonów z matriks do przestrzeni międzybłonowej (Alberts i wsp. 1999)
Oksydaza cytochromowa przejmuje elektrony z małego białka - cytochromu c - zawierającego żelazo w układzie hemowym i przekazuje je na tlen cząsteczkowy (Ryc. 3). Do redukcji cząsteczki tlenu (O2) do dwóch cząsteczek wody potrzebne są 4 elektrony (4 cząsteczki zredukowanego cytochromu c). Przeniesieniu dwóch elektronów przez związane z enzymem kofaktory (dwa jony
4
Wyszukiwarka
Podobne podstrony:
Tymczasowe przenośniki energii (równoważniki energii) - przenośniki elektronów i protonów H+ ■
img050 (15) Jeżeli w położeniu orto lub para w stosunku do grupy fenolowej lub aminowej znajduje się
skanuj0003 11. Gałki ocznej elektroda czynna mała 2x2cm podkład z lekiem na oczodó
skanuj0056 2 7APIEKANKIZapiekanka z twarogu z wiśniami (zdjęcie) 2 tytki masła lub margaryny utrze
Resize of!1 łania - po obróceniu klucza elektronicznego u stacyjce w położenie 1 lub 2. Lampka kontr
Resize of!1 łania - po obróceniu klucza elektronicznego u stacyjce w położenie 1 lub 2. Lampka kontr
skanuj0006 Dehydrogenazę 34. w łańcuchu oddechowym w przenoszeniu elektronów bierz
DSCI8525 Klasy enzymów: flil 1. oksydoreduktazy (oksydazy, dehydragenazy) j przenoszą elektrony i H
skanuj0033 (108) • elementy urządzeń elektrycznych, np. rdzenie do transformatorów, magnesy trwałe,
skanuj0175 348 Tabela 22Siły elektromotoryczne wybranych termoogniwSpojenie „zimne” znajduje się w t
skanuj0002 (330) 1. Wektor pola elektrycznego w dielektryku stratnym o impedancji
skanuj0002 (583) 26. Właściwości elektrostatyczne izolatorów. (Dielektrykipolarne
skanuj0137 (13) (O Sprzęgło przenosi moment obrotowy M = — lub (wg wzoru liczbowego) P &
więcej podobnych podstron