24

stężonego kwasu azotowego (7). Probówki ogrzewać we wrzącej łaźni wodnej przez 5 min, ostudzić i do każdej dodawać stopniowo 3,5 mi wodorotlenku sodowego (5). Ostrożnie!
4. Wykrywanie aminokwasów zawierających grupy hydrosulfidowe. Odmierzyć do jednej probówki 1 ml glicyny (2), do drugiej 1 ml białka (3), do każdej dodać po 2 ml wodorotlenku sodowego (5) oraz po 0,5 ml octanu ołowiawego (<S) i ogrzewać we wrzącej łaźni wodnej przez 3—5 min.
5. Koagulacja cieplna białka. Odmierzyć do probówki 1 ml białka (3) i ogrzewać nad palnikiem do wrzenia.
6. Wytrącanie białka kwasem. Odmierzyć do probówki 1 ml białka (3) i dodać 1 ml kwasu trichloro octowego (9).
7. Wytrącanie białka solami metali ciężkich. Odmierzyć do probówki 1 ml białka (3) i dodać kroplami 1 ml octanu ołowiawego (8).
(1|. Wysalanie białka. Do kolby stożkowej na 100 ml odmierzyć 10 ml roztworu białka jaja kurzego (2), dodać taką samą objętość nasyconego roztworu siarczanu amonowego (10) i wymieszać. Wytrącają się w tych warunkach globuliny. Część mieszaniny przesączyć przez sączek z bibuły i przesącz zebrać do suchej kolby stożkowej.
Do przesączu dodać małymi porcjami, mieszając, sproszkowany siarczan amonowy (22) aż do nasycenia roztworu. Przesączyć ok. 1 ml roztworu przez sączek z bibuły do probówki. Dodać kroplę kwasu octowego (22) i ogrzewać do wrzenia. Brak osadu &viadczy o usunięciu białek z roztworu.
Opracowanie wyników
Podać uzyskane wyniki (zabarwienie, osady) dla poszczególnych reakcji wykonanych przy użyciu glicyny i białka wraz z uzasadnieniem.
Pytania
1. Który atom węgla alaniny jest ośrodkiem asymetrii? Podać wzór dowolnego aminokwasu w formie L i D.
2. Który z aminokwasów występujących w białkach nie zawiera asymetrycznego atomu węgla? W jakiej konfiguracji występują w białkach wszystkie inne aminokwasy?
3. Co nazywamy punktem izoelektrycznym aminokwasu?
4. Jakie grupy funkcyjne aminokwasów biorą udział w wytwarzaniu wiązania peptydo-wego? Napisać jego schemat.
5. Co nazywamy denaturacją białka i jakie czynniki ją powodują? Jakie cechy struktury zanikają w białku zdenaturowanym, a jakie zostają zachowane?
6. Jaka reakcja umożliwia odróżnienie aminokwasów od innych związków organicznych? Napisać i omówić tę reakcję. v
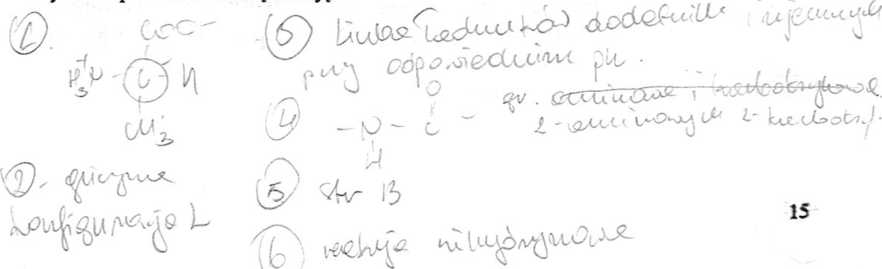
Wyszukiwarka
Podobne podstrony:
188 Cukry 2. Próby inkubować 5 minut we wrzącej łaźni wodnej. Po ochłodzeniu dodać 6 ml wod;-destylo
PrepOrg II166 (2) 169 56,0 g (69 cm3 0.635 mole). Mieszaninę ogrzewa się na łaźni wodnej i destyluje
DSC00234 IHWykonwriet Do 1 mt odczynnika dodać 1 ml roztworu cukru i 1 wstawić do wrzącej łaźni wodn
IMGD63 Jeżeli roztwór znajduje się w probówce - ogrzewanie prowadzimy na łaźni, jeżeli w zlewce lub
Img00100 104 2.40. Aluminium jest odporne na działanie stężonego kwasu azotowego,
chemiac2 4 wskaźnikowy ll i na lej podstawie określić pH roztwon. Lmicscic probówkę we wrzącej łazm
identyfikacja cukrowca str 5 zamieszaniu wstawić do wrzącej łaźni wodnej dokładnie na 3 minuty. Odcz
j ak przy krzywej wzorcowej DNA. Następnie wszystkie próby wstawić do wrzącej łaźni wodnej na 10 min
003 (2) 52 Ochrona środowiska. Przewodnik do ćwiczeń i ogrzewać w łaźni wodnej przez 2 godz. pod chł
DSCF6836 130 Następnie roztwór z osadem ogrzewać na łaźni wodnej przez ok. 1 godz., po czym odsączyć
Zadanie 16. (2 pkt) Do dwóch probówek wprowadzono po 5 cm3 wodnego roztworu chlorku chromu(lll). Do
str009 - w probówce zmieszać 5 cm3 20% roztworu kwasu azotowego (V), 5 kropli 5%
IMAG0589 (2) Nikorandil vy - ester nikotynamidu i kwasu azotowego o działaniu rozszerzającym tt. Wie
więcej podobnych podstron