299 [1024x768]

307
RÓWNOWAGI FAZOWE W UKŁADACH WIELOSKŁADNIKOWYCH
nością odczytać skład odpowiadający danemu punktowi lub znaleźć punkt odpowiadający danemu składowi.
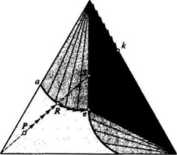
Zastosowanie diagramu trójkątnego rozpatrzymy na dwu przykładach. Na rys. 4.IB przedstawiono często spotykany przypadek trzech cieczy A, B, C, z których AC i BC mieszają się w dowolnych stosunkach, natomiast AB wykazują ograniczoną rozpuszczalność wzajemną (równowaga ciecz—ciecz).
Obszar poniżej krzywej obejmuje układy dwu faz ciekłych, powyżej zaś krzywej mamy jednorodny roztwór ciekły. Jeżeli weźmiemy skład początkowy określony punktem a> to odpowiada on mieszaninie dwu faz o składzie określonym punktami b i c; mamy do czynienia z układem dwuskładnikowym AB. Dodatek trzeciego składnika powoduje rozdzielenie go pomiędzy dwie fazy w proporcji odpowiadającej współczynnikowi podziału. Jednocześnie zachodzi wzrost wzajemnej rozpuszczalności składników A i B w obecności C. Jeżeli współczynnik podziału między składnikiem A i B jest większy od jedności, to skład powstających dwu faz ciekłych po dodaniu składnika C określony jest punktami b\ ć.
Linie łączące składy powstających faz noszą nazwę linii koniugacji. Prze-cinają się one w jednym punkcie D. Linia wyprowadzona z tego punktu, styczna do krzywej równowagi, wyznacza punkt krytyczny wzajemnej rozpuszczalności K. Dodawanie składnika C do roztworu a' prowadzi do dalszych zmian składu faz i stosunku ich mas. mjmf rośnie w miarę dodawania skład-nika*C. W punkcie d faza /? zanika w ogóle i otrzymujemy układ jednofazowy.
HjO b B
Rys. 4.19. Diagram rozpuszczalności dwóch soli A i B w wodzie, gdy sole nie tworzą hydratów
Na rys. 4.19 przedstawiono najprostszy diagram rozpuszczalności dwóch soli A i B w wodzie (równowaga ciecz—ciało stałe). Jest to przypadek, gdy sole nie tworzą krystalicznych hydratów, nie krystalizują też pod postacią soli
Wyszukiwarka
Podobne podstrony:
286 [1024x768] 295 RÓWNOWAGI FAZOWE W UKŁADACH WIELOSKŁADNIKOWYCH granicznym Ściśle związanym z praw
288 [1024x768] 297 RÓWNOWAGI FAZOWE W UKŁADACH WIELOSKŁADNIKOWYCH zastosowanie w analizie różnych di
292 [1024x768] 301 RÓWNOWAGI FAZOWE W UKŁADACH WIELOSKŁADNIKOWYCH z danym roztworem musi być obliczo
294 [1024x768] 303 RÓWNOWAGI FAZOWE W UKŁADACH WIELOSKŁADNIKOWYCH schodkowi mówimy o jednej półce te
296 [1024x768] 305 RÓWNOWAGI FAZOWE W UKŁADACH WIELOSKŁADNIKOWYCH nikowym w przypadku ograniczonej r
284 [1024x768] Równowagi fazowe w układach wieloskładnikowychZjawiska rozpuszczalności Rozpuszc
290 [1024x768] RÓWNOWAGI FAZOWI-: W UKŁADACH WIELOSKŁADNIKOWYCH 299 w roztworze wodnym? Jaki wynik z
05 1 I Równowagi fazowe w układach jednoskładnikowychRównowagi fazowe w układach
279 [1024x768] ROZTWORY I RÓWNOWAGI FAZOWE niż nad roztworem, wobec tego zachodzić będzie proces sta
287 [1024x768] ROZTWORY I RÓWNOWAGI FAZOWE %wag. fenolu *wag.
05 1 I Równowagi fazowe w układach jednoskładnikowychRównowagi fazowe w układach
05 1 I Równowagi fazowe w układach jednoskładnikowychRównowagi fazowe w układach
o- <a -ą * Równowagi fazowe w układach jednoskładnikowych
o- <a -ą * Równowagi fazowe w układach jednoskładnikowych
skanowanie0015 (60) UKŁADY RÓWNOWAGI FAZOWEJ Pojęcia podstawowe • Przemiany zachod
skanowanie0015 (60) UKŁADY RÓWNOWAGI FAZOWEJ Pojęcia podstawowe • Przemiany zachod
271 [1024x768] 280 ROZTWORY I RÓWNOWAGI FAZOWE jeżeli nie takie same, to w każdym razie bardzo podob
275 [1024x768] 284 ROZTWORY I RÓWNOWAGI FAZOWE czystego rozpuszczalnika i roztworu. Punkt krzepnięci
277 [1024x768] 286 ROZTWORY I RÓWNOWAGI FAZOWE — Iń jc, =A//. f dr r !rł A Hw / 1 r r,a//* / r-r,
więcej podobnych podstron