CCF20110129�025

6.3. Spektrofluorymetria
6.3.1. Wprowadzenie
Luminescencję definiuje się w sposób ogólny jako emisję światła przez ciała zimni w przeciwieństwie do żarzenia, które jest emisją światła przez ciała gorące. W uji, ciu molekularnym można natomiast powiedzieć, że cząsteczki w stanie wzbudzonym mogą emitować promieniowanie, przechodząc do stanu podstawowego, a zjawisko m nazywamy luminescencją.
Wyróżniamy różne rodzaje luminescencji, przyjmując nazwy od czynników, które ji wywołują. I tak może być:
• fotoluminescencja — substancja jest wzbudzona promieniowaniem elektronm gnetycznym
• chemiluminiscencja — wzbudzenie cząsteczki jest wynikiem reakcji chemii / nych;
• bioluminescencja — wzbudzenie cząsteczki jest wynikiem procesów biochemii; nych;
• elektroluminescencja — wzbudzenie cząsteczki następuje w polu elektrycznym W analizie chemicznej jest wykorzystywane głównie zjawisko fotoluminescencji. W
zależności od mechanizmów przejść elektronowych w zjawisku tym wyróżniamy fluort scencję i fosforescencję. Proces fotoluminescencji można przedstawić schematycznir
Stan absorpcja stan
podstawowy + v wzbudzenie wzbudzony
emisja stan fosforescencja ., ..
* podstawowy cleP0 fluorescencja ^ ' 1
x + hv X*
emisja
> X T ciepło hv'
(6.45)
Energia fluorescencji i fosforescencji hv' jest o wiele mniejsza niż energia promieniu wania wzbudzającego hv, co jest wynikiem degradacji energii cząsteczki na drotl/i przejść bezpromienistych, termicznych. Schemat przejść energetycznych w cząsteczo przedstawiono na rys. 6.30. Schemat jest uproszczony i ograniczony do przejść międ/y singletowym poziomem podstawowym S0 i pierwszym singletowym poziomem wzbu dzonym Si oraz odpowiadającym mu pierwszym trypletowym poziomem wzbudzonym 7j. Wzbudzenie jest wynikiem absorpcji promieniowania hv, a odpowiednie przejścir wyraża schemat:
S0 + hv -»• Si (6.4ft)
Dezaktywacja cząsteczki z poziomu St w temperaturze pokojowej może mieć różny przebieg, ale dominują następujące procesy:
1) Dezaktywacja oscylacyjna, bezpromienista.
2) Fluorescencja.
Te dwa procesy (II i III na rys. 6.30) można wyrazić schematem:
(6.47)
Si —>■ S0 + ciepło + hv'
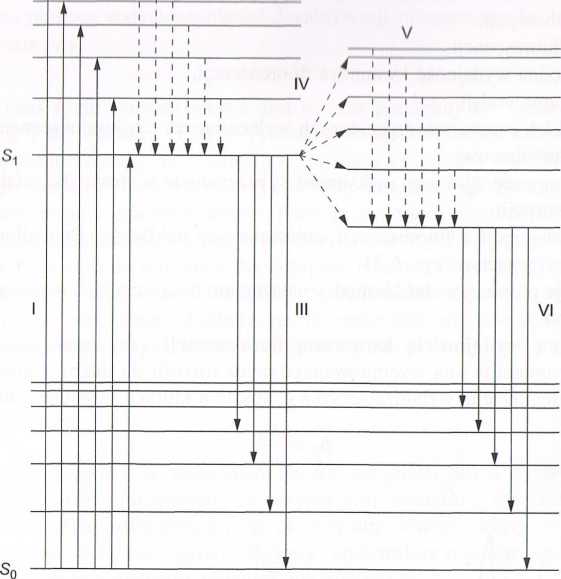
m( li 10. Schemat przejść energetycznych związanych z absorpcją promieniowania, fluorescencją i fosfo-n *i ‘ hi M|
Iłezpromieniste przejście międzysystemowe (wewnętrzna konwersja do stanu try-pltMowego) (przejście IV na rys. 6.30)
5, -> 7, (6.48)
I) Dezaktywacja oscylacyjna, bezpromienista wewnątrz stanu trypletowego (przejście \ im rys. 6.30).
.*>) Fosforescencja (przejście VI na rys. 6.30)
7, -> 50 (6.49)
Fotony emitowane mają niższą energię aniżeli fotony promieniowania wzbudzają-'i'go. Inaczej mówiąc, widmo emisyjne jest przesunięte w kierunku fal dłuższych.
W niektórych cząsteczkach możliwe jest przejście bezpromieniste z poziomu 5, do /, Przejście promieniste 7| -» So nazywamy fosforescencją. Widmo fosforescencji |i'n! przesunięte w kierunku fal dłuższych, zarówno w stosunku do widma absorpcji, |itk i do widma fluorescencji. Sytuację taką obrazuje widmo absorpcji, fluorescencji I Insforescencji tryptofanu przedstawione na rys. 6.31.
Wyszukiwarka
Podobne podstrony:
Rozdział 2 Rysunek 2.1 Tablica ustawień lokalizacji (AutoCAD 2010) Wprowadzanie danych odbywa się w
7. IA definiuje się w sposób następujący: Amper jest to stały prąd, który płynąc w dwóch równoległyc
23 luty 07 (27) Grupę strukturalną definiuje się w sposób umowny na podstawie liczby członów i par o
43347 Scan8 (4) Ogólnie rzecz biorąc bezpieczeństwo definiuje się nie tylko jako wolę przetrwania, a
Analizę ekonomiczną definiuje się też szeroko jako „dyscyplinę naukową dotyczącą zespołu metod
zadania publicznego. Definiuje się je Jakże jako względnie samodzielne jednostki organizacyjne, wypo
skanuj0024 2 262. Na pojęcie .prawo podmiotowo" składa Się: o) ogół norm określającymi i w spos
CCF20110611�049 DZIAŁANIA DYDAKTYCZNE WSPIERAJĄCE POJAWIANIE SIĘ STRATEGII W DZIAŁANIU GRUPOWYM W KL
CCF20101219�020 do jednostkowej. W ten sposób pojawił się pancerz określany jako torsowy bądź pancer
SPIS TREŚCI 1. Wprowadzenie - czym zajmuje się gleboznawstwo, definicja
1. WPROWADZENIE - CZYM ZAJMUJE SIĘ GLEBOZNAWSTWO, DEFINICJA GLEBY Gleboznawstwo (pedologia) jest nau
Definicja kolumn do wczytania W ten sposób definiuje się pola, które mają zostać
Zdjęcie3897 52 Rozdział 2. Definicje dyslcksji ganionych, które są niezbędne do uczenia się w sensie
CCF20101004�005 18 1. Wprowadzenie sposób błędy noszą nazwę błędów lub niepewności przypadkowych i s
CCF20120111�007 69. Jak definiuje się aktywności dla gazów doskonałych, dla czystych ciał stałych i
więcej podobnych podstron