3582428807
26. Przedstaw podział i scharakteryzuj enzymy należące do klasy oksydoreduktaz.
Oksydoreduktazy stanowiące w klasyfikacji enzymów kla.se pierwsza, katalizują procesy utleniania lub redukcji substratu.
Ze względu na mechanizm działania oksydoreduktazy dzieli się na następujące grupy
- oksydazy,
- oksygenazy,
- hydioksylazy,
- dehydrogenazy,
- per oksydazy
Oksydazy aktywują cząsteczkę tlenu dwoma lub czterema elektronami i katalizują pizyłączeme protonow do powstałych jonow tlenk oprych, pizy czym powstaje woda lub nadtlenek wodom Ze względu na produkt końcowy wyróżnia się dwa typy oksydaz
Oksydazy I zespołu, np oksydaza askoibimanowa. Enzymy te 2A,h
zawierają w swej cząsteczce atom metalu, np miedzi Schemat cfciałama oksydaz I zespołu można pizedstawic w następujący sposob Oksydazy I zespołu aktywną cząsteczkę tlenu czterema elektronami i katalizują powstanie wody
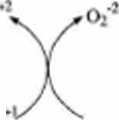
Oksydazy II zespołu, to gównie enzymy flawinowe zawierające jako koenzym dmukleotydflawinoademnowy (FAD) Dotr gupy oksydaz należą między innymi oksydazy L-1 D-aminokwasowe,. Schemat działania oksydaz II zespołu
Oksydazy II zespołu aktywują cząsteczkę tlenu dwoma elektronami i katalizyą powstawanie nadtlenku wodom
y
4CU
AH:
4Cu
* 4ir — 2HjO
4H-

FAD

FADH2 °2
Oksygenazy katalizują bezposiedme włączenie tlenu cząsteczkowego do związków organicznych
A *• Oj ■ ‘ AOj
Przykładem tych enzymów może byc lipooksygenaza, katalizująca utlenienie wielomenasyconychkwasów tłuszczowych. Oksygenazy odbywają ważną rolę w metabolizmie związków aromatycznych
Hydroksylazy katalizują bezposredbae włączenie połowy cząsteczki tlenu (atomu tlenu) do związków organicznych, pizy czym wymagqą obecności dodatkowo donora atomow wodom
AU * BHj 4 O: ——aoh 4 B ♦ HjO
Drugi atom tlenujest wiązany z udziałem czynnika redukującego (zredukowane NAD lub NADP) w cząsteczkę wody
Przykładem hydroksylaz jest 4-hyckoksylaza fenyloalamnowa katalizująca utlenienie fenyloalanmy do tyrozyny
Dehydrogenazy katalizują reakcje pizenoszenia atomow wodoruz subsóatunakoemymy lub inne akceptory Enzymy te współdziałają z koenzymami rnkotynamidoademnowymi 1 flawinowymi. Do współdziałających z NAD należy np dehydrogenaza mleczanów a. z NADP dehychogenaza gukozo-6-fosforanu zas typowa dehydrogenaza flawinowa to np dehydrogenaza bursztynianowa
Pereksydazy katalizują leakcje rozkładu nadtlenku wodom Nadtlenek wodoiujest silnym inhibitorem enzymów 1 dlatego kom orki wyposażone są w mechanizmy, dzięki ktoiym związek tenjest rozkładany Rozkład nadtlenku wodom katalizuj ą per oksydaza 1 katalaza
Peroksydaza (oksydoreduktaza donor:H^)^ jest to enzym występujący gównie w roślinach, choc spotyka się go także w niektórych organizm ach zwierzęcych. Istnieje kilka peroksydaz - większość z mchjest niespecyficzna, ale są 1 pei oksydazy specyficzne w stosunku do donora wodom, np per oksydaza cytochromowa czy per oksydaz a gutationowa.
Do peroksydaz niespecyficznych należy m m najlepiej poznana per oksydaza z chrzanu
All2 + HjOj -* A 4 2H20
Katalaza (oksydoreduktaza H;0;:H;0:) jest enzymem rozpowszechnionym w swiecie zwieizęcym (wątroba, nerki), występuje jednak również w niektórych roślinach oraz we wszystkich bakteriach tlenowych. Katalaza, podobnie jak per oksydazą, jest hemoproteina Cząsteczka katalazy składa się z czterech podjednostek, z których każda zawiera jedną cząsteczkę protohemu
Wyszukiwarka
Podobne podstrony:
Amylazy - enzymy należące do glikozydas z klasy hydrolaz. Katalizują hydrolityczny rozkład polisacha
str04 (7) CHARAKTERYSTYKA I OPIS ODS DS-y należą do klasy desantowców typu dwupokładowego. Ich długo
page0274 Rośclsław — Rosciszewski 266 Imm podziale państwa, Tmutorakań należał do księztwa
060 2 , 4()0. Koenzymem, związanym z białkiem enzymu należącego do klasy ligaz, poprzez jego grupę e
Stal należącą do klasy ciągliwości C spełnia wymaganie : 1,15<A< 1,35 7. Sta
4 (471) 110 morfologia — fleksja Pozostałe rzeczowniki pluraie tantum (a więc należące do klasy P-l)
Zbiornik ciśnieniowy spawany�5 7 Do III klasy zalicza się konstrukcje, które nie należą do klasy I i
Wrocław, 26.05.2020r.Lista kandydatów zakwalifikowanych do klasy 4 sportowej na rok szkolny
DSC00779 (2) Rodzaje drożdży należące do klasy Ascomyceles Rodzina Rodzaj I Ascoidiaceae Ambrosioz
DSC00780 (2) Tab. 1-5. Rodzaje drożdży należące do klasy) De u teromycetes
DSC00782 (3) Rodzaje drożdży należące do klasy
ziarna zbóż □ Zboża należą do klasy roślin jednoliścienny eh. rodj □
więcej podobnych podstron