107997
120 K. KAI.FTHA 121
tychmiastowcgo wytworzenia się kompleksu enzym-substrat (EA), który po uprzedniej aktywacji rozkłada się z odtworzeniem wolnej formy enzymu (E) i wytworzeniem produktu reakcji (P). W fazie prestacjonarnej, stężenie kompleksu EA początkowo szybko wzrasta, po czym szybkość jego tworzenia zostaje zrównoważona szybkością rozkładu. Wtedy stężenie kom] dek su enzym-substrat ustala się na określonym poziomie a szybkość reakcji osiąga wartość stałą—rozpoczyna sie druga faza reakcji zwana fazą stacjonarną lub inaczej fazą szybkości początkowej (inicjał veiocity phasc). Charakterystyczną cechą fazy stacjonarnej jest to, że w czasie jej trwania ilość wytwarzanego w jednostce czasu produktu (lub rozkładanego w jednostce czasu substratu) jest stała — zatem w* fazie tej reakcja enzymatyczna przebiega wedle kinetyki rzędu zerowego. Faza stacjonarna w przeciwieństwie do prestacjonarnej trwa wystarczająco długo, aby możliwe było dokonanie odpowiednich pomiarów szybokści reakcji bez pomocy technik wymagających specjalnej aparatury. Z chwilą, kiedy stężenie zużywającego się substratu obniży się na tyle, że przestaje wysycać enzym, kinetyka reakcji enzymatycznej /.mienia się z zerorzędowej na pierwszorzęduwą i rozpoczyna się trzeci, ostatni etap reakcji zwany fazą poststacjonarną (Ryc. 1).
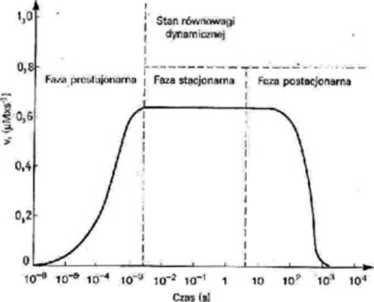
Hyc. L Skala czasowa reakcji enzymatycznej przebiegającej wedle mechanizmu Michaclisa (schemat 2): k*i = 10ł M_łs"\ k-i = 10* s’*, kła = 10*s“\ k j *» 0,[AJ« = - 2x 10”4M, IE]» - 10_ł M (19).
W reakcji enzymatycznej przebiegającej wedle najprostszego, ujętego w schemacie 1 mechanizmu,
li + A^EA — E + P
Schemat 1
Wyszukiwarka
Podobne podstrony:
120 K. KALETHA [2] tychmiastowego wytworzenia się kompleksu enzym-substrat (EA), który po uprze
120 K. KALETHA [2] tychmiastowego wytworzenia się kompleksu enzym-substrat (EA), który po uprze
Zdjęcie0157 Modele tłumaczące tworzenie się kompleksu enzym-substrat Model "klucza i zamka” (an
Zdjęcie0158 Modele tłumaczące tworzenie się kompleksu enzym-substrat Model indukowanego dopasowania
43544 IMG 57 (2) wytworzył się zespół ogólnie akceptowanych założeń, który spełnia funkcję teorii. Z
IMAG0327 (4) Centrum aktywne enzymu Tworzenie kompleksu enzym-substrat kl E + Sr:ES-E + P Centrum ak
Typy budowy centrów aktywnych Warunkiem biokatalizy jest powstawanie kompleksu enzym-substrat. Subst
Enzymy 123 *■ ijący ostatecznie kompleks enzym-substrat-inhibitor (ESI) jest nieaktywny ta - tycznie
skanuj0014 (233) zanika. Im wolniejsze i trudniejsze było wytworzenie się odruchu warunkowego, tym s
więcej podobnych podstron