74179
Wpływ stężenia enzymu i substratu na szybkość reakcji enzymatycznej.
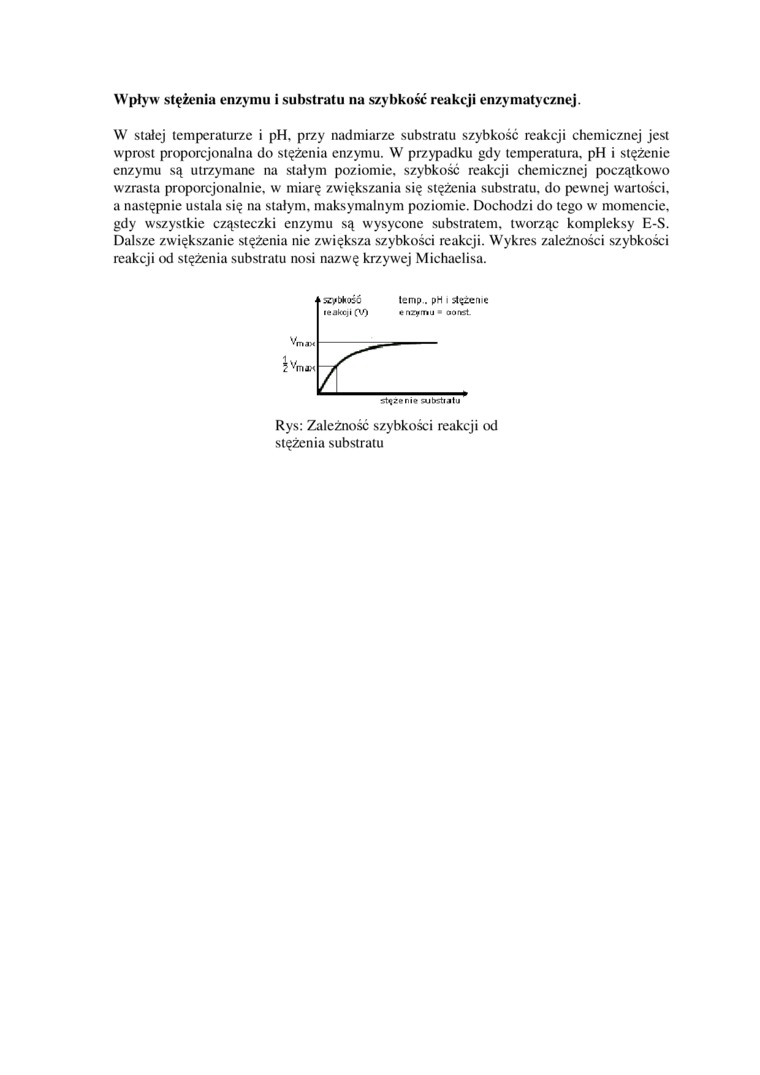
W stałej temperaturze i pH. przy nadmiarze substratu szybkość reakcji chemicznej jest wprost proporcjonalna do stężenia enzymu. W przypadku gdy temperatura. pH i stężenie enzymu są utrzymane na stałym poziomie, szybkość reakcji chemicznej początkowo wzrasta proporcjonalnie, w miarę zwiększania się stężenia substratu. do pewnej wartości, a następnie ustala się na stałym, maksymalnym poziomie. Dochodzi do tego w momencie, gdy wszystkie cząsteczki enzymu są wysycone substratem. tworząc kompleksy E-S. Dalsze zwiększanie stężenia nie zwiększa szybkości reakcji. Wykres zależności szybkości reakcji od stężenia substratu nosi nazwę krzywej Michaelisa.
szybkość temp.. pH i stężenie
icukcji (V) enzymu "floret

Rys: Zależność szybkości reakcji od stężenia substratu
Wyszukiwarka
Podobne podstrony:
DSC00036 (39) Wpływ stężenia substratu na szybkość reakcji enzymatycznej _
WYKŁAD 2 enzymy cz 1 (30) KINETYKA REAKCJI ENZYMATYCZNEJ 0 Wpływ stężenia substratu na szybkość r
IMAG0331 (4) Czynniki wpływające na szybkość reakcji enzymatycznej S Stężenie enzymu - szybkość reak
DSC00301 2 Czynniki wpływające na szybkoóć reakcji enzymatycznej f Stężenie substratu. . • Temperatu
Wpływ stężenia enzymu i czasu na aktywność enzymów Zależność szybkości reakcji od stężenia enzymu
IMAG0335 (4) 3. Wpływ pH na szybkość reakcji enzymatycznej Każdy enzym ma optymalne pH. w którym wyk
IMAG0336 (5) 4. Wpływ temperatury na szybkość reakcji enzymatycznej Reguła Van t HofFa - podwyższeni
DSC00033 (28) Czynniki wpływające na szybkość reakcji enzymatycznejStężenie enzymu Temperatura przeb
DSC00038 (38) Wpływ pH i temperatury na szybkość reakcji enzymatycznej
DSC00310 Wpływ temperatury na szybkość reakcji enzymatycznej
86111 WYKŁAD 2 enzymy cz 1 (29) WPŁYW pH NA SZYBKOSC REAKCJI ENZYMATYCZNEJ Większość enzymów funk
WYKŁAD 2 enzymy cz 1 (26) WPŁYW TEMPERATURY NA SZYBKOSC REAKCJI ENZYMATYCZNE A Temperatura ma wpł
122 Enzymy4.4.5. Wpływ inhibitorów enzymów na szybkość reakcji enzymatycznej . Wyróżnia się zasadnic
więcej podobnych podstron