4307685596
Ek = \mvl + \mvl + \mvl
Zgodnie z zasadą ekwipartycji energii, średnia energia każdego z członów wynosi;
:T, gdzie k jest stałą Boltzmana
stąd średnia energia atomu wynosi \kT, a średnia energia jednego mola atomów wynosi | RT (R - stała gazowa). Całkowita energia wewnętrzna jednego mola gazu doskonałego, wynosi:
Um = Um{0) +
gdzie Um(0) - oznacza molową energię wewnętrzną gdy T = 0, stąd:
(i)v“^=r8-31[J-K_1'morli
= 12.48 [J • K"1 • mol"1] = Cv
Gdy gaz składa się z cząsteczek wieloatomowych (ułożonych w sposób nieliniowy) oprócz ruchu translacyjnego w trzech wymiarach, cząsteczki mogą wykonywać rotację wokół trzech osi. Pojawia się (zgodnie z zasadą ekwipartycji energii nowy wkład energii pochodzący od rotacji, Eu = \RT. Dla cząsteczek liniowych \RT. Całkowita energia wewnętrzna (dla cząsteczek nieliniowych) wynosi wtedy:
Um = Um(0) + |RT = 2 • 8.31 = 25 J ■ K_1 • mor1 stąd pojemność cieplna:
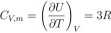
i odpowiednio dla gazu składającego się z wieloatomowych cząsteczek liniowych;
Um = Um(0) + ^RT
CVm=(~) = -J? =-• 8.31 [J • K-1 ■ mor1]
1 \ar)v 2 2 1 1
Energia wewnętrzna gazu wieloatomowego o nie liniowych cząsteczkach rośnie dwa razy szybciej z temperaturą i pojemność cieplna jest dwa razy wyższa, w porównaniu do gazu jednoatomo-wego. Na wartość energii wewnętrznej, składa się (w przypadku cząsteczek wieloatomowych) również człon pochodzący od energii ruchu oscylacyjnego, jednakże ten rodzaj energii nie można opisać w sposób klasyczny, gdyż energia związana z ruchem oscylacyjnym jest kwantowana. Wyrażenie na średnią energię oscylatora o częstości n ma postać:
8
Wyszukiwarka
Podobne podstrony:
I. 1. Kinetyczno-molekularna interpretacja temp. Zasada ekwipartycji energii. 2. Lepkość ujęcie makr
Image68 134 c. Przy zsuwaniu się bez tarcia ruch obrotowy nie występuje. Zgodnie z zasadą zachowania
Zadanie 2 Zasada ekwipartycji energii głosi, że ciepło właściwe i molowe jest jednakowe na każdy sto
4. Zasada Ekwipartycji Energii 3kT l średnia energia kinetyczna ruchu postępowego
4a, Zasada Ekwipartycji Energii, c.d« ■ może dochodzić energia ruchu drgającego ■
4b. Zasada Ekwipartycji Energii, c.d. adiabaty - € c = ■ różnica: C -Cr = R
23zasada ekwipartycji energii Zasada ekwipartycji energii Wynik(£
5. Definicja pojemności cieplnych; zasada ekwipartycji energii; oszacować
35360 Image68 (7) 134 c. Przy zsuwaniu się bez tarcia ruch obrotowy nie występuje. Zgodnie z zasadą
5.3a. I Zasada Termodynamiki, c.d. ■ energia wewnętrzna: U = N{Ek )= ^kTN=1- UTNAn U=nR-T=nCvT 2 1U=
Image044 Tablica takiego kodu jest tworzona zgodnie z zasadami tworzenia kombi* nacji k elementów z
więcej podobnych podstron