
Cz. XV Izomeria alkanów, cykloalkanów, alkenów i alkinów
Izomeria i izomery
1. Pojęcia i definicje
Izomeria – zjawisko występowania związków chemicznych o tym samym wzorze
sumarycznym, ale różniącym się połączeniem lub konfiguracją przestrzenną atomów
w cząsteczce, takie związki nazywamy izomerami.
Izomeria konstytucyjna (strukturalna) – rodzaj izomerii polegający na różnej
kolejności lub sposobie powiązania atomów w cząsteczkach izomerów, wyróżnia się
w szczególności izomerię: szkieletową, pozycyjną:
Izomeria szkieletowa – typ izomerii polegający na różnej budowie szkieletu
węglowego (łańcucha, pierścienia) cząsteczek izomerów. Izomeria szkieletowa
obejmuje: i. łańcuchową, i. pierścieniową, i, położenia wiązania wielokrotnego:
Izomeria łańcuchowa – typ izomerii szkieletowej, związany z różna budową
łańcucha węglowego w cząsteczkach izomerów.
- przykład dla cząsteczki C
5
H
12
– pentan
# CH
3
– CH
2
– CH
2
– CH
2
– CH
3
: n – pentan (normalny pentan)
1
2
3 4
# CH
3
– CH – CH
2
– CH
3
;
2
-
metyl
o
butan
ǀ
CH
3
4 3
2
1
# CH
3
– CH
2
– CH – CH
3
;
2
-
metyl
o
butan
ǀ
CH
3
CH
3
1
2
ǀ 3
# CH
3
– C – CH
3
;
2,2
-
di
metyl
o
propan
ǀ
CH
3
Izomeria pierścieniowa – typ izomerii szkieletowej związany z różną budową
pierścienia węglowego w cząsteczkach izomerów.
- przykład dla cząsteczki cykloheksanu – C
6
H
6
CH
3
CH
3
CH
3
4
1
1
3
2
3
2
H
3
C
H
3
C
CH
3
Cykloheksan;
metyl
o
cyklopentan ;
1,3
-
di
metyl
o
cyklobutan;
1,2,3
-
tri
metyl
o
cykloprapan

Zadanie do samodzielnego wykonania : dla cykloheksanu
można utworzyć
jeszcze
izomery o poniższych nazwach systematycznych, narysuj ich wzory
grupowe;
- etylocyklobutan,
-1,1-dimetylocyklobutan,
-1,2-dimetylocyklobutan,
- propylocykloprapan,
- 1- etylo-2-metylocyklopropan,
- 1-etylo-1-metylocykloprapan,
- 1,1,2 – trimetylocykloprapan.
Izomeria położenia wiązania wielokrotnego
–
typ izomerii szkieletowej związany
z różnym położeniem wiązań wielokrotnych (dot. alkenów i alkinów).
Przykład dla cząsteczek heksenu C
6
H
12
i heksynu C
6
H
10
;
1
2 3 4 5 6
CH
2
=
CH – CH
2
– CH
2
– CH
2
– CH
3
; heks-1-
en
;
1
2
3 4 5 6
CH
3
- CH
=
CH – CH
2
– CH
2
– CH
3
; heks-2-
en
;
1 2
3
4 5 6
CH
3
- CH
2
– CH
=
CH
– CH
2
– CH
3
; heks-3-
en
;
1
2 3 4 5 6
CH
≡
C – CH
2
– CH
2
– CH
2
– CH
3
; heks-1-
yn
;
1
2
3 4 5 6
CH
3
– C
≡
C – CH
2
– CH
2
– CH
3
; heks-2-
yn
;
1 2
3
4 5 6
CH
3
- CH
2
– C
≡
C
– CH
2
– CH
3
; heks-3-
yn
;
Zasady ustalania lokantów (numerów kolejnych at. C w szkieletach węglowych) i
ustalania nazw systematycznych:
- dla alkanów, cykloalkanów i ich izomerów łańcuchowych i pierścieniowych
suma lokautów na których znajdują się podstawniki alkilowe ( - C
n
H
2n+1
) lub
alkilowe i halogenowe (
-F, - Cl, - Br, - I
) musi być jak najmniejsza,
- w pierwszej kolejności wymienia się alfabetycznie podstawniki halogenowe z
podaniem ich lokautów, a w drugiej kolejności alfabetycznie podstawniki alkilowe
z podaniem ich lokautów.
Przykład:
Br
Cl
C
2
H
5
Br
CH
3
I I I I I
7
C
1
H
2
–
6
C
2
H –
5
C
3
–
4
C
4
H –
3
C
5
–
2
C
6
H –
1
C
7
H
3
I I I
C
2
H
5
Br
CH
3

-
nazwa wg lokantów górnych
: 1,4,5-tribromo-2-chloro-3,3-dimetylo-5,6-
dimetyloheptan (suma lokautów = 29),
-
nazwa wg lokantów dolnych:
3,4,7-tribromo-6-chloro-5,5-dietylo-2,3-
dimetyloheptan (suma lokautów = 35). Pierwsza nazwa jest prawidłowa.
- dla alkenów i alkinów lokant z wiązaniem wielokrotnym musi mieć jak
najmniejszą wartość i jest on nadrzędny w stosunku do innych lokautów na
których znajdują się podstawniki alkilowe lub halogenowe,
- pozostałe reguły są identyczne jak w przypadku alkanów i ich izomerów,
Przykład:
Br
Cl
C
2
H
5
Br
CH
3
I I I I I
7
C
1
H
2
–
6
C
2
H –
5
C
3
–
4
C
4
H –
3
C
5
–
2
C
6
=
1
C
7
H
2
I I I
C
2
H
5
Br
CH
3
-
w nazwie należy zastosować lokanty dolne
:
3,4,7-tribromo-6-chloro-5,5-dimetylo-2,3-dimetylohept-1-en.
Br C
2
H
5
Br CH
3
I I I I
7
C
1
≡
6
C
2
–
5
C
3
–
4
C
4
H –
3
C
5
–
2
C
6
H –
1
C
7
H
3
I I I
C
2
H
5
Cl
CH
3
-
w nazwie należy zastosowań lokanty górne
:
1,5-dibromo-4-chloro-3,3-dietylo-5,6-dimetylohept-1-yn.
Izomeria pozycyjna (podstawienia) – typ izomerii konstytucyjnej związanej z
różnym położeniem (pozycją) podstawników w takich samych szkieletach
węglowych cząsteczek izomerów;
Przykład dla cząsteczek: C
3
H
7
OH i C
3
H
7
Br
CH
3
– CH
2
– CH
2
– OH ; propan-1-ol,
CH
3
– CH (OH) – CH
3
; propan-2-ol
CH
2
Br – CH
2
-CH
3
; 1-bromopropan,
CH
3
–CHBr – CH
3
; 2-bromopropan.
Izomeria geometryczna (cis-trans) – typ stereoizomerii związany różnym
położeniem podstawników tego samego rodzaju (np. alkilowe, halogenowe,
wodór) po tej samej stronie lub po przeciwnych stronach płaszczyzny w której
leży wiązanie sztywne (nierotujące) między atomami węgla w cząsteczkach
izomeru. Jeżeli podstawniki tego samego rodzaju znajdują się po tej samej stronie
płaszczyzny – forma cis, jeżeli po przeciwnej – forma trnas.
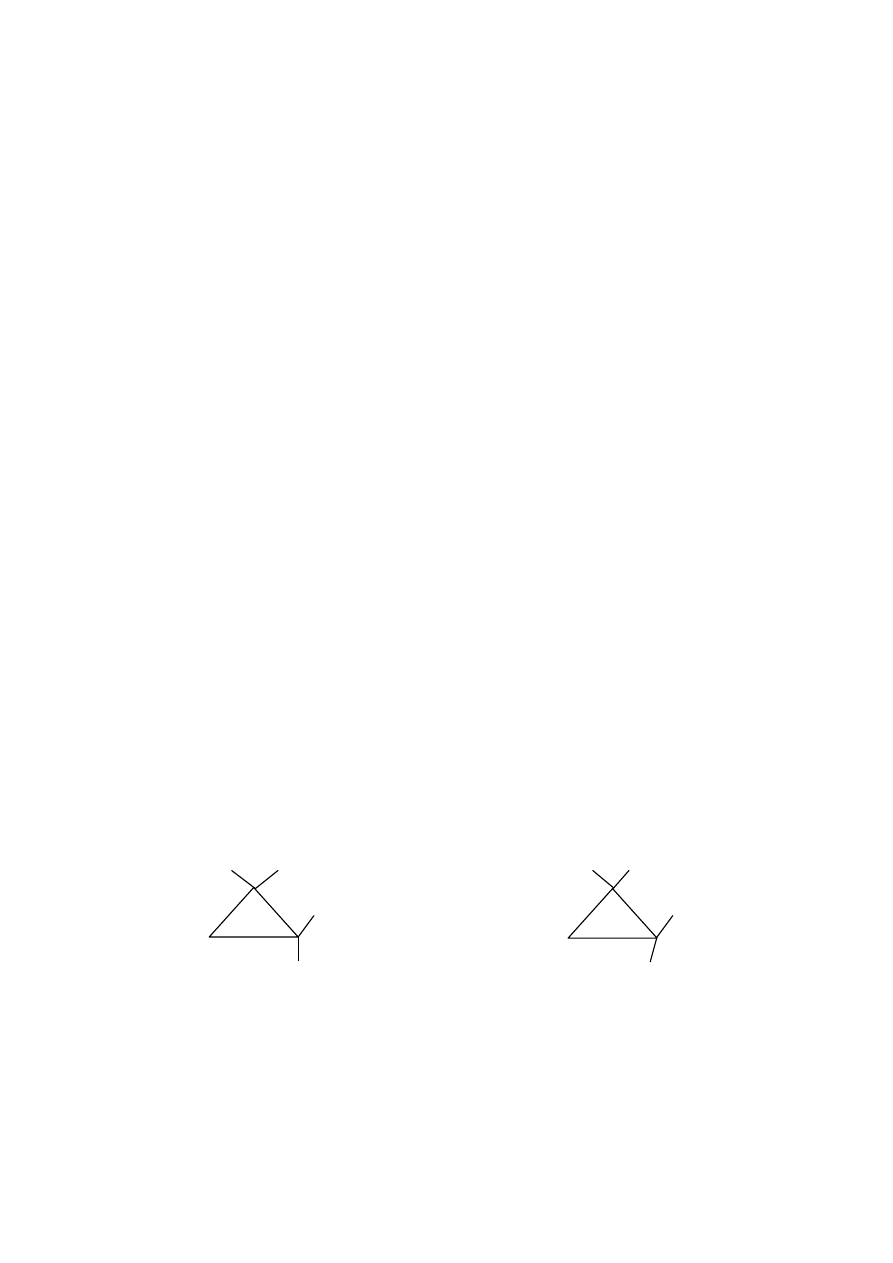
Przykład dla cząsteczki 1,2-dibromoeten.
H
H
\ /
C = C cis-1,2-dibromoeten
/ \
Br
Br
H
Br
\ /
C = C trans-1,2-dibromoeten
/ \
Br
H
Przykład dla cząsteczki but-2-enu
H
3
C CH
3
\ /
C = C cis-but-2-en
/ \
H
H
H
3
C
H
\ /
C = C trans-but-2-en
/ \
H
CH
3
Przykład dla cząsteczki : 1,2-dimetlocyklopropanu:
H
CH
3
H
CH
3
CH
3
H
H
CH
3
Cis-1,2-dimetylcyklopropan trans-1,2-dimetylocyklopropan
Izomery – różnią się między sobą właściwościami fizykochemicznymi; Tw, Tt,
aktywnością chemiczną, skręcalnością płaszczyzny światła spolaryzowanego
(ostatnia właściwość dotyczy związków o asymetrycznych atomach węgla –
posiadających 4-różne podstawniki, izomeria optyczna – enancjomeria).
Wyszukiwarka
Podobne podstrony:
Izomeria 4 id 221207 Nieznany
materialy z weglowodorow weglow Nieznany
BIALKA I WEGLOWODANY cz Weglow Nieznany (2)
Izomeria[1] id 221209 Nieznany
AEwiczenie 12 Weglowodory Nieznany
System rzadow w Konstytucji RP Nieznany
historyczne konstytucje nowela Nieznany
historyczne konstytucje marcowa Nieznany
historyczne konstytucje kwietni Nieznany
23 Wytwarzanie olefin i weglowo Nieznany (2)
ustawy prawo konstytucyjne zasa Nieznany
jednofunkcyjne pochodne weglowo Nieznany (2)
jednofunkcyjne pochodne weglowo Nieznany
Izomeria 2 id 221205 Nieznany
Izomeria wsród węglowodanów
prawo konstytucyjne (sylabus) i Nieznany
1 Klasyfikacja izomerów Izomeria konstytucyjna Izomeria konfiguracyjna i konformacyjna – zarys ogóln
Konstytucja 3 id 246532 Nieznany
więcej podobnych podstron