
ZAKŁAD OPAKOWALNICTWA I BIOPOLIMERÓW
CHEMIA ŻYWNOŚCI
Ćwiczenia laboratoryjne nr 5
Właściwości enzymów - ich chemiczna i fizyczna dezaktywacja
(przemiany chemiczne i fizyczne enzymów występujących w żywności)
Artur Bartkowiak, Szczecin 2003
Reakcje enzymatyczne w żywności
Świeże owoce i warzywa zawierają bardzo wiele aktywnych enzymów które powodują często
zarówno korzystne jak i niekorzystne zmiany w produkcie podczas składowania i przetwarzania.
Takie zmiany często zachodzą nawet kiedy produkt jest zamrożony. Dlatego owoce i warzywa są
często poddawane procesowi blanszowania przed procesem zamrażania czy pakowania
w hermetycznie zamykane puszki, tak by dezaktywować takie enzymy.
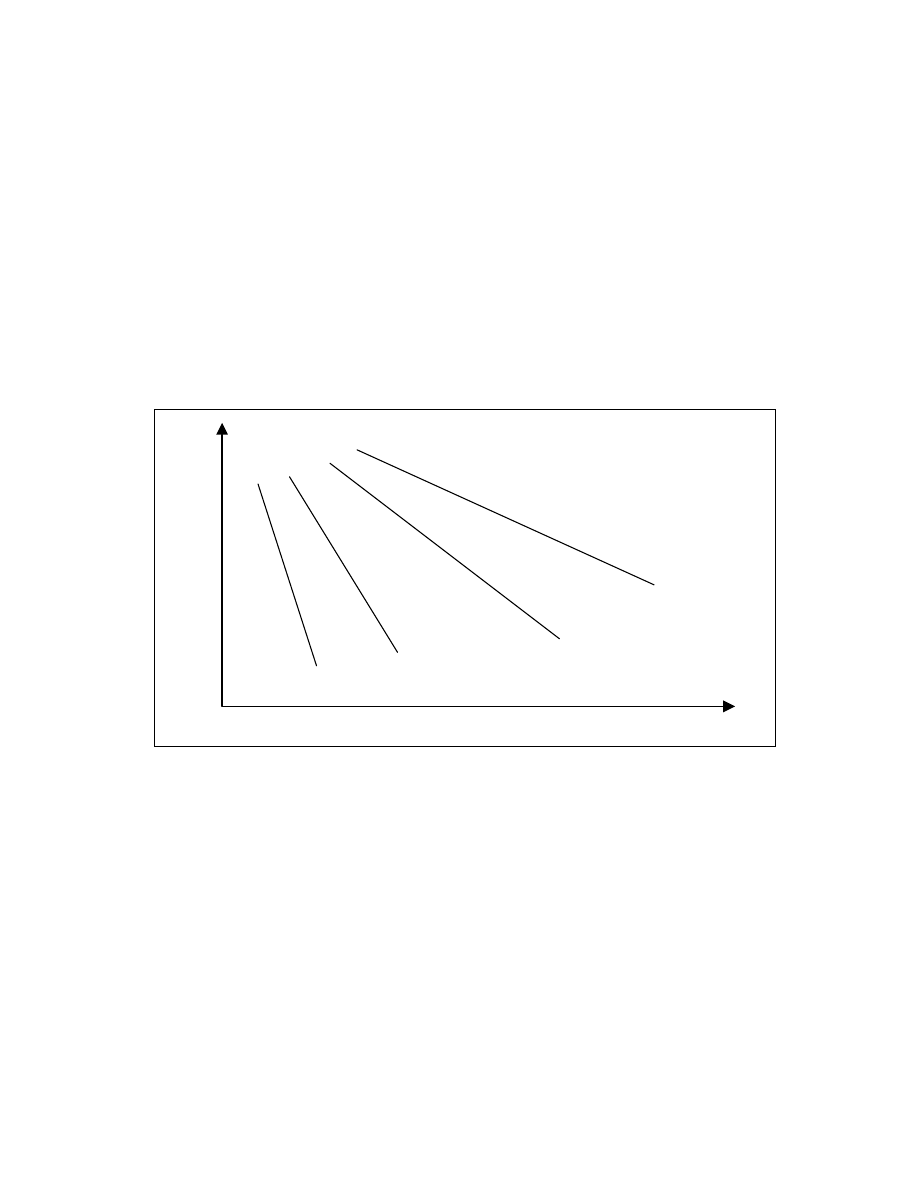
Stabilność termiczna enzymów zmienia się w dość szerokim zakresie. Dlatego, warunki
blanszowania (termicznej obróbki mającej na celu dezaktywację większości enzymów) powinny być
tak dobierane aby następowała dezaktywacja nawet najbardziej odpornych termicznie enzymów
(rys. 1).
lipaza
lipoksygenaza
polifenylooksydza
peroksydaza
Log D
Temperatura
Rys. 1. Zależność stałej D termicznej dezaktywacji dla wybranych enzymów w funkcji
temperatury (wartość D oznacza czas w określonej temperaturze po jakim następuję dezaktywacja
90% określonych enzymów
Peroksydaza jest jednym z najbardziej odpornych termicznie enzymów występujących w roślinach.
Dlatego też jest ona dobrym wskaźnikiem efektywności procesu blanszowania, gdzie zakłada się że
ilość ciepła potrzebna do dezaktywacji tego enzymu będzie dezaktywowała wszystkie inne enzymy
występującej w określonej próbce.
Peroksydazy są grupą oksydoreduktaz, to znaczy należą do grupy enzymów katalizujących reakcję
utleniania/redukcji (redox). Jak sama nazwa wskazuje jednym z substratów reakcji są nadtlenki
(schemat poniżej):
2
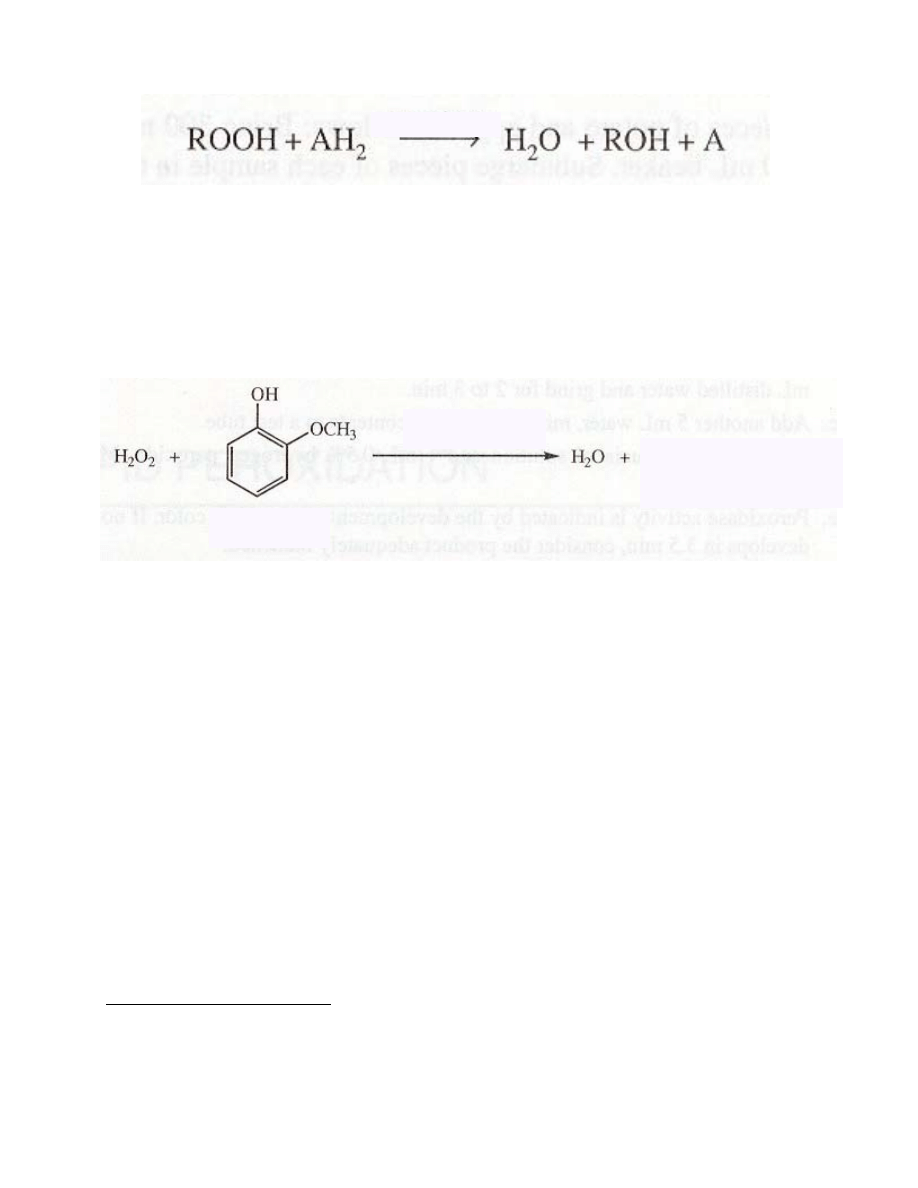
peroksydaza
W powyżej reakcji AH
2
jest typowym donorem wodorowym, który jest utleniany przez nadtlenek.
Wiele peroksydaz charakteryzuje się niską specyficznością tzn. katalizują różne związki o
charakterze wodoro-donorowym. Substraty fenolowe czy ogólnie aromatyczne są typowymi
substratami. Dodatkowo, albo lipidowy hydronadtlenek lub nadtlenek wodoru mogą działać jak
czynniki utleniające.
Zw. chem.
o kolorze czerw-brąz.
peroksydaza
Gwajakol
Gwajakol (2-metosyfenol, orto-metosyfenol) jest utleniana przez nadtlenek wodoru w wyniku czego
powstają skomplikowane związki o charakterze kompleksów charakteryzujących się czerwonym lub
brązowym kolorem. Ta reakcja jest katalizowana przez peroksydazy. W celu określenia
aktywności peroksydaz występujących w różnych warzywach i owocach często stosuje się
powyższą reakcję. Odpowiednią ilość roztworu gwajakolu i nadtlenku wodoru miesza się z
odpowiednią niewielką ilością materiału badanego, gdzie aktywność peroksydaz uwidacznia się
poprzez powstanie kolorowych czerwono-brązowych związków kompleksowych.
Celem poniżej opisanego ćwiczenia jest określenie czasu ogrzewania oraz czynników chemicznych
na dezaktywację peroksydaz pochodzenia roślinnego.
Ćwiczenie1.
Wpływ warunków obróbki termicznej i chemicznej na efektywność blanszowania.
Aparatura i szkło laboratoryjne:
- zlewki 600 cm3
- łyżeczka porcelanowa lub z tw. sztucznego
- nóż
3

- moździerz i tłuczek,
- cylinder miarowy 10 cm
3
- pipety polipropylenowe 2 cm
3
- łaźnia wodna (100
°C)
- probówki
Odczynniki chemiczne
- świeże ziemniaki i jabłka (samodzielnie przyniesione przez studentów - po jednej sztuce na
grupę),
- o-metoksyfenol (1% obj. w 95% etanolu)
- roztwór nadtlenku wodoru (0,5%)
- piasek
- 0,1 M HCl
- 0,1 M NaOH
- 0,1 M NaCl
Opis ćwiczenia
Do 12 probówek dodać po 5 cm
3
wody destylowanej i dodatkowo roztwory zgodnie z zestawieniem
w poniższej tabeli. Do 9 probówek zawierających wrzące ciecze (umieszczonych w stojaku w łaźni
wodnej) dodać odpowiednie po 1 gramie pociętych na małe kostki jabłka i ziemniaki (Tabela
poniżej - dla każdego z surowców indywidualne doświadczenie po 12 probówek) i następnie
ogrzewać kolejne probówki w określonym czasie, po czym natychmiast probówki schłodzić pod
strumieniem bieżącej wody. Podobne doświadczenie wykonać z 4 nie ogrzewanymi probówkami.
Zawartość kolejnych probówek przenieść do moździerza zawierającego odrobinę piasku u następnie
wszystko rozgnieść za pomocą tłuczka; po czym dodać 5 cm3 wody i przenieść całość z powrotem
do probówki). Wykonać dla każdej w ten sposób otrzymanej próbki reakcję na obecność aktywnej
peroksydazy (do każdej probówki dodać 1 cm
3
roztworu o-metoksyfenolu i 1 cm
3
0,5% H
2
O
2
-
wymieszać przez obrócenie probówki)
Po wykonaniu każdorazowej próby opisać zachodzące zmiany - pojawienie się czerwonawego
koloru (zanotować czas po którym nastąpiło pojawienie się barwy i określić jej intensywność).
4
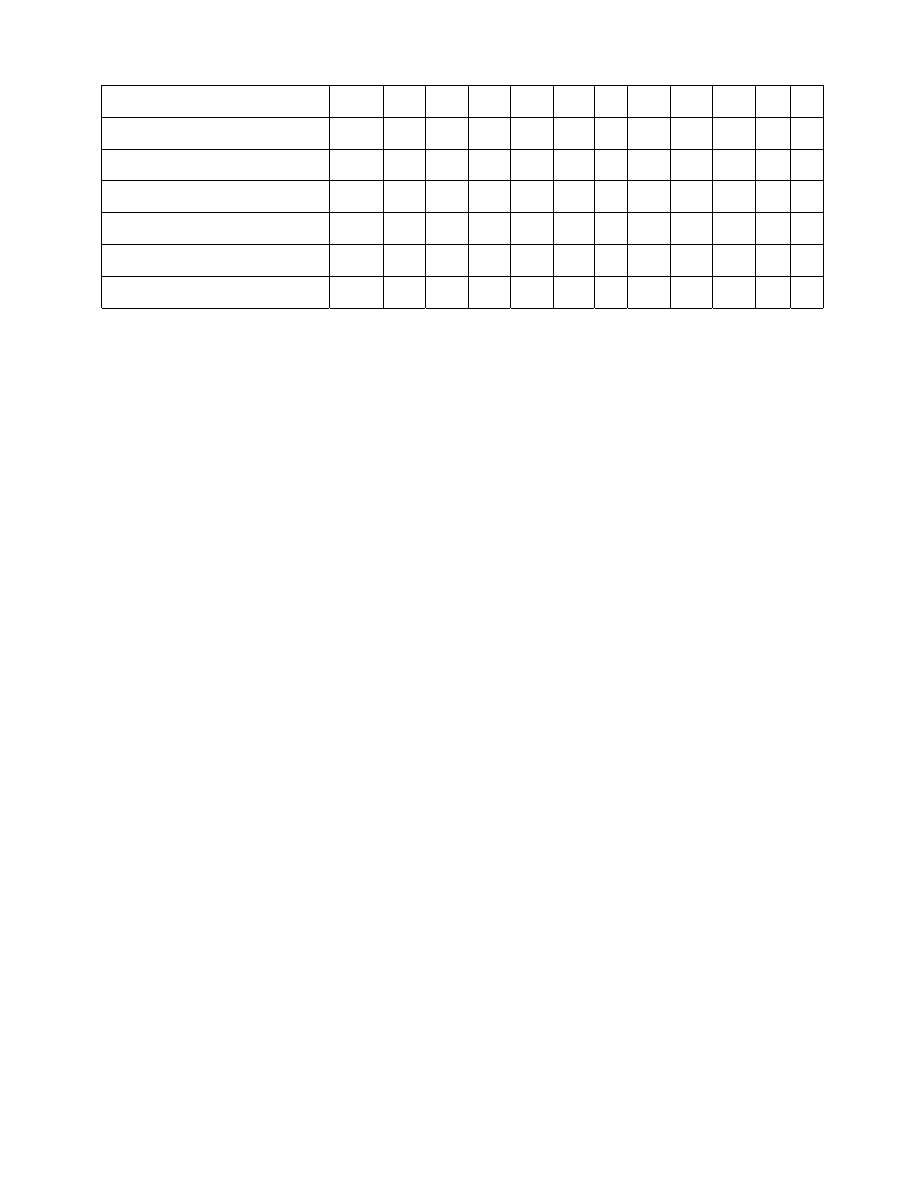
Probówka
1 2 3 4 5 6 7 8 9 10
11
12
0,1 M HCl [cm
3
]
- - - 1 1 1 - - - - - -
0,1 M NaOH [cm
3
]
- - - - - - 1 1 1 - - -
0,1 M NaCl [cm
3
]
- - - - - - - - - 1 1
1
Woda [cm
3
]
5 5
5
4
4
4
4
4
4
4
4
4
Jabłko/ziemniak[ g]
1 1 1 1 1 1 1 1 1 1 1 1
Czas ogrzewania [min]
0 2 4 0 2 4 0 2 4 0 2 4
5
IMIĘ I NAZWISKO GRUPA DATA
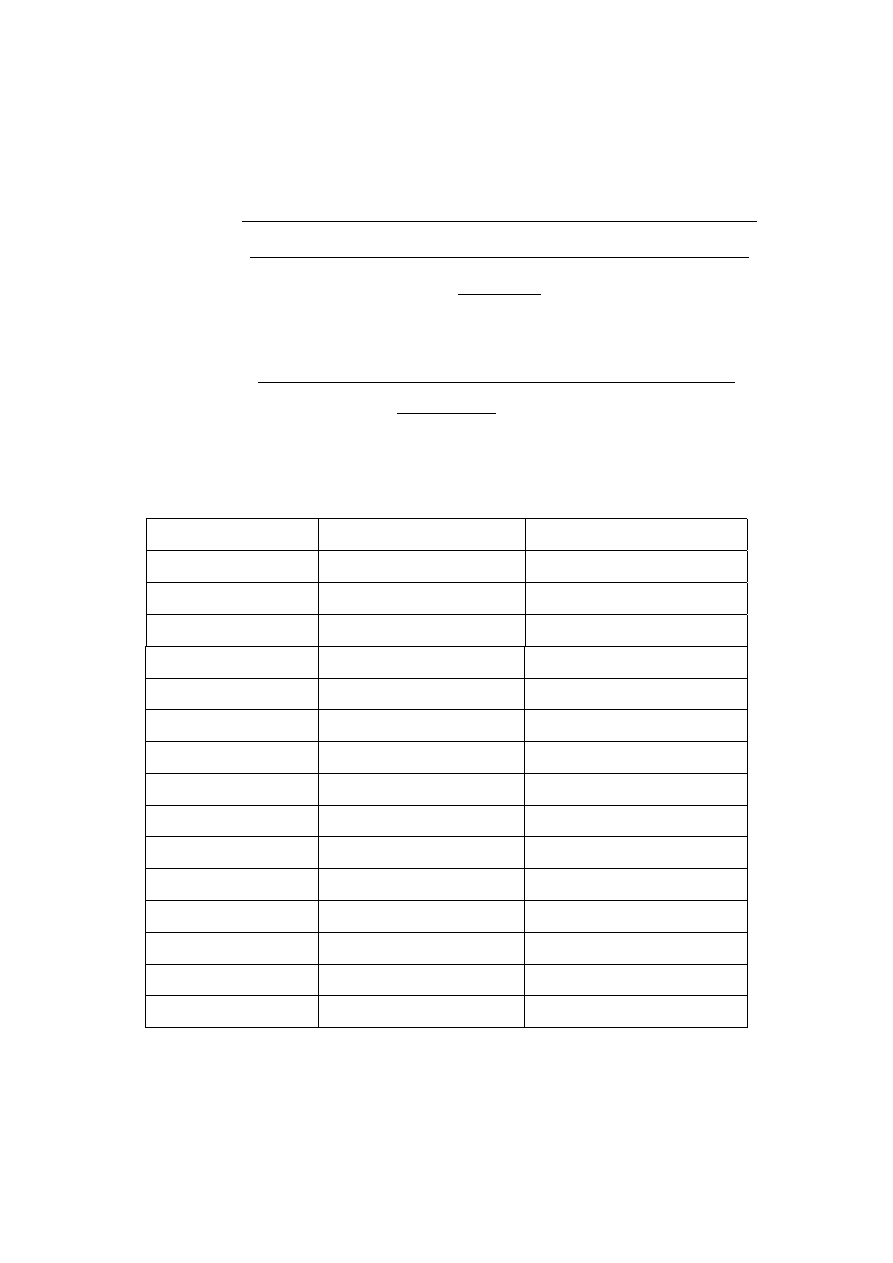
SPRAWOZDANIE Z ĆWICZENIA NR 5
Właściwości enzymów-ich chemiczna i fizyczna dezaktywacja
(przemiany chemiczne i fizyczne enzymów występujących w
żywności)
Ćwiczenie 1. Wpływ warunków obróbki termicznej i chemicznej na efektywność
blanszowania
Zmiana barwy próbek po dodaniu o-metoksyfenolu i H
2
O
2
.
Czas ogrzewania
Jabłko + woda
Ziemniak + woda
0
2
4
Czas ogrzewania
Jabłko + HCl + woda
Ziemniak + HCl + woda
0
2
4
Czas ogrzewania
Jabłko + NaOH + woda
Ziemniak + NaOH + woda
0
2
4
Czas ogrzewania
Jabłko + NaCl +woda
Ziemniak + NaCl + woda
0
2
4
+++ - czerwony intensywny
++ - czerwony
+ - lekko czerwony
brak zabarwienia
6

IMIĘ I NAZWISKO GRUPA DATA
1. Jakie różnice można zaobserwować w zależności od czasu ogrzewania a jakie w
zależności od rodzaju substancji dodatkowej?
2. Z czego wynikają zaobserwowane różnice (kiedy barwa nie pojawi się w ciągu 3,5 min
od momentu dodania roztworu nadtlenku wodoru należy uważać próbkę za dobrze
zblanszowaną)?
Suma punktów ………
7

IMIĘ I NAZWISKO GRUPA DATA
8
Wyszukiwarka
Podobne podstrony:
Ćwiczenie 8.5, technologia chemiczna, Fizyczna, Labolatorium
Ćwiczenie 7.2, technologia chemiczna, Fizyczna, Labolatorium
III kolokwium, technologia chemiczna, Fizyczna, Ćwiczenia
Ćwiczenie 5.5. i 7.4, technologia chemiczna, Fizyczna, Labolatorium
Ćwiczenie 8.1, technologia chemiczna, Fizyczna, Labolatorium
Ćwiczenie 8.3, technologia chemiczna, Fizyczna, Labolatorium
Ćwiczenie 6.1, technologia chemiczna, Fizyczna, Labolatorium
Ćwiczenie 10.6, technologia chemiczna, Fizyczna, Labolatorium
cwiczenie 91-93, Technologia chemiczna, Chemia fizyczna, 3 semestr, laboratorium
Ćwiczenie 10.1, technologia chemiczna, Fizyczna, Labolatorium
3 Elementy symetrii, enancjomery, projekcje Fischera, pojecie chiralności, Właściwości chemiczne i f
Badanie optoelektrycznych właściwości przyrządów półprzewodnikowych 5 , LABORATORIUM FIZYCZNE
7 Klasyfikacja enzymów i ich rola w metaboliźmie komórki
1 ćwiczenie (Analiza jakościowa wody) PARAMETRY FIZYCZNE WODY
PN EN 1744 1 2000 Badania chemicznych wlasciwosci kruszyw Analiza chemiczna
Furmański P Izolacje cieplne, mechanizmy wymiany ciepła, właściwości cieplne i ich pomiary
Ćwiczenie 4 Właściwości magnetyczne metali i stopów
więcej podobnych podstron