1
w w w. o p e r o n . p l
Poziom rozszerzony
Modele odpowiedzi do przyk∏adowego arkusza
egzaminacyjnego z chemii
Arkusz II
Nr
zadania
Modele odpowiedzi
Suma
punktów
1
2
3
21.
za 3 poprawne przyporzàdkowania – 2 pkt
za 2 poprawne przyporzàdkowania – 1 pkt
a) izotony, b) izotopy, c) izobary
0–2
22.
za schemat przemian – 1 pkt
208
82
Pb
$
204
80
X +
α $
200
78
Y +
α $
200
79
Z +
β
–
$
200
80
Hg +
β
–
za podanie iloÊci wyemitowanych czàstek
α i β
–
– 1 pkt
2 czàstki
α i 2 czàstki β
–
0–2
23.
za wybór zwiàzku: NH
4
Cl – 1 pkt
za narysowanie wzoru strukturalnego – 1 pkt
0–2
24.
za 3 poprawne przyporzàdkowania – 2 pkt
za 2 poprawne przyporzàdkowania – 1 pkt
a) P, b) F, c) P
0–2
25.
za ka˝de poprawne okreÊlenie charakteru chemicznego wraz z równaniem reak-
cji – po 1 pkt
NH
4
+
– kwas Brönsteda
NH
4
+
$ NH
3
+ H
+
NH
3
– zasada Brönsteda
NH
3
+ H
+
$ NH
4
+
H
3
O
+
– kwas Brönsteda
H
3
O
+
$ H
2
O + H
+
0–3
26.
za poprawne podanie barwy wskaênika dla ka˝dej probówki – 2 pkt
za poprawne podanie barwy wskaênika dla 2 probówek – 1 pkt
I czerwony, II ˝ó∏ty, III niebieski
za 3 poprawne równania reakcji wraz z ocenà – 2 pkt
za 2 poprawne równania reakcji wraz z ocenà – 1 pkt
I P
4
O
10
+ 6 H
2
O
$ 4 H
3
PO
4
(odczyn kwasowy)
II SiO
2
+ H
2
O
$ brak reakcji (odczyn oboj´tny)
III K
2
O + H
2
O
$ 2 KOH (odczyn zasadowy)
0–4
27.
za równania reakcji dysocjacji – 1 pkt
H
2
SO
4
$
#
H2O
H
+
+ HSO
4
–
HSO
4
–
$
#
H2O
H
+
+ SO
4
2–
0–2
N
H
+
H
H
H
–
Cl

za podanie sta∏ych równowagi obu reakcji – 1 pkt
K
I
=
K
II
=
[SO
4
2–
].[H
+
]
–––––––––––
[HSO
4
–
]
[HSO
4
–
].[H
+
]
–––––––––––
[H
2
SO
4
]
28.
za napisanie poprawnego równania reakcji – 1 pkt
2 Al + 3 H
2
SO
4
$ Al
2
(SO
4
)
3
+ 3 H
2
-
za podanie nazwy gazu: wodór – 1 pkt
za obliczenie iloÊci moli ka˝dego z substratów – 1 pkt
n
H
2
SO
4
= C
m
. V = 0,5 mol/dm
3
. 0,1 dm
3
= 0,05 mola
n
Al
= m
Al
/M
Al
= 3 g/27 g/mol = 0,11 mola
za zauwa˝enie, ˝e glinu jest nadmiar – 1 pkt
za obliczenie iloÊci gazu w oparciu o dane dla kwasu – 1 pkt
3 mole kwasu dajà 3 . 22,4 dm
3
wodoru
0,05 mola kwasu daje
x wodoru
x = 1,12 dm
3
0–5
29.
za równanie reakcji – 1 pkt
NaOH + HCl
$ NaCl + H
2
O
za obliczenie iloÊci zasady i kwasu – 1 pkt
C
P
= (m
s
/m
r
) . 100%
( m
s
= (C
P
. m
r
)/100%
m
NaOH
= 10 g, m
HCl
= 7,5 g
za zamian´ masy zasady i kwasu na mole – 1 pkt
n = m/M
n
NaOH
= 0,25 mola, n
HCl
= 0,2 mola
za zauwa˝enie, ˝e zasady jest nadmiar – 1 pkt
za podanie poprawnej odpowiedzi – 1 pkt
Papierek zabarwi si´ na niebiesko.
0–5
30.
za podanie prawid∏owego opisu obu reakcji – 1 pkt
reakcja I: egzotermiczna (egzoenergetyczna), reakcja II: endotermiczna (endo-
energetyczna)
za ka˝dy z wykresów – po 1 pkt
0–3
31.
za równania po∏ówkowe – 1 pkt
za podanie nazw procesów – 1 pkt
+II +VII
Mn
2+
$ Mn + 5e proces utleniania
+IV
+II
Pb + 2 e
$ Pb proces redukcji
za dobranie wspó∏czynników – 1 pkt
2 Mn
+2
+ 5 PbO
2
+ 4 H
+
$ 2 MnO
4
–
+ 5 Pb
+2
+ 2 H
2
O
za podanie utleniacza i reduktora – 1 pkt
utleniacz – o∏ów w PbO
2
, reduktor – jony Mn
2+
0–4
1
2
3
Reakcja I
t
E
E
sub
∆H
E
prod
Reakcja II
t
E
E
sub
∆H
E
prod
2
w w w. o p e r o n . p l
■
C H E M I A – P O Z I O M R O Z S Z E R Z O N Y
3
w w w. o p e r o n . p l
A R K U S Z I I – M O D E L E O D P O W I E D Z I
■
1
2
3
32.
za ka˝de równanie reakcji – po 1 pkt
CaC
2
+ 2 H
2
O
$ Ca(OH)
2
+ CH–
–
–CH
CH–
–
–CH + 2 H
2
$ CH
3
–CH
3
CH
3
–CH
3
+ Cl
2
/h
υ $ CH
3
–CH
2
Cl + HCl
CH
3
–CH
2
Cl + KOH/H
2
O
$ CH
3
–CH
2
OH+ KCl
Uwaga! Reakcja otrzymywania etanu z etynu mo˝e byç zapisana w dwóch eta-
pach, ale punkt przyznajemy za otrzymanie etanu.
0–4
33.
za ka˝dy wzór wraz z nazwà zwiàzku – po 1 pkt
0–3
34.
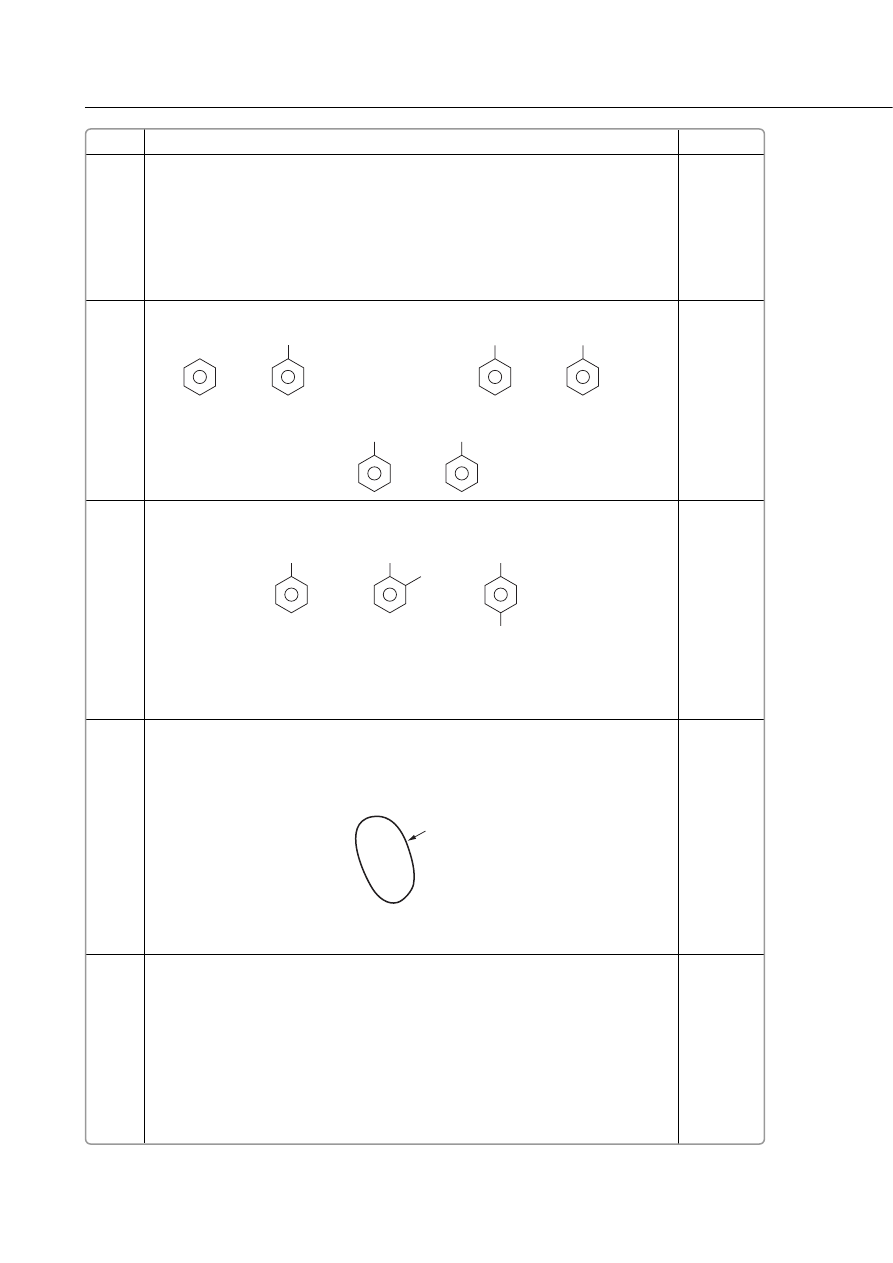
za podanie równania reakcji – 1 pkt
za podanie nazw produktów – 1 pkt
produkt I 1-nitro-2-metylobenzen, produkt II 1-nitro-4-metylobenzen
za podanie, który zwiàzek wyst´puje w przewadze – 1 pkt
W przewadze znajduje si´ 1-nitro-2-metylobenzen.
0–3
35.
za podanie mo˝liwych dipeptydów – 1 pkt
Ala-Ala, Cys-Cys, Ala-Cys, Cys-Ala
za przyk∏adowe równanie reakcji otrzymywania dipeptydu – 1 pkt
za zaznaczenie wiàzania peptydowego – 1 pkt
0–3
36.
za napisanie równania reakcji i nazwanie produktów – 1 pkt
2 C
12
H
22
O
11
+ H
2
0
$
H
+
C
6
H
12
O
6
+ C
6
H
12
O
6
glukoza
fruktoza
(cukier owocowy)
za wyznaczenie mas molowych sacharozy i fruktozy – 1 pkt
M
C
12
H
22
O
11
= 342 g/mol, M
C
6
H
12
O
6
= 180 g/mol
za obliczenie iloÊci fruktozy – 1 pkt
342 g sacharozy daje 180 g fruktozy
10000 g daje
x
x = 536,3 g
0–3
nitrobenzen
$
HNO
3
H
2
SO
4
NO
2
anilina
NO
2
NH
2
$
[H]
chlorowodorek aniliny
NH
2
NH
3
Cl
$
HCl
produkt I
produkt II
$
HNO
3
H
2
SO
4
CH
3
CH
3
NO
2
CH
3
NO
2
2
+
$
$
CH
3
––
CH
––
COOH+H
2
N
––
CH
––
COOH
CH
2
––
SH
NH
2
––
––
CH
3
––
CH
––
C
––
N
––
CH
––
COOH
O
wiàzanie peptydowe
CH
2
––
SH
NH
2
––
H
––
–– ––
––
Wyszukiwarka
Podobne podstrony:
0001 01 02 odp
0000 01 01 odp
0000 01 01 odp
03 0000 015 02 Leczenie dystonii miesniowych toksyna botulinowa
01 02 tytulowa
ei 2005 01 02 s078
03 0000 035 02 Leczenie immunosupresyjne sirolimusem
LKM cw 01 02
03 0000 034 02 Leczenie immunosupresyjne mykofenolanem mofetylu lub mykofenolanem sodu
01 02 2013
03 0000 020 02 Zastosowanie abciximabu w angioplastyce wiencowej
2007 05 02 odp
03 0000 013 02 Leczenie przedwczesnego dojrzewania plciowego
01 02 (3)
więcej podobnych podstron