
Transfer masy i ciepła w przemyśle chemicznym i
biochemicznym
Techniki separacji. Flokulacja, sedymentacja
Precypitacja
Rozbijanie ścian komórek
Techniki zagęszczania
Ekstrakcja
Filtracja
Ultrafiltracja
Odwrócona osmoza
Wirowanie
ELEMENTY BIOTECHNOLOGII
WYKŁAD NR 6
literatura wykorzystana do wykładu
K. Szewczyk: Technologia biochemiczna, Wydawnictwa
Politechniki Warszawskiej 1997
Aiba, Humprey, Millis: Inżynieria biochemiczna, WNT
Warszawa 1977.
S. Russel: Biotechnologia, PWN Warszawa 1990.
Basic Biotechnology, Ed: C. Ratledge & B. Kristiansen,
Cambridge University Press, 2001

Transfer ciepła
FERMENTACJA JEST PROCESEM EGZOTERMICZNYM
dla prędkości wydzielania ciepła > 20 MJ m
-3
(tj. pochłanianie tlenu z prędkością ok. 5 kg m
3
h
-1
) proces chłodzenia jest trudny
w dużych bioreaktorach czynnikiem limitującym wzrost mikroorganizmów
może być transfer ciepła a nie transfer O
2
(transfer masy)
typowa aktywność drobnoustrojów w
bioreaktorze powoduje wydzielanie się:
10-50 MJ/m
3
empirycznie:
szybkość wydzielania ciepła [ MJ L
-1
h
-1
]=12% szybkości pochłaniania tlenu [mmolO
2
L
-1
h
-1
]
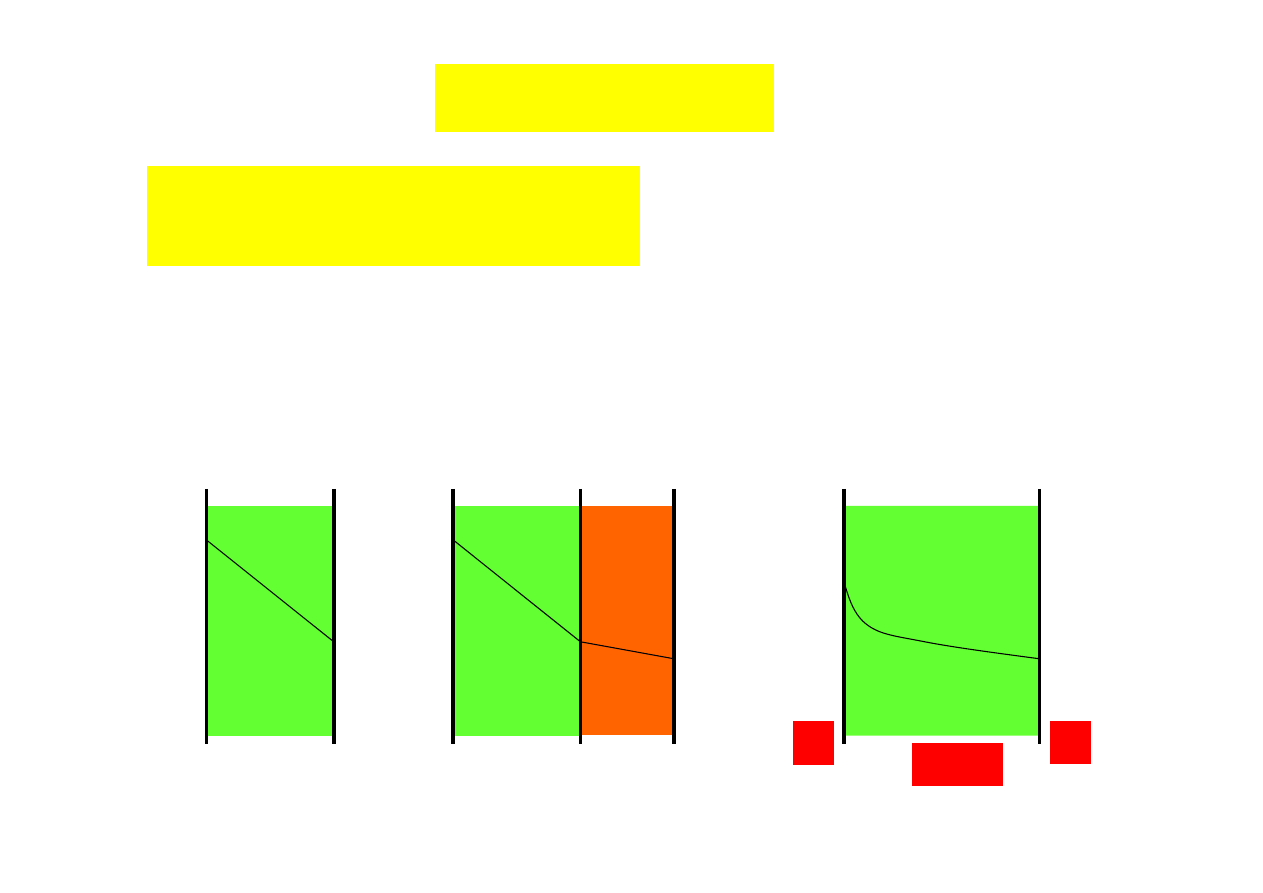
Transfer ciepła
szybkość wymiany ciepła
Q = -
λ ∆t F/s
λ -ogólny wspólczynnik przewodzenia ciepła
F - powierzchnia wymiany ciepła
s - grubość ścianki
∆t- średnia różnica temperatur
znak ujemny wynika z kierunku przepływu
1/λ jest opornością przewodzenia ciepła
1/λ = Σ(1/λ
i
)
np. oporność:
warstewki cieczy
ścian reaktora
warstewki wody chłodzącej
t
1
t
2
t
1
t
2
t
3
t
1
t
2
ścianka płaska
dwuwarstwowa
ścianka płaska
jednowarstwowa
ścianka cylindryczna
r
1
r
2
r
1
< r
2
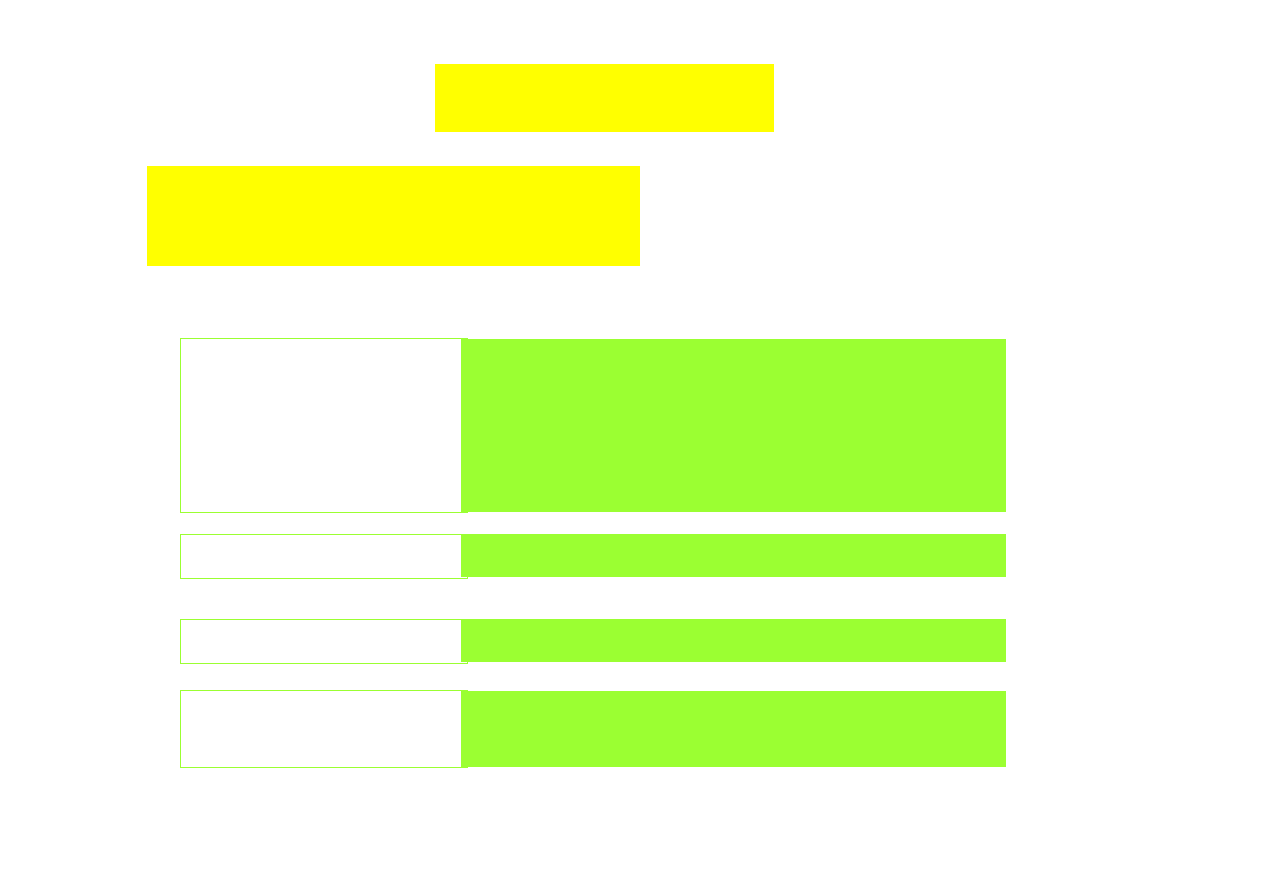
Transfer ciepła
szybkość wymiany ciepła
Q = -
α ∆t F
α -wspó
ł
czynnik wnikania ciepła
współczynnik przewodzenia ciepła
współczynnik lepkości dynamicznej
współczynnik rozszerzalności objętościowej
ciepło właściwe strumienia
gęstość płynu
własności
fizykochemicznych
płynu
rozmiary liniowe
kształtu ścianki
liniowa prędkość przepływu
stanu ruchu
współczynnik wnikania ciepła jest zależny od
różnica temperatur między ścianką i
płynem
stanu termicznego
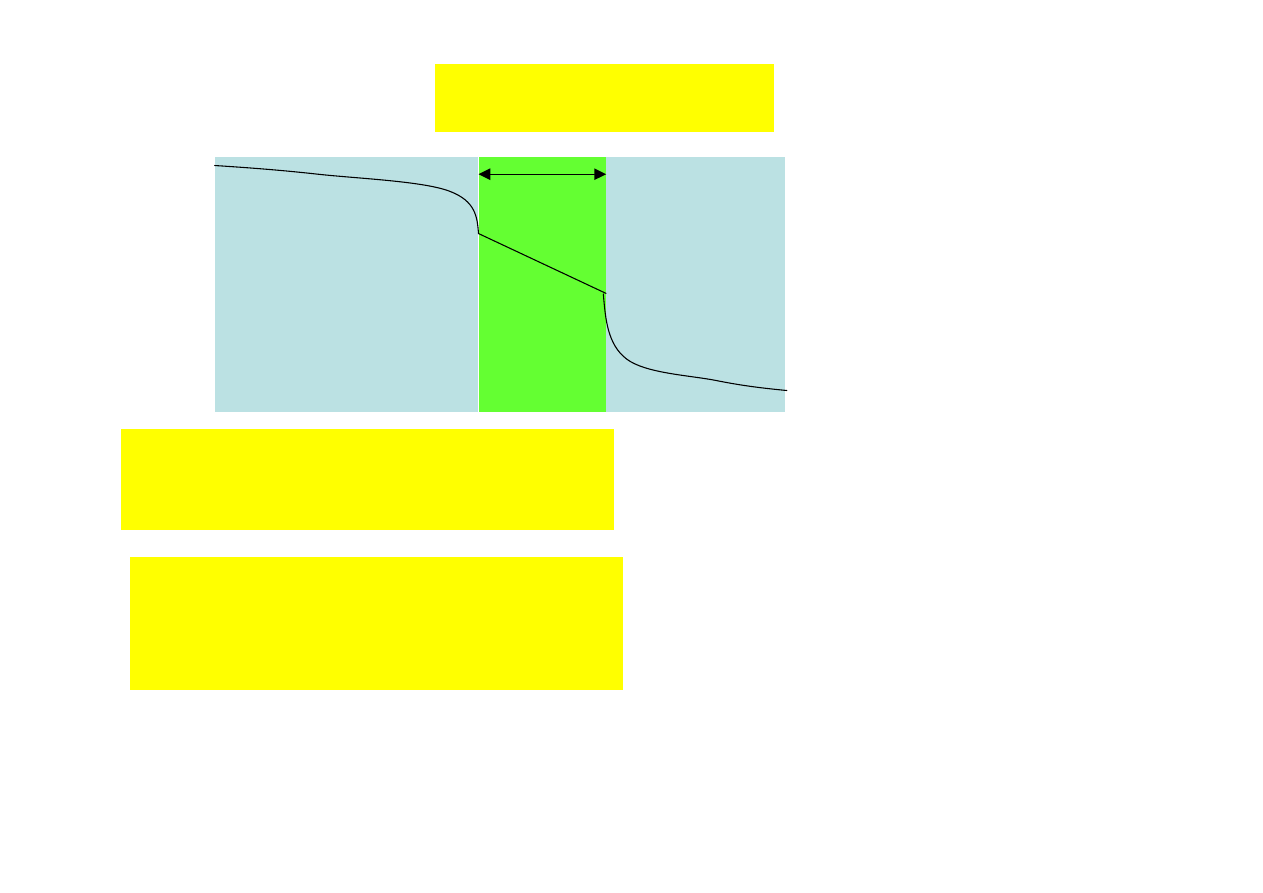
Transfer ciepła
t
2
t
3
t
1
t
4
płyn 1
płyn 2
ścianka
szybkość przenikania ciepła
Q = K F
∆t
λ -wspólczynnik przewodzenia ciepła
s- grubość ścianki
α
1
-współczynnik wnikania w warstwie 1
α
2
-współczynnik wnikania w warstwie 2
sumaryczny współczynnik przenikania
ciepła
1/K = 1/
α
1
+ s/λ + 1/α
2
∆t- całkowita napędowa różnica temperatur
∆t = t
1
-t
4
s
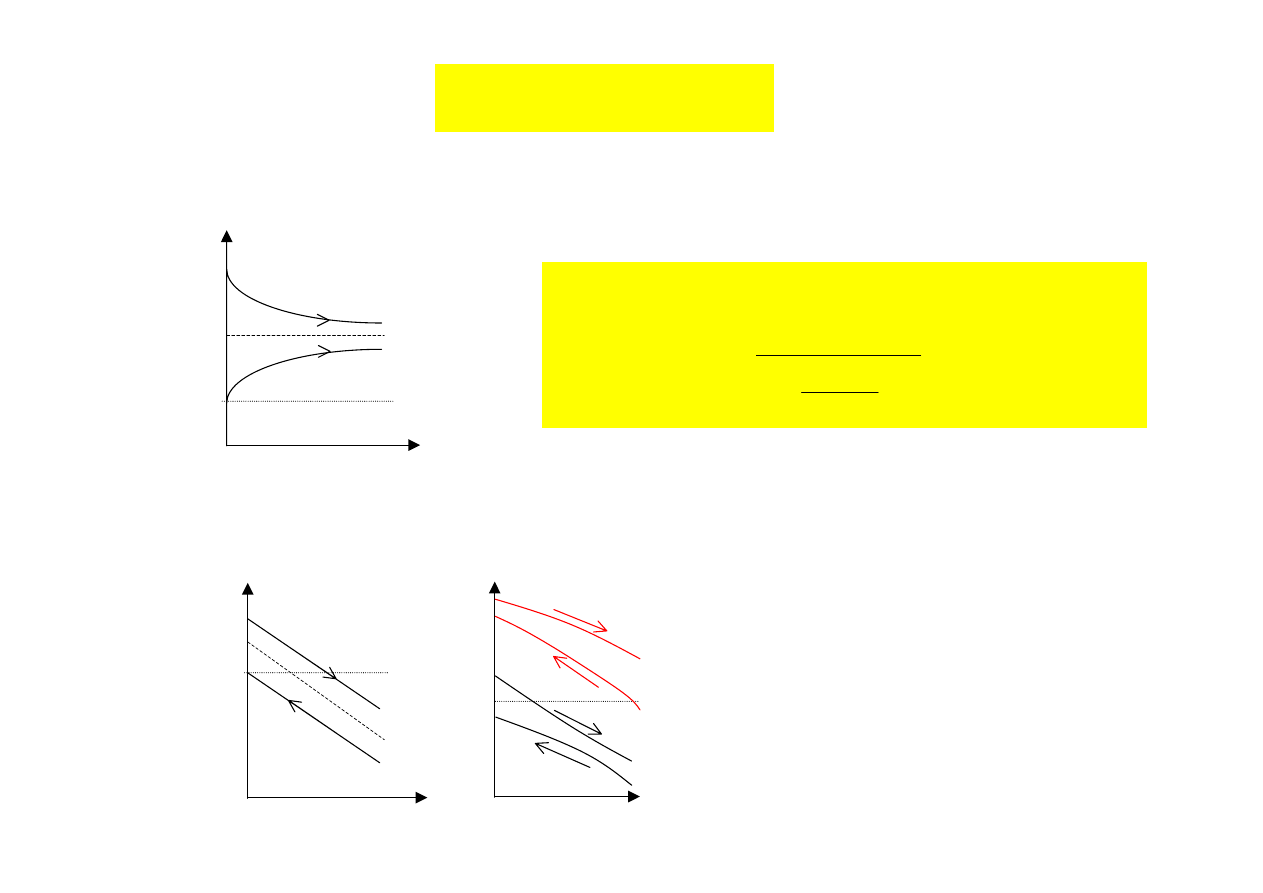
Transfer ciepła
KIERUNEK PRZEPŁYWU STRUMIENI WYMIENIAJĄCYCH CIEPŁO
•
współprąd t
∞
= t
średnia
•
przeciwprąd
symetria zależy od
stosunku pojemności cieplnej obu mediów
M
i
C
i
-
iloczyn natężenia przepływu i ciepła
właściwego czynnika i-tego
dł. ścianki
zastępcza różnica temperatur dla obu typów wymiany :
(T
1
-t
1
)- (T
2
-t
2
)
(T
1
-t
1
)
(T
2
-t
2
)
∆t
zast
=
ln
T
1
i t
1
- temperatury początkowe czynników 1 i 2
T
2
i t
2
- temperatury końcowe czynników 1 i 2
długość ścianki
T
1
T
2
t
1
t
2
dł. ścianki
T
1
t
2
T
2
t
1
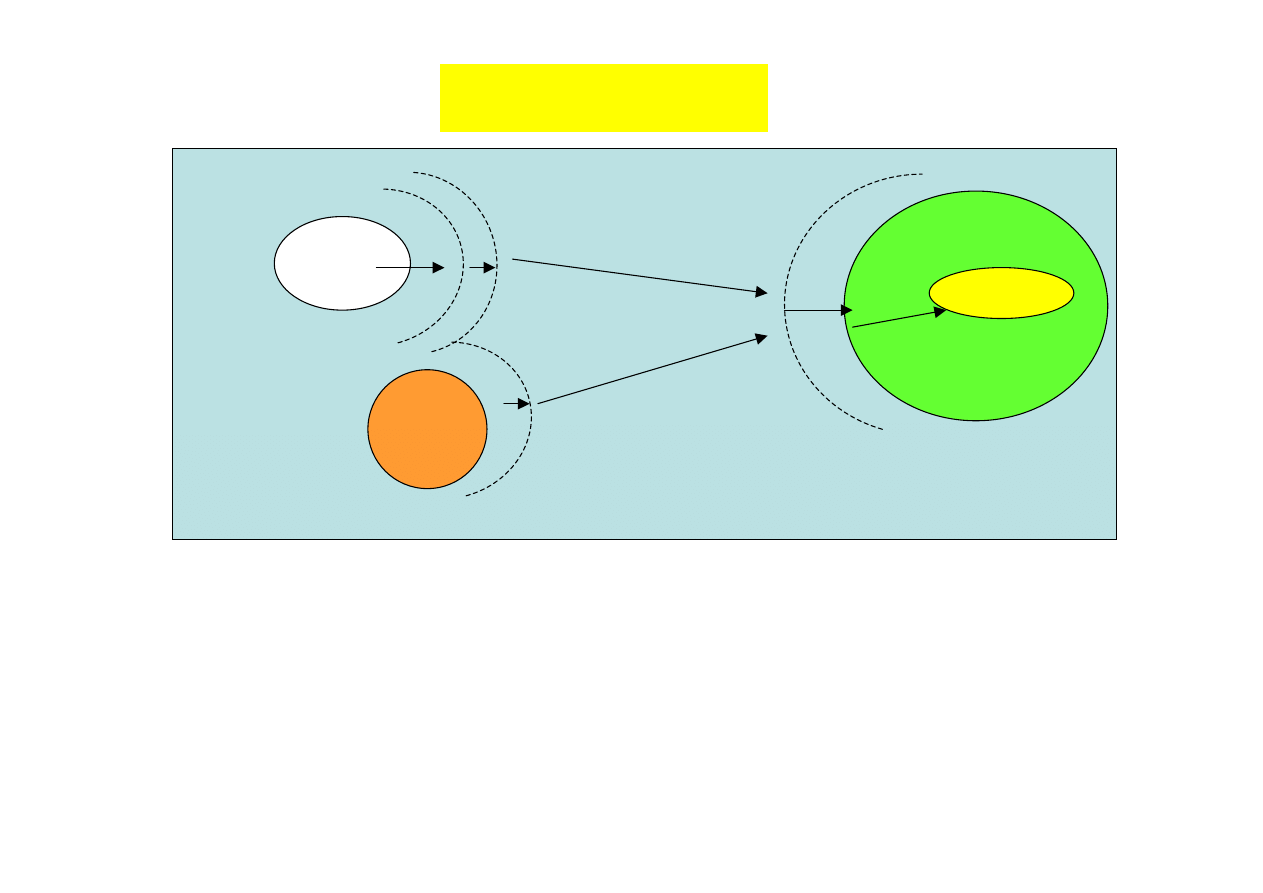
Transfer masy
gaz
1. Transfer z fazy gazowej do cieczy
2. Transfer dyfuzyjny i konwekcyjny przez cienką warstewkę (film) cieczy
3. Transport przez fazę ciągłą
4. Dyfuzja przez warstewkę otaczającą mikroorganizm lub agregat
mikroorganizmów
5. Transport bierny (dyfuzja) lub czynny (enzymy transportujące) do miejsca
reakcji.
1
2
2
3
3
4
5
pożywka
mikroorganizm /
komórka
Transfer masy
1. Transfer na granicy faz jest zazwyczaj najwolniejszy
gaz- ciecz (O
2
), ciecz-ciecz (węglowodory-woda), reaktory membranowe itd.
2. Transfer wewnątrz jednej fazy (np. gdy komórki są unieruchomione)
3. Transport przez błony komórkowe:
CZYNNIKI LIMITUJĄCE TRANSPORT
reguła 1 - najwolniejszy etap jest czynnikiem limitującym
reguła 2 - ogólny opór transportu jest sumą oporów poszczególnych etapów
•transport bierny (dyfuzyjny)
- od stężenia większego do mniejszego (zgodnie z gradientem stężeń)
•transport wspomagany
- przy użyciu czynników transportujących
- od stężenia większego do mniejszego (zgodnie z gradientem stężeń)
•transport aktywny (dyfuzja wspomagana działaniem białek
transportujących)
- od stężenia mniejszego do większego (niezgodnie z gradientem stężeń), wymaga
dostarczenia energii z zewnątrz
dwuwarstwy lipidowe są nieprzepuszczalne dla cząsteczek polarnych !
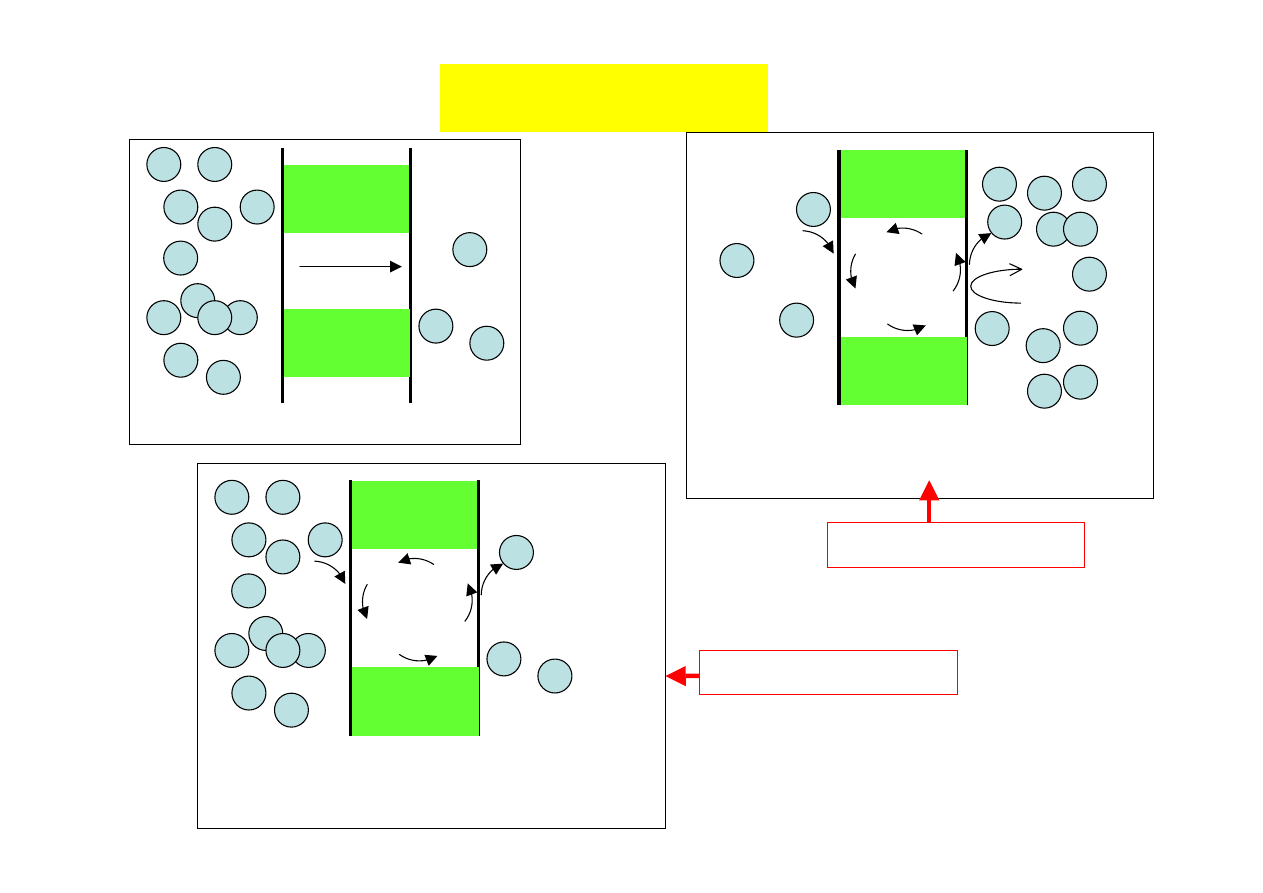
Transfer masy
C
A1
C
A2
A
A
A
A
A
A
A
A
A
A
A
A
A
A
A
transport bierny
(dyfuzyjny)
C
A1
C
A2
A
A
A
A
A A
A
A
A
A
A
A
A
A
A
transport aktywny
działanie białek transportujących
C
CA
C
CA
ADP
ATP
C
A1
C
A2
A
A
A
A
A
A
A
A
A
A
A
A
A
A
A
transport wspomagany
(dyfuzja wspomagana działaniem
białek transportujących)
C
CA
C
CA
∆G = RT ln (C
A2
/C
A1
)
C
A2
> C
A1
∆G > O
C
A2
< C
A1
∆G < O
konieczna jest dodatkowa energia
proces samorzutny
∆G = RT ln (C
A2
/C
A1
) + ZF
∆Ψ
Z-ładunek, F-stała Faradaya
∆Ψ-różnica potencjałów po obu stronach membrany
Transfer masy
∆G = + 33.6 kJ/mol
pH w plazmie krwi = 7.4
pH w żołądku ssaków = ok. 1
∆G = RT ln (C
A2
/C
A1
) + ZF
∆Ψ
Z-ładunek, F-stała Faradaya
∆Ψ-różnica potencjałów po obu stronach membrany
gradient H
+
= 10
-1
/10
-7
hydroliza ATP to
+ 30.5 kJ/mol ATP
szybko
ść
transportu
stężenie
tran
spo
rt b
iern
y
transport wspo
magany
w transporcie wspomaganym
stosowane są reguły kinetyki
Michaelisa-Menten
nasycenie
wzrost
liniowy
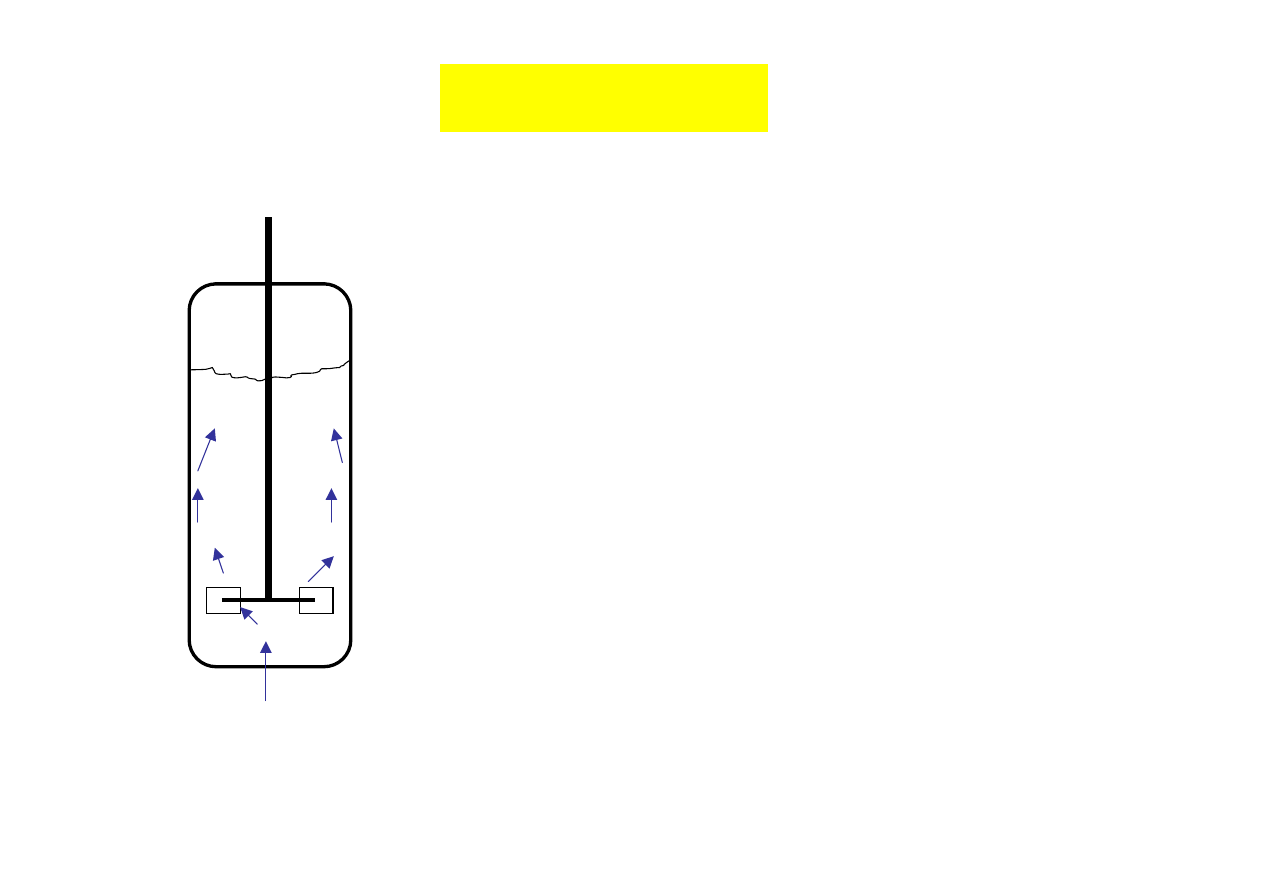
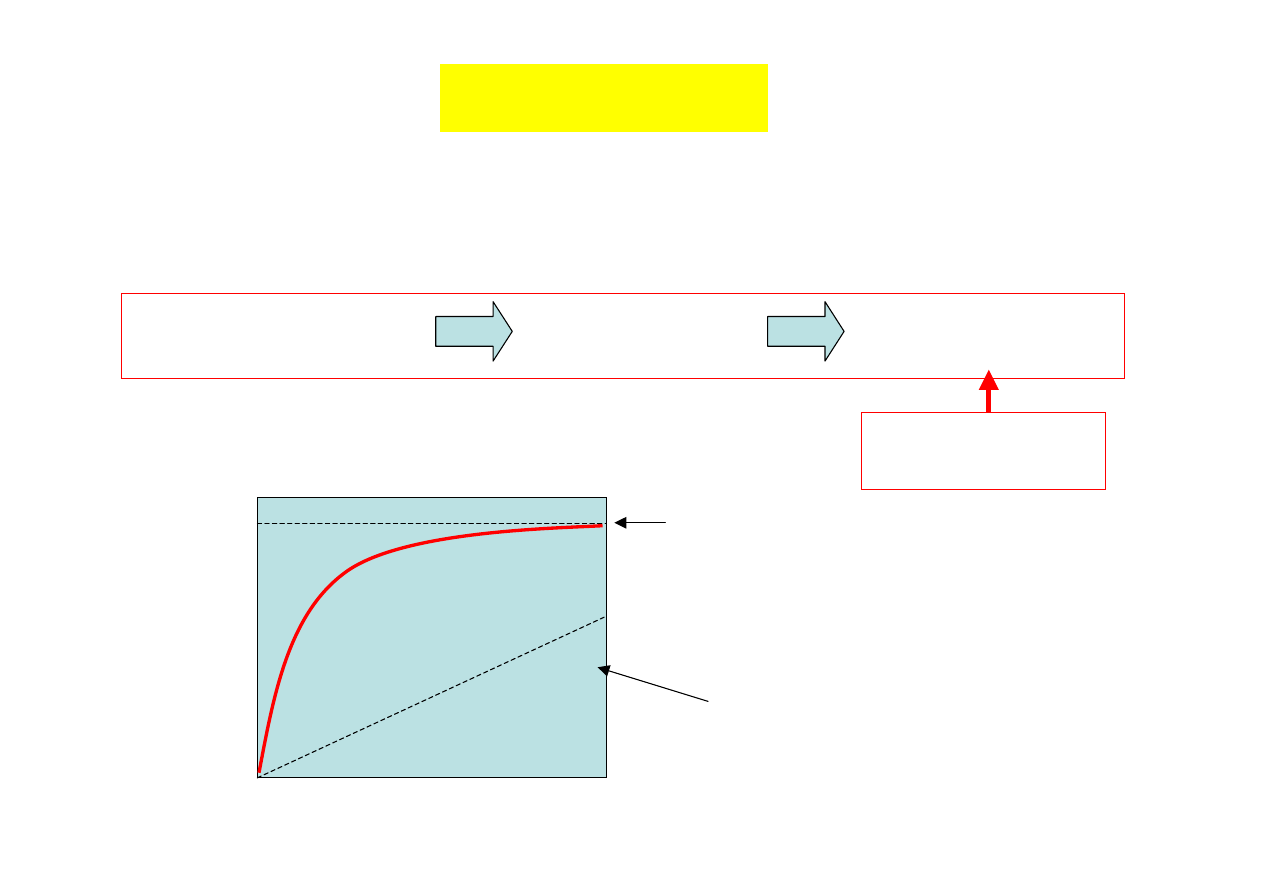
Transfer masy
powietrze
niskie
stęż. O
2
wysokie
stęż. O
2
CZYNNIKI LIMITUJĄCE TRANSPORT TLENU W DUŻYCH BIOREAKTORACH
•trudności konstrukcyjne (gdy > 300 m
3
)
dla reaktorów >10m
3
procesy transportu są relatywnie powolne
•zużycie mocy nie powinno być większe niż 5 kW / m
3
•prędkość przepływu tlenu nie powinna być > 0.1 m / s
•wzrasta również ciśnienie CO
2
•ciśnienie O
2
spada w miarę przesuwania się w górę
reaktora
(maleje siła napędowa procesu)
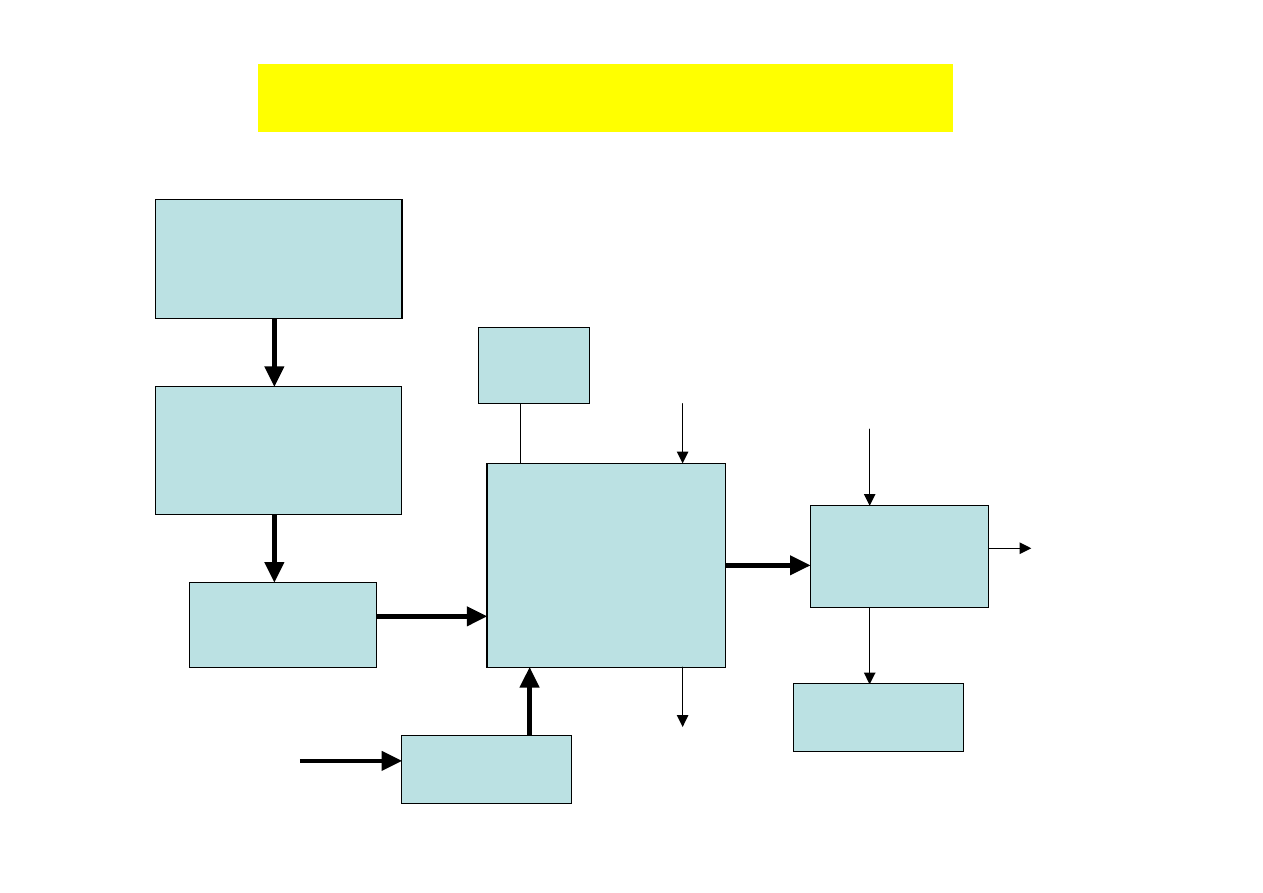
Techniki wydzielania produktów
gromadzenie i
przechowywanie
surowców
przygotowanie
surowców
feedstock storage
raw materials preparation
and pretreatment
wyjaławianie
sterilization
bioreaktor
kontrola
procesu
sprężanie
compression
powietrze
energia
ciepło
wydzielenie
produktów
product recovery
energia
odpady
waste
produkt
Techniki wydzielania produktów
Downstream processing - termin określający fazy wydzielania i oczyszczania
bioproduktów
w masie poreakcyjnej mogą być np.
całe komórki, aminokwasy, rozpuszczalniki, antybiotyki, enzymy, białka,
substancje farmaceutyczne, produkty uboczne i odpadowe, nieprzereagowane pożywki
TECHNIKI SPECJALNIE UŻYTECZNE W BIOTECHNOLOGII:
• oddzielanie ciał stałych i cieczy (solid liquid separation or clarification)
• zatężanie
(concentration)
• oczyszczanie (purification)
• tworzenie preparatu
( formulation)
Upstream processing - fazy przygotowywania surowców i dostarczenie ich
do bioreaktora
stężenie produktu w masie poreakcyjnej:
etanol , kwas cytrynowy - powyżej 10% masowych
większość bioprocesów - około 0.5 % masowych
witamina B
12
- 20 g/m
3
(tj. ok. 0.002 %)
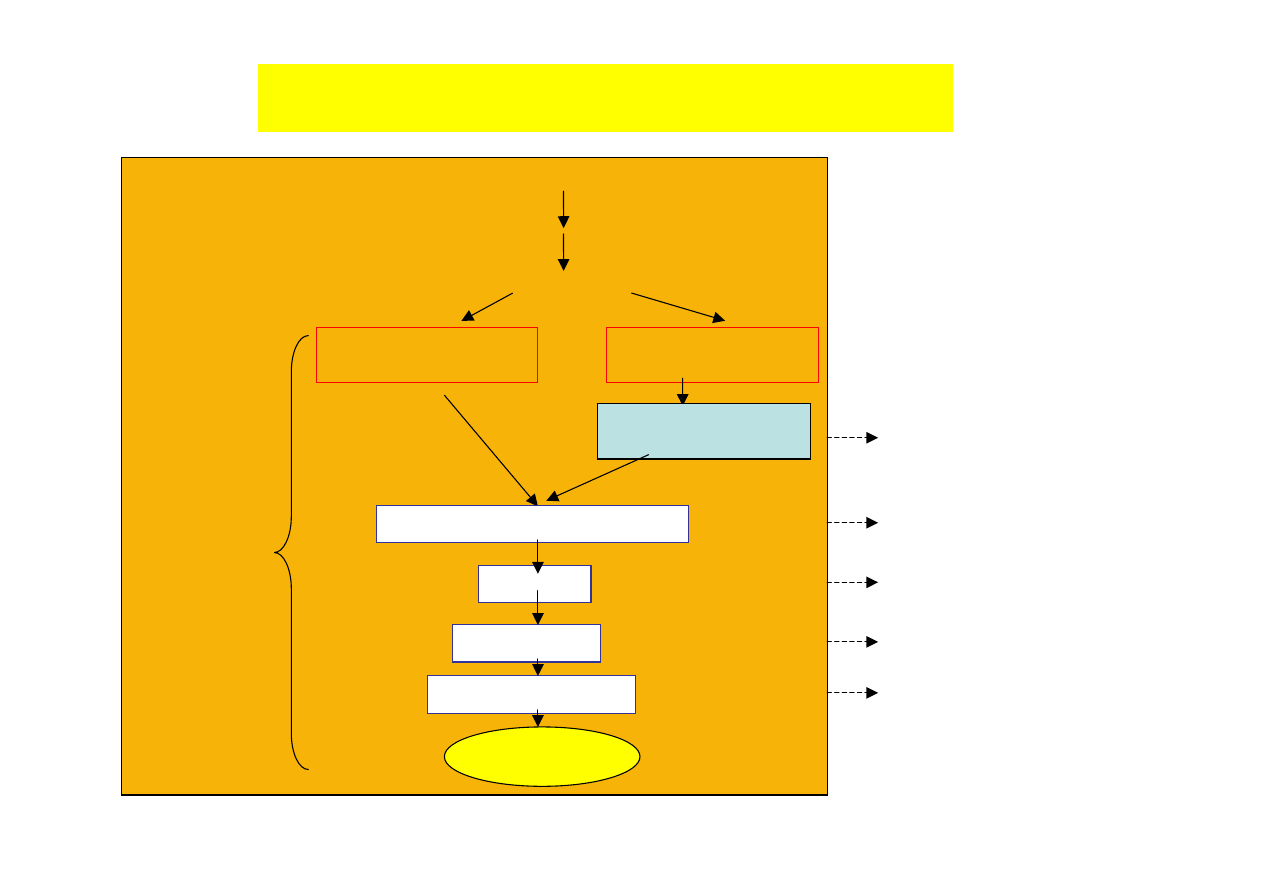
Techniki wydzielania produktów
Upstream process
produkcja
Downstream
process
produkt wewnątrz
komórkek
produkt na zewnątrz
komórkek
rozbijanie
komórkek
oddzielanie ciał stałych i cieczy
zatężanie
oczyszczanie
tworzenie preparatu
produkt końcowy
chemiczne, fizyczne
mechaniczne, enzymatyczne
odwirowanie, sedymentacja,
ekstrakcja, filtracja
odparowanie, ultrafiltracja,
adsorpcja, wytrącanie
chromatografia
krystalizacja, liofilizacja
rozpylanie,
filtracja wyjałowiająca
Rozbijanie ścian komórek
dezintegracja komórek
mechaniczna
niemechaniczna
w fazie ciekłej
- ultradźwięki
- ciśnienie
- mieszanie
w fazie stałej
-rozcieranie
odwadnianie
- powietrzem
- próżniowe
- rozpuszczalnikami
liza
- fizyczna
- chemiczna
- enzymatyczna
- biologiczna
•dezintegracja jest stosowana gdy metabolit nie jest wydzielany na zewnątrz mikroorganizmu
•komórki drobnoustrojów są bardziej odporne na zniszczenie niż komórki zwierzęce

Rozbijanie ścian komórek
dezintegracja komórek na skalę przemysłową
metoda ciśnieniowa
ekspansja zawiesiny komórek przy wypływie przez dyszę, p=ok. 60 MPa do 100 MPa
1. ochłodzenie mieszaniny do ok. 4
o
C
2. sprężanie (towarzyszy temu wzrost temp. o 2,2-2,4
o
C / 10 MPa)
wydajność aparatów: do 6 m
3
/godz
homogenizat jest trudny do obróbki (zawiesina drobnych cząsteczek o właściwościach żelujących)
mielenie w młynach kulowych
poziome bębny wypełnione kulkami szklanymi o średnicy 0.3-0.4 mm
dezintegracja komórek na skalę laboratoryjną
• dezintegratory wysokoobrotowe,
• dezintegratory ultradźwiękowe
• metody enzymatyczne: enzymy proteolityczne
• kilkakrotne zamrażanie i rozmrażanie mieszaniny komórek
• operacje termiczne i suszenie (szok termiczny)
• szok osmotyczny
• metody chemiczne (stosowanie kwasów, ługów, detergentów, rozpuszczalników, antybiotyków)

Oddzielanie ciał stałych i cieczy
operacje jednostkowe: filtracja, odwirowanie, flokulacja i sedymentacja
filtracja plackowa
filtracja objętościowa
filtracja dynamiczna
zatrzymywanie cząstek stałych na placku filtracyjnym
prasa filtracyjna, próżniowe filtry obrotowe, filtry taśmowe
ociekanie
przemywanie
suszenie
usuwanie
osadu
próżniowy filtr obrotowy
(przykład filtracji plackowej)
próżnia
wewnątrz
zastosowanie: do wydzielania grzybni i drożdży, krystalicznych metabolitów, precypitatów
osady i zawiesiny biologiczne mają dużą ściśliwość i małą przepuszczalność,
pozorna lepkość wzrasta w miarę filtracji
zatrzymywanie cząstek stałych
na przegrodzie filtracyjnej -
w metodzie tej chodzi o czystość filtratu
(przesączu) a nie o wydzielenie osadu
szybkoobrotowe mieszadło lub obracający się
filtr nie dopuszcza do powstawania placka
następuje zatężanie a nie osadzanie się zawiesin
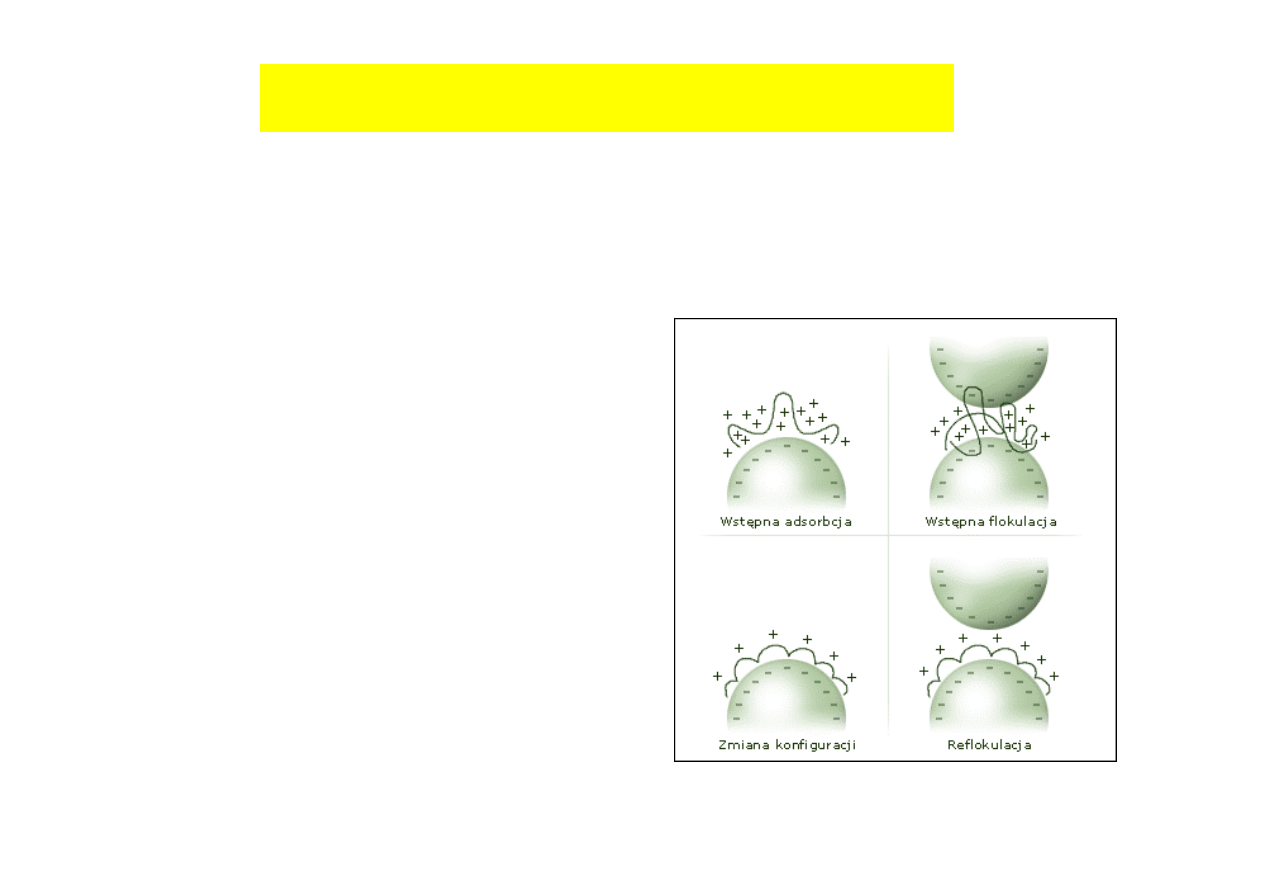
Oddzielanie ciał stałych i cieczy
flokulacja,
kłaczkowanie
- wytrącanie osadu w wyniku neutralizacji
ładunków na powierzchni komórek,
- powodowana dodatkiem odpowiednich
elektrolitów (sole nieorganiczne,
hydrokoloidy, polielektrolity organiczne,
kwasy lub zasady)
- flokulacja odwracalna i nieodwracalna
- zależy od pH, temperatury, siły jonowej,
- prowadzona w odstojnikach
- w przypadku bakterii i komórek- konieczna jest wstępna obróbka
w celu powstania aglomeratów
sedymentacja
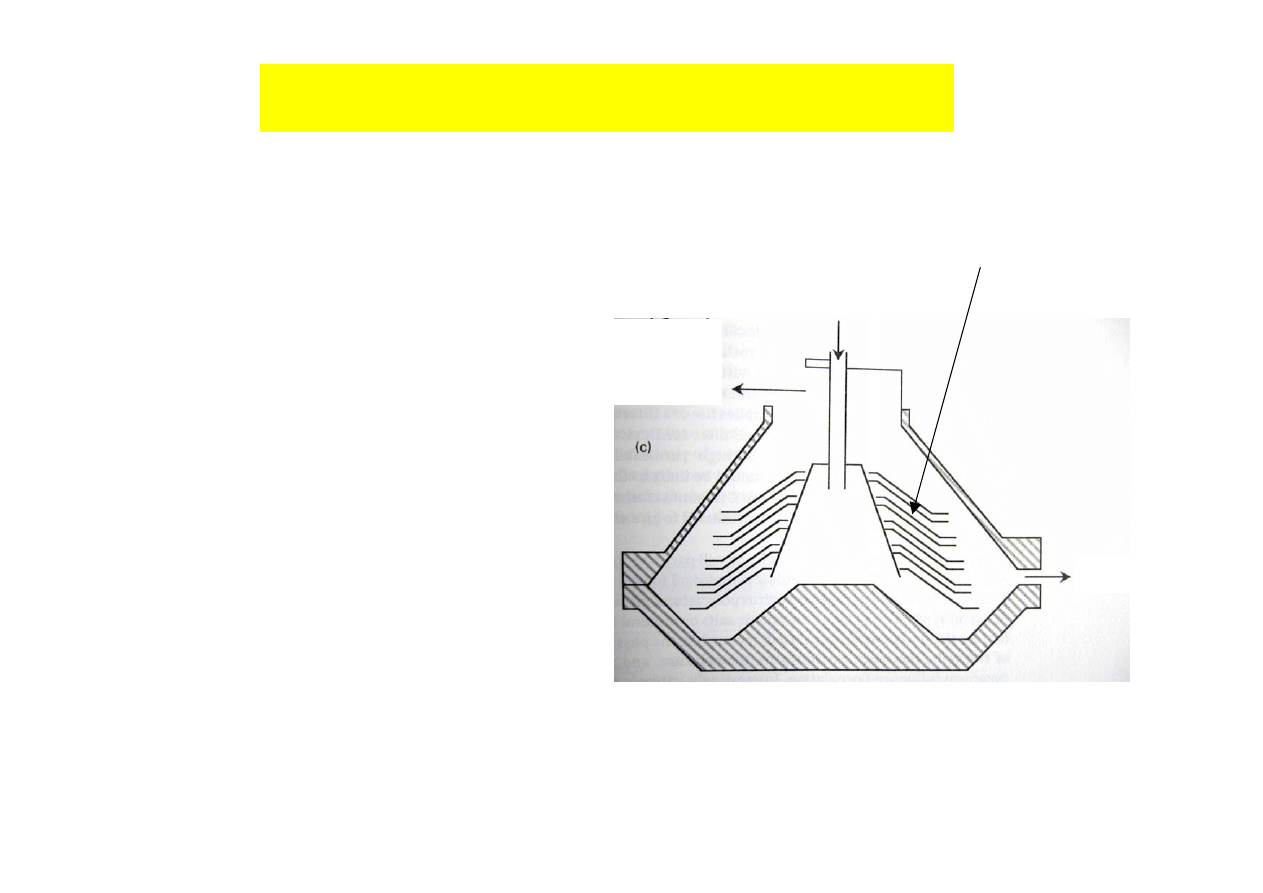
Oddzielanie ciał stałych i cieczy
odwirowanie
wady wirowania:
•wysokie koszty,
•niezbyt dużą dokładność
odwirowania (supernatant zawiera
10
3
-10
5
komórek na ml)
wirówki sedymentacyjne (do zagęszczania biomasy)
i filtracyjne ( do wydzielania osadu)
dyski (od 30 do 200)
osad
odpływ
ciecz
pofiltracyjna
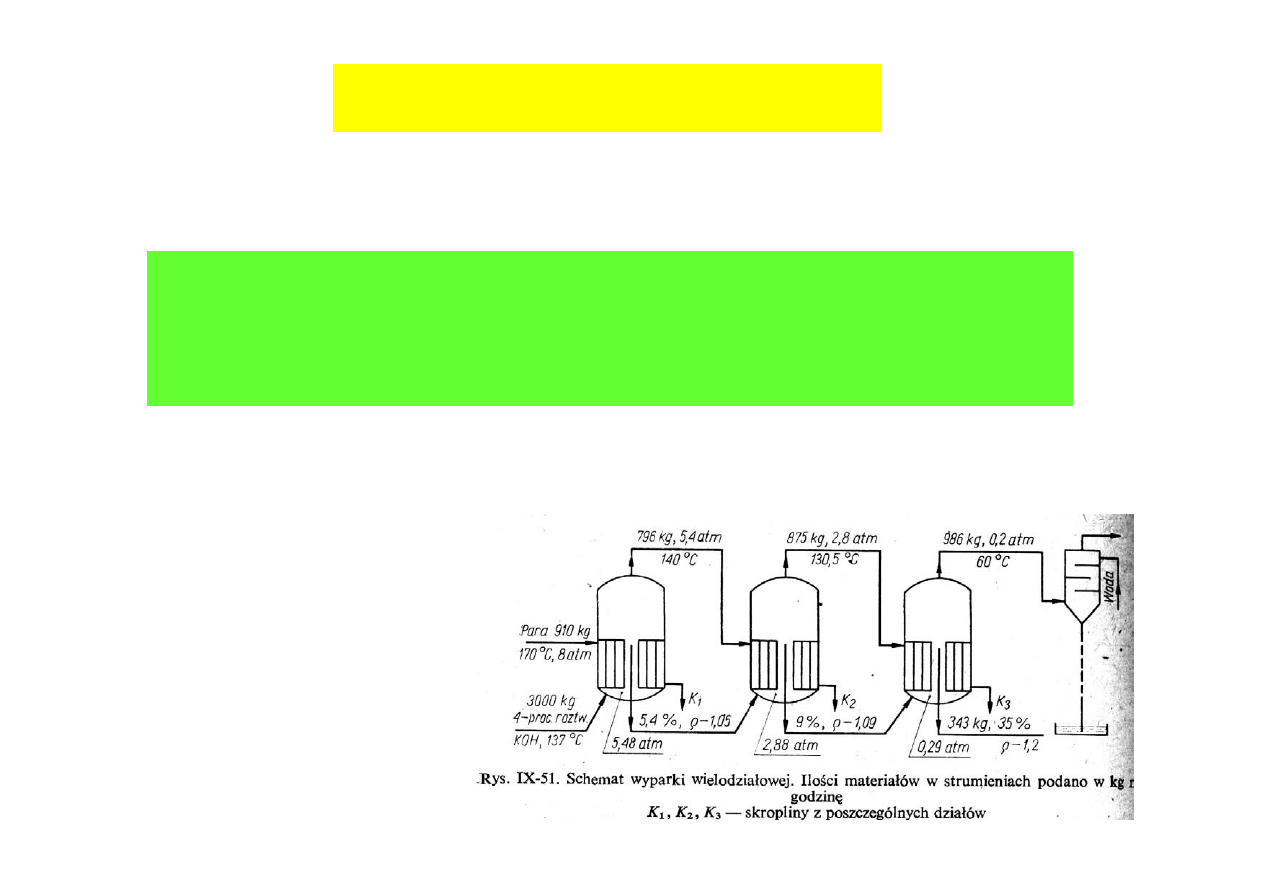
Zagęszczanie roztworów
zagęszczanie termiczne (odparowanie)
PROBLEM: bioprodukty są zazwyczaj wrażliwe na wzrost temperatury
rozwiązanie:
1. krótki czas kontaktu zagęszczanego roztworu (aparaty wyparne cienkowarstwowe)
2. stosowanie podciśnienia
stosowane zwłaszcza wtedy, gdy trzeba odzyskać rozpuszczalnik po ekstrakcji
wady tej metody: wysoki koszt, możliwość powstawania piany,
przypomnienie: zasada najlepszego wykorzystania energii (wykład 1)
Zagęszczanie roztworów
ekstrakcja
ekstrakcja ciecz-ciecz
współczynnik podziału: K= C
faza1
/C
faza2
1. ekstrakcja
fizyczna
związki nie zmieniają swojego stopnia zjonizowania.
poszukuje się rozpuszczalnika dla którego K będzie największe
2. ekstrakcja dysocjacyjna
różnica stałych dysocjacji solutu powoduje preferowanie jednego z rozpuszczalników
3. reakcyjna
do rozpuszczalnika dodana jest substancja czynna (np. amina, eter koronowy)
selektywnie kompleksująca ekstrahowaną substancję.
Metoda doskonała dla substancji dobrze rozpuszczalnych w wodzie.
penicylina:
1. ekstrakcja octanem butylu z płynu pofermentacyjnego o pH 2,5-3
2. re-ekstrakcja do fazy wodnej w pH 5-7.5
4. ekstrakcja nadkrytyczna
rozpuszczalniami są substancje w warunkach poniżej temperatury lub ciśnienia krytycznego
(wyższa dyfuzyjność, niższa lepkość, nie są toksyczne),
t
kryt
CO
2
=31.3
o
C , p
kryt
CO2=72.9 bar
łatwość wydzielenia produktu (zamiana cieczy na gaz)
współprąd i przeciwprąd materiałowy
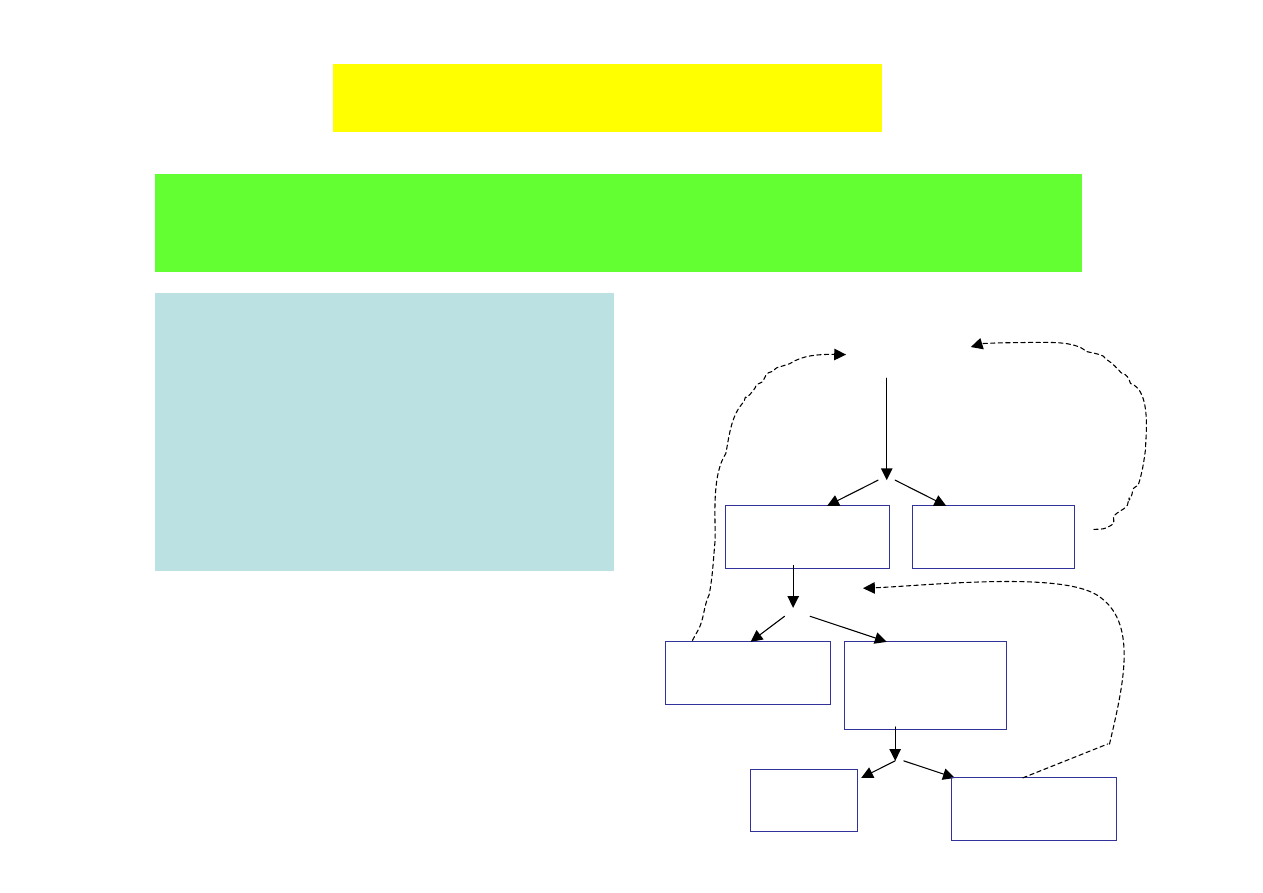
Zagęszczanie roztworów
ekstrakcja c.d.
PROBLEM: niektóre substancje biologiczne ulegają denaturacji w rozpuszczalnikach
organicznych
rozwiązanie: czasem możliwe jest zastosowanie wielofazowych układów wodnych
5. ekstrakcja białek wielofazowymi
układami wodnymi:
układy woda (80-95%) + polimer + sole
w odpowiednim stężeniu
dodatek glikolu polietylenowego do fazy
1 i dodatek dekstranu do fazy 2.
powolna separacja faz (od kilku minut do
2 godzin)
homogenat
+
glikol + sól
równowagowanie
rozdział faz
warstwa górna
H2O +glikol
odsalanie
warstwa dolna
H2O +sól
warstwa górna
H2O +glikol
warstwa dolna
H2O +sól
(produkt)
retentat
(produkt)
permeat
zawierający sól
recykling
oczyszczanie
i recykling

Zagęszczanie roztworów
PERMEACJA
permeacja (przenikanie) substancji przez ciekłe membrany
etapy
1. adsorpcja cząsteczek na zewnętrznej stronie membrany,
2. rozpuszczanie powierzchniowe zaadsorbowanych cząsteczek i ich dyfuzja poprzez
materiał membrany.
3. desorpcja lub odparowanie cząsteczek z drugiej strony membrany do medium
odbierającego (gaz nośny, roztwór pochłaniający, stały sorbent).
ciekła membrana - membrana emulsyjna lub unieruchomiona
mikroporowate membrany stałe nasycone
cieczą spełniającą rolę membrany ciekłej
faza rozproszona w postaci mikroemulsji

Zagęszczanie roztworów
filtracja membranowa
ultrafiltracja (0.001-0.02
µm)
siła napędowa - różnica ciśnień hydrostatycznych po obu stronach membrany
różnice ciśnień 0.2-1 MPa
zależnie od membran - zatrzymywane są składniki o M
cz
od 5000 g/mol (czasem od 10
6
g/mol)
membrany o strukturze
niesymetrycznej
- pochodne celulozy,
- polimery syntetyczne,
- spieki ceramiczne
nominalna zdolność rozdzielcza
masa cząsteczkowa substancji dla której
skuteczność filtracji wynosi 90%
typy aparatów
- nucza filtracyjna
- moduł kapilarny
- moduł spiralny ze zwiniętą
membraną płaską
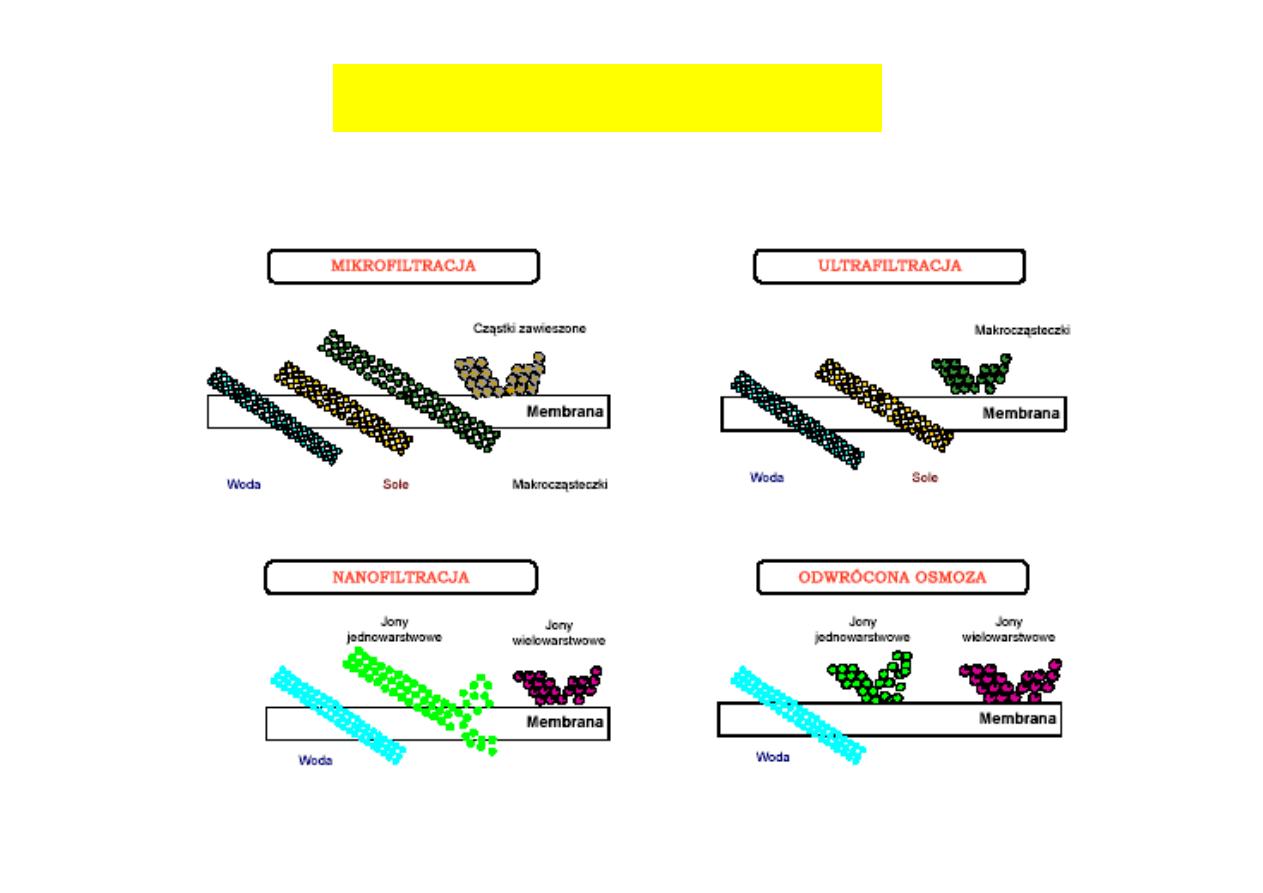
Zagęszczanie roztworów
filtracja membranowa
typy filtracji

Odwrócona osmoza
<0.001
µm
-przez membranę przenika
prawie wyłącznie
rozpuszczalnik.
Stosowana do
- otrzymywania czystej
wody
-zatężania substancji
mikrofiltracja i nanofiltracja
0.02-10
µm
Zagęszczanie roztworów
Wyszukiwarka
Podobne podstrony:
04 Elementy Biotechnologii
Wykład 06 Element Belkowy (Mech)
02 Elementy Biotechnologii
Psychologia osobowości - Pervin - Rozdział 06 - Elementy genetyki zachowania, Elementy genetyki zach
06 elementy teorii wzglŕdnoťci, 6
05 Elementy Biotechnologii
03 Elementy Biotechnologii
06 PLATHELMINTHES, Biotechnologia, I rok, Zoologia D
Wykład 06 Element Prętowy (Mech)
06 Elementary Schools Grade 6 (M Satou)
06 funkcje zmiennej rzeczywistej 3 1 funkcje elementarne
06 Biotechnologia
więcej podobnych podstron