
Rozdział I
ROZWÓJ KOMÓREK ROZRODCZYCH (GAMETOGENEZA)
Początek rozwoju człowieka: zapłodnienie – połączenie plemnika i oocytu → powstanie zygoty
Zmiany zachodzące w komórkach płciowych:
1. redukcja diploidalnej liczby chromosomów (46 → 23):
◦
podziały mejotyczne (dojrzewania)
2. zmiana kształtu komórek płciowych
◦
męskie: duże, okrągłe → utrata cytoplazmy → główka, szyjka, witka
◦
żeńskie: przyrost obj. cytoplazmy → powiększanie się → dojrzały oocyt: 120 мm
Mitoza i komórka nie dzieląca się: chromosomy daleko od siebie. Podczas mejozy: bezpośredni
kontakt.
Mitoza
Przed: Replikacja – chromosomy bardzo długie, rozproszone, niewidoczne pod mikroskopem
1. Profaza: spiralizacja, kondensacja, skrócenie, pogrubienie
◦
chromosom: dwie chromatydy, połączone kinetochorem w centromerze
2. Metafaza: chromosomy można odróżnić (prometafaza)
◦
ułożenie w płaszczyźnie równikowej
◦
połączenie kinetochor → mikrotubule (wrzeciono podziałowe) → centrosom
3. Anafaza: chromatydy do przeciwnych biegunów wrzeciona
4. Telofaza: despiralizacja, wydłużenie, odtworzenie otoczki jądrowej, podział cytoplazmy
Efekt: komórka otrzymuje tyle samo chromosomów co komórka-matka
Mejoza I [oocyty i spermatocyty I-rzędu]
Przed: replikacja (→ podwojona ilość DNA, 46 chromosomów x 2 chromatydy)
Cechy charakterystyczne:
1. synapsis – tworzenie par homologicznych chromosomów (biwalenty); połączenia punkt po
punkcie, brak połączeń w centromerach; chromosomy XY łączą się w części kodującej cechy
somatyczne
2. crossing-over – wymiana odc. chromatyd
rozdzielenie wzdłuż dwuchromatydowych chromosomów → pęknięcia w chromatydach →
wymiana segmentów chromatyd
chiasma - przejściowe miejsca połączenia chromosomów w miejscach, gdzie odbywało się
crossing-over (kształt X)
Dalej jak mitoza: rozdzielanie chromosomów homologicznych, łączenie z włóknami wrzeciona,
wędrówka to przeciwnych biegunów
Efekt: każda komórka potomna ma 23 chromosomy (po 1 z 1 pary) → ilość DNA taka sama jak w
kom. somatycznych
Mejoza II
BRAK SYNTEZY DNA
Efekt: 23 chromatydy w każdej nowej komórce → ilość DNA – 1/2 ilości w normalnej kom.
somatycznej
Cel:
1. zapewnienie zmienności genetycznej przez crossing-over
1

2. haploidalny zestaw chromosomów i 1/2 ilości DNA
Nieprawidłowe podziały mejotyczne
nondisjunction – brak rozdzielenia chromosomów → trisomie, monosomie; może zachodzić podczas
I lub II podziału mejotycznego kom. płciowych
ZMIANY MORFOLOGICZNE PODCZAS DOJRZEWANIA
Oocyty i spermatocyty I rzędu
ścian pęcherzyka żółtkowego [3 tydz.] → pierwotne komórki płciowe (prapłciowe) → WĘDRÓWKA :D
ruchem amebowatym do gonad → docierajom 4/5 tydz.
Owogeneza
kom. prapłciowe XX → oogonia → podziały mitotyczne → skupienia otoczone kom. nabłonkowymi
[ 3 m-c]
1 kom. prapłciowe: wszystkie oogonie z 1 grupy
nabłonek powierzchowny pokrywający jajnik: kom. nabłonkowe (ziarniste)
oogonie
Po urodzeniu:
•
wszystkie oocyty I rzędu w profazie mitozy I,w:
stadium diplotenu – stadium spoczynkowe w okresie profazy: chromatyna – koronkowata
siateczka
•
w takim stadnie do okresu pokwitania – wynik działania OMI ( oocyte maturation inhibitor) z
kom. pęcherzykowych
•
całkowita liczba:
w okresie okołoporodowym: 700 tys. - 2 mln
w okresie pokwitania: 400 tys.
owulowanych w czasie reprodukcyjnym: 500
Stadium diplotenu może być najkorzystniejszym dla zapewnienia ochrony przed wpływami
środowiska. Wydłużenie podziału mejotycznego może zwiększać podatność oocytów na uszkodzenia.
Ale nic nie wiadomo :P.
Dalsze etapy owogenezy:
•
5-15 pęcherzyków pierwotnych dojrzewa w każdym cyklu jajnikowym
•
oocyt I rzędu [diploten] powiększa się → otaczające go kom. nabłonkowe zmieniają się z
2
podziały mitotyczne
oocyty I rzędu → replikacja DNA → profaza mejozy I
[większe]
szybki wzrost, do 5 mca: max. – 7 mln kom.płciowych
→ degeneracja, atrezja licznych owogonii i oocytów I
rzędu
7 m-c: większość ulega zwyrodnieniu;
pozostające przy pow. jajnika - po I podziale mejotycznym,
otoczone kom. nabłonkowymi – pęcherzyki jajnikowe
pierwotne
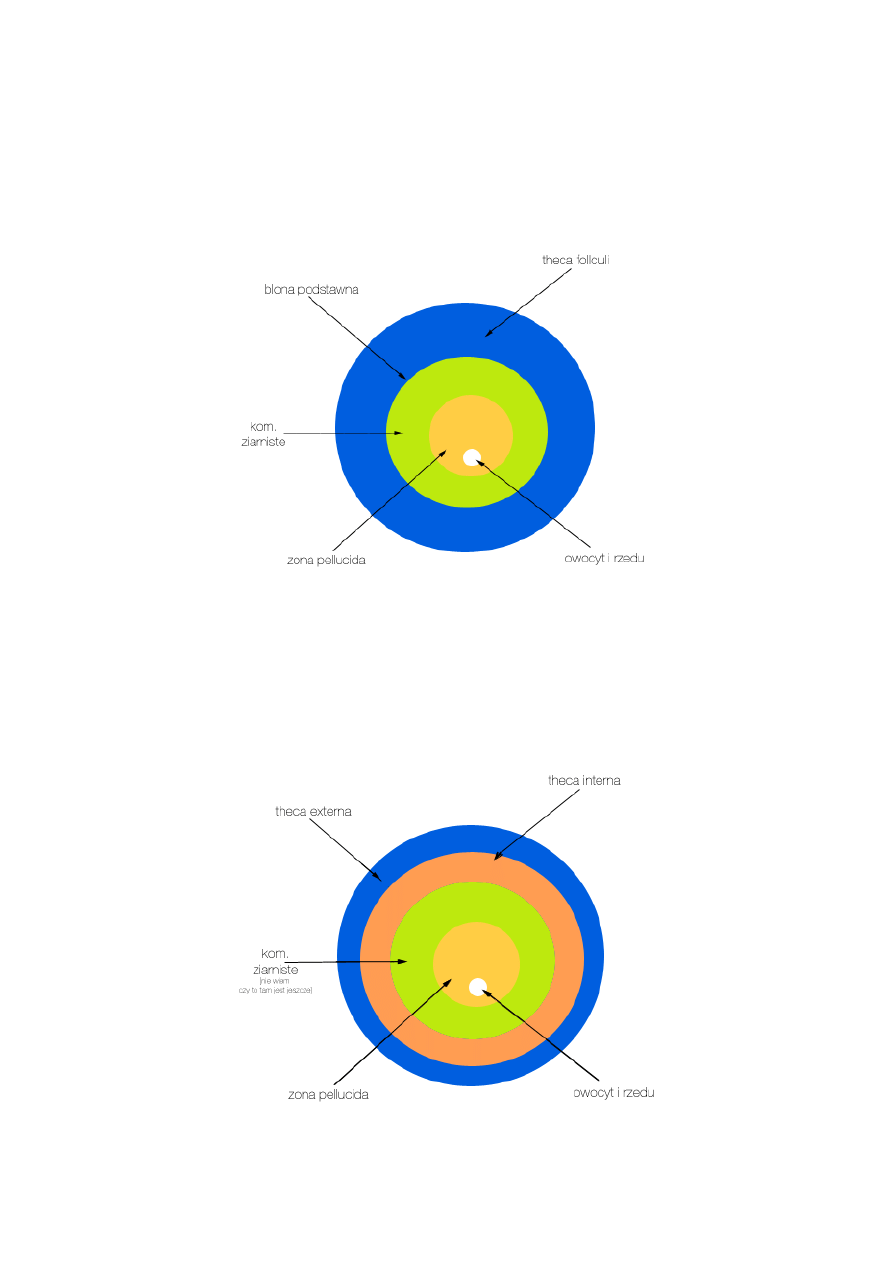
płaskich na sześcienne → rozmnażają się → wytwarzają kilkupokładową warstwę komórek
ziarnistych → powstaje: pęcherzyk jajnikowy wzrastający (folliculus ovarius crescens)
•
układ pęcherzyka wzrastającego (od wewnątrz do zewnątrz)
◦
osłonka przejrzysta (zona pellucida) – glikoproteiny wydzielane przez kom. ziarniste i
oocyt
◦
komórki ziarniste
◦
osłonka pęcherzyka (theca folliculi) – kom. zrębu
•
później:
◦
zróżnicowanie na:
tunica interna – warstwa wydzielnicza
tunica externa – tk. łączna, kom fibroblastopodobne
◦
komórki pęcherzykowe ( co to?) wytwarzają wypustki przechodzące przez osłonkę
przejrzystą i przeplatają się z mikrokosmkami bł. oocytu; znaczenie przy transporcie kom.
pęcherzykowe → oocyt
3

Jeszcze później... (nie cierpię tej książki!):
•
płynne przestrzenie między kom. ziarnistymi → łączę się ze sobą → powstaje: cavum folliculi
[kształt półksiężyca, powiększa się] → PĘCHERZYK JAJNIKOWY WTÓRNY (DOJRZEWAJĄCY)
•
komórki otaczające oocyt niezmienione, tworzą wzgórek jajonośny (cumulus oophorus)
Pęcherzyk jajnikowy dojrzały (Graafa, folliculus ovaricus maturus):
•
średnica: 10 mm
•
otoczony :
◦
warstwą wewnętrzną osłonki pęcherzyka – składa się z kom. wywarzających steroidy,
bogato unaczyniona
◦
warstwą zewnętrzną – zlewa się z tkanką jajnika
Podczas cyklu tylko 1 pęcherzyk uzyskuje pełną dojrzałość. Reszta – atrezja. Po osiągnięciu
dojrzałości: mejoza I. W jej wyniku powstają:
1. oocyt II rzędu – otrzymuje prawie całą cytoplazmę
2. I ciałko kierunkowe – bark cytoplazmy; układa się między osłonką przejrzystą a błoną kom.
oocytu II rzędu (przestrzeń okołożółtkowa)
Zakończenie mejozy I na krótko przed owulacją.
Mejoza II bezpośrednio po mejozie I ( niecałkowite odtworzenie jadra oocytu II rzędu, brak replikacji
DNA). Owulacja i wydalenie – po utworzeniu wrzeciona podziałowego i płytki równikowej. Kończy się
tylko w przypadku zapłodnienia. Inaczej po 24 h degeneruje.
Ciałko kierunkowe I być może się dzieli.
Spermatogeneza
przekształcenie spermatogonii w plemniki
Start: okres pokwitania
Okres okołoporodowy:
sznury płciowe jądra – niedojrzałe kanaliki nasienne kręte
•
w sznurach płciowych można rozpoznać komórki płciowe mężczyzn: duże, słabo zabarwione,
otoczone młodymi komórkami podporowymi (z nabłonka pow. gruczołu)
Krótko przed pokwitaniem:
•
światło w sznurach płciowych → kanaliki nasienne kręte
•
pierwotne kom. płciowe → spermatogonie:
a) typu A – dzielą się mitotyczne, stałe źródło kom. macierzystych;
niektóre opuszczają populację kom. macierzystych i dają początek populacjom
spermatogonii (każda następna bardziej zróżnicowana)
b) typu B – powstają z nich spermatocyty I rzędu; same powstają w wyniku ostatniego
podziału spermatogonii typu A
Spermatocyty I rzędu:
•
po powstaniu; wydłużona profaza (21/22 dni) → szybkie zakończenie mejozy I → powstanie
spermatocytów II rzędu
4

Spermatocyty II rzędu → mitoza II → spermatydy [23 chromosomy; brak cytokinezy w poprzednich
podziałach – komórki połączone mostkami cytoplazmatycznymi; kom. utworzone z jednej
spermatogonii typu A tworzą grupę ]
Spermatogonie i spermatydy podczas rozwoju są pogrążone w zachyłkach komórek podporowych –
w celu podtrzymania , ochrony i odżywiania. Kom. Sertolego uczestniczą również w uwalnianiu
dojrzałych plemników.
Spermiogeneza
zmiany prowadzące do przekształcenia: spermatydy → plemniki (64 dni)
a) utworzenie akrosomu - ponad 1/2 pow. jądra, zawiera enzymy pomocne w czasie
zapłodnienia
b) kondensacja jądra
c) utworzenie szyjki, wstawki, witki
d) utrata cytoplazmy
pełna ruchliwość: najądrze
Nieprawidłowe gamety
•
2,3 oocyty I rzędu w pęcherzyku jajnikowym → bliźnięta
•
rzadko 2,3 jądra w oocycie → obumarcie
•
nieprawidłowe główki, witki plemników
•
zbyt małe, zbyt duże plemniki
•
zlewanie się ze sobą plemników
10% nieprawidłowych plemników bez zmniejszenia płodności; 25% obniżenie zdolności zapłodnienia
Rozdział II
OD OWULACJI DO ROZWOJU
Cykl jajnikowy
•
w okresie pokwitania
•
pod kontrolą podwzgórza (GnRH) → FSH i LH – pobudzają i kontrolują cykliczne zmiany jajnika
Przebieg:
FSH
↓
wzrost od 5 do 15 pęcherzyków pierwotnych
1 osiąga dojrzałość i 1 oocyt zostaje
wydalony na zewnątrz
reszta degeneruje i przekształca się w pęcherzyki
atrezyjne
powstawanie dużej ilości komórek
ziarnistych i osłonki pęcherzyka
↓
wytwarzanie przez nie estrogenów
↓
degeneracja oocytu i otaczających kom.
pęcherzykowych
↓
zastąpienie ich przez tk łączną
↓
5

wejście błony śluzowej macicy w fazę
wzrostu, pobudzanie wydzielania LH
↓
↑LH
↓
owulacja
powstanie pęcherzyka/ciałka atrezyjnego
Owulacja
FSH, LH (kilka dni przed owulacją)
↓
gwałtowne pęknięcie pęcherzyka (15 mm)
↓
ostatnia faza rozwoju pęcherzyka: oocyt I rzędu z diplotenu przechodzi do mejozy I
↓
uwypuklenie pow. jajnika w jednym miejscu
↓
na szczycie uwypuklenia nieunaczyniona plamka → stigma
↓
miejscowe osłabienie i zwyrodnienie
↓
w obrębie stigmy powstaje otwór
↓
wysączenie płynu pęcherzykowego
↓
płyn wypływa, napięcie ściany ↓
↓
oocyt + kom. wzgórka uwalniają się (wypływają z jajnika)
↓
część kom. wzgórka → corona radiata
↓
opuszczenie jajnika
↓
zakończenie mejozy I
↓
oocyt II rzędu rozpoczyna mejozę II
ból środka cyklu – lekki ból odczuwany w czasie owulacja, (uwaga! Zaskoczenie!) ma miejsce w
połowie cyklu
owulacja: ↑ temp.
Corpus luteum
naczynia krwionośne (od naczyń otaczających pęcherzyk)
↓ do
6

komórek ziarnistych w ścianie pękniętego pęcherzyka
[przybierają kształt wielościanów]
↓LH
w kom. ziarnistych pojawia się żółty barwnik
↓↓↓
komórki luteinowe = CIAŁKO ŻÓŁTE
•
synteza
•
uwalnianie
Z estrogenami wywołuje fazę wydzielniczą (progesteronową) – przygotowanie do implantacji.
Transport komórki jajowej
•
zbliżenie strzępek jajowodu do powierzchni jajnika
•
rytmiczne skurcze jajowodu
•
zgarniające ruchy strzępek i rzęsek nabłonka
komórka w jajowodzie
↓
komórki wzgórka tracą kontakt z oocytem
[wyciąganie wypustem cytoplazmatycznych z osłonki przejrzystej]
↓
przesuwanie oocytu ku światłu macicy dzięki rytmicznym skurczom jajowodu
Szybkość przemieszczania
~
stopień stężenie hormonu.
Dotarcie zapłodnionej kom. jajowej do światła macicy: 3-4 dni.
Corpus albicans
brak zapłodnienia: 9 dzień najwyższy stopień rozwoju corpus luteum
później: wyrodnienie kom. luteinowych, zmniejszanie ciałka, przekształcenie w:
corpus albicans – włóknista zbliznowaciała tk → zmniejszenie wydzielania progesteronu →
krwawienie miesięczne
zapłodnienie:
ciałko żółte nie wyrodnieje
↓
ciałko żółte rośnie
↓
CORPUS LUTEUM GRAVIDITATIS
ok. 3 m-ca ciąży – 1/3-1/2 jajnika, wytwarzanie progesteronu do 4 m-ca; później jego funkcję
przejmuje łożysko, a ciałko zanika
Antykoncepcja
Progestageny przyjmowane doustnie między 5 a 25 dniem cyklu hamują owulację. Dodatek
niewielkiej ilości estrogenu również hamuje owulację.
Składnik progestagenowy zapewnia normalnie krwawienie miesięczne (odstawienie po 25 dniach
cyklu).
Hormony jako leki antykoncepcyjne działają na zasadzie sprzężenia zwrotnego. Całkowicie hamują
7
PROGESTERONU
HCG – gonadotropina kosmówkowa

wzrost pęcherzyków.
Zapłodnienie (fertilisatio)
proces łączenia się gamety męskiej i żeńskiej
Miejsce zachodzenia: bańka jajowodu
Żywotność gamet: plemniki – ok 24 h; oocyt II rzędu – 12-24 h
Plemniki uzyskują zdolność zapłodnienia oocytu w wyniku:
•
kapacytacji – zachodzi w drogach rodnych kobiety, polega na usunięciu osłonki
glikoproteinowej i białek płynu nasiennego z błony kom. leżącej nad akrosomem; trwa ok. 7 h
•
reakcja akrosomowa – zachodzi w bezpośrednim sąsiedztwie oocytu, pod wpływem
substancji z corona radiata i kom. jajowej, polega na powstawaniu licznych punktowych
połączeń pomiędzy błoną kom. plemnika i zew. błoną akrosomową; umożliwia przeniknięcie
plemnika przez corona radiata i zona pellucida; substancje biorące udział:
◦
hialuronidaza → corona radiata
◦
enzymy trypsynopodobne → zona pellucida
◦
akrozyna – związana z wew. powierzchnią błony akrosomowej → zona pellucida
Fazy zapłodnienia:
1. Przenikanie plemników przez corona radiata
◦
300 -500 plemników/ 200-300 mln wprowadzonych do dróg rodnych kobiety dociera do
miejsca zapłodnienia
◦
zapłodnienia dokonuje 1 plemnik
◦
pozostałe są pomocne przy przechodzeniu przez corona radiata
◦
corona radiata (pierwsza bariera chroniąca żeńską gametę) rozpuszczana jest przez
enzymy nasienia (hialuronidaza) i enzymy błony śluzowej jajowodu
2. Przenikanie plemników przez zona pellucida
◦
za pomocą enzymów z wewnętrznej błony akrosomowej
◦
plemnik styka się z osłonką → silne związanie → szybkie przeniknięcie
◦
po zetknięciu głowy plemnika z pow. oocytu → uwolnienie enzymów lizosomalnych →
reakcja osłony - zmiana przepuszczalności osłonki ORAZ inaktywacja swoistych
gatunkowo receptorów plemników
◦
tylko 1 plemnik może wniknąć do oocytu, rzadko 2
3. Zlewanie się (fuzja) błony kom. oocytu i plemnika
◦
natychmiast po zetknięciu plemnika z oocytem
◦
fuzja między: błoną oocytu a błoną pokrywającą tylną część główki plemnika
◦
główka i witka – wchodzą do oocytu
◦
błona komórkowa – pozostaje na powierzchni oocytu
◦
reakcje kom. jajowej po wniknięciu plemnika:
1. reakcja korowa i reakcja osłony ← uwolnienie ziarnek korowych oocytu (enzymy
lizosomalne):
◦
błona oocytu: nieprzepuszczalna dla innych plemników
◦
zona pellucida zmienia budowę i skład ← usuwanie receptorów dla plemników
8

2. zakończenie mitozy II
◦
natychmiast po wniknięciu plemnika
◦
powstają: dojrzały/ostateczny oocyt i II ciałko kierunkowe
◦
przedjądrze żeńskie – pęcherzykowate jądro oocytu ostatecznego
3. aktywacja metaboliczna komórki jajowej
◦
czynnik aktywujący prawdopodobnie dostarczany przez plemnik
◦
dotyczy reakcji na poziomie komórkowym i molekularnym, związanych z wczesną
embriogenezą
◦
plemnik przesuwa się w głąb jaja → okolice żeńskiego przedjądrza
◦
tworzy się przedjądrze męskie (jądro plemnika pęcznieje)
◦
przedjądrzy nie da się odróżnić
◦
witka odczepia się i wyrodnieje
◦
przedjądrza wchodzą w ścisły kontakt, tracą otoczkę jądrową
◦
przedjądrza powiększają się i replikują DNA
◦
po syntezie DNA chromosomy wiążą się z wrzecionem podziałowym → podział
mitotyczny
◦
siostrzane chromosomy wędrują do biegunów, na powierzchni pojawia się bruzda
dzieląca cytoplazmę
Skutki zapłodnienia:
•
przywrócenie diploidalnej liczby chromosomów
•
determinacja płci
•
zapoczątkowanie bruzdkowania
Zapłodnienie in vitro
wzrost pęcherzyków pobudzany gonadotropinami
↓
pobranie oocytów z pęcherzyków jajnikowych tuż przed owulacją (za pomocą aspiratora)
[późny okres mitozy I]
↓
umieszczenie oocytu w pożywce hodowlanej + nasienie
↓
obserwacja zapłodnionych jaj do stadium 8 blastomerów
↓
przeniesienie zapłodnionych jaj do macicy
Dzięki in vitro:
•
przezwyciężenie skutków niepłodności (zarośnięcie jajowodu, szkodliwy dla plemników śluz
szyjki macicy, uczulenie na plemniki;))
•
możliwość określenia kariotypu – unikanie wszczepiania zarodków z wadami chromosomów
Zarodek w okresie przedimplantacyjnym jest wysoce odporny na działanie czynników teratogennych
– ryzyko uzyskania potomstwa z wadami rozwojowymi jest bardzo niewielkie.
Niski odsetek powodzeń: 20 %. Aby go zwiększyć do macicy wszczepia się kilka zapłodnionych jaj.
9

Prowadzi to do ciąży bliźniaczych.
Bruzdkowanie (3 dzień)
zygota: stadium 2-óch komórek
↓
seria podziałów; powstają małe komórki – blastomery
↓3-4 podziały
morula [3 dzień po zapłodnieniu, na krótko przed dojściem do macicy; 12-16 komórek]:
•
komórki wewnętrzne – powstaną tkanki zarodka
•
komórki zewnętrzne – tworzą trofoblast (→ łożysko)
Powstawanie blastocysty (1 tydzień)
morula przesuwa się do jamy macicy
↓
przez zona pellucida przenika płyn – gromadzi się pomiędzy leżącymi wewnątrz komórkami
↓
wypełnione płynem przestrzenie zlewają się → jama blastuli (blastocele) – pojedyncza jama
zarodek = BLASTOCYSTA
embrioblast, węzeł zarodkowy – komórki wewnątrz blastocysty, znajdują się na jednym biegunie
trofoblast – komórki zewnętrzne; spłaszczają się, tworzą nabłonkową ścianę blastocysty
↓
zanik zona pellucida
↓
rozpoczęcie implantacji
↓
enzymy proteolityczne wytwarzane przez trofoblast niszczą komórki nabłonkowe błony śluzowej
macicy i wnikają między nie
↓
błona śluzowa wspomaga proteolityczną aktywność blastocysty
↓
implantacja – wynik współdziałania macicy i blastocysty
Nieprawidłowe zygoty
Nieprawidłowe zygoty (3-5 dni po zapłodnieniu):
•
wielojądrowe blastomery
•
różny stopień zwyrodnienia komórek
•
niezdolne do implantacji
•
od pacjentek z normalną płodnością
Dokładna liczba nieprawidłowych zygot nie jest znana – zarodki giną w okresie ciąży (2-3 tyg. po
zapłodnieniu). 50% wszystkich ciąż kończy się spontanicznym poronieniem, ich 1/2 spowodowana
wadami chromosomowymi – sposób odsiewu uszkodzonych zarodków, zmniejszenie występowania
wad wrodzonych.
Macica w czasie implantacji
Warstwy ściany macicy:
1. błona śluzowa (endometrium) – wyścieła jamę macicy
10

2. błona mięśniowa (myometrium) – gruba warstwa kom. mięśniowych gładkich
3. błona surowicza (perimetrium) – pokrywa macicę od zewnątrz
Od pokwitania do menopauzy występują cykliczne zmiany błony śluzowej macicy (cykl miesiączkowy
ok. 28 dni) kontrolowane przez hormony jajnika.
Fazy cyklu miesiączkowego – brak zapłodnienia:
1. faza folikularna (wzrostu) – po zakończeniu fazy złuszczania, pod wpływem hormonów
estrogennych, równolegle do wzrostu pęcherzyków jajnikowych
2. faza wydzielnicza (progesteronowa) – 2-3 dni po owulacji w odpowiedzi na progesteron z
ciałka żółtego
3. faza złuszczania (miesiączkowa) – żyłki i sinusoidy wypełniają się krwinkami → przechodzą do
otaczających tkanek, z powierzchownych tętnic wydobywa się krew i następuje odrywanie
fragmentów błony śluzowej oraz gruczołów → złuszcza się warstwa zbita i warstwa gąbczasta
endometrium (3-4 dni), pozostaje jedynie warstwa podstawna
Zamiany endometrium w przypadku zapłodnienia:
Podczas implantacji – faza wydzielnicza:
•
gruczoły maciczne i tętnice ulegają spiralizacji
•
błona ulega rozpulchnieniu → posiada 3 warstwy (od najbardziej powierzchownej):
1. warstwa zbita
2. warstwa gąbczasta
3. błona podstawna – zawiera własne naczynia: tętnice podstawne (proste), ma charakter
warstwy regeneracyjnej – odtwarza gruczoły i tętnice
Blastocysta wszczepia się do błony śluzowe w obrębie tylnej lub przedniej ściany trzonu macicy
(między ujściami gruczołów).
Rozdział III
DWUBLASZKOWA TARCZA ZARODKOWA (drugi tydzień rozwoju)
8 dzień rozwoju
•
blastocysta częściowo zagłębiona w endometrium
•
trofoblast podzielony na:
1. cytotrofoblast – warstwa wewnętrzna, komórki jednojądrowe; występują figury
mitotyczne
2. syncytiotrofoblast – warstwa zewnętrzna, wielojądrowa, pozbawiona wyraźnych granic
międzykomórkowych; brak figur mitotycznych
Namnażanie komórek w obrębie cytotorofoblastu → migracja do syncytiotrofoblastu →
fuzja
•
embrioblast podzielony na:
1. hipoblast – małe, sześcienne komórki; sąsiadują z jamą blastocysty
2. epiblast – wysokie, walcowate komórki; sąsiadują z jamą owodni
•
w obrębie epiblastu pojawia się mała jamka → powiększa się → staje się jamą owodniową
11
dwublaszkowa tarcza
zarodkowa
(obie warstwy w kształcie
płaskiego krążka)

(cavum amnioticum)
amnioblasty – komórki epiblastu przylegające do cytotrofoblastu, wyścielają jamę
owodniową
•
błona śluzowa macicy w okolicy miejsca implantacji: obrzęknięta, silnie unaczyniona
•
gruczoły maciczne: powiększone, skręcone, wydzielają dużo glikogenu i śluzu
9 dzień rozwoju (stadium lakunowe)
•
blastocysta wnika głębiej w błonę śluzową macicy
•
ubytek powstały w nabłonku powierzchniowym zasklepiony przez skrzep
•
znaczny rozwój trofoblastu:
na biegunie zarodkowym syncytium pojawiają się wakuole → łączą się ze sobą → tworzą
lakuny
•
na biegunie przeciwzarodkowym:
a) spłaszczone kom. wywodzące się z hipoblastu tworzą cienką błonę (błona
zewnątrzzarodkowej jamy ciała, Heusera), która wyściela wewnętrzną powierzchnię
cytotrofoblastu;
b) błona zewnątrzzarodkowej jamy ciała + hipoblast → wyścielają zewnątrzzarodkową jamę
ciała/pęcherzyk żółtkowy pierwotny (exocoeloma, saccus vitellinus primus )
11-12 dzień rozwoju
•
blastocysta całkowicie zagłębiona w endometrium
•
nabłonek powierzchowny prawie zupełnie pokrywa ubytek powstały w czasie implantacji
•
blastocysta tworzy niewielkie uwypuklenie zwrócone do światła macicy
•
w syncytium trofoblastu: lakuny – szczególnie widoczne na biegunie zarodkowym
•
biegun przeciwzarodkowy: komórki cytotrofoblastu
•
niszczenie śródbłonka naczyń włosowatych matki (naczynia zatokowe, sinusoidy) przez
wrastający w endometrium syncytiotrofoblast
•
lakuny + sinusoidy → wpływanie krwi matki do lakun → ustanowienie krążenia maciczno-
łożyskowego
•
tworzenie mezodermy pozazarodkowej – delikatna, luźna tk łączna, pomiędzy wewnętrzną
powierzchnią cytotrofoblastu i zewnętrzną powierzchnią zewnątrzzarodkowej jamy ciała;
wywodzi się z pęcherzyka żółtkowego; ostatecznie: wypełnia przestrzeń między trofoblastem
od zewnątrz i owodnią oraz ścianą zewnątrzzarodkowej jamy ciała od wewnątrz
•
pozazarodkowa jama ciała (jama kosmówkowa) – duże rozstępy w mezodermie
pozazarodkowej; jama ta otacza pierwotny pęcherzyk żółtkowy i jamę owodniową poza
miejscem połączenia tarczy zarodkowej z trofoblastem (za pomocą szypuły łączącej)
•
dwublaszkowa tarcza zarodkowa rośnie wolniej niż trofoblast – pozostaje bardzo niewielka
pozazarodkowa mezoderma ścienna – wyściela cytotrofoblast i owodnię
pozazarodkowa mezodermie trzewna – pokrywa pęcherzyk żółtkowy
reakcja doczesnowa – zespół zmian zachodzących w macicy:
•
kom. przybierają kształt wielokątny
•
kom. wypełniają się: glikogenem i lipidami
•
gromadzenie się płynu w przestrzeniach międzykomórkowych
•
spulchnienie zrębu błony śluzowej
12

początkowo ogranicza się do miejsca implantacji, później rozprzestrzenia się na całą błonę śluzową
macicy
13 dzień rozwoju
•
zagojenie błony śluzowej w obrębie ubytku
•
w miejscu implantacji może nastąpić krwawienie – zwiększony dopływ krwi do lakun – ok. 28
dzień cyklu, można pomylić z krwawieniem miesięcznym (błędne określenie daty
spodziewanego porodu!)
•
pojawienie się pierwszych kosmków w trofoblaście
kom. cytotrofoblastu mnożą się i wnikają do syncytiotrofoblastu → kolumny komórek
otoczone syncytium → KOSMKI PIERWOTNE
•
utworzenie wtórnego/ostatecznego pęcherzyka żółtkowego (saccus vitellinus definitus) –
komórki powstałe z hipoblastu wędrują po wew. powierzchni błony zewnątrzzarodkowej jamy
ciała, a następnie się rozmnażają tworząc nową jamę
•
pęcherzyk żółtkowy wtórny – znacznie mniejszy od zewnątrzzarodkowej jamy ciała/
pęcherzyka żółtkowego pierwotnego
•
torbiele zewnątrzzarodkowej jamy ciała – powstają w wyniku odsznurowania (!?) dużych
fragmentów pozazarodkowej jamy ciała; często spotykane w jamie kosmówkowej
•
tworzy się jama kosmówkowa (cavum chorionicum) – znacznie powiększona pozazarodkowa
jama ciała
•
blaszka kosmówki – mezoderma zewnątrzzarodkowa pokrywająca wew. powierzchnię
cytotrofoblastu
•
szypuła łącząca (szypuła brzuszna, caulis connectionis) – miejsce przejścia jamy
kosmówkowej w mezodermę pozazarodkową
•
w trakcie rozwoju szypuła łącząca przekształca się w sznur pępowinowy (pępowina, funiculus
umbilicalis)
Do końca drugiego tygodnia tarcza zarodkowa składa się z dwóch przylegających do siebie krążków:
1. epiblast – tworzy dno jamy owodniowej
2. hipoblast – tworzy sklepienie ostateczne pęcherzyka żółtkowego; w części głowowej –
niewielkie zgrubienie: płytka przedstrunowa (lamina prochordalis) – miejsce występowania
walcowatych komórek ściśle przylegających do epiblastu
Nieprawidłowe miejsca implantacji
Normalne miejsce implantacji: tylna/przednia ściana trzonu macicy
Inne:
1. w pobliżu ujścia wewnętrznego cieśni macicy → łożysko ponad cieśnią (łożysko przodujące,
placenta previa) → obfite krwawienie w II połowie ciąży i podczas porodu
2. ciąże pozamaciczne (graviditas extrauterina s. ectopica) – zazwyczaj: obumarcie zarodka, silny
krwotok u matki w 2 m-cu ciąży
◦
jama brzuszna (! najczęściej zagłębienie odbytniczo-maciczne = kieszonka Douglasa, in.
otrzewna, sieć)
◦
jajnik (garviditas primaria ovarica)
◦
jajowód (graviditas tubaris) – pęka ok. 2 m-ca ciąży → ciężki krwotok wewnętrzny
Nieprawidłowe blastocysty
•
nieprawidłowości w blastocystach: samo syncytium, hipoplazja trofoblastu, brak
13

embrioblastu, niewłaściwe położenie tarczy zarodkowej
•
nie wywołują objawów ciąży – trofoblast zbyt słabo rozwinięty by wytworzyć hormony
utrzymujące ciałko żółte → zarodki poronione w czasie następnego cyklu miesiączkowego
•
badania Hertiga ( na płodnych kobietach, optymalne warunki zajścia w ciążę) :
◦
15% oocytów nie ulega zapłodnieniu mimo kontaktów z plemnikami
◦
10-15% zygot rozpoczyna bruzdkowanie, ale nie jest zdolne do implantacji
◦
spośród 70-75% zarodków, które dokonały implantacji, do drugiego tygodnia ciąży dożyje
58% zarodków (w tym 16% nieprawidłowych)
◦
summa summarum :D : do dnia w którym powinna wystąpić miesiączka przeżyje tylko
42% jaj będących uprzednio w kontakcie z plemnikami (część ulegnie poronieniu później,
a część będzie miała wady)
Rozdział IV
TRÓJBLASZKOWA TARCZA ZARODKOWA (trzeci tydzień rozwoju)
Gastrulacja: tworzenie mezodermy i endodermy zarodkowej
Gastrulacja – proces prowadzący do utworzenia w zarodku trzech listków zarodkowych.
Przebieg:
utworzenie smugi pierwotnej (linea primitiva) na pow. epiblastu
•
wyraźnie widoczna u 15-16-dniowego zarodka: wąska rynienka z lekko uwypuklonym
obwałowaniem
•
w dogłowowym końcu smugi (węzeł pierwotny, nodus primitivus) znajduje się zgrubienie
otaczające mały dołek pierwotny (fovea primitiva) a w nim: komórki butelkowatego kształtu,
pomiędzy epiblastem i hipoblastem rozwija się nowa warstwa komórek
↓
komórki epiblastu wędrują w kierunku smugi pierwotnej → utworzenie mezodermy i endodermy
wewnątrzzarodkowej
↓
po dotarciu mają kształt (no jaki, jaki mają kształt? proszęęproszęęę powiedzzz !)
BUTELKOWATY
↓
odłączają się od epiblastu
↓
wnikają pod epiblast – wklęśnięcie (inwaginacja)
↓
I część kom. :
zajmuje miejsce hipoblastu
↓
tworzą endodermę zarodkową
II część kom.:
układa się pomiędzy
epiblastem a nowo powstałą
endodermą
↓
tworzą mezodermę
III część kom.:
pozostaje w epiblaście
↓
tworzy ektodermę
EPIBLAST W CZASIE GASTRULACJI JEST ŹRÓDŁEM WSZYSTYCH TRZECH LISTKÓW ZARODKOWYCH
W miarę wywędrowywania coraz większej liczby komórek do przestrzeni między epiblastem, a
hipoblastem, komórki te zaczynają przesuwać się na boki i w kierunku dogłowowym. Przechodzą
poza granice tarczy i stykają się z mezodermą pozazarodkowa (pokrywa pęcherzyk żółtkowy,
14

owodnię). Omijają płytkę przedstrunową, stykając się poza jej obrębem – tworzą tam pole (płytkę)
sercotwórcze.
Powstawanie struny grzbietowej
komórki wchodzące do dołka pierwotnego przesuwają się w linii prostej w kierunku dogłowowym aż
do płytki przedstrunowej
↓
tworzą cewkowaty wyrostek struny grzbietowej (wyrostek głowowy); kanał w jego środku –
przedłużenie dołka pierwotnego
↓
17 dzień: warstwa mezodermy i wyrostek struny grzbietowej całkowicie oddziela endodermę od
ektodermy (! wyjątek: płytka przedstrunowa i błona stekowa → ekto- i endoderma ściśle przylegają
do siebie)
↓
18 dzień: dno struny zlewa się z leżącą pod nim endodermą
↓
obie warstwy wyrostka rozpadają się
↓
światło wyrostka struny grzbietowej całkowicie zanika (pozostałość: płytka wklinowująca się w listek
endodermalny)
↓
dalszy rozwój: kom. struny rozmnażają się
↓
powstaje ostateczna struna grzbietowa (lita struktura)
↓
odłącza się od endodermy (ponownie staje się ciągłą warstwą → sklepienie pęcherzyka żółtkowego)
Struna grzbietowa (notochorda) – pośrodkowa oś, wokół której powstanie szkielet osiowy, rozciąga
się od błony gębowo-gardłowej do węzła pierwotnego
kanał nerwowo-jelitowy (canalis neurentericus) – przez pewien czas łączy pęcherzyk żółtkowy i jamę
owodniową
uchyłek omoczniowo-jelitowy, omocznia (allantois) – pojawia się ok. 16 dnia rozwoju, jednocześnie z
błoną stekową; znajduje się w tylnej ścianę pęcherzyka żółtkowego, wnika do szypuły łączącej; u
człowieka jest narządem szczątkowym
Rozwój tarczy zarodkowej
początkowo: płaska i okrągła
↓
przybiera kształt wydłużony z szerokim końcem głowowym i wąskim ogonowym
↓
powiększanie tarczy zarodkowej: głównie w okolicy głowowej – powodowane migracją komórek z
okolicy smugi pierwotnej
↓
wklęśnięcie (invaginatio) i migracja pow. komórek w obrębie smugi pierwotnej i ich wędrówka trwa
15

do końca 4 tygodnia rozwoju
↓
później: zmiany regresyjne smugi, gwałtowne zmniejszenie i zniknięcie
[pozostałości mogą powodować guzy w okolicy krzyżowo-ogonowej,
tk z 3 listków zarodkowych]
Ważne: koniec doogonowy tarczy zarodkowej aż do 4 tygodnia stale dostarcza nowe komórki.
Różnicowanie listków zarodkowych:
•
w części głowowej: połowa 3 tyg.
•
w części ogonowej: koniec 4 tyg.
3 tydzień rozwoju: powstawanie somitów z mezodermy i OUN z ektodermy
Dalszy rozwój trofoblastu
13 dzień: wytworzenie kosmków pierwotnych; później do rdzenia kosmków wnikają kom.
mezodermalne i rosną w kierunku doczesnej → kosmki drugorzędowe
koniec 3 tygodnia:
z kom. mezodermalnych rdzenia kosmka powstają komórki układu krwiotwórczego i małe naczynia
krwionośne (ukł. naczyń włosowatych kosmka) → kosmek trzeciorzędowy (ostateczny kosmek
łożyskowy)
↓
Naczynia włosowate kosmków łączą się z naczyniami włosowatymi mezodermy blaszki kosmówki i
szypuły łączącej
↓
naczynia mezodermy blaszki kosmówki i szypuły łączącej nawiązują kontakt z wewnątrzzarodkowym
układem krwionośnym → połączenie łożyska z zarodkiem
w 4 tygodniu:
•
układ kosmków gotowy do zaopatrywania zarodka w substancje odżywcze i krew
•
serce zarodka podejmuje pracę
•
powiększenie jamy kosmówkowej
•
komórki cytotrofoblastu kosmków wnikają w leżące nad nimi syncytium i dochodzą do
endometrium → łączą się z podobnymi pasmami cytotrofoblastu z sąsiednich kosmków i
wytwarzają zewnętrzną pokrywę cytotrofoblastyczną → pokrywa otacza cały trofoblast,
mocno zakotwicza kosmówkę w endometrium
kosmki palowe (czepne) – biegną od blaszki kosmówki do doczesnej podstawnej
kosmki wolne (końcowe) – od bocznych powierzchni kosmków palowych
5 tydzień: zarodek łączy się z trofoblastem tylko za pomocą szypuły łączącej (→ sznur pępowinowy)
Rozdział V
OKRES ZARODKOWY (3-5 tydzień rozwoju; ok. 2 m-ca – widać główne cechy zew. ciała)
Tkanki i narządy pochodzące z ektodermalnego listka zarodkowego
16

3 tydzień:
•
początek: ektodermalny listek zarodkowy ma kształt płaskiej tarczy
•
okolica głowowa szersza od ogonowej
•
indukcyjny wpływ struny grzbietowej: ektoderma pod nią grubieje → tworzy płytkę nerwową
(lamina neuralis)
neuroektoderema – komórki płytki nerwowej
•
indukcja płytki – początkowy proces neurulacji
•
wydłużona, o kształcie podeszwy płytka powiększa się w kierunku smugi pierwotnej
•
koniec 3 tygodnia: boczne brzegi płytki nerwowej unoszą się ku górze tworząc fałdy
nerwowe (plicae neurales), a obniżona okolice środkowa rynienkę nerwową (sulcus neuralis)
•
fałdy zbliżają się do siebie i łączą w linii pośrodkowej (połączenie: od 4 somitu [okolica szyi] w
kierunku doogonowym) → powstaje cewa nerwowa (tubus neuralis)
•
cewa nerwowa pozostaje przez jakiś czas otwarta na końcu dogłowowym i doogonowym,
łącząc się z jamą owodniową otworami cewy nerwowej – przednim i tylnym (neuroporus –
rostralis/caudalis)
•
zamknięcie otworów: przedni – 25 dzień (stadium 18-20 somitów), tylny – 27 dzień (stadium
25 somitów) → zakończenie neurlulacji
Po zakończeniu neurulacji OUN ma postać cewy:
◦
zamkniętej
◦
wąska część doogonowa → rdzeń kręgowy
◦
szeroka część dogłowowa z pęcherzykami mózgowia
Kolejne etapy rozwoju OUN:
•
wznoszenie i zlewanie fałdów nerwowych: komórki położone przy bocznych brzegach
(komórki neuroektoderemalne) oddzielają się od fałdów → wytworzenie grzebienia
nerwowego (crista neuralis)
•
komórki neuroektoderemalne (które nie wytworzyły grzebienia, chyba) przekształcają się w
komórki nabłonkowe lub mezenchymatyczne opuszczając neuroektoderemę i
przemieszczając się do leżącej pod nią mezodermy
mezoderma – komórki powstałe z epiblastu i tkanka pozazarodkowa
mezenchyma – luźno zorganizowana tk łączna zarodkowa, niezależnie od pochodzenia
•
komórki grzebienia nerwowego wytwarzają:
◦
zwoje kręgowe (czuciowe)
◦
zwoje autonomiczne
◦
niektóre elementy zwojów nerwów czaszkowych V, VII, IX, X
◦
lemmocyty (kom. Schwanna)
◦
oponę miękką
◦
pajęczynówkę
◦
melanocyty
◦
rdzeń nadnercza
◦
kości i tk łączną struktur twarzoczaszki
◦
komórki grzebieni pnia tętniczego i stożka tętniczego w sercu
17

•
podczas zamykania się cewy nerwowej w okolicy dogłowowej pojawiają się następujące
zgrubienia ektodermy:
1. płytka uszna (placoda otica) → wpuklenie się → utworzenie pęcherzyka usznego
(vesicula otica) → EWOLUCJA w narząd przedsionkowo-ślimakowy
↓
2. płytka oczna (placoda optica)
komórki ektodermy stykające się z pęcherzykiem ocznym zaczynają się wydłużać i
tworzą płytkę soczewki (placoda lentis) → pęcherzyk soczewki (vesicula lentis) →
wytworzenie soczewki w 5 tygodniu
Tkanki i narządy pochodzące z ektodermy:
•
z ektodermalnego lista zarodkowego powstają narządy i struktury służące do utrzymywania
kontaktów ze światem zewnętrznym:
◦
Obwodowy UN
◦
Ośrodkowy UN
◦
nabłonki zmysłowe: ucha, nosa, oka
◦
naskórek (+ włosy i paznokcie)
•
inne:
◦
gruczoły potowe i łojowe
◦
przysadka
◦
szkliwo
Tkanki i narządy pochodzące z mezodermalnego listka zarodkowego
•
komórki mezodermalnego listka zarodkowego tworzą cienką warstwę luźno ułożonej tkanki
po obu stronach linii pośrodkowej ciała
•
komórki umiejscowione w pobliżu tej linii intensywnie rozmnażają się i tworzą zgrubiałą
płytkę: mezodermę przyosiową (mesoderma paraxiale)
•
z boku: mezoderma boczna pozostaje w postaci cienkiej płytki
•
pomiędzy komórkami mezodermy bocznej pojawiają się szczeliny → zlewają się →
mezoderma boczna rozdziela się na 2 warstwy:
a) mezodermę ścienną (mesoderma somaticum s. parietale) - łączy się z mezodermą
pokrywającą owodnię
b) mezodermę trzewną (mesoderma splanchnicum s. viscerale) – pokrywa pęcherzyk
żółtkowy
↓wspólnie wyścielają nowo powstałą przestrzeń
18
placoda otica
vesicula otica
narząd
przedsionkowo-ślimakowy

JAMĘ CIAŁA WEWNĄTRZZARODKOWĄ (coeloma intraembryonicum)
•
łączy się po obu stronach zarodka z jamą ciała pozazarodkową
•
mezoderma pośrodkowa (mesoderma intermedium) – tk łącząca mezodermę przyosiową i
boczną
•
początek 3 tygodnia: mezoderma przyosiowa organizuje się w segmenty (somitomery) –
-pierwsze w okolicy głowowej zarodka, później w kierunku doogonowym
-somitomer złożony jest ze spiralnie ułożonych warstw kom. mezodermalnych
-w okolicy głowowej somitomery powstają w powiązaniu z neuromerami, są źródłem
większości mezenchymy w obrębie głowy
-w kierunku doogonowym (od okolicy potylicznej) somitomery przechodzą w somity
•
pierwsza para somitów: okolica szyjna zarodka, ok. 20 dnia rozwoju
•
później: po 3 somity dziennie w kierunku doogonowym, do końca 5 tygodnia (42-44 pary)
•
ostateczne pary somitów:
‒ 4 potyliczne
‒ 8 szyjnych
‒ 12 piersiowych
‒ 5 lędźwiowych
‒ 8-10 ogonowych
•
w tym okresie wiek zarodka określa się liczbą somitów
Różnicowanie somitu
•
4 tydzień: komórki brzusznej i przyśrodkowej ściany somitu przestają ściśle do siebie
przylegać, stają się wielokształtne i układają się w wokół struny grzbietowej → tworzą
sklerotom – stanowi luźne utkanie (mezenchyma)
→ [przyszłość: otoczenie rdzenia kręgowego i struny grzbietowej
→ uformowanie kręgosłupa]
•
z grzbietowej ściany somitu (dermomiotom) powstaje nowa warstwa komórek: zawiera jasne
jądra z silnie barwiącymi się jąderkami → komórki te stanowią miotom – wytworzy
umięśnienie swojego segmentu
•
komórki dermomiotomu po wytworzeniu miotomu tracą cechy kom. nabłonkowych,
rozprzestrzeniają się pod leżąca ponad nimi ektodermą wytwarzając:
◦
skórę właściwą
◦
tkankę podskórną
→ z każdego somitu powstaje sklerotom (chrząstka i kość), miotom (mięśnie) i dermatom
(skóra)
KAZDY MIOTOM I DERMATOM MA WŁASNY NERW SEGMENTOWY
Mezoderma pośrodkowa
•
różnicuje się całkowicie odmiennie od somitów
•
w regionie szyi i górnym odc. piersiowym → powstają z niej: ułożone w segmenty skupienia
komórek (przyszłe nefrotomy)
•
doogonowo: tworzy tkankę niesegmentowaną – pasmo nerkotwórcze → rozwijają się
elementy wydzielnicze układu moczowego
Mezoderma ścienna i mezoderma trzewna
•
wyściela jamę ciała wewnątrzzarodkową
•
ściana z ektodermą →wytworzą boczną i brzuszną ścianę tułowia
•
trzewna z endodermą wewnątrzzarodkową → ściana przewodu pokarmowego
19
→ 1 para potylicznych, 5-7 par ogonowych ZANIKA
Pozostałe wytwarzają szkielet osiowy.

•
komórki zwrócone do powierzchni jamy ciała → cienka błona surowicza wyścielająca jamę
otrzewnej, opłucnej, osierdzia
Krew i naczynia krwionośne
•
3 tydzień: komórki mezodermy ściennej pokrywające ścianę pęcherzyka żółtkowego różnicują
się w komórki krwiotwórcze i komórki naczyń krwionośnych
•
komórki naczyń krwionośnych (angioblasty) tworzą skupienia i pasma (wsypy
naczyniotwórcze) → łączenie się szczelin międzykomórkowych → kanalizacja
•
z komórek w środkowej części → pierwotne komórki krwiotwórcze
•
komórki obwodowe → spłaszczenie → komórki śródbłonka na obwodzie wysp
krwiotwórczych
•
pączkowanie komórek śródbłonka → wyspy krwiotwórcze zbliżają się do siebie → zlewają się
→ wytwarzają małe naczynia krwionośne
•
w szypule łączącej rozwijają się komórki krwiotwórcze i naczynia włosowate
•
pączkowanie → naczynia włosowate rozrastają się
•
pozazarodkowe naczynia krwionośne zlewają się z naczyniami wewnątrz zarodka →
połączenie zarodek-łożysko
•
naczynia wewnątrz zarodkowe i serce powstają tak samo jak naczynia pozazarodkowe
Tkanki i narządy pochodzące z mezodermy:
a) tk podporowe: tk łączna, chrząstka, kość
b) mięśnie gładkie i poprzecznie prążkowane
c) komórki krwi i limfy
d) ściana serca, naczyń krwionośny i limfatycznych
e) nerki i gonady (+ ich przewody)
f) kora nadnercza
g) śledziona
Tkanki i narządy powstające z endodermalnego listka zarodkowego
•
główna struktura powstające z endodermalnego listka zarodkowego: przewód pokarmowy
•
powstawanie fałdów zarodka w kierunkach:
◦
głowowo-ogonowym – szybkie wydłużanie się OUN
◦
bocznym – zależy od pojawienia się gwałtownie rosnących somitów
•
powstawanie jelita (kształt cewy) – bierny proces polegający na włączeniu części wysłanego
endodermą pęcherzyka żółtkowego w obręb jamy ciała
•
dodatkowy efekt powstawania fałdów: zwężenie połączenia pomiędzy zarodkiem i
pęcherzykiem żółtkowym (odsznurowanie) i powstanie wąskiego, długiego przewodu
żółtkowego (ductus vitellinus)
•
początkowo: endodermalny listek zarodkowy – płaski krążek, stanowiący sklepienie
pęcherzyka żółtkowego i ektodermy
•
formowanie się i wzrost pęcherzyków mózgowia → uwypuklenie tarczy zarodkowej do jamy
owodniowej i wytworzenie fałdów w kierunku głowowo-ogonowym
•
najintensywniejsze wytwarzanie fałdów: okolice głowy i ogona → powstanie fałdu
głowowego i ogonowego
•
rezultat wytwarzania fałdów: coraz większa część wysłanej endodermą jamy pęcherzyka
żółtkowego włączana jest w obręb ciała zarodka
20

•
odcinki endodermy wytwarzają:
◦
jelito przednie (proenteron) – przednia część zarodka; przejściowo zamknięte w końcu
dogłowowym błoną gębowo-gardłową, ustno-gardłową (membrana somatopharyngealis)
[wcześniej: płytką przedstrunową] → koniec 3 tygodnia: przerwanie błony → utworzenie
połączenia pomiędzy jelitem pierwotnym a jamą owodniową
◦
jelito środkowe (mesenteron) – pomiędzy jelitem przednim a tylnym; łączy się przez
pewien okres z pęcherzykiem żółtkowym za pośrednictwem przewodu pępkowo-
jelitowego, żółtkowego (ductus omphalomesentericus, vitellinus; w miarę rozwoju
zarodka zwęża się i wydłuża)
◦
jelito tylne (metenteron) – tylna część zarodka; przejściowo zamknięte błoną stekową
(membrana cloacalis)
•
szybkie powiększanie się somitów → płaska tarcza zarodkowa wytwarza boczne fałdy ciała →
zarodek zaokrągla się; jednocześnie: formowanie przedniej ściany tułowia (! wyjątek – mała
część w okolicy brzusznej, miejsce występowania szypuły pęcherzyka żółtkowego)
•
podczas formowania proenteron, mesenteron i metenteron (wynik utworzenia fałdów:
głowowego i ogonowego) mesenteron pozostaje połączone z pęcherzykiem żółtkowym;
później: wytworzenie fałdów bocznych → „odsznurowanie” (zwężenie, wydłużenie)
połączenia → powstaje przewód żółtkowy → później przewód zarasta → brak połączenia
między mesenteron a zewnątrzzarodkową jamą ciała, wysłaną pierwotną endodermą →
mesenteron leży swobodnie w jamie brzusznej
•
inny skutek fałdowania: częściowe włączenie omoczni w obręb zarodka i jej przekształcenie w
stek (cloaca); dystalana część omoczni pozostaje w szypule łączącej; 5 tydzień: szypuła
pęcherzyka żółtkowego a szypuła łącząca zlewają się → tworzą sznur pępowinowy
•
pęcherzyk żółtkowy u człowieka: narząd szczątkowy; odgrywa rolę w odżywianiu zarodka we
wczesnych etapach rozwoju; 2 m-c – w jamie owodniowej
Tkanki i narządy pochodzące z endodermy:
Początkowo:
a) wyściółka jelita pierwotnego
b) wewnątrzzarodkowa część omoczni
c) wewnątrzzarodkowa część przewodu żółtkowego
Później:
a) nabłonek wyściełający drogi oddechowe
b) miąższ tarczycy, gruczołów przytarczycznych, wątroby, trzustki
c) część zrębu migdałków i grasicy
d) nabłonek wyściełający pęcherz moczowy i cewkę moczową
e) nabłonek wyściełający jamę bębenkową i trąbkę słuchową
Zewnętrzny wygląd zarodka w drugim miesiącu rozwoju
•
koniec 4 tygodnia (28 somitów), główne cechy: somity, łuki gardłowe
wskaźnik wieku zarodka: długość ciemieniowo-siedzeniowa w mm, mierzona od szczytu
głowy (vertex) do punktu środkowego między wierzchołkami pośladków
•
w 2 m-cu: wygląd zewnętrzny zarodka bardzo się zmienia:
◦
znaczne powiększenie wymiarów głowy
◦
uformowanie się:
- kończyn
- twarzy
- uszu
21

- nosa
- oczu
•
początek 5 tygodnia: kończyny górne i dolne – płetwopodobne pączki
◦
zawiązki kończyn górnych: grzbietowo od wyniosłości serca, poziom C4-Th1 →
unerwienie ze splotu ramiennego
◦
zawiązki kończyn dolnych: nieco później, za przyczepem szypuły łączącej, w kierunku
doogonowym, poziom somitów lędźwiowych i górnych krzyżowych
•
dalszy rozwój: końcowe odcinki pączków spłaszczają się id oddzielają pierścieniowym
przewężeniem od bliższego bardziej walcowatego segmentu, następnie w dalszej części
pączków pojawiają się 4 promieniście ułożone bruzdy, rozdzielające pączek na 5 części →
wyodrębnienie się palców
•
ww. bruzdy – promienie, najpierw na dłoniach, później na stopie
•
formowanie palców: pojawia się drugie przewężenie, rozdzielające bliższe części pączków na
2 segmenty (3 odc. charakterystyczne dla dorosłego osobnika)
•
wszystkie główne narządy i układy powstają między 4 i 8 tygodniem rozwoju – okres
organogenezy, zarodek najbardziej wrażliwy na czynniki zakłócające rozwój
•
identyfikacja okresu zadziałania czynnika zakłócającego rozwój w zależności od wady:
◦
anencephalia – 23-25 dzień rozwoju
◦
amelia (brak kończyn) – 5 tydzień rozwoju
Rozdział VI
OKRES PŁODOWY (tempus fetale, od 3 m-ca ciąży do urodzenia)
Rozwój płodu
•
różnicowanie tkanek i narządów
•
szybki wzrost całego organizmu
•
wady rozwojowe – nie powstają lub powstają nieliczne
•
czynniki cytotoksyczne mogą powodować obumieranie komórek OUN → zaburzenia
czynności OUN w życiu pozapłodowym
•
długość płodu – długość ciemieniowo-siedzeniowa (pozycja siedząca) lub pozycja stojąca – od
vertex do pięty
•
wyraźny przyrost długości płodu: 3-5 m-c ciąży
•
przyrost masy ciała: dwa ostatnie miesiące ciąży
•
trwanie ciąży:
◦
280 dni (40 tygodni) od początku ostatniej miesiączki
◦
266 dni (38 tygodni) od zapłodnienia
Zmiany w budowie płodu w poszczególnych miesiącach okresu płodowego
Względne spowolnienie wzrostu głowy w porównaniu zresztą ciała:
•
3 m-c: 1/2 długości ciemieniowo-siedzeniowej
•
5 m-c: 1/3 długości ciemieniowo-siedzeniowej
•
w momencie urodzenia: 1/4 długości ciemieniowo-siedzeniowej
3 miesiąc:
•
twarz nabiera cech ludzkich
22

•
oczy na przedniej powierzchni twarzy
•
uszy na powierzchni bocznej głowy
•
kończyny osiągają długość proporcjonalną do reszty ciała (dolne krótsze i mniej uformowane
niż górne)
•
12 tydzień ciąży: można odróżnić płeć płodu – uformowane narządy płciowe zewnętrzne
•
duże rozszerzenie pępowiny przez pętle jelitowe (cofają się do jamy brzusznej w 11 tygodniu)
•
poronione płody z końca 3 miesiąca ciąży wykazują reakcje odruchowe wskazująca na
aktywność mięśni (słabe, matka nie wyczuwa)
4 i 5 miesiąc:
•
długość płodu szybko wzrasta ( do 15 cm → 1/2 długości noworodka)
•
waga wzrasta tylko nieznacznie – do 0,5 kg
•
meszek (lanugo) – delikatne włoski pokrywające płód
•
ma brwi i włosy na głowie
•
w 5 m-cu ciąży matka zazwyczaj wyraźnie czuje ruchy płodu
Druga połowa życia wewnątrzmacicznego:
•
waga płodu znacznie wzrasta
•
ostatnie 2,5 m-ca – płód zwiększa swą wagę o 50% wagi donoszonego płodu (3200 g)
6 m-c: płód ma czerwonawą i pomarszczoną skórę (brak tk podskórnej)
płód urodzony w 6 m-cu lub pierwszej połowie 7-ego trudno utrzymać przy życiu:
OUN i układ oddechowy niewystarczająco dojrzałe, niezdolne do współdziałania
Ostatnie miesiące rozwoju płodowego: kształty płodu ulegają zaokrągleniu (tłuszczyk, tk podskórna);
skóra pokryta białawą tłuszczową substancją złożoną z produktów gruczołów łojowych– mazią
płodową (vernix caseosa) ; płód 28 tygodni da się utrzymać przy życiu
koniec 9 m-ca:
czaszka ma największy obwód w porównaniu z pozostałymi częściami ciała – znaczenie przy
przechodzeniu przez kanał rodny (ductus genitalis)
Charakterystyka płodu w okresie okołoporodowym:
•
waga: 3000-3400 g
•
długość ciemieniowo-siedzeniowa: ok. 36 cm; całkowita: 50 cm
•
cechy płciowe wyraźnie zaznaczone
•
u chłopczyków: jądra w mosznie
Określanie czasu porodu
•
266 dni (38 tygodni) po zapłodnieniu
•
ginekolog oblicza: 280 dni (40 tygodni) od pierwszego dnia ostatniej miesiączki
◦
u regularnych 28-dniowych cykli:
◦
u nieregularnych cykli:
23
włosy?rly?
Czas pomiędzy owulacją i następującym po nim krwawieniem miesięcznym jest stały (14 +- 1 dzień),
ALE czas pomiędzy owulacją i poprzedzającą ją miesiączką jest wysoce ZMIENNY!
Dodatkowa komplikacja: krwawienie podczas implantacji (mylnie uważane za miesiączkę)
wcześniak – noworodek urodzony przed terminem
ciążą przenoszona – urodzenie noworodka po terminie
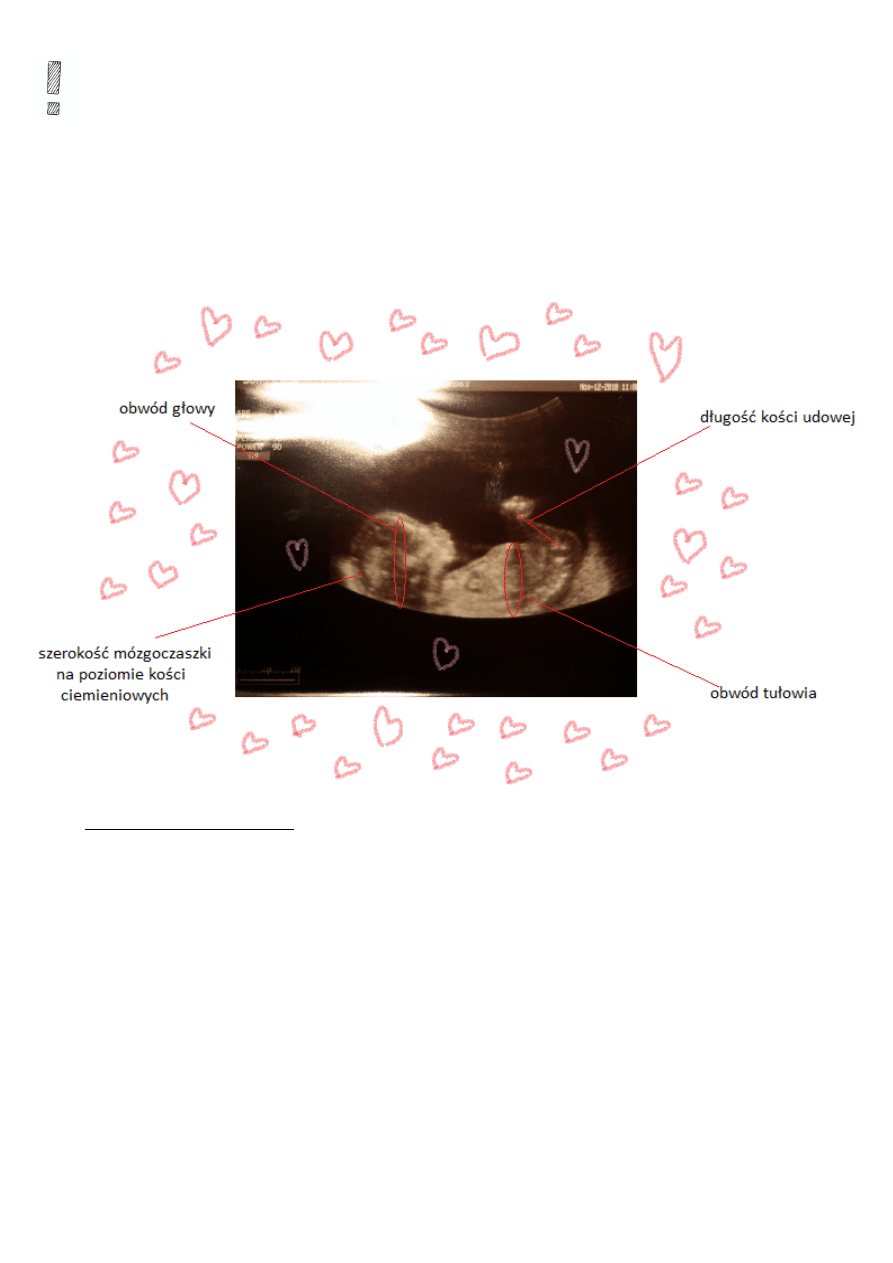
Przy określaniu wieku zarodka/płodu pomocne USG: dokładne ocenienie wymiaru ciemieniowo-
siedzeniowego (7-14 tydzień), później: długość mózgoczaszki na poziomie kości ciemieniowych,
obwód głowy, brzucha i k. udowej.
Nieprawidłowy wzrost płodu
wewnątrzmaciczne opóźnienie płodu – noworodki wykazująca wagę o 10 lub więcej percentyli
mniejszą od wagi właściwej; noworodki „zbyt małe w stosunku do wieku ciążowego”,
niedożywione w okresie płodowym, niedojrzałe; 1/10 niemowląt; zagrożenia:
◦
zaburzenia neurologiczne
◦
wady wrodzone
◦
zachłystywanie się smółką
◦
hipoglikemia
◦
hipokalcemia
◦
zespół niedomogi oddechowej (RDS – respiratory disstres syndrome)
czynniki powodujące:
•
wady chromosomowe (10%)
•
wewnątrzmaciczne zakażenia (różyczka, wirus cytomegaliczny, toksoplazmoza, kiła)
•
zły stan zdrowia matki (nadciśnienie, schorzenia nerek i układu krążenia)
24

•
stan odżywienia/pozycja społeczno-ekonomiczna matki
•
używanie tytoniu, alkoholu, narkotyków
Zagrożenia występują również w przypadku noworodków zbyt dużych:
•
podwyższona śmiertelność i zachorowalność
•
uszkodzenia barku (wynikające z niestosunku porodowego???)
•
przeważnie chłopczyki:D z przenoszonej ciąży
•
cukrzyca matki sprzyja → wzrost stymulowany przez epizody hipoglikemii → wywołują
kompensacyjne wydzielanie insuliny u płodu
Diagnostyka prenatalna
USG – najmniej traumatyzujące, użycie ultradźwięku do uzyskania obrazu łożyska i płodu, określenia
ich wielkości i pozycji; pozwala wykryć ciążę mnogie oraz zaburzenia rozwojowe
amniocenteza – pobranie płynu owodniowego; igła poprzez ścianę jamy brzusznej i macicy matki →
jama owodniowa → pobranie 20-30 ml płynu
nie przeprowadza się przed 14 tygodniem ciąży (brak wystarczającej ilości płynu)
- w płynie oznacza się zawartość alfa-fetoproteiny (APF) – białko płodowe występujące w
wysokim stężeniu w wypadku wad cewy nerwowej np. spina bifida i anencephalia
- komórki obecne w płynie namnaża się w hodowli tkanek i wykrywa wady chromosomowe
biopsja kosmków kosmówki -pobieranie małego fragmentu kosmówki z kosmkami, zawiera liczne,
szybko dzielące się komórki płodowe → nadają się do diagnozowania wad morfologicznych i
biochemicznych; można wykonywać we wczesnym okresie ciąży (8 tydzień) i bezpośrednio
wykonać analizę (bez czekania na namnożenie); wada: niemożność oznaczenia APF
Wskazania do zastosowania testów:
a) zaawansowany wiek matki (>35 lat)
b) występowanie wad cewy nerwowej w rodzinie
c) wcześniejsze urodzenie dziecka z wadami chromosomowymi
d) wady chromosomowe u jednego z rodziców
e) matka jest nosicielem schorzeń recesywnych związanych z chromosomem X
Rozdział VII
BŁONY PŁODOWE I ŁOŻYSKO
Początek 2 m-ca ciąży – trofoblast zawiera duża liczbę kosmków 2-go i 3-cio rzędowych,
zakotwiczonych w blaszce kosmówki i łączących się na obwodzie z doczesną za pośrednictwem
pokrywy cytotrofoblastycznej. Na powierzchni kosmków: syncytium, które spoczywa na warstwie
komórek cytotrofoblastycznych, pokrywających rdzeń zbudowany z unaczynionej mezodermy.
Układ naczyń włosowatych kosmków palowych łączy się z naczyniami włosowatymi w blaszce
kosmówki i szypule łączącej → ustanawia pozazarodkowy układ naczyniowy.
W następnych miesiącach rozwoju z kosmków palowych wrastają odgałęzienia do otaczających je
lakun. Nowo powstające kosmki zawierają cytotrofoblast, ale jego komórki zanikają na początku 4 m-
ca wraz z częścią komórek tkanki łącznej. Jedyna warstwa oddzielająca krążenie matczyne od
25

płodowego : syncytium i śródbłonkowa ściana naczyń krwionośnych. Do przestrzeni
międzykosmkowych dostają się guzki sycycjalne (kilkunastojądrowe fragmenty syncytium) →
przedostają się do krążenia matki → wyrodnieją bez objawów. Zanik komórek cytotrofoblastycznych
następuje najpierw w małych później w dużych kosmkach (tu: niecałkowity; te kosmki nie biorą
udziału w wymianie substancji).
Kosmówka kosmata i doczesna podstawna
Kosmówka:
a) kosmata (chorion frondosum) – dobrze rozwinięta kosmówka na biegunie zarodkowym
b) gładka (chorion laeve) – pozbawiona kosmków kosmówka bieguna przeciwzarodkowego
(degeneracja kosmków w 3 m-cu ciąży)
Doczesna – czynnościowa warstwa endometrium:
a) podstawna (decidua basalis) - styka się z kosmówką kosmatą, zawiera zbitą warstwę dużych
komórek doczesnowych, bogatych w lipidy i glikogen
b) torebkowa (decidua capsularis) – pokrywa biegun przeciwzarodkowy; w miarę powiększania
się worka kosmówki ulega rozciągnięciu i degeneracji, a kosmówka gładka dochodzi do
przeciwległej ściany macicy pokrytej doczesną ścienną (decidua parietalis) → doczesne łączą
się ze sobą, worek kosmówki całkowicie wypełnia światło macicy
Jedyną częścią kosmówki biorącą udział w wymianie między krążeniem matki i płodu jest
kosmówka kosmata. Wraz z doczesną podstawną tworzy łożysko (placenta).
Połączenie owodni i kosmówki i utworzenie błony owodniowo-kosmówkowej doprowadza do zaniku
jamy kosmówkowej. Błona ta pęka w czasie porodu.
Budowa łożyska
Na początku 4 m-ca:
•
Łożysko składa się z:
1. części płodowej (pars fetalis) – kosmówka kosmata
2. części matczynej (pars materna) – doczesna podstawna
•
po stronie płodowej łożysko ogranicza blaszka kosmówki (lamina chorii), a po matczynej –
doczesna podstawna.
•
najściślej wbudowana w łożysko: blaszka doczesnej.
•
strefa wewnętrzna, łącząca (zona intima) – strefa w której komórki trofoblastu i doczesnej
mieszają się ze sobą; w strefie tej występują olbrzymie komórki syncytiotrofoblastu i
doczesnej, a pomiędzy nimi dużo ilość bezpostaciowego materiału
•
większość komórek cytotrofoblastycznych zdegenerowała
•
pomiędzy blaszką kosmówki i doczesnej: przestrzenie międzykosmkowe wypełnione krwią
matki (z lakun syncytiotrofoblastu, wysłane syncytium pochodzenia płodowego)
•
odgałęzienia kosmków kontaktują się z krwią matki w przestrzeniach międzykosmkowych
Podczas 4 i 5 miesiąca:
•
doczesna podstawna wytwarza przegrody łożyskowe (septa) wnikające do przestrzeni
międzykosmkowych (nie dochodzą do blaszki kosmówki)
•
warstwy przegród:
◦
rdzenna – pochodzenia matczynego
26

◦
powierzchowna – warstwa komórek syncycjalnych
•
przegrody dzielą łożysko na płaty – liścienie (cototyledones)
•
połączenie pomiędzy przestrzeniami miedzykosmkowymi różnych liścieni jest zachowane –
przegrody nie dochodzą do blaszki kosmówki
•
łożysko wzrasta wraz z płodem
•
przyrost pola powierzchni łożyska wraz z powiększaniem się macicy
•
pod koniec ciąży: łożysko pokrywa 15-30% powierzchni wewnętrznej macicy
•
pogrubienie łożyska skutkiem rozgałęziania się kosmków (wrastanie wgłąb tkanek matki już
nie zachodzi)
Łożysko w okresie okołoporodowym
•
kształt krążka
•
średnica: 15-20 cm
•
grubość: 3 cm
•
waga: 0,5-0,6 kg
•
w czasie porodu: oderwanie od ściany macicy, wydalenie 30 minut po wydaleniu płodu
•
powierzchnia matczyna – widoczne 15-20 lekkich uwypukleń (liścieni) pokrytych warstwą
doczesnej podstawnej; bruzdy między liścieniami wywołane przegrodami
•
większa część doczesnej wydalona dopiero w czasie następnej miesiączki
•
powierzchnia płodowa – pokryta blaszką kosmówki, widoczne duże tętnice i żyły (naczynia
kosmówkowe), biegną w kierunku sznura pępowinowego
•
kosmówka pokryta owodnią
•
przyczep pępowiny umiejscowiony mimośrodkowo, niekiedy w pobliżu brzegu łożyska
przyczep welonowy (infixio velamentosa) – poza obrębem łożyska, na błonie kosmówkowej
Krążenie w łożysku
•
krew do liścieni: 80-100 tętnic spiralnych (przenikają przez blaszkę doczesnej do przestrzeni
międzykosmkowych)
•
wąskie światło tętnicy spiralnej
↓
utlenowana krew wpływa do przestrzeni międzykosmkowych pod zwiększonym ciśnieniem
↓
krew przedostaje się głęboko do przestrzeni międzykosmkowych
↓
obmywa liczne małe odgałęzienia drzewiastych kosmków
↓
spadek ciśnienia
↓
krew zawraca do blaszki kosmówki i w kierunku doczesnej
↓
krew uchodzi do żył błony śluzowej macicy
•
zawartość krwi w przestrzeniach międzykosmkowych: 150 ml
•
częstotliwość wymieniania krwi w przestrzeniach międzykosmkowych: 3-4 razy/min.
•
łączna powierzchnia kosmków kosmówki: 4-14 m
2
•
wymiana substancji wyłącznie w kosmkach w których naczynia płodowe stykają się
27

bezpośrednio z syncytiotrofoblastem pokrywającym kosmki
•
w kosmkach gdzie zachodzi wymiana: rąbek szczoteczkowy (zwiększa szybkość wymiany)
•
bariera łożyskowa – błona rozdzielająca krążenie płodowe i matczyne, składa się z:
1. śródbłonka wyścielającego płodowe naczynia krwionośne
2. tkanki łącznej w rdzeniu kosmków
3. cytotrofoblastu
4. syncytiotrofoblastu
•
od 4 m-ca ciąży bariera staje się cieńsza – śródbłonek przylega do syncytium → zwiększenie
szybkości wymiany
•
ludzkie łożysko: łożysko typu krwiokosmówkowego – krew matki oddzielona od krwi płodu
przez tkanki kosmówki
Czynność łożyska
Główne:
1. wymiana produktów metabolicznych i gazów
2. wytwarzanie hormonów
Wymiana gazów:
Wymiana O
2
, CO
2
i CO na drodze biernej dyfuzji.
W okresie okołoporodowym: płód pobiera 20 do 30 ml O
2
/ min.
→ krótka przerwa w dopływie tlenu → ZABÓJCZA
Wymiana substancji odżywczych i elektrolitów:
Płód pobiera: aminokwasy, WKT, węglowodany, witaminy i elektrolity bardzo szybko. Pobieranie
nasila się w miarę postępu ciąży.
Przekazywanie przeciwciał matczynych (IgG):
przeciwciała są wytwarzane przez matkę
↓
wychwytywanie na drodze endocytozy przez syncytiotrofoblast
↓
transport do naczyń włosowatych płodu
Przez IgG dzidzia jest chroniona przed: niektórymi chorobami zakaźnymi, nabiera biernej odporności
przeciwko błonicy, ospie, odrze (! nie przeciwko wyspie wietrznej i kokluszowi).
niezgodność grupowa Rh – płód ma Rh+, mama Rh- → krwinki płodu przedostają się do krwioobiegu
matki (niewielkie krwawienia z powierzchni kosmków) → powstanie przeciwciał →
przeciwciała przechodzą do krążenia płodu → niszczenie erytrocytów płodu
choroba hemolityczna noworodków (erythroblastosis fetalis) – zniszczenie krwinek
czerwonych płodu, może powodować wewnątrzmaciczne obumarcie płodu; aby wykryć
nasilenie choroby należy zbadać płyn owodniowy; obumarciu można zapobiec poprzez
wewnątrzmaciczne przetoczenie krwi lub wymienną transfuzję krwi po urodzeniu
Wytwarzanie hormonów:
•
pod koniec 4 m-ca: wywarzanie ilości progesteronu wystarczającej do utrzymania ciąży
•
synteza hormonów – syncytiotrofoblast:
28

◦
hormony estrogenne (głównie estradiol) – ilość wystarczająca do końca ciąży
◦
gonadotropina (HGC, ludzka gonadotropina kosmówkowa) – działanie podobne do
lutropiny; HGC w moczu = ciąża
◦
somatomammotropina (laktogen łożyskowy) – podobna do hormonu wzrostu, zapewnia
płodowi pierwszeństwo przy pobieraniu glukozy z krwi matki, wywołuje u matki objawy
cukrzycy
Większość hormonów wytwarzanych przez matkę nie przechodzi przez łożysko lub przechodzi bardzo
powoli (np. tyroksyna). Niebezpieczne:
•
syntetyczne progestageny – szybko przechodzą przez łożysko, wywołują maskulinizację
płodów płci żeńskiej
•
syntetyczny estrogen (dietylostilbestrol) – również szybko przechodzi przez łożysko, wywołuje
raka pochwy lub zaburzenia rozwojowe jąder u płodów
Przenikanie czynników infekcyjnych
Łożysko nie chroni przed: licznymi wirusami np. różyczki, Coxsackie, ospy, ospy wietrznej, odry,
poliowirusami – przechodzą przez nie. Niektóre wywołują infekcje powodujące zwyrodnienie
komórek i wrodzone zniekształcenia.
Przenikanie leków
Większość łatwo przechodzi przez łożysko (również ich metabolity). Mogą poważnie uszkadzać
zarodek. W okresie płodowym może rozwinąć się uzależnienie od narkotyków np. heroiny, kokainy.
Owodnia i sznur pępowiny
złączenie owodniowo-ektodermalne, pierścień pępkowy pierwotny (anulus umbilicalis primitivus) –
owalnego kształtu linia styku pomiędzy ektodermą owodniową i zarodkową; w 5
tygodniu przechodzą przez niego:
a) szypuła łącząca – zawiera: omocznie, dwie tętnice pępkowe i żyłę
b) szypuła pęcherzyka żółtkowego + naczynia żółtkowe
c) kanał łączący jamę ciała wewnątrzzarodkową z jamą ciała pozazarodkową
Pęcherzyk żółtkowy znajduje się w jamie kosmówkowej tzn. w przestrzeni między owodnią a
kosmówką.
Dalszy rozwój:
jama owodniowa szybko powiększa się kosztem jamy kosmówkowej
↓
owodnia zaczyna otaczać szypułę łączącą i pęcherzyka żółtkowego zbliżając je do siebie
↓
formuje się sznur pępowinowy pierwotny
Zawartość pępowiny:
•
część dalsza: szypuła pęcherzyka żółtkowego, naczynia żółtkowe
•
część bliższa: kilka nie cofniętych pętli jelitowych, resztki omoczni
Pęcherzyk żółtkowy znajduje się w jamie kosmówkowej i łączy z pępowiną za pośrednictwem
szypuły.
29

Koniec 3 m-ca: owodnia wzrasta do tego stopnia, że styka się z kosmówką, wypełniając w ten sposób
jamę kosmówkową → jama kosmówkowa przestaje istnieć. Pęcherzyk żółtkowy ulega obkurczeniu i
stopniowo zarasta.
Przez pewien czas jama brzuszna jest za mała aby pomieścić pętle jelita. Część z nich zostaje
wypchnięta do pozazarodkowej jamy ciała w obrębie sznura pępowinowego (jamy ciała
śródpępkowej). W ten sposób powstaje fizjologiczna przepuklina pępkowa. Do końca 3 m-ca pętle
jelitowe cofają się do jamy brzusznej, jama w pępowinie zmniejsza się i zarasta. Po zarośnięciu
przewodu omoczniowego i przewodu żółtkowego oraz towarzyszących im naczyń w sznurze
pozostają:
•
naczynia pępkowe
•
otaczająca je tk łączna galaretowata (galareta Whartona) – zawiera dużo proteoglikanów,
stanowi warstwę ochronną dla naczyń krwionośnych
Tętnice pępkowe – typu mięśniowego, ale zawierają liczne włókna sprężyste → szybkie zwężenie i
obkurczenie naczyń po zawiązaniu i odcięciu pępowiny.
Zmiany w łożysku pod koniec ciąży – zmniejszenie wymiany:
a) zwiększenie ilości włóknistej tk łącznej
b) pogrubienie błony podstawnej płodowych naczyń włosowatych
c) zarastanie małych naczyń włosowatych w kosmkach
d) odkładanie się włóknika na powierzchni kosmków w strefie wewnętrznej i blaszce kosmówki
- nadmierne wytwarzanie włóknika powoduje zawały kosmków, a nawet całego liścienia
(przybiera białawy wygląd)
Sznur pępowinowy w okresie okołoporodowym ma średnicę ok. 2 cm i długość 50-60 cm. W wyniku
spiralizacji pojawiają się węzły rzekome. Bardzo długa pępowina może zapętlić się wokół szyi płodu.
Zbyt krótka pępowina może wyrywać łożysko ze ściany macicy w czasie porodu.
Płyn owodniowy
•
przejrzysty, wodnisty
•
głównie: z krwi matki, dodatkowo wytwarzany prze komórki owodniowe
•
ostateczna ilość płynu: 0,8 – 1 l
•
we wczesnym okresie spełnia funkcję amortyzacyjno-ochronną (zarodek zawieszony na
pępowinie w płynie)
•
absorbuje wstrząsy
•
zapobiega przyleganiu zarodka do ściany jamy owodni
•
umożliwia ruchy płodu
•
woda ulega wymianie co 3 godziny
•
od 5 m-ca ciąży płód połyka płyn (wypija 400 ml dziennie) → absorbowanie płynu w jelitach
płodu → przechodzi do krążenia płodu → do krwi matki w łożysku
•
pod koniec ciąży do płynu wydzielany jest mocz płodowy: składa się z wody, produkty
przemiany materii płodu zużywane przez łożysko
•
w czasie porodu: owodnia + kosmówka → hydrostatyczny klin rozszerzający kanał szyjki
macicy
wielowodzie (hydramnion s. polyhydramnion) – nadmiar płynu owodniowego (1,5-2 l) przyczyny:
nieznane (idiopatyczne), cukrzyca matki, wady wrodzone np. OUN (brak mózgu) i układu
pokarmowego (zarośnięcie np. przełyku) → uniemożliwiają płodowi normalne płakanie płynu
30

skąpowodzie (oligohydramnion) – rzadkie, bark zawiązków nerek
Wielowodzie i skąpowodzie łączą się ze zwiększoną częstotliwością wad wrodzonych i uszkodzeń
płodu.
Błony płodowe u bliźniąt
Układ błon różny. Zależny od rodzaju ciąży bliźniaczej. W przypadku bliźniąt monozygotycznych od
momentu rozdzielenia.
Bliźnięta dizygotyczne (dwujajowe)
•
zdarzają się najczęściej
•
powstają po owulacji dwóch oocytów, każdy zapłodniony przez inny plemnik
•
zygoty indywidualnie implantują się w jamie macicy
•
każda wytwarza własne łożysko, owodnię i worek kosmówki
•
niekiedy łożyska lub ściany worków kosmówkowych zlewają się ze sobą
•
mozaikowatość erytrocytów – każde z bliźniąt posiada erytrocytów należące do dwóch grup
krwi ← wymiana erytrocytów przy dokładnym złączeniu się łożysk
Bliźnięta monozygotyczne (jednojajowe):
•
z pojedynczej zapłodnionej komórki
•
rozdzielenie zygoty może nastąpić w różnych stadiach rozwojowych
•
najwcześniej: stadium dwóch komórek → dwie odrębne zygoty → obie blastocysty
implantują się oddzielnie → każdy zarodek ma własne łożysko i worek kosmówki [tak samo
jak w dizygotycznych, tyle że PODOBNE FHUJ]
•
w większości przypadków rozdzielenie zygoty w stadium wczesnej blastocysty
z węzła zarodkowego dwie grupy komórek w tej samej jamie blastocysty → wspólne łożysko,
jama kosmówkowa ALE odrębne jamy owodniowe
•
rzadko: rozdzielenie w stadium dwublaszkowej tarczy zarodkowej, tuż przed pojawieniem się
smugi pierwotnej → pojedyncze wszystko
•
mimo wspólnego łożyska ilość krwi dopływającej do każdego z zarodków jest podobna
•
niekiedy w wyniku dużych zespoleń między naczyniami powstaje jeden bliźniak duży, drugi
mały
Inne opcje: trojaczki, czworaczki, pięcioraczki, sześcioraczki. Ostatnio ciążę mnogie zdarzają się
częściej ze względu na podawanie matkom hormonów gonadotropowych w przypadku barku
owulacji.
31
70%
30%
Bliźnięta zrośnięte
Rozdzielanie się zygoty w późniejszych stadiach rozwoju może doprowadzić do nieprawidłowego lub
niekompletnego podziału w okolicy tarczy zarodkowej. W efekcie powstają bliźnięta zrośnięte:
a) thoracopagus – bliźnięta zrośnięte w odcinku piersiowym
b) pygophagus – w odcinku grzbietowym
c) carniopagus – w obrębie czaszki
d) bliźnięta syjamskie – zrośnięte mostkiem skórnym lub wątrobowym
Można rozdzielić chirurgicznie.
Rozdział VIII
WADY WRODZONE – widoczne przy urodzeniu uszkodzenia w zakresie budowy
Częstość występowania
Szacowana na ok. 2-3% niemowląt żywo urodzonych; najwyższa: USA, najniższa: Niemcy.
Pod koniec pierwszego roku życia podwaja się – rozpoznawanie wad niezauważalnych przy
urodzeniu.
Teratologia – nauka badająca wady wrodzone, ich przyczyny oraz zmiany w zakresie budowy i
czynności
Teratogeny – czynniki powodujące wady wrodzone
Częstotliwość oraz rodzaje zniekształceń zmieniają się w zależności od rasy.
Czynniki środowiskowe
Do początku lat 40. przyjmowano, ze wady wrodzone są wywołane przez czynniki dziedziczne.
Przełomem było odkrycie, że różyczka matek we wczesnych okresach ciąży wywołuje anomalie u
płodów (Gregg). Pierwsze prace na temat czynników środowiskowych jako teratogenów – Warkany i
Kalter (badania na szczurach, brak pewnego składnika w diecie → zmiany wrodzone).
Od tego momenty datuje się szybki rozwój teratologii. Mimo tego wiedza o wadach wrodzonych u
ludzi nie zwiększyła się znacznie. Obecnie przyjmuje się, że:
•
10% wad wrodzonych – czynniki środowiskowe
•
10% - genetyczne i chromosomalne
•
80% - współdziałanie obu
Czynniki zakaźne
Czynnik zakaźny
Charakter wad wrodzonych
Różyczka
Anomalie:
a) oczu – zaćma, mikroftalmia
b) ucha wewnętrznego – uszkodzenie narządu Cortiego → wrodzona
głuchota
c) serca – przetrwały ductus arteriosus, ubytki w przegrodach
międzykomorowych i przedsionkowych
d) zębów – uszkodzenie warstwy szkliwa
e) uszkodzenie mózgu, opóźnienie rozwoju umysłowego
32

f) wewnątrzmaciczne opóźnienie wzrostu
g) uszkodzenie mięśnia sercowego i układu naczyniowego
Inne:
•
rodzaj wad uzależniony od stadium rozwoju płodu podczas zakażenia
np. zaćma – 6 tydzień, głuchota – 9 tydzień, serce 5-10 tydzień,
szkliwo – 2-9 tydzień, oun – drugi trymestr ciąży
•
trudno określić częstotliwość „poróżyczkowych” wad wrodzonych –
choroba może mieć przebieg łagodny, lub nietypowy obraz; inne
choroby powodujące wysypkę mogą być za nią brane
•
ryzyko wystąpienia wad: 47 % - infekcja w pierwszych 4 tyg. ciąży
22% - 5-8 tydzień, 7% - 9-12 tydzień, 6% - 13-16 tydzień
•
infekcja w pierwszych 8 tygodniach może prowadzić do obumarcia
płodu, porodów przedwczesnych
•
obecnie: testy pozwalające na wykrycie wirusa w materiale pacjentek,
możliwość ustalenie czy pacjentka jest uczulona (ma przeciwciała)
•
wirus przenika przez łożysko, infekcja dziecka może przetrwać wiele
miesięcy/lat (zakażenia personelu szpitalnego)
•
istnieje bezpieczna i skuteczna szczepionka przeciwko różyczce
Wirus cytomegalii
wrodzona cytomegalia: występowanie w komórkach noworodka ciałek
wtrętowych
Objawy:
a) mikrocefalia
b) zwapnienie mózgu
c) ślepota
d) zapalenie siatkówki
e) powiększenie wątroby i śledziony
f) ciężka żółtaczka mózgowa
g) osutki wybroczynowe na skórze
h) opóźniony rozwój umysłowy
i) zapalenie opon mózgowych i mózgu
j) ciałka wtrętowe głównie w komórkach: kanalików nerkowych i
znajdujących się w moczu
•
przyczyna: zakażenie in utero ludzkim wirusem cytomegalii przez
matki o bezobjawowym przebiegu choroby
•
zwykle nierozpoznawalna u a matek → nie wiadomo jaki wpływ na jej
przebieg ma wiek płodu; prawdopodobnie zakażenie we wczesnej
fazie uniemożliwia przeżycie płodu
Wirus opryszczki
(herpes simplex)
Zakażenie śródmaciczne na krótko przed urodzeniem.
Najczęściej zakażenie, jako chorobą weneryczną, od matki podczas porodu
objawy podczas pierwszych 3 tygodni życia – manifestacja reakcji
immunologicznych.
Objawy:
a) mikrocefalia
b) mikroftalmia
c) dysplazja siatkówki
33
d) powiększenie wątroby i śledziony
e) upośledzenie rozwoju umysłowego
Inne infekcje
wirusowe
i hipertermia
Inne infekcje wirusowe:
•
odra
•
świnka
•
zapalenie wątroby
•
poliomyelitis (choroba Heinego-Medina)
•
ospa wietrzna
•
ECHO
•
Coxsackie
•
grypa
Hipertermia:
•
wywołują ja zakażenia wirusowe
•
hipertermia (infekcja, SAUNA!!!) w czasie schodzenia się fałdów
nerwowych płytki nerwowej podczas tworzenia cewy nerwowej →
niemowlęta bezczaszkowe
Toksoplazmoza
(pierwotniak)
Uszkodzenia:
a) zwapnienia mózgu
b) wodogłowie
c) opóźnienie rozwoju umysłowego
d) uszkodzenia gałki ocznej: zapalenie naczyniówki i siatkówki,
mikroftalmia
Zwykle nierozpoznawalna u ciężarnych kobiet.
Kiła
(bakteria:
krętek blady)
Dawniej uznawana za główną przyczynę powstawania wad wrodzonych.
Może powodować:
a) głuchotę
b) opóźnienie rozwoju umysłowego
c) rozległe zwłóknienia w płucach i wątrobie
Promieniowanie
Powoduje (promienie X lub rad):
a) mikrocefalię
b) uszkodzenia czaszki
c) rozszczep kręgosłupa
d) rozszczep podniebienia
e) uszkodzenia kończyn
f) ślepota
Oprócz wpływu bezpośredniego należy pamiętać o wpływie na komórki rozrodcze → mutacje.
Czynniki chemiczne
•
teratogenność trudna do oceny ze względu na fakt uzyskiwania danych na postawie badań
retrospektywnych oraz dużą ilość środków farmakologicznych zażywanych przez kobiety
ciężarne (przeciętnie: 4)
34
Badania prospektywne:
Mały wpływ tych czynników
na wady wrodzone,
negowanie wpływu

Czynnik chemiczny
Objawy
Thalidomid -
środek nasenny,
zapobiegający nudnościom
a) brak, zniekształcenie kości długich
b) zarośniecie jelit
c) wady serca
d) amelia i meromelia
Aminopteryna– antymetabolit,
antagonista kwasy foliowego
a) wrodzony brak mózgu
b) wystąpienie przepukliny oponowej
c) wodogłowie
d) rozszczep wargi i podniebienia
W dawkach niewiele wyższych niż teratogenne powoduje
zatrzymanie ciąży – był stosowany w przerywaniu ciąży
gruźliczek.
Lek był stosowany dość powszechnie i nie wywoływał zmian
teratogennych – działanie nieudowodnione.
Difenylohydantonina -
lek przeciwpadaczkowy
a) wady serca
b) rozszczep twarzy
c) mikrocefalia
d) uszkodzenia mózgoczaszki
e) niedorozwój palców i paznokci
f) zahamowanie wzrostu
g) niedorozwój umysłowy
→ zespół płodowy hydantoniny
Trimetadion–
leczenie padaczki typu petit mal
a) wady serca
b) rozszczep twarzy
c) mikrocefalia
d) deformacja uszu
e) rozszczepienie podniebienia
f) anomalie układu moczowo-płciowego i szkieletowego
g) opóźnienie rozwoju fizycznego i umysłowego
→ zespół trimetadionu
Leki psychotropowe
i uspokajające
Fenotiazyna, lit, meprobamat, tlenek chlorodiazepiny, diazepina
(valium)
•
znaczny wzrost anomalii rozwojowych np. rozszczepu
wargi, podniebienia
Inne leki
•
propylotiouracyl
•
jodek potasu (wole, niedorozwój umysłowy)
•
streptomycyna (głuchota)
•
sulfonamidy (żółtaczka mózgowa)
•
impiramina – antydepresant (uszkodzenia kończyn)
•
tetracykliny (anomalie układu szkieletowego i uzębienia)
•
warfarin – obniża krzepliwość krwi (chondrodysplazja,
mikrocefalia)
•
chinina (głuchota)
•
aspiryna w dużych dawkach
35

Narkotyki
LSD, PCP, marihuana, alkohol, kokaina (brak jednoznacznych
dowodów)
palenie papierosów → obniżenie wagi noworodków
Alkohol
a) anomalie mózgoczaszki
b) niedorozwój szczęki
c) zwężenia szpary powiekowej
d) deformacja kończyn (zmiana ruchomości stawów)
e) deformacja układu naczyniowo-sercowego (ubytki
przegrody międzykomorowej)
→ FAS (płodowy zespół alkoholowy)
Nawet umiarkowane spożywanie alkoholu w ciąży jest szkodliwe
dla zarodka.
Izotreonina -
leczenie wyprysków
torbielowatych i przewlekłych
dermatoz
a) niedorozwój uszu
b) spłaszczenie nosa
c) niedorozwój szczęki
d) rozszczep podniebienia
e) wodogłowie
f) uszkodzenia serca
g) uszkodzenia pnia naczyniowego
→ embriopatia izotreoninowa, witaminy A
Hormony
Hormon
Objawy
Czynniki androgenne
- progestageny, w celu
zapobieżenia poronieniom
(etisteron, noretisteron)
a) działanie androgenne
b) maskulinizacja narządów płciowych żeńskich
c) przerost łechtaczki
d) zaburzenia związane z fuzją guzków wargowo-mosznowych
Dietylostilbestrol
-syntetyczny
estrogen
zapobiegający poronieniom
a) płody żeńskie zapadają na raka szyjki macicy
b) dysfunkcje rozrodcze: wady wrodzone macicy, jajowodów,
sklepienia pochwy
c) płody męskie: zmiany w zakresie jąder i spermatogenezy; nie
wzrasta ryzyko nowotworów
Kortyzon
Rozszczep podniebienia u potomstwa myszy i królic, u ludzi nie
stwierdzono (…).
36
Cukrzyca matek
•
porody martwych dzieci, zgony noworodków, nienormalnie duże płody
•
ryzyko wad 3-4 razy większe
•
u kobiet z długotrwałą cukrzycą: 80% potomstwa ma wady wrodzone
•
wady serca, układu szkieletowego, OUN
•
zespół zaniku ogonowego – niedorozwój kręgów krzyżowych oraz kończyn dolnych
•
za powstawanie wad odpowiedzialny poziom glukozy i insuliny
•
korelacja pomiędzy stopniem zaawansowania i czasem trwania cukrzycy a występowaniem
wad wrodzonych
•
leczenie insuliną lub preparatami tarczycy – mniej poronień
Niedobory pożywienia
Brak bezpośrednich dowodów na teratogenny efekt braku witamin, poza brakiem jodu wywołującym
endemiczny kretynizm.
Hipoksja
Wywołuje wady wrodzone u zwierząt. Nie stwierdzono u ludzi. Dzieci urodzone wysoko ponad
poziomem morza ważą mniej i są drobniejsze, niż dzieci urodzone na poziomie morza – nie
obserwuje się u nich wad wrodzonych.
Czynniki chemiczne związane ze środowiskiem naturalnym
•
organiczne związki rtęci z ryb (Japonia)
•
mięso świń karmionych kukurydzą zaprawianą środkami przeciwgrzybiczymi z rtęcią (USA)
•
ziarno zaprawiane środkami przeciwgrzybiczymi z rtęcią (Iran)
→ –objawy neurologiczne, przypominające pląsawicę mózgową
•
preparat defoliacyjny (Wietnam, Laponia, Arizona) – nie wykazano aby był teratogenny dla
ludzi !!!
Czynniki chromosomalne i genetyczne
Zaburzenia w obrębie chromosomów autosomalnych:
Zaburzenie
Charakterystyka
Trisomia 21
Zespół Downa
Spowodowany nierozejściem się chromosomów podczas mejozy.
•
częstość pojawiania się wzrasta wzrasta z wiekiem matki
•
jest wynikiem zburzeń mejozy w owogenezie !!! (nie
spermatogenezie)
•
twarz mongoidalna
•
duża, poprzeczna bruzda na doni (małpia bruzda)
•
opóźnienia rozwoju fizycznego i umysłowego
•
wrodzone wady serca
•
czasem spowodowany translokacją chromosomu 21, a nie trisomią
Trisomia 17-18
•
opóźnienie rozwoju umysłowego
•
wole wrodzone
•
niskie osadzenie uszu
•
wygięcia palców i rąk
37
•
mikrognacja - niezwykle mała szczęka lub żuchwa
•
anomalie w budowie nerek
•
syndaktylia – zrośnięcie się palców
•
deformacje układu szkieletowego
Na ogół: śmierć w wieku 2-óch m-cy.
Trisomia 13-15
•
opóźnienia rozwoju umysłowego
•
głuchota
•
wrodzona wada serca
•
rozszczep wargi i podniebienia
•
zmiany w obrębie gałki ocznej – mikroftalmia, anoftalmia, szczelina
tęczówki i powieki (coloboma)
Na ogół: śmierć w wieku 3 m-cy.
Procent anomalii chromosomowych w przypadku poronień jest 50 razy wyższy niż u płodów
donoszonych. Najczęściej spotykana anomalia w przypadkach poronień samoistnych: monosomia
chromosomu X.
Zaburzenia w obrębie chromosomów płciowych
Zaburzenie
Charakterystyka
Zespół Klinefeltera
XXY
Objawy kliniczne tylko u osobników płci męskiej. Są to:
a) niepłodność
b) niedorozwój jąder
c) zmiany szkliste w obrębie kanalików nasiennych krętych
d) ginekomastia – powiększenie gruczołów mlekowych
e) w 80% ciałka Barra
Przyczyna: nierozdzielenie się homologów XX.
Niekiedy XXXY lub inne nieprawidłowe zestawy chromosomów
(mozaikowatość)
Zespół Turnera
XO
Występuje u kobiet o niewątpliwych cechach fenotypowych żeńskich.
Objawy:
a) niedorozwój jajników (dysgenezja gonad)
b) kark błoniasty
c) obrzęki kończyn dolnych (zastój limfy)
d) zniekształcenia układu szkieletowego
e) opóźnienie rozwoju umysłowego
Przyczyna: brak rozdzielenia chromosomów w czasie mejozy w gametach
męskich. Może występować mozaikowatość.
Zespół potrójnego
chromosomu X
XXX
Objawy:
a) infantylność
b) zahamowanie rozwoju umysłowego
c) skąpe miesiączkowanie
d) w komórkach dwa ciałka Barra → „nadkobiety”
Przyczyna: zapłodnienie oocytu XX plemnikiem zawierającym X.
Niektóre pacjentki są płodne. Mają normalne potomstwo.
Zaburzenia struktury chromosomów
38

•
wywołane rozerwaniami i złamaniami
•
w wyniku wirusów, napromieniowania, leków
zespół miauczenia kota (cri du chat syndome) – wywołany częściowym ubytkiem jednego z
chromosomów pary 4-5; płacz dziecka przypomina miauczenie kota, występuje mikrocefalia,
opóźnienie rozwoju umysłowego, wady serca
Uszkodzenia genów
•
wady związane z mutacją pojedynczego genu (jednogenowe), ok. 10% wad wrodzonych;
dziedziczą się według praw Mendla
•
mogą powodować zniekształcenia strukturalne lub metaboliczne np. fenyloketonuria,
homocystynuria (zaburzenia metabolizmu siarkowych aminokwasów, brak aktywności
enzymu syntetazy cysteinowej), galaktozemia
•
wadom tym towarzyszy opóźnienie rozwoju umysłowego
Działanie teratogenów
1. Wrażliwość na czynnik teratogenny zależy od stadium rozwoju zarodka.
Stadia rozwoju zarodka:
a) stadium poprzedzające różnicowanie, stadium przed powstaniem listków zarodkowych –
szybkie namnażanie się komórek b. mało zróżnicowanych, od zapłodnienia do
wytworzenia listków zarodkowych
Działanie teratogenu w tym okresie powoduje uszkodzenie większości lub wszystkich
komórek zarodka → obumarcie lub uszkodzenie części komórek. W drugim przypadku
mechanizmy regulacyjne zarodka mogą ubytek naprawić → brak wady. Niektóre czynniki
teratogenne wybitnie teratogenne w późniejszych stadiach rozwoju (hiperwitaminoza,
promieniowanie) nie wpływają na rozwój zarodka we wcześniejszych fazach rozwoju.
b) stadium zarodkowe – ujawniają się różnice morfologiczne, wywołane zmianami na
poziomie chemicznym; intensywne różnicowanie się komórek
Większość teratogenów w tym okresie jest bardzo niebezpieczna i doprowadza do
powstania wad wrodzonych. Rodzaj zmian zależy od wrażliwości poszczególnych
narządów w danym okresie (patrz: wirus różyczki)
c) stadium końcowe, płodowe – wytwarzanie układów narządów
Gwałtowny spadek wrażliwości na czynniki teratogenne. Wrażliwe pozostają: móżdżek,
kora mózgu, elementy układu moczowo-płciowego
2. Wpływ czynników teratogennych zależy od genotypu
Czynniki teratogenne zwiększają wartości wskaźników wad występujących spontanicznie (bez
udziału czynnika teratogennego). U podstaw tego zwiększenia leży niestabilność genetyczna.
Zarówno geny matczyne jak i geny zarodka mają wpływ na czynnik teratogeny.
3. Czynniki teratogenne działają swoiście na danym etapie metabolizmu
Mogą wpływać na funkcje komórki lub ich produkty. Mogą hamować syntezę kwasów
nukleinowych lub białek, zmieniać ECM lub uszkadzać cytoarchitektonikę komórek zarodka.
39

POWODZENIA!
40
M
. O
.
Document Outline
- Rozdział I
- ROZWÓJ KOMÓREK ROZRODCZYCH (GAMETOGENEZA)
- Rozdział II
- Rozdział III
- Rozdział IV
- Rozdział V
- Rozdział VI
- Rozdział VII
- Rozdział VIII
Wyszukiwarka
Podobne podstrony:
Embrio Bartel Skrypt
Embrio ogólna skrypt
Embrio Bartel Skrypt
06 pamięć proceduralna schematy, skrypty, ramyid 6150 ppt
embriologia rozrodczy meski
geodezja satelitarna skrypt 2 ppt
Mój skrypt 2011
Mechanika Techniczna I Skrypt 2 4 Kinematyka
MNK skrypt
bo mój skrypt zajebiaszczy
praktyka skrypt mikrobiologia id 384986
Leki przeciwbakteryjne skrypt
Patrologia Ćwiczenia Skrypt
Mechanika Techniczna I Skrypt 4 2 4 Układ belkowy złożony
Biochemia skrypt AGH
więcej podobnych podstron