
„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
MINISTERSTWO EDUKACJI
NARODOWEJ
Honorata Życka
Wytwarzanie amoniaku, kwasu azotowego(V) i nawozów
azotowych 311[31].Z5.04
Poradnik dla nauczyciela
Wydawca
Instytut Technologii Eksploatacji – Państwowy Instytut Badawczy
Radom 2006

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
1
Recenzenci:
mgr inż. Halina Bielecka
dr Jacek Górski
Opracowanie redakcyjne:
mgr inż. Małgorzata Urbanowicz
Konsultacja:
dr inż. Bożena Zając
Korekta:
Poradnik stanowi obudowę dydaktyczną programu jednostki modułowej 311[31].Z5.04
„Wytwarzanie amoniaku, kwasu azotowego(V) i nawozów azotowych” zawartej
w modułowym programie nauczania dla zawodu technik technologii chemicznej.
Wydawca
Instytut Technologii Eksploatacji – Państwowy Instytut Badawczy, Radom 2006

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
2
SPIS TREŚCI
1. Wprowadzenie
2. Wymagania wstępne
3. Cele kształcenia
4. Przykładowe scenariusze zajęć
5. Ćwiczenia
4.1 5.1. Produkcja amoniaku
5.1.1. Ćwiczenia
5.2. Produkcja kwasu azotowego(V)
5.2.1. Ćwiczenia
5.3. Produkcja nawozów azotowych(V)
5.3.1. Ćwiczenia
6. Ewaluacja osiągnięć uczniów
7. Literatura
3
5
6
7
13
13
13
15
15
18
18
20
35

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
3
1. WPROWADZENIE
Przekazujemy Państwu Poradnik dla nauczyciela, który będzie pomocny w prowadzeniu
zajęć dydaktycznych w szkole kształcącej w zawodzie technik technologii chemicznej.
W poradniku zamieszczono:
−
wymagania wstępne,
−
wykaz umiejętności, jakie uczeń opanuje podczas zajęć,
−
przykładowe scenariusze zajęć,
−
propozycje ćwiczeń, które mają na celu wykształcenie u uczniów umiejętności
praktycznych,
−
wykaz literatury, z jakiej uczniowie mogą korzystać podczas nauki.
Wskazane jest, aby zajęcia dydaktyczne były prowadzone różnymi metodami ze szczególnym
uwzględnieniem:
−
tekstu przewodniego,
−
metody projektów,
−
pokazu z objaśnieniem,
−
wycieczek dydaktycznych,
−
ćwiczeń praktycznych.
Formy organizacyjne pracy uczniów mogą być zróżnicowane, począwszy od samodzielnej
pracy uczniów do pracy zespołowej.
W celu przeprowadzenia sprawdzianu wiadomości i umiejętności ucznia, nauczyciel może
posłużyć się zamieszczonym w rozdziale 6 zestawem zadań testowych oraz testem typu próba
pracy”.
W tym rozdziale podano również:
−
plan testu w formie tabelarycznej,
−
propozycje norm wymagań,
−
instrukcję dla nauczyciela,
−
instrukcję dla ucznia,
−
kartę odpowiedzi,
−
zestaw zadań testowych.
„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
4
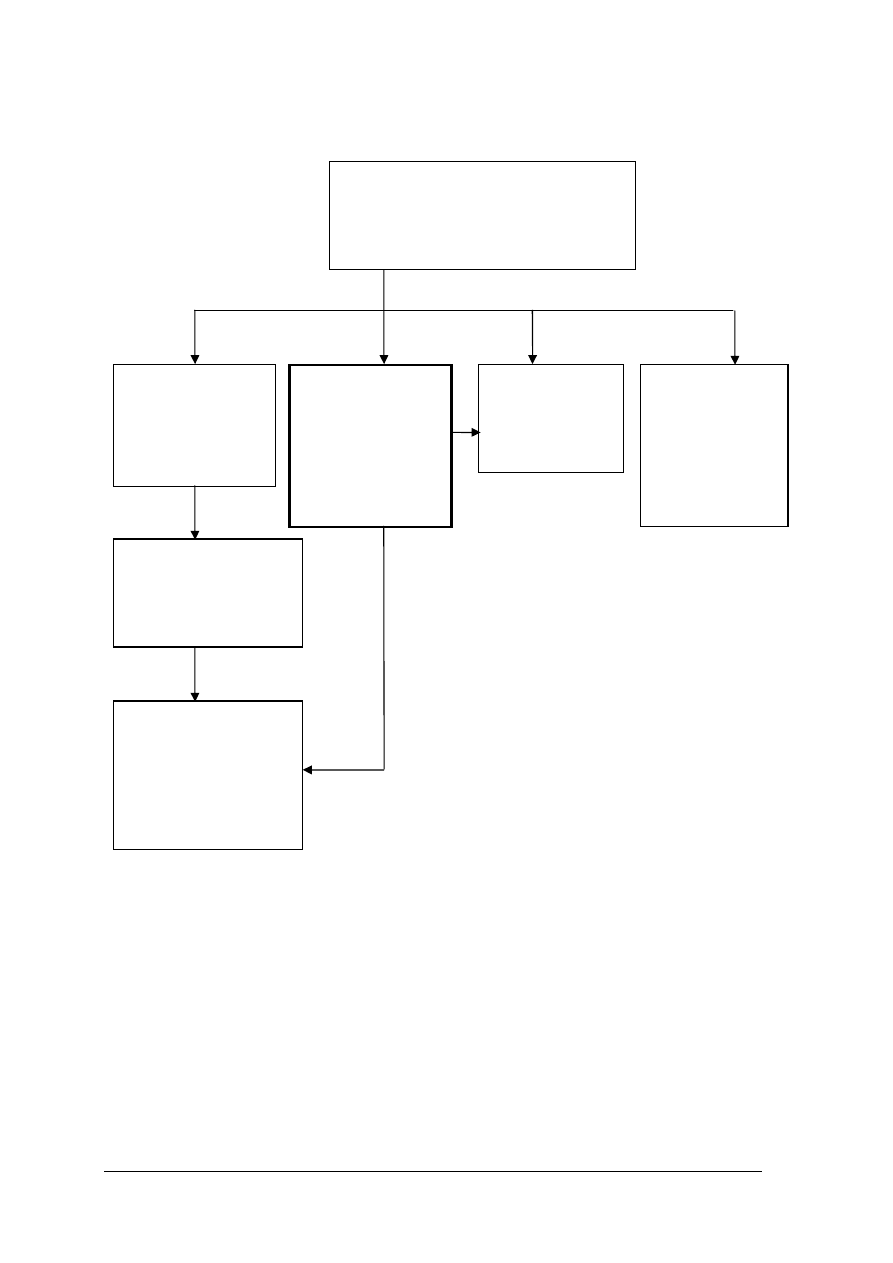
311[31].Z5
Technologia wytwarzania
półproduktów i produktów
nieorganicznych
311[31].Z5.01
Wytwarzanie siarki
odzyskiwanej
z siarkowodoru
311[31].Z5.04
Wytwarzanie
amoniaku, kwasu
azotowego(V)
i nawozów
azotowych
311[31].Z5.05
Wytwarzanie
sody
kalcynowanej
311[31].Z5.02
Wytwarzanie kwasu
siarkowego(VI)
z siarki
311[31].Z5.03
Wytwarzanie kwasu
fosforowego(V)
oraz nawozów
fosforowych
i wieloskładnikowych
Schemat układu jednostek modułowych
311[31].Z5.06
Wytwarzanie
chloru
i wodorotlenku
sodu metodą
elektrolizy
przeponowej

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
5
2. WYMAGANIA WSTĘPNE
Przystępując do realizacji programu jednostki modułowej „Wytwarzanie amoniaku, kwasu
azotowego(V) i nawozów azotowych” uczeń powinien umieć:
−
korzystać z różnych źródeł informacji, np. katalogi handlowe, opisy technologiczne, itp.,
−
czytać schematy procesów technologicznych,
−
zorganizować stanowisko pracy zgodnie z wymogami ergonomii,
−
nazwać związki chemiczne na podstawie ich wzoru sumarycznego,
−
pisać równania reakcji chemicznych,
−
wykonywać proste obliczenia oparte na równaniach reakcji,
−
interpretować przebieg reakcji odwracalnych,
−
stosować regułę przekory,
−
stosować prawo działania mas,
−
określać zasady technologiczne,
−
rozróżniać rodzaje zniszczeń korozyjnych.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
6
3. CELE KSZTAŁCENIA
W wyniku realizacji programu jednostki modułowej uczeń powinien umieć:
−
zinterpretować schemat ideowy wytwarzania związków azotowych: NH
3
, HNO
3
,
nawozów azotowych,
−
scharakteryzować etapy wytwarzania i oczyszczania surowego gazu syntezowego
do produkcji amoniaku,
−
określić zależność wydajności reakcji syntezy amoniaku od temperatury i ciśnienia,
−
określić sposób przygotowania katalizatora syntezy amoniaku,
−
scharakteryzować pracę radialnego reaktora do utleniania amoniaku,
−
wyjaśnić przebieg produkcji amoniaku w oparciu o uproszczony schemat instalacji
przemysłowej,
−
określić metody odzyskiwania energii w wytwórniach amoniaku,
−
określić znaczenie amoniaku i kwasu azotowego(V) jako półproduktów w produkcji
saletry amonowej i mocznika,
−
przedstawić sekwencję zasadniczych reakcji przebiegających w aparatach wytwórni kwasu
azotowego(V),
−
ocenić wpływ temperatury i czasu zetknięcia reagentów na stopień utlenienia amoniaku
na katalizatorze platynowo-rodowym,
−
uzasadnić wybór temperatury i szybkości objętościowej w procesie utleniania amoniaku
z zastosowaniem umiaru technologicznego,
−
określić przebieg produkcji HNO
3
w oparciu o uproszczony schemat instalacji
przemysłowej,
−
uzasadnić korzyści z wyboru podwyższonego, ale różnego ciśnienia w węzłach utleniania
NH
3
i absorpcji NO
2
,
−
scharakteryzować zasady bhp obowiązujące w wytwórniach NH
3
i HNO
3
,
−
ocenić zagrożenia wybuchowym rozkładem saletry amonowej podczas procesu
wytwarzania, magazynowania i użytkowania
−
zinterpretować uproszczony schemat wytwarzania saletry amonowej oraz zatężania
jej roztworów i granulacji,
−
wyjaśnić chemizm wytwarzania mocznika z ciekłego NH
3
,
−
podać przykłady zastosowania mocznika,
−
zastosować zasady bhp, ochrony ppoż. oraz ochrony środowiska obowiązujące
na stanowiskach prac,
−
sporządzić prosty bilans materiałowy.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
7
4. PRZYKŁADOWE SCENARIUSZE ZAJĘĆ
Scenariusz zajęć 1
Osoba prowadząca …………………………………….………….
Modułowy program nauczania: Technik technologii chemicznej 311[31]
Moduł: Technologia wytwarzania półproduktów i produktów nieorganicznych 311[31].Z5
Jednostka modułowa:
Wytwarzanie amoniaku, kwasu azotowego(V) i nawozów
azotowych 311[31].Z5.04
Temat: Analiza zagrożeń środowiska w wyniku procesów prowadzonych podczas
wytwarzania kwasu azotowego(V).
Cel ogólny: scharakteryzować zasady ochrony środowiska i bhp w zakładzie
wytwarzającym kwas azotowy(V).
Po zakończeniu zajęć edukacyjnych uczeń potrafi:
–
analizować schemat wytwarzania kwasu azotowego(V) pod kątem powstawania
odpadów produkcyjnych,
–
rozpoznać
związki
chemiczne
szkodliwe
dla
środowiska,
powstające
w procesie technologicznym kwasu azotowego(V),
–
podać sposób ograniczenia ich emisji do środowiska,
–
określić wtórne zanieczyszczenia środowiska,
–
scharakteryzować zasady bhp obowiązujące pracownika zakładu wytwarzającego
kwas azotowy(V),
–
podać sposób postępowania przy udzielaniu pierwszej pomocy poszkodowanemu w
związku z istniejącymi zagrożeniami.
Metody nauczania – uczenia się:
−
metoda tekstu przewodniego.
Formy organizacyjne pracy uczniów:
−
grupowa, jednolita
Czas: 45 minut.
Środki dydaktyczne:
–
rysunek 9 z materiału nauczania (4.2.1),
–
literatura do jednostki modułowej 311[31].Z5.04,
–
Karta charakterystyki substancji niebezpiecznej i preparatu niebezpiecznego:
amoniaku, kwasu azotowego(V) 50%, tlenków azotu.
Przebieg zajęć:
Zadanie dla ucznia
Przeprowadź analizę zagrożeń środowiska w wyniku procesów prowadzonych podczas
wytwarzania kwasu azotowego(V).
FAZA WSTĘPNA
Czynności organizacyjno-porządkowe, podanie tematu zajęć, zaznajomienie uczniów
z pracą metodą tekstu przewodniego.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
8
FAZA WŁAŚCIWA
INFORMACJE
1. Czy potrafisz dokonać analizy schematu wytwarzania kwasu azotowego(V)?
2. W jaki sposób ustalisz, że dany związek chemiczny jest szkodliwy dla środowiska?
3. Czy potrafisz zastosować odpowiednie zasady bhp?
PLANOWANIE
1. Dokonaj analizy schematu wytwarzania kwasu azotowego(V) i ustal substraty, produkt
główny i produkty uboczne procesu.
2. Wymień, które z nich stanowią zagrożenie dla środowiska.
3. Zaplanuj kolejne czynności, jakie podejmiesz w celu ustalenia działań ograniczających
wpływ zanieczyszczeń pierwotnych i wtórnych na środowisko otaczające zakład
wytwarzający kwas azotowy(V).
4. Uwzględnij zasady bhp dla pracownika ww. zakładu.
5. Ustal formę sprawozdania z wykonanego ćwiczenia.
UZGODNIENIE
1. Omów wszystkie punkty z fazy planowania z nauczycielem.
2. Odnieś się do uwag i propozycji nauczyciela.
3. Ustal wspólnie z nauczycielem kryteria oceniania zadania.
WYKONANIE
1. Dokonaj analizy dostępnych źródeł informacji pod kątem zagrożeń, jakie stwarza dla
środowiska produkcja kwasu azotowego(V).
2. Wymień i scharakteryzuj potencjalne zagrożenia, jakie stwarza dla środowiska oraz
pracownika proces wytwarzania kwasu azotowego(V).
3. Zaproponuj sposób ograniczenia emisji szkodliwych związków do środowiska.
4. Wymień wtórne zanieczyszczenia środowiska, jakie mogą powstać z uwolnionych
przez zakłady produkujące kwas azotowy(V).
5. Opisz sposób postępowania przy udzielaniu pierwszej pomocy poszkodowanemu
w przypadku wystąpienia wypadku.
6. Zaproponuj rozwiązania pozwalające zminimalizować zagrożenia dla środowiska.
7. Sporządź sprawozdanie z wykonanego ćwiczenia, nie zapominając o podaniu
wniosków.
SPRAWDZANIE
1. Sprawdzenie przygotowanych sprawozdań.
ANALIZA
Uczniowie wraz z nauczycielem wskazują, które etapy ćwiczenia sprawiły im najwięcej
trudności. Nauczyciel podsumowuje całe ćwiczenie, wskazuje, jakie nowe, ważne umiejętności
zostały
wykształcone,
jakie
wystąpiły
nieprawidłowości
i
jak
ich
unikać
w przyszłości.
FAZA KOŃCOWA
Zakończenie zajęć
Praca domowa
Odszukaj w dostępnych źródłach informacji, jakie działania w celu ochrony środowiska
podejmują Zakłady Azotowe „Puławy” S.A.
Sposób uzyskania informacji zwrotnej od ucznia po zakończonych zajęciach:
–
anonimowe ankiety ewaluacyjne dotyczące sposobu prowadzenia zajęć, trudności podczas
realizowania zadania i zdobytych umiejętności.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
9
Scenariusz zajęć 2
Osoba prowadząca …………………………………….………….
Modułowy program nauczania: Technik technologii chemicznej 311[31]
Moduł: Technologia wytwarzania półproduktów i produktów nieorganicznych 311[31].Z5
Jednostka modułowa: Wytwarzanie amoniaku, kwasu azotowego(V) i nawozów azotowych
311[31].Z5.04
Temat: Obserwacja obsługi aparatów instalacji produkcyjnych przemysłu
azotowego.
Cel ogólny: kształtowanie umiejętności charakteryzowania pracy urządzeń, etapów
wytwarzania produktów i zasad bhp zakładów azotowych.
Po zakończeniu zajęć edukacyjnych uczeń potrafi:
–
podać zasady bhp obowiązujące na terenie zakładów azotowych,
–
ocenić zagrożenia pojawiające się w czasie pracy zakładów azotowych,
–
scharakteryzować pracę wybranych urządzeń zakładów azotowych,
–
scharakteryzować etapy produkcji wybranych produktów przemysłu azotowego,
–
wymienić produkty odpadowe i uboczne pochodzące z zakładów przemysłu
azotowego,
–
scharakteryzować sposoby zagospodarowania i utylizacji wybranych produktów
odpadowych i ubocznych z zakładów azotowych.
Metody nauczania – uczenia się:
−
wycieczka dydaktyczna,
−
metoda tekstu przewodniego.
Formy organizacyjne pracy uczniów:
−
grupowa, jednolita.
Czas: 180 minut.
Środki dydaktyczne:
–
karta obserwacji,
–
instrukcja dla ucznia,
–
Karty charakterystyki produktów zakładów azotowych.
Przebieg zajęć:
1. Czynności organizacyjne. Podział zespołu uczniowskiego na zespoły trzyosobowe.
2. Zapoznanie z celami zajęć.
3. Wydanie kart obserwacji i instrukcji.
4. Wprowadzenie na teren zakładu.
5. Zapoznanie z przepisami bhp na terenie zakładu.
6. Wycieczka po terenie zakładu. Zapoznanie z surowcami i produktami wytwarzanymi
na terenie zakładu. Zapoznanie z technologią produkcji zakładów azotowych. Obserwacja
pracy urządzeń i obsługi.
7. Podsumowanie zajęć. Sprawdzenie wypełnienia kart obserwacji.
8. Omówienie zasad wykonania sprawozdania

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
10
Zakończenie zajęć
Praca domowa
Na podstawie wypełnionej karty obserwacji przygotuj sprawozdanie z wycieczki.
Sposób uzyskania informacji zwrotnej od ucznia po zakończonych zajęciach:
−
sprawdzenie przygotowanych sprawozdań.
Załączniki do scenariusza:
Załącznik 1:
INSTRUKCJA DLA UCZNIA
W czasie wycieczki po zakładzie przemysłu azotowego należy wykonać następujące
zadania:
1) zapoznanie się z obowiązującymi na terenie zakładu przepisami bhp i stosowanie się
do nich,
2) zebranie informacji o surowcach wykorzystywanych w procesie produkcyjnym,
3) zebranie informacji o produktach końcowych procesu,
4) zebranie informacji o urządzeniach stosowanych w procesie produkcji,
5) zebranie informacji o zagrożeniach związanych z procesem produkcji,
6) zebranie
informacji
o
odpadach
z
procesu
produkcyjnego
i
sposobach
ich zagospodarowania,
7) narysowanie schematu blokowego obserwowanego procesu produkcyjnego.
Ponadto w domu, na podstawie wypełnionej w czasie wycieczki karty obserwacji,
powinniście przygotować sprawozdanie zgodnie z zasadami podanymi przez nauczyciela.
W wykonaniu zadań opisanych w instrukcji pomoże Ci karta obserwacji, z którą należy się
dokładnie
zapoznać
przed
rozpoczęciem
wycieczki.
W
przypadku
problemów
ze zrozumieniem informacji zapisanych w instrukcji lub karcie obserwacji poproś o pomoc
nauczyciela.
Załącznik 2:
KARTA OBSERWACJI
I. Osoby prowadzące obserwacje:
.......................................
......................................
......................................
II. Przepisy bhp obowiązujące w czasie zwiedzania zakładu
1. Wymień zakazy obowiązujące na terenie zakładu produkcyjnego
−
−
−
−
„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
11
2. Wymień nakazy (bhp) obowiązujące na terenie zakładu produkcyjnego
−
−
−
−
−
III. Surowce wykorzystywane w procesie produkcji
Lp.
Nazwa surowca
Wzór
chemiczny
Zużycie
surowca
Sposób
wprowadzania
surowca
Zagrożenia związane
z użyciem surowca
IV. Produkty końcowe
Lp.
Nazwa
Właściwości
Zastosowanie
Zagrożenia związane
z użyciem produktu
V. Urządzenia i procesy w ciągu technologicznym
Lp.
Nazwa
urządzenia
Nazwa procesu
technologicznego
Warunki
prowadzenia procesu
Zagrożenia związane
z prowadzonym procesem

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
12
VI. Odpady i produkty uboczne powstające w zakładzie
Lp.
Nazwa produktu
odpadowego/ubocznego
Miejsce powstawania
(w ciągu technologicznym)
Sposób
zagospodarowania/utylizacji
VII. Miejsce na schemat blokowy
Poszczególne elementy schematu rysuj zgodnie z kolejnością zachodzących procesów,
uwzględnij również wszystkie wykorzystywane w procesie surowce i powstające produkty.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
13
5. ĆWICZENIA
5.1. Produkcja amoniaku
5.1.1. Ćwiczenia
Ćwiczenie 1
Dokonaj analizy instrukcji obsługi reaktora do syntezy amoniaku.
Wskazówki do realizacji:
Analizę instrukcji obsługi można przeprowadzić, w zależności od potrzeb, dla innego
urządzenia biorącego udział w procesie produkcji amoniaku. Instrukcje obsługi urządzeń
i aparatów znajdują się na każdym stanowisku pracy w zakładzie przemysłowym.
Przed przystąpieniem do realizacji ćwiczenia, nauczyciel powinien omówić zakres
i technikę wykonania ćwiczenia, a także sposób zaprezentowania wyników pracy. Powinien
również zapoznać uczniów z zasadami bezpiecznej pracy.
Sposób wykonania ćwiczenia
Uczeń powinien:
1) uważnie przeczytać instrukcję obsługi reaktora do syntezy amoniaku,
2) wypisać kolejne etapy obsługi urządzenia,
3) napisać cel wykonywanej czynności przy kolejnych etapach obsługi urządzenia,
4) podkreślić czynności o szczególnie istotnym znaczeniu dla prawidłowego przebiegu
procesu,
5) wypisać zagrożenia związane z obsługą aparatu,
6) uzupełnić tabelę:
Etapy obsługi
urządzenia
Cel wykonanej
czynności
Uwagi – porady
techniczne
i technologiczne
Uwagi
(specjalne
przepisy bhp)
Zalecane metody nauczania – uczenia się:
–
metoda tekstu przewodniego,
Środki dydaktyczne:
–
instrukcja obsługi reaktora do syntezy amoniaku.
Ćwiczenie 2
Zaprojektuj sposób prowadzenia ruchu w wytwórni amoniaku.
Wskazówki do realizacji:
Przed przystąpieniem do realizacji ćwiczenia, nauczyciel powinien omówić zakres
i technikę wykonania ćwiczenia, a także sposób zaprezentowania wyników pracy. Powinien
również zapoznać uczniów z zasadami bezpiecznej pracy.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
14
Sposób wykonania ćwiczenia
Uczeń powinien:
1) zapoznać się z materiałem dotyczącym wytwarzania amoniaku (4.1.1),
2) określić, od jakich parametrów zależy wydajność procesu,
3) scharakteryzować te parametry,
4) wymienić, jakie czynniki mogą wpłynąć na zmianę poszczególnych parametrów,
5) zaproponować, jakie działania należy podjąć, jeżeli poszczególne parametry procesu
ulegną zmianie,
6) zaprezentować wykonane ćwiczenie,
7) dokonać oceny poprawności wykonanego ćwiczenia.
Zalecane metody nauczania – uczenia się:
– metoda tekstu przewodniego,
Środki dydaktyczne:
−
materiał nauczania (4.1.1),
−
literatura do jednostki 311[31].Z5.04.
Ćwiczenie 3
Zanalizuj schemat obiegu kołowego gazów podczas wytwarzania amoniaku. Określ
korzyści wynikające z zastosowania obiegu gazów.
Wskazówki do realizacji:
Przed przystąpieniem do realizacji ćwiczenia nauczyciel powinien omówić zakres
i technikę wykonania ćwiczenia a także sposób zaprezentowania wyników pracy. Powinien
również zapoznać uczniów z zasadami bezpiecznej pracy.
Sposób wykonania ćwiczenia
Uczeń powinien:
1) zapoznać się z materiałem dotyczącym wytwarzania amoniaku (4.1.1),
2) określić zawartość amoniaku w gazach poreakcyjnych,
3) uzasadnić potrzebę zastosowania obiegu kołowego w procesie wytwarzania amoniaku,
4) zapoznać się z rysunkiem 5 (materiał nauczania punkt 4.1.1),
5) wyjaśnić, na podstawie schematu zasadę działania obiegu kołowego gazów w wytwórni
amoniaku,
6) wymienić korzyści wynikające z zastosowania obiegu kołowego,
7) opisać zasady technologiczne realizowane w obiegu kołowym,
8) zaprezentować wykonane ćwiczenie,
9) dokonać oceny poprawności wykonanego ćwiczenia.
Zalecane metody nauczania-uczenia się:
– metoda projektów,
Środki dydaktyczne:
−
schemat otrzymywania amoniaku w obiegu kołowym,
−
materiał nauczania (4.1.1),
−
literatura dla jednostki 311[31].Z5.04.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
15
5.2. Produkcja kwasu azotowego(V)
5.2.1. Ćwiczenia
Ćwiczenie 1
Sporządź bilans materiałowy procesu utleniania amoniaku w odniesieniu do masy
amoniaku potrzebnej do wyprodukowania 1000 kg 100% kwasu azotowego(V). Obliczenia
należy przeprowadzić, przyjmując następujące dane wyjściowe:
−
zawartość amoniaku w mieszaninie amoniakalno-powietrznej wynosi 10,5% obj., z czego
97% utlenia się do tlenku azotu(II), a pozostałe 3% do azotu,
−
powstały tlenek azotu(II) przereagowuje na kwas azotowy z wydajnością procesu – 98%.
Wskazówki do realizacji:
Przed przystąpieniem do realizacji ćwiczenia, nauczyciel powinien omówić zakres
i technikę wykonania ćwiczenia, a także sposób zaprezentowania wyników pracy. Powinien
również zapoznać uczniów z zasadami bezpiecznej pracy.
Szczególny nacisk należy położyć na zasady wykonywania bilansów materiałowych.
Nauczyciel powinien również omówić sposób prezentacji wyników obliczeń.
Sposób wykonania ćwiczenia
Uczeń powinien:
1) obliczyć teoretyczną masę NH
3
potrzebną do wyprodukowania 1000 kg 100% HNO
3
,
2) obliczyć rzeczywistą masę NH
3
potrzebną do wyprodukowania 1000 kg 100% HNO
3
,
uwzględniając wydajność procesu,
3) ustalić objętość mieszaniny amoniakalno-powietrznej zawierającej potrzebną ilość
amoniaku do wyprodukowania 1000 kg 100% HNO
3
,
4) obliczyć masę tlenku azotu(II) otrzymanego w wyniku utlenienia amoniaku,
5) obliczyć masę azotu otrzymanego w wyniku utlenienia amoniaku,
6) obliczyć masę pary wodnej wytworzonej w reakcji utlenienia amoniaku,
7) obliczyć masę nieprzereagowanego tlenu,
8) obliczyć masę azotu w gazach odlotowych,
9) sporządzić zestawienie bilansowe.
Zalecane metody nauczania – uczenia się:
– ćwiczenia obliczeniowe.
Środki dydaktyczne:
−
układ okresowy pierwiastków,
−
przykładowe zestawienie bilansowe,
−
kalkulator,
−
literatura z rozdziału 7.
Ćwiczenie 2
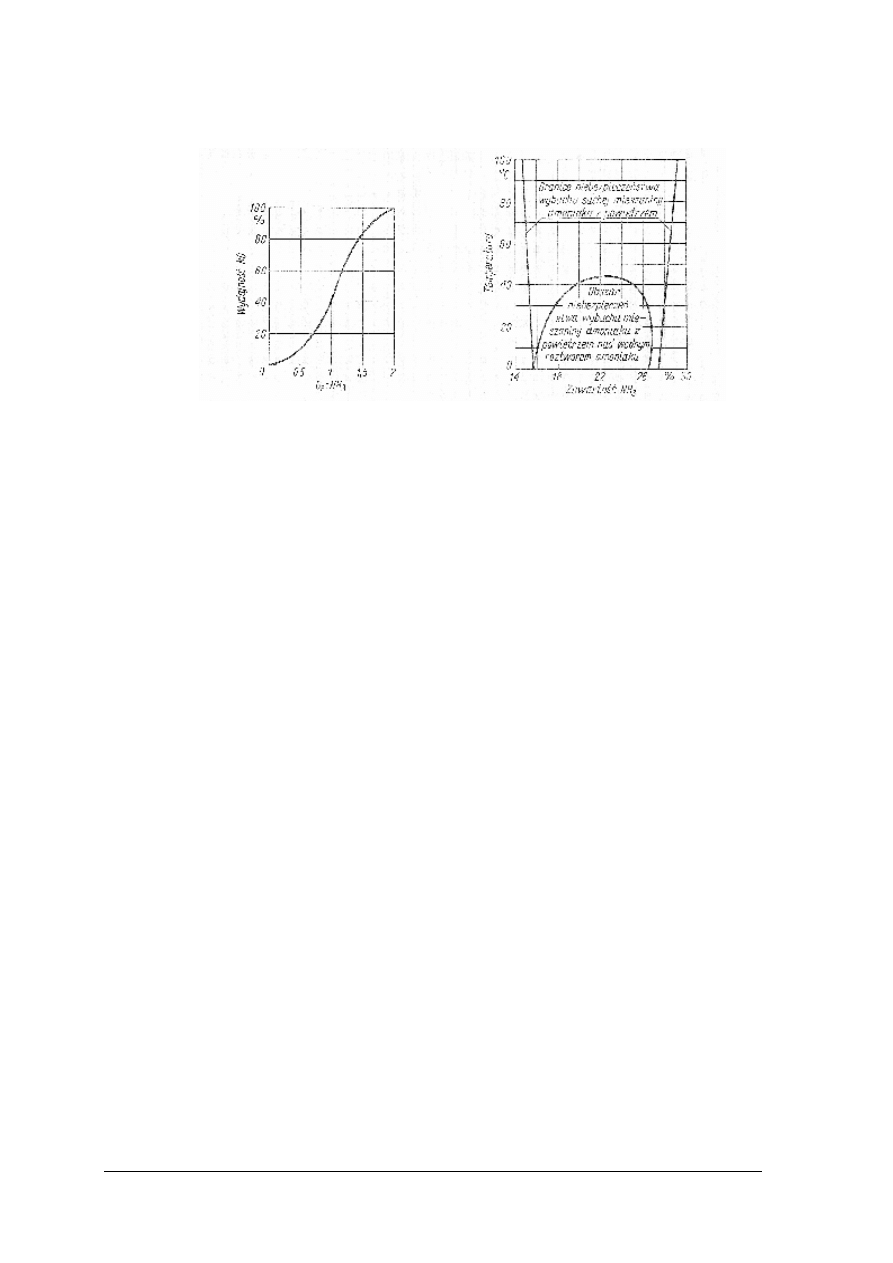
Jednym z etapów procesu otrzymywania kwasu azotowego(V) z amoniaku jest utlenianie
kontaktowe amoniaku w reaktorze. Ustal optymalny skład mieszaniny amoniaku
z powietrzem, uwzględniając wydajność tego etapu produkcji i zagrożenia wynikające
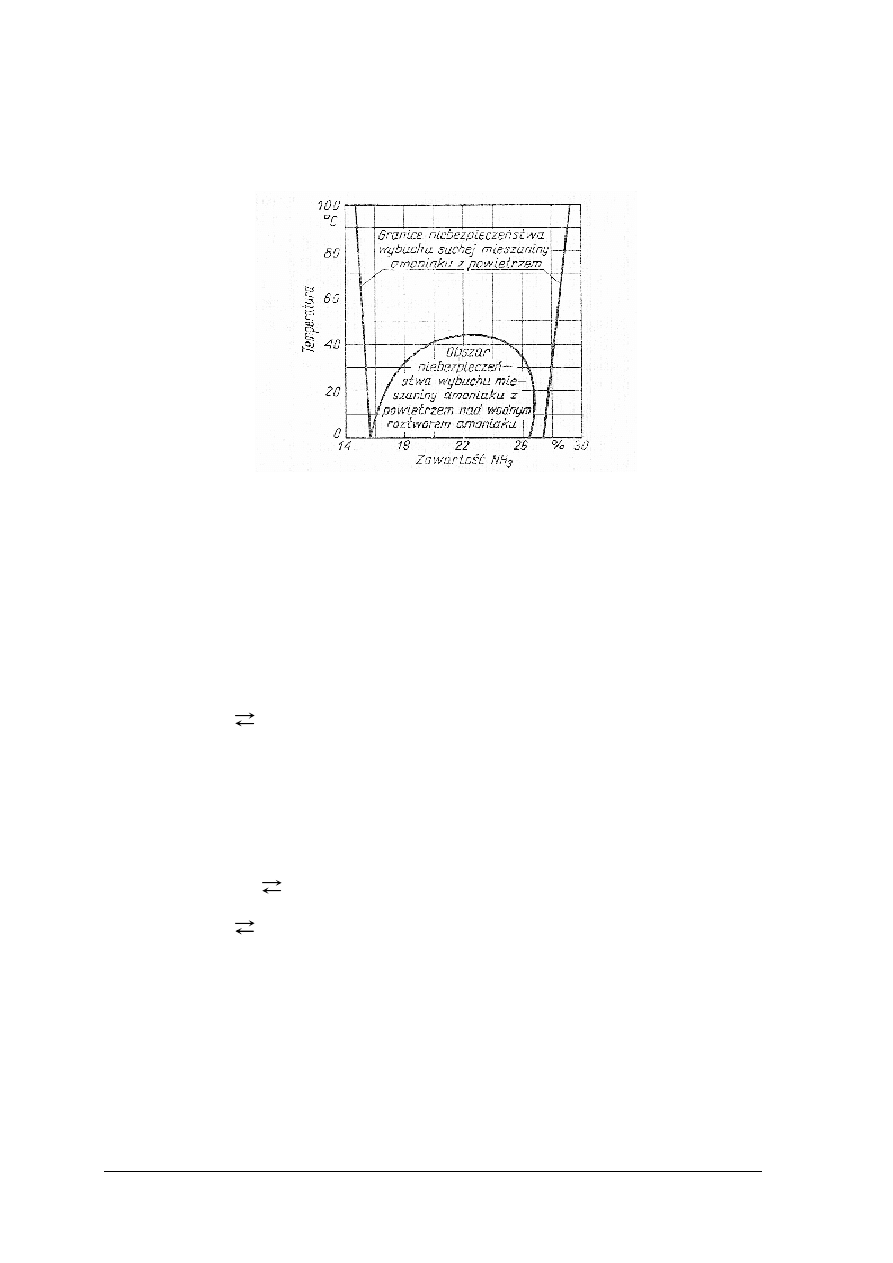
z właściwości wybuchowych mieszaniny, w oparciu o załączone wykresy fizykochemiczne.
„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
16
Rys. 11. A – zależność wydajności NO od stosunku stężenia O
2
: NH
3
w mieszaninie,
B – zawartość NH
3
w powietrzu, powodująca niebezpieczeństwo wybuchu mieszaniny [4]
Wskazówki do realizacji:
Przed przystąpieniem do realizacji ćwiczenia, nauczyciel powinien omówić zakres
i technikę wykonania ćwiczenia, a także sposób zaprezentowania wyników pracy. Powinien
również zapoznać uczniów z zasadami bezpiecznej pracy.
Sposób wykonania ćwiczenia
Uczeń powinien:
1) napisać równanie reakcji utleniania amoniaku tlenem do NO,
2) odczytać z wykresu (rys. 11 A) stosunek tlenu do amoniaku, jeżeli wydajność procesu
otrzymywania NO wynosi od 90–100%,
3) obliczyć, jaki musi być stosunek powietrza z amoniakiem, aby wartości stosunku stężenia
tlenu i amoniaku w mieszaninie reakcyjnej ustalone na podstawie wykresu zostały
zachowane (do obliczeń przyjmij zawartość tlenu w powietrzu 21%),
4) odczytać z wykresu zawartość amoniaku w powietrzu, powodującą niebezpieczeństwo
wybuchu mieszaniny,
5) ocenić, czy ustalony skład mieszaniny reakcyjnej amoniaku w powietrzu w procesie
utleniania do NO jest bezpieczny i nie grozi wybuchem,
6) ustalić, jakie czynniki zwiększają granice wybuchowości mieszaniny,
7) ustalić, jakie czynniki powodują zmniejszenie granicy wybuchowości mieszaniny,
8) porównać otrzymane wyniki z danymi zawartymi w materiale nauczania (4.2),
9) dokonać oceny poprawności wykonanych obliczeń.
A
B

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
17
Zalecane metody nauczania – uczenia się:
– metoda tekstu przewodniego.
Środki dydaktyczne:
−
kalkulator,
−
wykresy fizykochemiczne zamieszczone w treści ćwiczenia,
−
podstawy fizykochemiczne produkcji kwasu azotowego(V) (materiał nauczania 4.2.),
−
przybory do pisania.
Ćwiczenie 3
Przeprowadź analizę zagrożeń środowiska w wyniku procesów prowadzonych podczas
wytwarzania kwasu azotowego(V).
Wskazówki do realizacji:
Przed przystąpieniem do realizacji ćwiczenia, nauczyciel powinien omówić zakres
i technikę wykonania ćwiczenia, a także sposób zaprezentowania wyników pracy. Powinien
również zapoznać uczniów z zasadami bezpiecznej pracy.
Sposób wykonania ćwiczenia
Uczeń powinien:
1) zapoznać się z materiałem nauczania punkt 4.2.1,
2) zapisać wzory i nazwać tlenki azotu znajdujące się w gazach odlotowych wytwórni kwasu
azotowego(V),
3) zaproponować sposób usunięcia ich z gazów odlotowych, napisać równania reakcji
ilustrujące te procesy,
4) ustalić, jakie wartości NDS (Największe Dopuszczalne Stężenie) są dopuszczalne dla
środowiska,
5) wymienić, jakie zagrożenia dla środowiska wynikają z przekroczenia NDS dla tlenków
azotu,
6) określić, jakie inne związki chemiczne szkodliwe dla środowiska mogą powstać
z uwolnionych do otoczenia tlenków azotu, napisać odpowiednie równania reakcji,
7) przewidzieć, jakie reagenty procesu wytwarzania kwasu azotowego(V) mogą powodować
zagrożenia dla pracowników wytwórni,
8) zaproponować środki ochrony osobistej dla pracowników wytwórni kwasu azotowego(V)
w związku z istniejącymi zagrożeniami,
9) opisać po zapoznaniu się z Kartą charakterystyki substancji niebezpiecznej i preparatu
niebezpiecznego
sposoby
postępowania
przy
udzielaniu
pierwszej
pomocy
poszkodowanym
w związku z istniejącymi zagrożeniami,
10) zaprezentować wykonane ćwiczenie,
11) dokonać oceny poprawności wykonanego ćwiczenia.
Zalecane metody nauczania – uczenia się:
– metoda tekstu przewodniego.
Środki dydaktyczne:
– materiał nauczania (4.2.1),
– literatura do jednostki 311[31].Z5.04,
– Karta charakterystyki substancji niebezpiecznej i preparatu niebezpiecznego dla: amoniaku,
kwasu azotowego(V) 50%, tlenków azotu.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
18
5.3. Produkcja nawozów azotowych
5.3.1. Ćwiczenia
Ćwiczenie 1
Obserwacja pracy sterowni zakładów azotowych.
Wskazówki do realizacji:
W celu przeprowadzania poniższego ćwiczenia, konieczne jest zorganizowanie wycieczki
na teren zakładów azotowych, najlepiej o pełnym zakresie produkcji produktów azotowych
(amoniak, kwas azotowy(V), nawozy).
Przed przystąpieniem do realizacji ćwiczenia nauczyciel powinien zapoznać uczniów
z przepisami bhp obowiązującymi na terenie zakładu przemysłowego. Powinien omówić zakres
i technikę wykonania ćwiczenia ze szczególnym uwzględnieniem sposobu wypełnienia karty
obserwacji i sposobu przygotowania sprawozdania. Należy zwrócić uwagę na konieczność
zadawania pytań oprowadzającemu grupę personelowi zakładu w celu uzyskania potrzebnych,
do wykonania ćwiczenia, informacji. Przed wejściem na teren zakładu, nauczyciel powinien
również rozdać uczniom instrukcje i karty obserwacji.
Sposób wykonania ćwiczenia
Uczeń powinien:
1) zapoznać się z obowiązującymi na terenie zakładu przepisami bhp i stosować się do nich,
2) pobrać od nauczyciela instrukcję i kartę obserwacji, która pomoże Ci w zbieraniu
informacji,
3) zebrać informacje o zasadach pracy sterowni,
4) zebrać informacje o obowiązkach pracowników sterowni,
5) zebrać informacje o monitorowanych w sterowni procesach produkcyjnych,
6) narysować uproszczony schemat blokowy monitorowanej wytwórni,
7) na podstawie wypełnionego arkusza obserwacji przygotować sprawozdanie zgodnie
z zasadami podanymi przez nauczyciela.
Zalecane metody nauczania – uczenia się:
– wycieczka dydaktyczna,
– metoda tekstu przewodniego.
Środki dydaktyczne:
−
karta obserwacji,
−
instrukcja dla ucznia.
Ćwiczenie 2
Obserwacja obsługi aparatów instalacji produkcyjnych przemysłu azotowego.
Wskazówki do realizacji:
W celu przeprowadzania poniższego ćwiczenia konieczne jest zorganizowanie wycieczki
na teren zakładów azotowych, najlepiej o pełnym zakresie produkcji produktów azotowych
(amoniak, kwas azotowy(V), nawozy).

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
19
Przed przystąpieniem do realizacji ćwiczenia, nauczyciel powinien zapoznać uczniów
z przepisami bhp obowiązującymi na terenie zakładu przemysłowego. Powinien omówić zakres
i technikę wykonania ćwiczenia ze szczególnym uwzględnieniem sposobu wypełnienia karty
obserwacji i sposobu przygotowania sprawozdania. Należy zwrócić uwagę na konieczność
zadawania pytań oprowadzającemu grupę personelowi zakładu w celu uzyskania potrzebnych,
do wykonania ćwiczenia, informacji. Przed wejściem na teren zakładu, nauczyciel powinien
również rozdać uczniom instrukcje i karty obserwacji.
Sposób wykonania ćwiczenia
Uczeń powinien:
1) zapoznać się z obowiązującymi na terenie zakładu przepisami bhp i stosować się do nich,
2) pobrać od nauczyciela instrukcję i kartę obserwacji,
3) zebrać informacje o wykorzystywanych w procesie produkcyjnym surowcach,
4) zebrać informacje o produktach końcowych procesu,
5) zebrać informacje o urządzeniach stosowanych w procesie produkcji,
6) zebrać informacje o zagrożeniach związanych z procesem produkcji,
7) zebrać informacje o odpadach z procesu produkcyjnego i sposobach ich
zagospodarowania,
8) narysować schemat blokowy obserwowanego procesu produkcyjnego,
9) na podstawie wypełnionego arkusza obserwacji przygotować sprawozdanie zgodnie
z zasadami podanymi przez nauczyciela
Zalecane metody nauczania – uczenia się:
– wycieczka dydaktyczna,
– metoda tekstu przewodniego.
Środki dydaktyczne:
−
karta obserwacji,
−
instrukcja dla ucznia,
−
karty charakterystyki produktów.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
20
6. EWALUACJA OSIĄGNIĘĆ UCZNIA
Przykłady narzędzi pomiaru dydaktycznego
Test dwustopniowy do jednostki modułowej
„Wytwarzanie amoniaku, kwasu
azotowego(V) i nawozów azotowych”
Test składa się z 20 zadań wielokrotnego wyboru, z których:
−
zadania 1, 2, 4, 5, 9, 11, 13, 15, 16, 17, 18, 20 są z poziomu podstawowego,
−
zadania 3, 6, 7, 8, 10, 12, 14, 19 są z poziomu ponadpodstawowego.
Punktacja zadań: 0 lub 1 punkt
Za każdą prawidłową odpowiedź uczeń otrzymuje 1 punkt. Za złą odpowiedź lub jej brak
uczeń otrzymuje 0 punktów.
Proponuje się następujące normy wymagań – uczeń otrzyma następujące
oceny szkolne:
−
dopuszczający – za rozwiązanie co najmniej 8 zadań z poziomu podstawowego,
−
dostateczny – za rozwiązanie co najmniej 12 zadań z poziomu podstawowego,
−
dobry – za rozwiązanie 16 zadań, w tym co najmniej 4 z poziomu ponadpodstawowego,
−
bardzo dobry – za rozwiązanie 19 zadań, w tym co najmniej 7 z poziomu
ponadpodstawowego.
Klucz odpowiedzi: 1. b, 2. c, 3. a, 4. d, 5. b, 6.c, 7. d, 8. b, 9. a, 10. c, 11. b,
12. b, 13. c, 14. a, 15. d, 16. c, 17. d, 18. a, 19. c, 20. c
Plan testu
Nr
zad.
Cel operacyjny
(mierzone osiągnięcia ucznia)
Kategoria
celu
Poziom
wymagań
Poprawna
odpowiedź
1
Scharakteryzować przygotowanie
surowca do syntezy amoniaku
B
P
B
2
Określić skład gazu syntezowego
stosowanego do syntezy amoniaku
A
P
C
3
Scharakteryzować zależność
wydajności syntezy amoniaku do
ciśnienia i temperatury
C
PP
A
4
Określić wpływ czynników
zewnętrznych na proces korozji
wodorowej
A
P
C
5
Określać sposób przygotowania
katalizatora/kontaktu do syntezy
amoniaku
A
P
B
„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
21
Nr
zad.
Cel operacyjny
(mierzone osiągnięcia ucznia)
Kategoria
celu
Poziom
wymagań
Poprawna
odpowiedź
6
Scharakteryzować trucizny kontaktu w
reaktorze radialnym do otrzymywania
amoniaku
C
PP
D
7
Ocenić, które parametry mają wpływ na
stopień utlenienia amoniaku
C
PP
D
8
Scharakteryzować, zawartość amoniaku
w powietrzu, powodującą wybuch
C
PP
B
9
Określić, które z niebezpiecznych
substancji stosowanych w zakładach
wytwarzających kwas azotowy(V)
stanowią zagrożenie dla środowiska
A
P
A
10 Sporządzać prosty bilans materiałowy
C
PP
D
11
Rozróżniać reakcje zachodzące
w wytwórni kwasu azotowego(V)
B
P
B
12
Scharakteryzować przebieg produkcji
HNO
3
w oparciu o uproszczony
schemat instalacji przemysłowej
C
PP
B
13 Określić skład saletry amonowej
A
P
C
14
Przedstawić chemizm produkcji
mocznika
C
PP
A
15
Podać przykłady zastosowania
mocznika
A
P
D
16
Zinterpretować uproszczony schemat
wytwarzania saletry amonowej
C
P
C
17
Dobrać surowce do produkcji saletry
amonowej jako nawozu
B
P
D
18
Scharakteryzować zasady ochrony
ppoż. w zakładzie produkcji saletry
amonowej
B
P
A
19
Scharakteryzować zasady ochrony
środowiska w zakładach nawozów
azotowych
C
PP
C
20
Zinterpretować schemat wytwarzania
związków azotowych
C
P
C

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
22
Przebieg testowania
INSTRUKCJA DLA NAUCZYCIELA
1. Ustal z uczniami termin przeprowadzenia sprawdzianu z wyprzedzeniem co najmniej
jednotygodniowym.
1. Omów cel stosowania pomiaru dydaktycznego.
2. Zapoznaj uczniów z rodzajem zadań podanych w zestawie oraz z zasadami punktowania.
3. Omów z uczniami sposób udzielania odpowiedzi (karta odpowiedzi).
4. Zapewnij uczniom możliwość samodzielnej pracy.
5. Rozdaj uczniom zestawy zadań testowych i karty odpowiedzi, podaj czas przeznaczony na
udzielanie odpowiedzi.
6. Postaraj się stworzyć odpowiednią atmosferę podczas przeprowadzania pomiaru
dydaktycznego (rozładuj niepokój, zachęć do sprawdzenia swoich możliwości).
7. Kilka minut przed zakończeniem sprawdzianu przypomnij uczniom o zbliżającym się czasie
zakończenia udzielania odpowiedzi.
8. Zbierz karty odpowiedzi oraz zestawy zadań testowych.
9. Sprawdź wyniki i wpisz do arkusza zbiorczego.
10. Przeprowadź analizę uzyskanych wyników sprawdzianu i wybierz te zadania, które
sprawiły uczniom największe trudności.
11. Ustal przyczyny trudności uczniów w opanowaniu wiadomości i umiejętności.
12. Opracuj wnioski do dalszego postępowania, mającego na celu uniknięcie niepowodzeń
dydaktycznych – niskie wyniki przeprowadzonego sprawdzianu.
INSTRUKCJA DLA UCZNIA
1. Przeczytaj uważnie instrukcję.
2. Podpisz imieniem i nazwiskiem kartę odpowiedzi.
3. Zapoznaj się z zestawem zadań testowych.
4. Test zawiera 20 zadań wielokrotnego wyboru o różnym stopniu trudności. W każdym
zadaniu tylko jedna odpowiedź jest prawidłowa.
5. Udzielaj odpowiedzi tylko na załączonej karcie odpowiedzi, stawiając w odpowiedniej
rubryce znak X. W przypadku pomyłki należy błędną odpowiedź zaznaczyć kółkiem,
a następnie ponownie zakreślić odpowiedź prawidłową.
6. Pracuj samodzielnie, bo tylko wtedy będziesz miał satysfakcję z wykonanego zadania.
7. Kiedy udzielenie odpowiedzi będzie Ci sprawiało trudność, wtedy odłóż jego rozwiązanie
na później i wróć do niego, gdy zostanie Ci czas wolny.
8. Na rozwiązanie testu masz 45 min.
Powodzenia
Materiały dla ucznia:
– instrukcja,
– zestaw zadań testowych,
– karta odpowiedzi.

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
23
ZESTAW ZADAŃ TESTOWYCH
1. Gaz syntezowy używany do produkcji amoniaku musi być oczyszczony z:
a) związków siarki,
b) związków siarki, CO i CO
2
,
c) związków siarki i CO,
d) CO i CO
2
.
2. Skład procentowy gazu syntezowego używanego do produkcji amoniaku to:
a) 75% N
2
i 25% H
2
,
b) 50% N
2
i 50% H
2
,
c) 25% N
2
i 75% H
2
,
d) 65% N
2
i 35% H
2
.
3. Aby zwiększyć wydajność reakcji
N
2
+ 3H
2
2 NH
3
ΔH
0
= -92,4 kJ/mol
należy układ:
a) ochłodzić i zwiększyć ciśnienie,
b) ogrzać i zwiększyć ciśnienie,
c) ochłodzić i zmniejszyć ciśnienie,
d) ogrzać i zmniejszyć ciśnienie.
4. Korozja wodorowa polegająca na przenikaniu wodoru do sieci krystalicznej, tworzeniu
metanu i pękaniu metalu:
a) nasila się – tylko ze wzrostem temperatury,
b) nasila się – tylko z obniżeniem ciśnienia,
c) nasila się – ze wzrostem ciśnienia i temperatury
d) nie zależy od ciśnienia i temperatury.
5. Najlepszym kontaktem w syntezie amoniaku jest:
a) żelazo aktywowane dodatkiem Al
2
O
3
,
b) żelazo aktywowane tlenkami glinu i potasu,
c) stop platyny i rodu,
d) żelazo i platyna.
6. Do zatrucia kontaktu w syntezie amoniaku może dojść na skutek obecności:
a) siarki i węglowodorów w tym metanu,
b) siarki, metanu i wody,
c) węglowodorów z wyjątkiem metanu,
d) siarki, węglowodorów (z wyjątkiem metanu) i wody.
7. Na wydajność procesu utleniania amoniaku na katalizatorze platynowo-rodowym wpływa:
a) tylko temperatura siatki Pt–Rh,
b) tylko czas zetknięcia gazu z kontaktem,
c) tylko zawartość amoniaku w mieszaninie,
d) wszystkie wymienione parametry.
„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
24
8. Do wybuchu mieszaniny amoniaku z powietrzem nad wodnym roztworem amoniaku może
dojść, jeżeli zawartość amoniaku w temperaturze 30ºC w mieszaninie wynosi:
a) 11%,
b) 18%,
c) 28%,
d) 16%.
9. Która/które z substancji stanowią największy problem ekologiczny dla zakładów
wytwarzających kwas azotowy(V):
a) tlenki azotu,
b) amoniak,
c) kwas azotowy(V),
d) kwas siarkowy(VI).
10. Podczas syntezy amoniaku wg równania
N
2
+ 3H
2
2 NH
3
otrzymano 140 t amoniaku w ciągu doby. Ile azotu zużyto w procesie jeżeli wydajność
procesu wynosiła 98%:
a) 105 ton,
b) 107 ton,
c) 36 ton,
d) 143 tony.
11. W procesach technologicznych wytwórni kwasu azotowego(V) nie zachodzi reakcja:
a) 3NO
2
+ H
2
O 2HNO
3
+ NO,
b) NH
4
NO
3
→ NH
3
+ HNO
3
,
c) 2NO + O
2
2NO
2
,
d) 4NH
3
+ 5O
2
→ 4NO + 6H
2
O.
„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
25
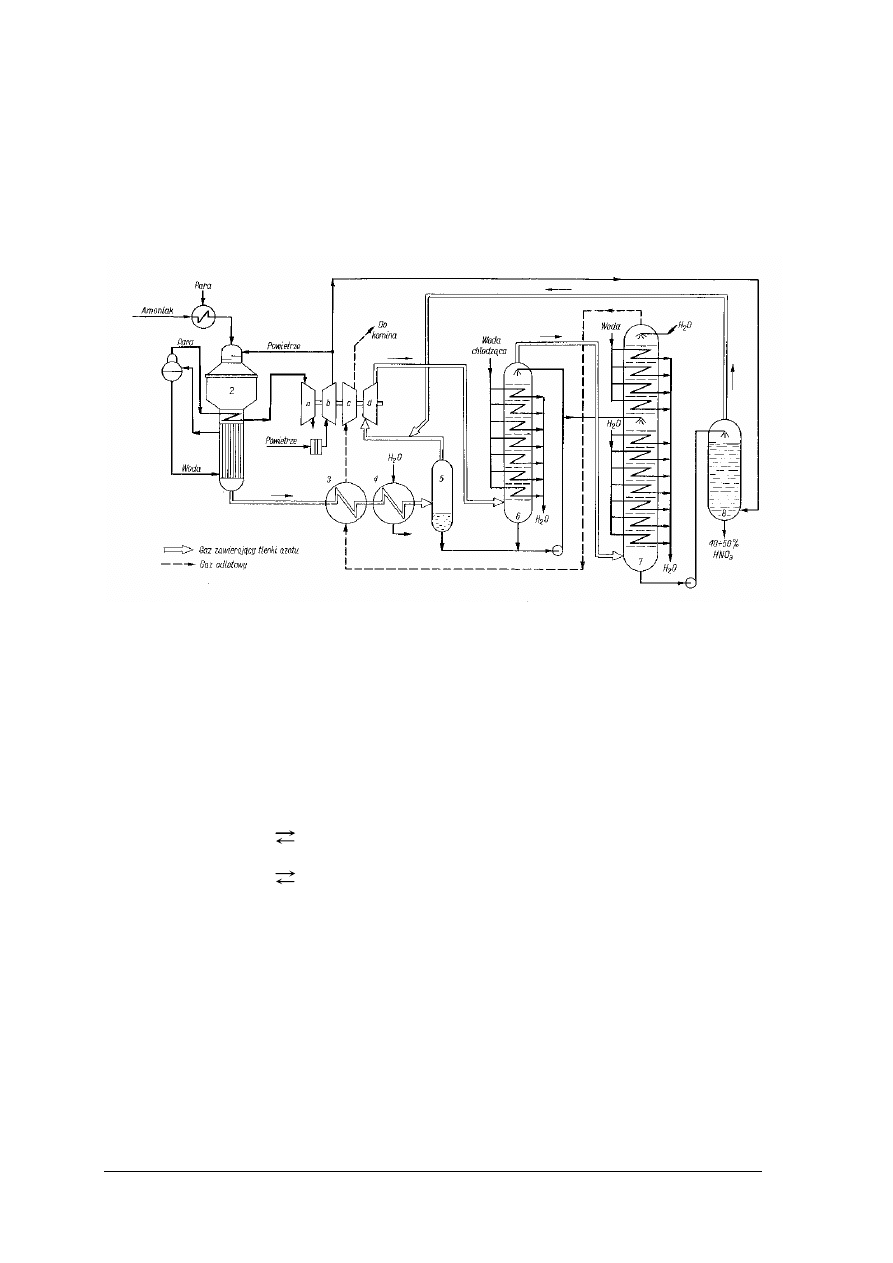
12. Zgodnie z poniższym schematem produkcja kwasu azotowego(V) przebiega
w następującej kolejności procesów jednostkowych:
a) utlenianie amoniaku, absorpcja NO
2
, utlenianie NO do NO
2
, chłodzenie,
b) utlenianie amoniaku, chłodzenie, utlenianie NO do NO
2
, absorpcja NO
2
,
c) chłodzenie, utlenianie amoniaku, utlenianie NO do NO
2
, absorpcja NO
2
,
d) utlenianie amoniaku, chłodzenie, absorpcja NO
2
, utlenianie NO do NO
2
.
Rys. 9. Schemat produkcji kwasu azotowego(V) [2]
1a–1d – sprężarki, 2 – reaktor, 3 – wymiennik ciepła, 4 – chłodnica wodna, 5 – oddzielacz,
6 – kolumna dotleniająca, 7 – kolumna absorpcyjna, 8 – kolumna bieląca
13. W celu zmniejszenia właściwości wybuchowych saletry w procesie produkcji dodaje się
do niej:
a) pył węglowy,
b) mocznik,
c) węglan wapnia,
d) sole miedzi.
14. Reakcją niepożądaną w procesie produkcji mocznika jest:
a) 2NH
2
−CO−NH
2
NH
2
−CO−NH−CO−NH
2
+ NH
3
,
b) 2NH
3
+ CO
2
→ NH
2
−CO−NH
2
+ H
2
O,
c) 2NH
3
+ CO
2
NH
2
−CO−ONH
4
,
d) NH
2
−CO−ONH
4
→ NH
2
−CO−NH
2
+ H
2
O.
15. Mocznika nie wykorzystuje się w produkcji:.
a) środków chwastobójczych,
b) melaminy,
c) dodatków do pasz,
d) superfosfatów.
„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
26
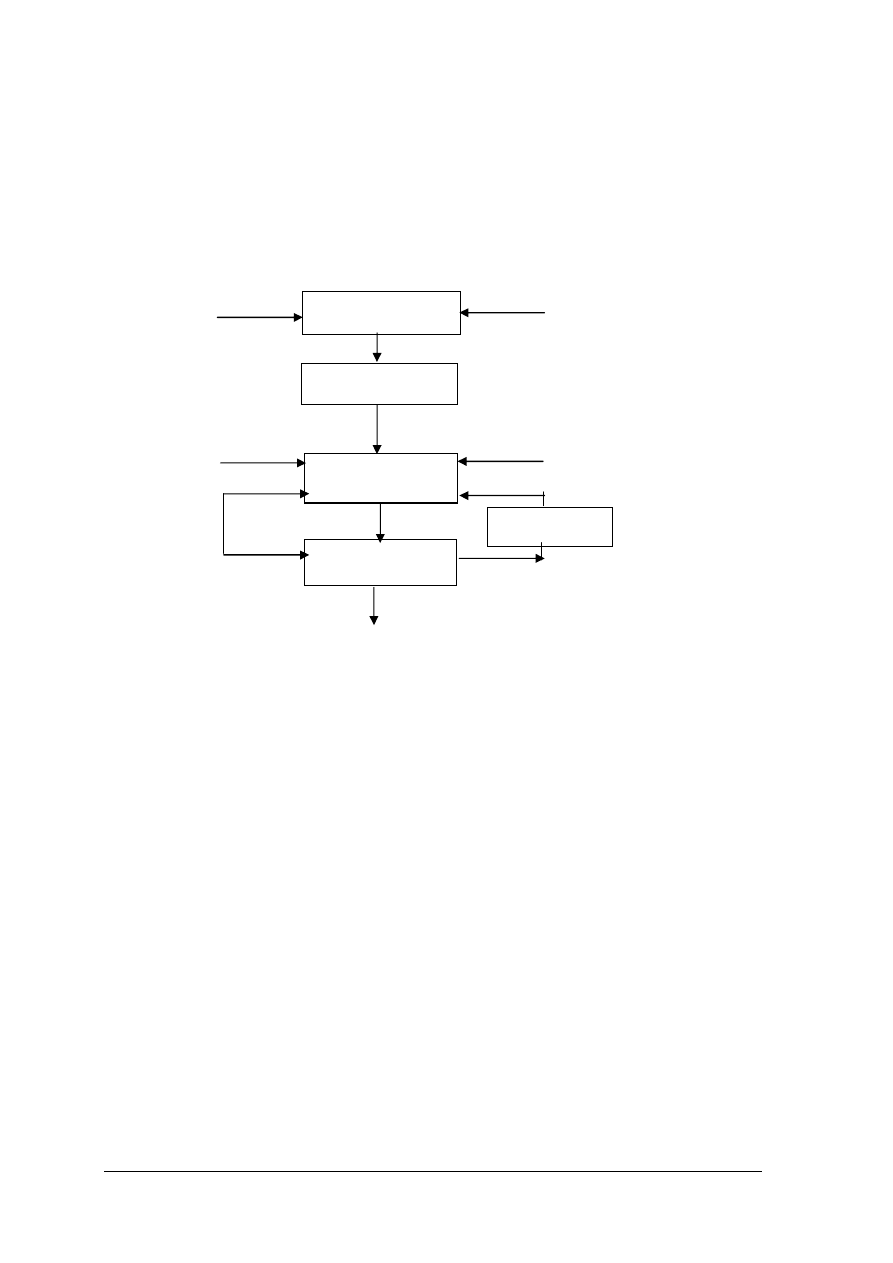
16. Zgodnie z poniższym schematem do granulacji mechanicznej saletry amonowej
wykorzystuje się:
a) zawrót i NH
3
,
b) surowce stałe i roztwór NH
3
,
c) surowce stałe i roztwór NH
4
NO
3
,
d) roztwór NH
4
NO
3
i HNO
3.
17. Do produkcji saletry amonowej jako nawozu używa się:
a) ciekłego NH
3
i gazowego CO
2
,
b) gazowego NH
3
i 96% HNO
3
,
c) ciekłego NH
3
i 56% HNO
3
,
d) gazowego NH
3
i 56% HNO
3
.
18. W miejscu produkcji i magazynowania saletry amonowej nie wolno pracować z otwartym
ogniem, ponieważ:
a) saletra amonowa jest utleniaczem i podtrzymuje palenie innych materiałów,
b) saletra amonowa jest łatwo palna,
c) ogień powoduje, że saletra amonowa zmniejsza wilgotność i zbryla się,
d) powoduje to wysychanie powietrza, a saletra amonowa powinna być przechowywana
w środowisku wilgotnym.
19. Wody odpadowe z produkcji saletry amonowej nie są w Polsce:
a) wykorzystywane jako ciecz absorpcyjna przy produkcji kwasu azotowego,
b) poddawane wymianie jonowej, a odzyskane w ten sposób związki azotu
wykorzystywane do produkcji saletry,
c) poddawane odwróconej osmozie, a odzyskane w ten sposób związki azotu
wykorzystywane do produkcji amoniaku,
d) wykorzystywane jako surowiec do produkcji nawozów płynnych głównie RSM.
granulowana saletra amonowa
neutralizacja
odparowanie
granulacja
mechaniczna
frakcjonowanie
kruszenie
NH
3
HNO
3
podziarno
nadziarno
(1)
(2)
„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
27
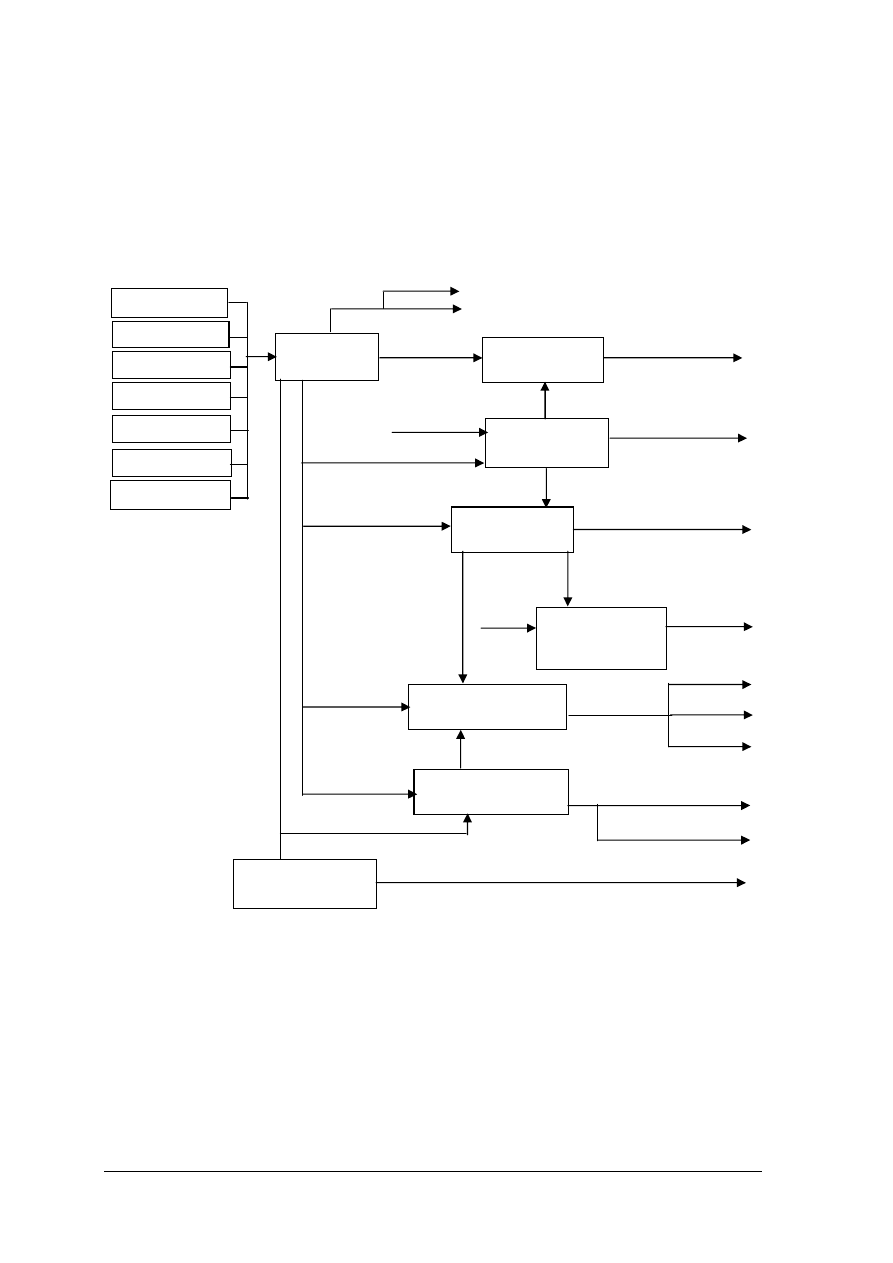
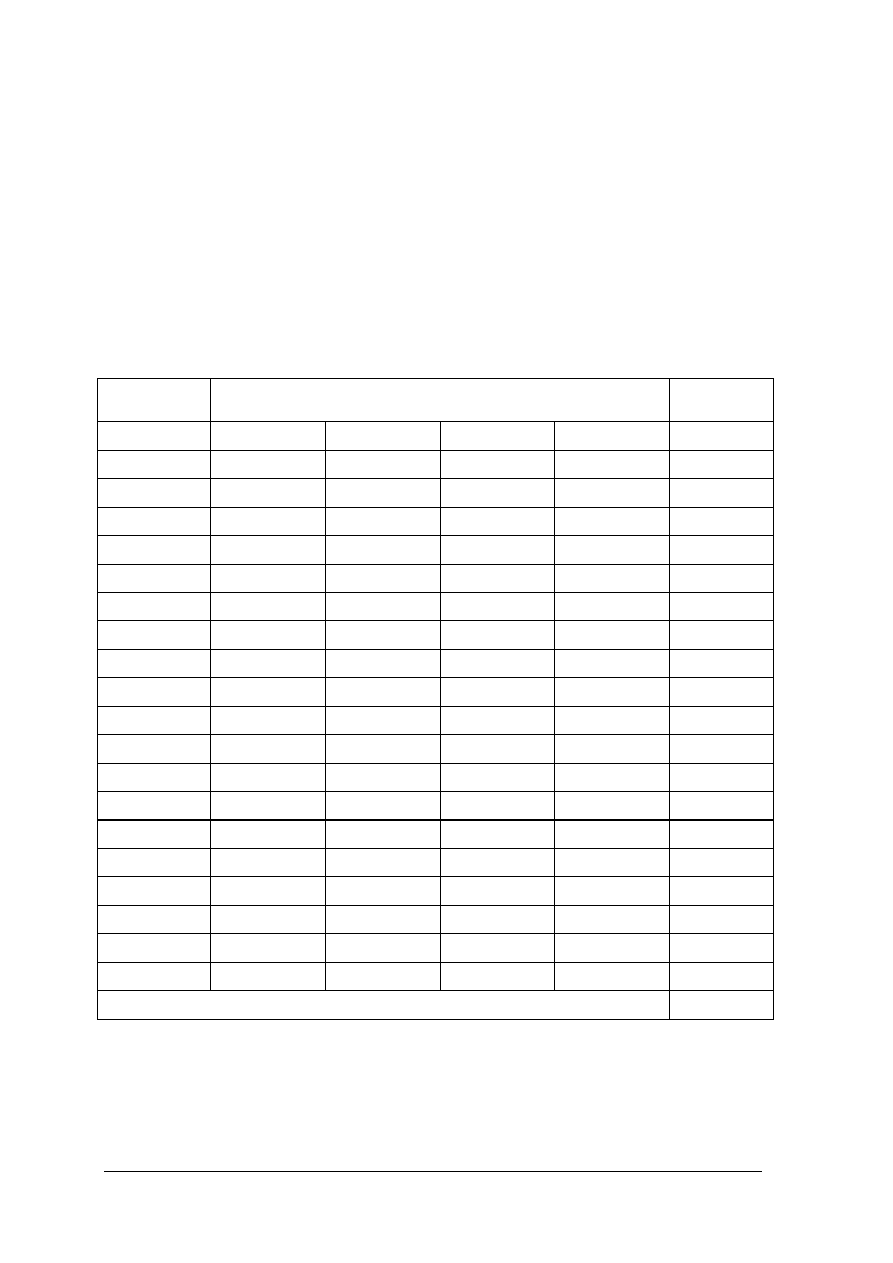
20. Zgodnie z poniższym schematem do produkcji roztworów azotowych jako nawozów
używa się:
a) HNO
3
, NH
3
, dolomit,
b) HNO
3
, mocznik, NH
3
,
c) NH
3
, mocznik, saletra amonowa,
d) NH
4
NO
3
, dolomit, amoniak.
biomasa
woda
powietrze
gaz ziemny
gaz rafineryjny
nafta
węgiel
wytwórnia
amoniaku
amoniak techniczny
amoniak nawozowy
NH
3
+ CO
2
wytwórnia
mocznika
wytwórnia roztworów
azotowych
wytwórnia
nitrofosfatów
nitrofosfaty
NP
wytwórnia kwasu
azotowego(V)
HNO
3
wytwórnia azotanu
amonowego z
wypełniaczem
wytwórnia saletry
amonowej
techniczny kwas
azotowy
powietrze
NH
3
HNO
3
saletra
amonowa
roztwór
NH
4
NO
3
dolomit
NH
3
saletrzak
roztwór
NH
4
NO
3
NH
3
RMA
RSM
RSA
roztwory
azotowe
techniczny mocznik
mocznik nawozowy
CO(HN
2
)
2
wytwórnia ciekłego
CO
2
CO
2
-
p
roduk
t
ubo
cz
ny
p
roduk
cji
am
on
ia
ku
CO
2
NH
3
techniczny CO
2
„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
28
KARTA ODPOWIEDZI
Imię i nazwisko..........................................................................................
Wytwarzanie amoniaku, kwasu azotowego(V) i nawozów azotowych
Zakreśl poprawną odpowiedź.
Nr
zadania
Odpowiedź
Punktacja
1
a
b
c
d
2
a
b
c
d
3
a
b
c
d
4
a
b
c
d
5
a
b
c
d
6
a
b
c
d
7
a
b
c
d
8
a
b
c
d
9
a
b
c
d
10
a
b
c
d
11
a
b
c
d
12
a
b
c
d
13
a
b
c
d
14
a
b
c
d
15
a
b
c
d
16
a
b
c
d
17
a
b
c
d
18
a
b
c
d
19
a
b
c
d
20
a
b
c
d
Razem

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
29
Zadanie praktyczne wysoko symulowane
Proponowany test sumujący jest przeznaczony do przeprowadzenia po zakończonym procesie
kształcenia w jednostce modułowej „Wytwarzanie amoniaku, kwasu azotowego(V) i nawozów
azotowych”. Test ma charakter próby pracy i pozwala na ocenę umiejętności uczniów w
zakresie, posługiwania się schematem aparatu, interpretowania wykresów fizykochemicznych i
wzorów matematycznych, dobierania parametrów procesu, obliczania wydajności,
scharakteryzowania wpływu różnych czynników na wydajność procesu technologicznego.
Test ma charakter sprawdzający, tzn. ukierunkowany jest na porównanie wyników
z założonymi w programie celami kształcenia.
Instrukcja dla nauczyciela
1. Czas trwania testu 60 minut.
2. Należy przygotować indywidualne stanowisko pracy dla każdego ucznia.
3. Zapewnić dostęp do literatury potrzebnej do wykonania zadania.
4. Omówić z uczniami przebieg testu praktycznego.
5. Podczas przeprowadzenia testu nauczyciel pełni rolę obserwatora.
Uczeń może maksymalnie otrzymać 21 punktów.
Test uczeń zaliczy, jeśli uzyska 9 punktów,
aby otrzymać ocenę dostateczną, powinien uzyskać 11–14 punktów,
na ocenę dobrą, powinien uzyskać 15–18 punktów,
na ocenę bardzo dobrą, powinien uzyskać 19–21 punktów wykonując wszystkie zadania.
Instrukcja dla ucznia
1. Przeczytaj uważnie instrukcję.
2. Możesz korzystać z dołączonego materiału do zadania (załącznik), tablic
matematycznych, kalkulatora.
3. Obliczając wydajność aparatu do syntezy amoniaku, przyjmij następujące dane
techniczne i ruchowe:
−
wysokość reaktora – 14 m,
−
średnica wewnętrzna reaktora – 850 mm,
−
zawartość inertów w gazach obiegowych – 7%,
−
wkraplanie amoniaku w temperaturze – 5ºC,
−
szybkość objętościowa gazu – 25000 h
-1
,
−
ciśnienie – 300 atm,
−
współczynnik wykorzystania wewnętrznej przestrzeni reaktora – 35%.
4. Zanim przystąpisz do wykonania zadania, zaplanuj pracę. Pomoże Ci w tym
KARTA PRACY.
5. Odpowiedzi wpisuj w wyznaczonych miejscach KARTY.
6. Pracuj samodzielnie.
7. Po zakończeniu zadania oddaj nauczycielowi KARTĘ PRACY.
8. Na wykonanie zadania masz 45 minut.
Powodzenia

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
30
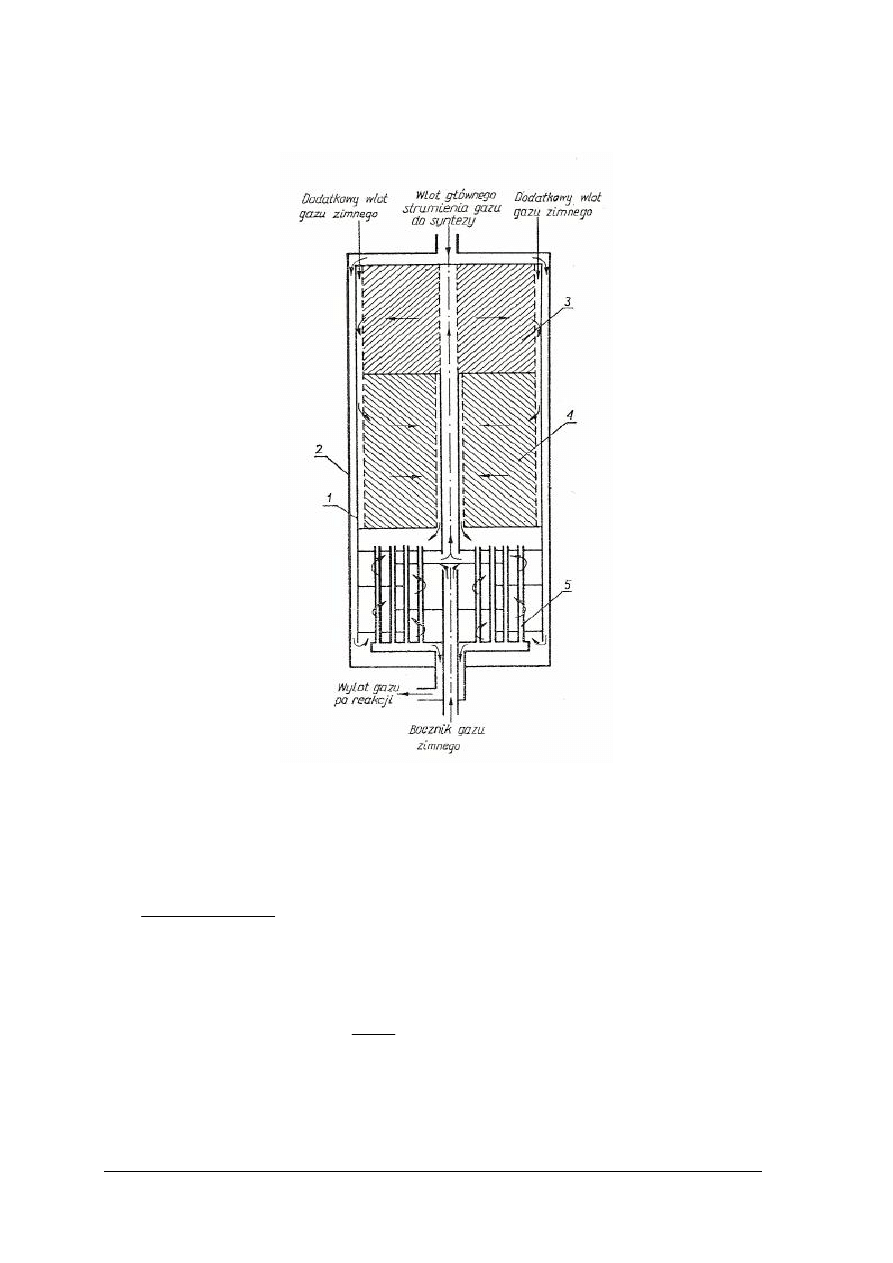
Treść zadania
„Scharakteryzuj budowę i pracę reaktora radialnego do syntezy amoniaku”
Działanie Twoje powinno przebiegać w trzech etapach:
ETAP I – faza przygotowawcza:
−
zapoznaj się z dołączoną dokumentacją do zadnia,
−
zapoznaj się ze schematem reaktora radialnego do syntezy amoniaku,
−
zinterpretuj wzór na obliczanie wydajności reaktora radialnego,
−
odczytaj potrzebne dane z wykresów do obliczenia wydajności reaktora.
ETAP II – faza realizacyjna:
−
opisz pracę reaktora radialnego do syntezy amoniaku,
−
scharakteryzuj budowę reaktora radialnego, pamiętając, że jest to aparat pracujący pod
zwiększonym ciśnieniem,
−
oblicz wydajność reaktora,
−
oceń, jak na wydajność aparatu wpłynie wzrost objętości masy kontaktowej oraz zużycie
katalizatora.
ETAP III – faza oceniająca:
−
zinterpretuj uzyskane wyniki.
„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
31
Załącznik
Schemat reaktora radialnego do syntezy amoniaku [4]
1 – kosz z kontaktem, 2 – zewnętrzny płaszcz ciśnieniowy, 4 – dolna warstwa kontaktu,
5 – rura wymiennika ciepła
Wydajność aparatu do syntezy amoniaku oblicza się ze wzoru: [4]
G =
(
1
1
2
100
771
,
0
)
C
C
C
v
V
+
−
⋅
gdzie:
G – wydajność aparatu, kg/h,
V – szybkość objętościowa gazu,
h
m
m
⋅
3
3
,
v – objętość masy kontaktowej, m
3
,
C
1
– zawartość amoniaku w mieszaninie azotowo-wodorowej przy wejściu do aparatu, %,
C
2
– zawartość amoniaku przy wyjściu z aparatu, %,
0,771 – gęstość amoniaku, kg/m
3
.
„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
32
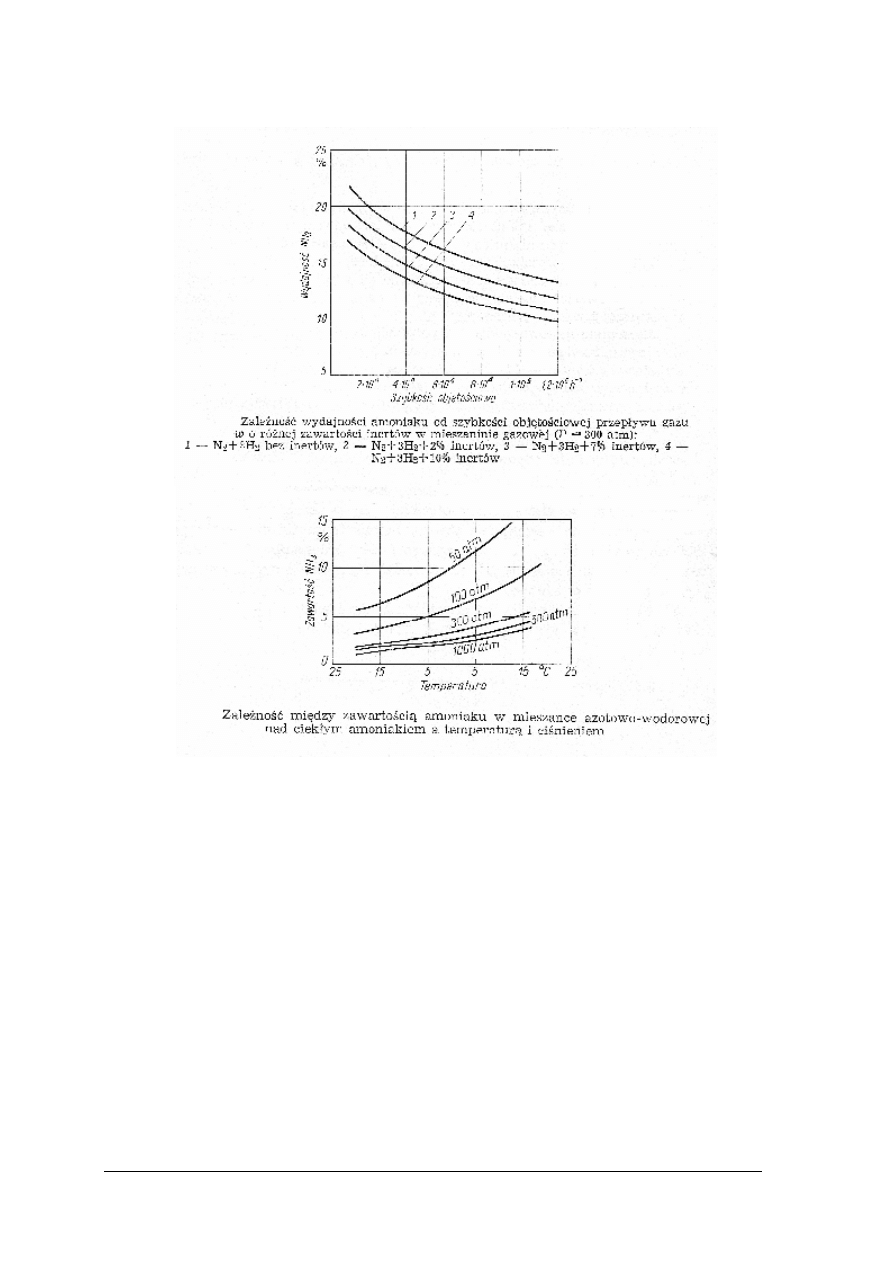
Dane do obliczeń odczytasz z wykresów: [4]
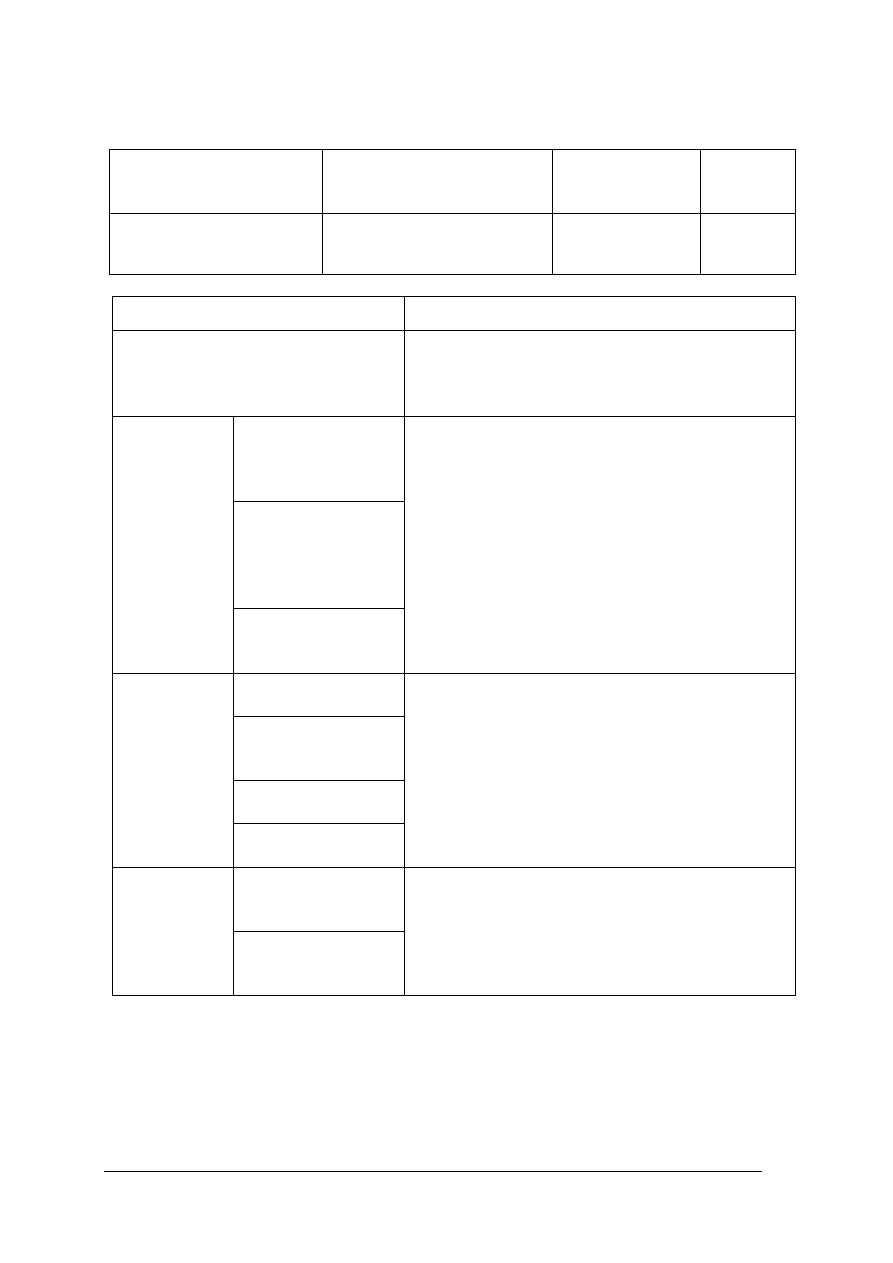
„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
33
Karta pracy
Nazwa i adres szkoły
Nazwisko i imię ucznia
Data
Uzyskana
suma
punktów
Zadanie
Odpowiedź
Opisz pracę reaktora radialnego
do syntezy amoniaku
Cechy materiału,
z jakiego jest
wykonany (trzy cechy
Kształt
Budowa ścianek
aparatu
Sposób łączenia
elementów
Opisz budowę
aparatu
do syntezy
amoniaku
Zasady bhp
podczas obsługi
aparatu
Ustalenie wzoru na
objętość walca
Obliczenie objętości
masy kontaktowej
w reaktorze
Odczytanie wartości
C
1
, C
2
, z wykresów
Wykonaj
obliczenia
dotyczące
wydajności
reaktora
Obliczenie
wydajności reaktora
Zmniejszenie
aktywności
katalizatora
Wnioski
dotyczące
aktywności
reaktora
Zwiększenie masy
kontaktowej
„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
34
Proponowana ocena zadania
Lp.
Czynności
Maksymalna
liczba punktów
możliwa do
uzyskania
Uzyskana
liczba
punktów
1
Opisanie pracy reaktora radialnego
do syntezy amoniaku na podstawie schematu
5
podanie trzech cech
materiału, z jakiego jest
wykonany
3
określenie kształtu
określenie sposobu
wykończenia ścianek aparatu
podanie sposobu łączenia
elementów
3
2
Opisanie
budowy aparatu
do syntezy
amoniaku
podanie zasad bhp
w przypadku usuwania
zauważonych nieszczelności
2
ustalenie wzoru na objętość
walca
1
obliczenie objętości masy
kontaktowej w reaktorze
1
odczytanie wartości C
1
, C
2
,
z wykresów
2
3
Obliczenie
dotyczące
wydajności
reaktora
obliczenie wydajności
reaktora
2
określenie, jak wpłynie
zmniejszenie aktywności
katalizatora na aktywność
reaktora
1
4
Ocena
dotyczące
aktywności
reaktora
określenie, jak wpłynie na
aktywność reaktora
zwiększenie masy
kontaktowej
1

„Projekt współfinansowany ze środków Europejskiego Funduszu Społecznego”
35
7.
LITERATURA
1. Bortel E., Koneczny H.: Zarys technologii chemicznej. PWN, Warszawa 1992
2. Molenda J.: Chemia techniczna. WNT, Warszawa 1985
3. Molenda J.: Technologia chemiczna. WSiP, Warszawa 1996
4. Muchlenow I., Kuzniecow D. i inni: Ogólna technologia chemiczna. WNT, Warszawa
1974
5. Najlepsze Dostępne Techniki (BAT). Wytyczne dla Branży Chemicznej w Polsce.
Przemysł Wielkotonażowych Chemikaliów Nieorganicznych, Amoniaku, Kwasów
i Nawozów Sztucznych. Wersja II. Ministerstwo Środowiska, Warszawa 2005
6. www.hse.gov.uk/pubns/indg230.pdf- The Health and Safety Executive UK
Wyszukiwarka
Podobne podstrony:
35 Wytwarzanie amoniaku, kwasu azotowego
25 Wytwarzanie metanolu i kwasu Nieznany (2)
11 Wytwarzanie specjalnych wyro Nieznany (2)
12 Wytwarzanie zakladek, podnos Nieznany (3)
35 Wykonywanie dokumentacji kon Nieznany
16 Wytwarzanie podstawowych pol Nieznany (2)
Bartoszek 35 44 id 80431 Nieznany
21 Wytwarzanie odziezy miarowej Nieznany (2)
28 Wytwarzanie styrenu z etylob Nieznany
(wytwarzanie materialow nanokry Nieznany (2)
36 Wytwarzanie sody kalcynowane Nieznany (2)
11 Wytwarzanie pieczywa cukiern Nieznany (2)
32 Wytwarzanie siarki odzyskiwa Nieznany (2)
35 W sprawie metodologii oblicz Nieznany (2)
10 Wytwarzanie wyrobow cukierni Nieznany (2)
23 Wytwarzanie olefin i weglowo Nieznany (2)
BCH Wytwarzanie energii w komor Nieznany (2)
17 Wytwarzanie podstawowych pol Nieznany (2)
więcej podobnych podstron