
Gazownictwo
2. Równania stanu gazów
Równanie Clapeyrona, obliczanie p,V,m,n,Ri,T,
wsp. pseudościśliwości, wyznaczenie w oparciu o wykres
Standinga-Katza, równanie Van der Walsa, Redlicha -
Kwonga

Gazownictwo
Gaz doskonały:
1. objętość cząsteczek gazu jest zaniedbywalnie mała w porównaniu z objętością
zbiornika i odległościami pomiędzy cząsteczkami,
2. pomiędzy cząsteczkami lub cząsteczkami i ścianami zbiornika nie występują siły
wzajemnego oddziaływania (przyciągania lub odpychania). Jedną z konsekwencji
tego założenia jest nieuwzględnienie przez równanie stanu gazu doskonałego
zjawiska przemian fazowych.

Gazownictwo
Równanie stanu gazu doskonałego Clapeyrona [połączenie praw Boyle’a-Mariotte’a
(T=idem), Gay-Lusaca (p=idem), Charlesa (V=idem)]
pV=n*R*T
pV=m*R
i
*T pυ = R
i
*T p/ρ = R
i
*T pV
m
= R*T
p – ciśnienie [Pa]
V – objętość [m
3
]
n – ilość moli [mol]
R – uniwersalna stała gazowa 8,314 [kJ/kmol*K]
M - masa molowa [kg/kmol]
R
i
= R/M [J/kg*K]
m – masa [kg]
T – temperatura [K]
υ – objętość właściwa V/m = 1/ ρ [m
3
/kg]
Vm – objętość molowa [m
3
/mol]

Gazownictwo
Zadanie
Oblicz ile waży 1m3 powietrza (gas doskonały) w warunkach normalnych [gęstość
powietrza]

Gazownictwo
Rozwiązanie

Gazownictwo
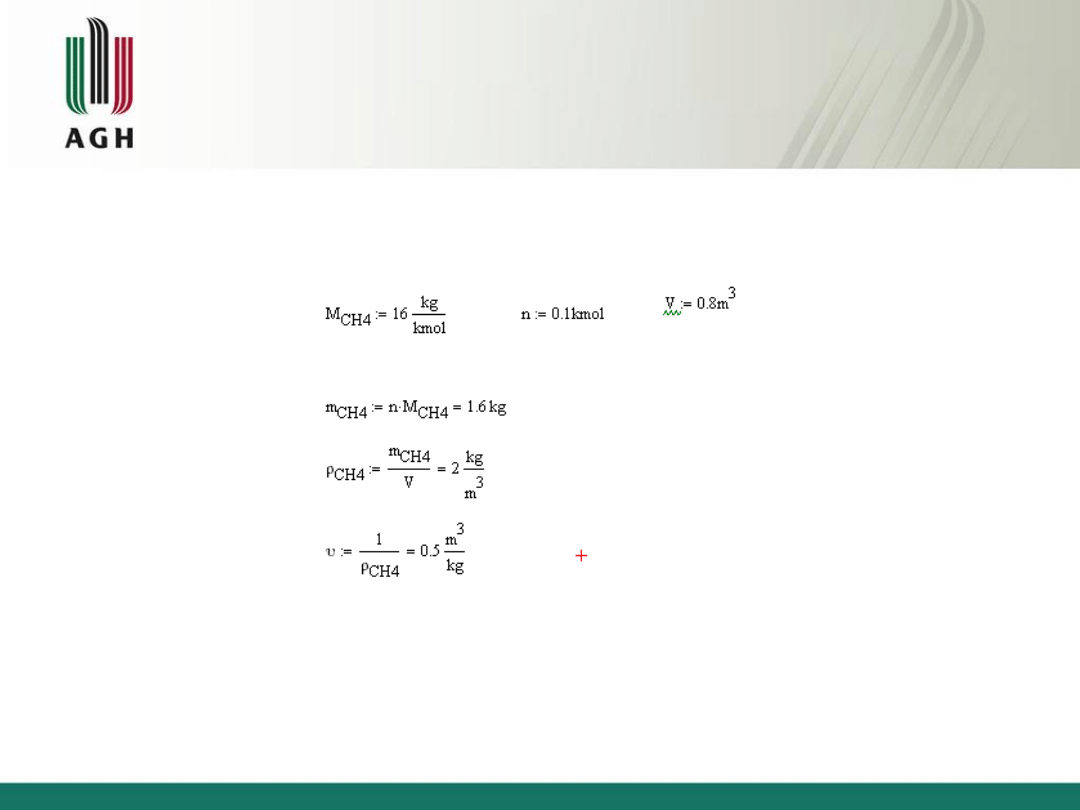
Zadanie
W zbiorniku o objętości V = 0.8[m3 ] znajduje się 0.1[kmol ] metanu. Ile wynosi
objętość właściwa oraz gęstość metanu w zbiorniku?
Gazownictwo
Rozwiązanie

Gazownictwo
Zadanie
Pusty zbiornik o objętości V
zb
=40[m3] został napełniony metanem.
Ciśnienie po jego napełnieniu wynosi p
zb
=7,75[bar], a temperatura
t
zb
= 37[
o
C]. Rurociąg doprowadzający gaz ma średnicę d = 50 [mm].
Parametry czynnika zmierzone przed zaworem umieszczonym na
rurociągu wynosiły:
T
r
= 280 K
p
r
= 10.75 [bar]
u (średnia prędkość dopływającego gazu) = 30 [m/s]
Obliczyć ilość doprowadzonego gazu oraz czas napełniania

Gazownictwo
Rozwiązanie

Gazownictwo
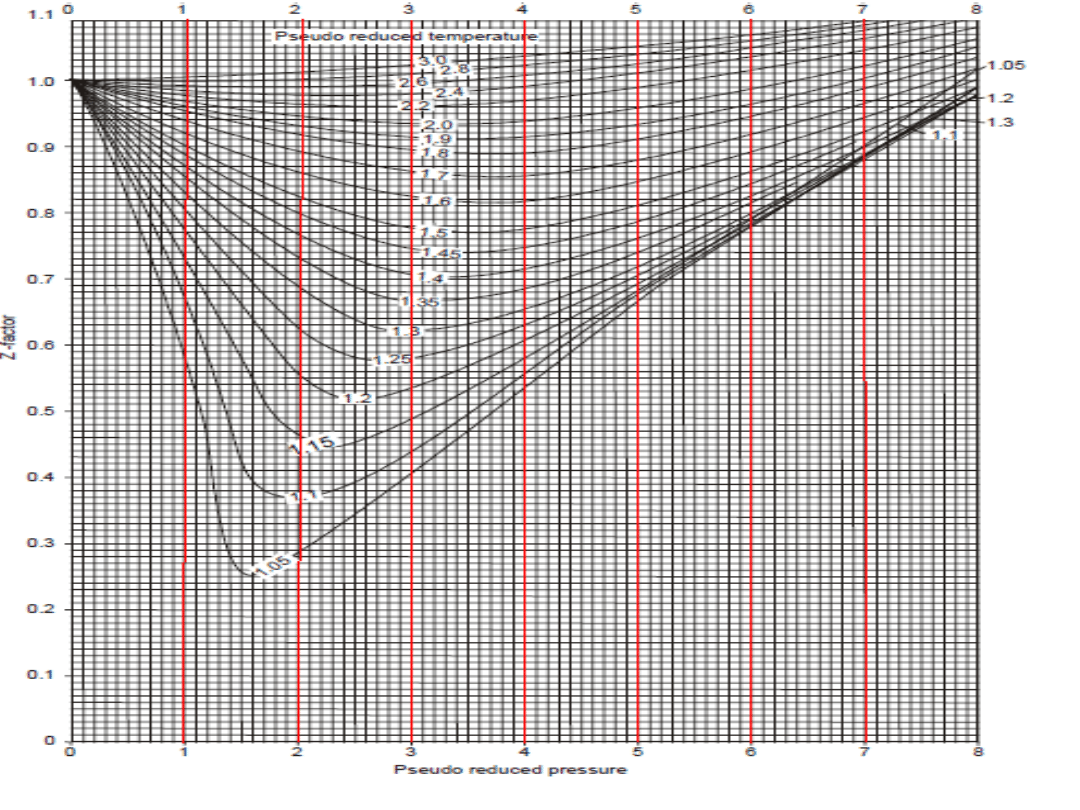
Współczynnik pseudościśliwości z = f(p,T) wyznaczany metodą S-K
Dla gazu jednoskładnikowego
p
r
= p/p
cr
T
r
= T/T
cr
Mając p
r
oraz T
r
z wykresu S-K odczytujemy wartość wsp. z
Dla gazów wieloskładnikowych parametry pseudo
p
pr
= p/Σ(x
i
*p
cri
)
T
pr
= T/Σ(x
i
*T
cri
)
p
pcr
= Σ(x
i
*p
cri
)
T
pcr
= Σ(x
i
*T
cri
)
Gazownictwo

Gazownictwo
Równanie stanu gazu rzeczywistego
Równanie Van der Waalsa
b – wsp. uwzględniający objętość molekuł [m
3
/mol]
a – wsp. uwzględniający wzajemne oddziaływania między molekułami [N*m
4
/mol
2
]
p – ciśnienie układu [Pa]
R- stała uniwersalna 8,314 [J/mol*K]
V – objętość molowa [m3/mol]

Gazownictwo
Równanie stanu gazu rzeczywistego
Równanie Van der Waalsa (Magdziarz => wyprowadzenie tych współczynników)

Gazownictwo
Równanie stanu gazu rzeczywistego
Równanie Redlicha Kwonga

Gazownictwo
Równanie stanu gazu rzeczywistego
Równanie Redlicha Kwonga
b – wsp. uwzględniający objętość molekuł [m
3
/mol]
a – wsp. uwzględniający wzajemne oddziaływania między molekułami [N*m
4
*K
0.5
/mol
2
]
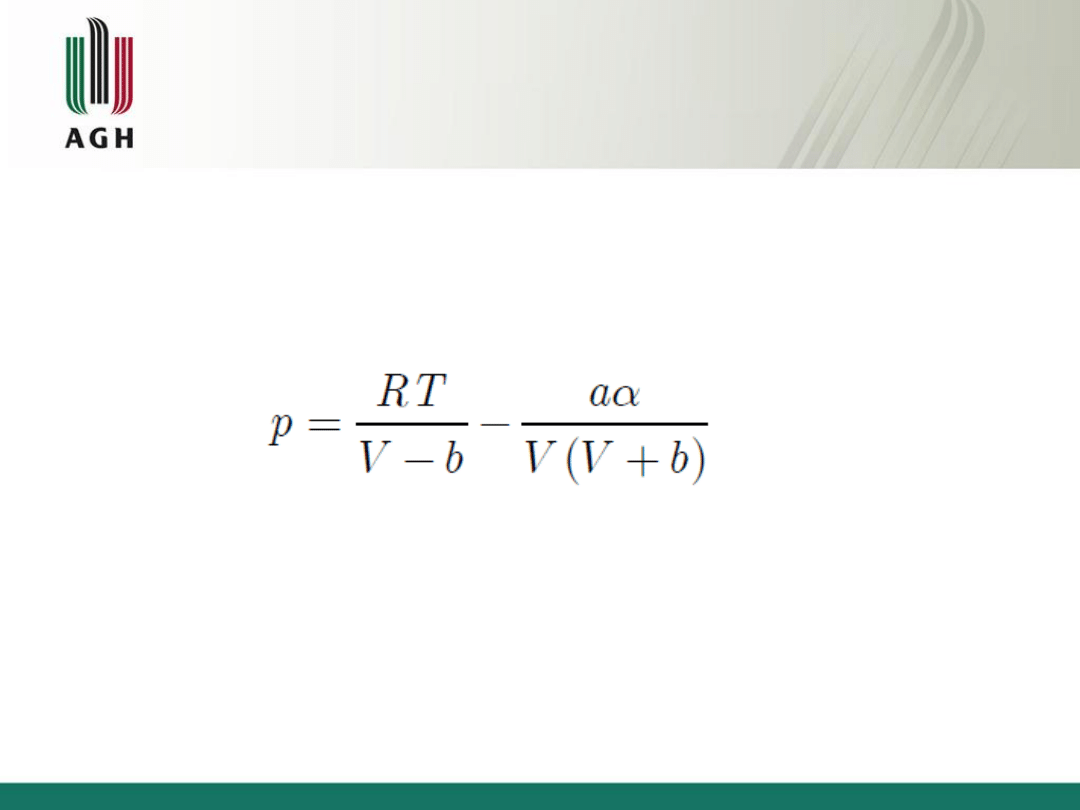
Gazownictwo
Równanie stanu gazu rzeczywistego
Równanie Soave - Redlicha Kwonga

Gazownictwo
Równanie stanu gazu rzeczywistego
Równanie Soave - Redlicha Kwonga

Gazownictwo
Równanie stanu gazu rzeczywistego
Równanie Soave - Redlicha Kwonga

Gazownictwo
Zadanie
Gaz o następującym składzie, w temperaturze 110
o
C, ma gęstość 18
[kg/m3]. Pod jakim ciśnieniem znajduje się ten gaz? Porównaj wyniki
otrzymane w oparciu o:
-Równanie stanu gazu doskonałego
-Równanie VdW
-Równanie R-K
-Równanie S-R-K

Gazownictwo
Rozwiązanie

Gazownictwo
Rozwiązanie

Gazownictwo
Rozwiązanie

Gazownictwo
Rozwiązanie
Wyszukiwarka
Podobne podstrony:
rownanie stanu
9 Rownania rozniczkowe id 4845 Nieznany (2)
Termiczne równanie stanu Przemiana termodynamiczna
Okreslanie stanu i zasobow srod Nieznany
POPRAWA STANU SRODOWISKA W POLS Nieznany
Kontrola stanu sanitarno higien Nieznany
24 Ocena stanu technicznego na Nieznany
Badanie stanu naprezen w cienko Nieznany (2)
równanie stanu gazu, roztwory
Sygn&Sys sem3 C2-Rownanie stanu, Studia, Semestr 1, Sygnały i Systemy, Sprawozdania
Równania stanu, Politechnika Łódzka Elektrotechnika, magisterskie, 1 sem
Referaty, Stała gazowa R, Równanie stanu gazów doskonałych ( równanie Clapeyrona )
Równanie Clapeyrona to równanie stanu opisujące związek pomiędzy temperaturą
Ocena Stanu zdrowia i Badania F Nieznany
rownanie stanu
9 Rownania rozniczkowe id 4845 Nieznany (2)
zadania rownania stanu 2
rownania stanu gazu rzeczywistego
więcej podobnych podstron