
LABORATORIUM METROLOGII
ANALIZA SKŁADU GAZU ZA POMOCĄ
CHROMATOGRAFU
Cel ćwiczenia: zapoznanie z metodyką wyznaczenia składu gazu za pomocą
chromatografu
1

WPROWADZENIE
Chromatografia gazowa to analityczna technika chromatograficzna, w której fazą nośną jest
gaz (najczęściej hel, coraz rzadziej wodór). Technika ta umożliwia procentowe ustalenie
składu mieszanin związków chemicznych, w których występuje ich nawet kilkaset. nie
umożliwia natomiast bezpośredniej identyfikacji struktury chemicznej związków, za
wyjątkiem aparatów z detektorem masowym.
Chromatografia gazowa jest najczęściej stosowaną metodą do szybkiej analizy złożonych
mieszanin związków chemicznych oraz oceny czystości tych związków, zarówno w
przemyśle jak i w rozmaitych laboratoriach. Chromatografię gazową stosuje się m.in. w:
•
przemyśle petrochemicznym - np. do oceny składu chemicznego produkowanej benzyny
•
ochronie środowiska - do oceny stopnia zanieczyszczenia, gleby, powietrza i wody.
•
kryminalistyce - np. do analizy źródła pochodzenia narkotyków na podstawie składu
zawartych w nich zanieczyszczeń
•
kontroli antydopingowej - gdzie aparaty GC-MS (Gas chromatography - mass
spectrometry) stanowią podstawową metodę wykrywania niedozwolonych substancji w
krwi, pocie, moczu i ekstrakcie z włosów sportowców.
Zasada działania. Metoda ta jest oparta na rozdzielaniu mieszanin na długich i cienkich
kolumnach z odpowiednim wypełnieniem stałym lub żelowym, a następnie detekcji stężenia
kolejno wychodzących związków na wylocie kolumny. Mechanizm rozdziału oparty jest na
występowaniu oddziaływań międzycząsteczkowych między związkami rozdzielanych
mieszanin i wypełnieniem kolumn. Oddziaływania te hamują przepływ związków
chemicznych przez kolumnę. Czym są one silniejsze, tym czas przejścia związku
chemicznego przez kolumnę jest dłuższy. Czas przejścia danego związku chemicznego przez
całą kolumnę jest nazywany jego retencją. Przy odpowiednio długiej i cienkiej kolumnie
czasy retencji związków są na tyle różne, że wychodzą one z kolumny osobno, przy czym
cała objętość związku wychodzi w stosunkowo krótkim czasie.
Próbka analizowanej mieszaniny jest wstrzykiwana do tzw. odparowywacza, gdzie panuje na
tyle wysoka temperatura, aby wszystkie jej składniki przeszły w stan gazowy. Następnie
próbka jest porywana przez gaz nośny i kierowana na kolumnę. Na końcu kolumny znajduje
się detektor, który mierzy stężenie związków w gazie nośnym, które wychodzą z kolumny.
Próbki analizowane metodą chromatografii gazowej muszą być lotne oraz nie ulegać
rozpadowi w podwyższonej temperaturze. Najczęściej są to rozmaite mieszaniny gazów i
roztwory zawierająca lotne (zdolne do parowania) związki chemiczne. Zaletą chromatografii
gazowej jest możliwość użycia bardzo niewielkiej próbki analizowanej substancji (od nawet
0,01 µl do maksymalnie 100 µl).
2

KONSTRUKCJA CHROMATOGRAFU GAZOWEGO
Chromatograf gazowy składa się ogólnie z następujących podstawowych elementów:
1. Układ nastrzykowy
2. Termostatowany piec
3. Kolumna chromatograficzna
4. Detektor
5. Rejestrator
Układ nastrzykowy. Tradycyjny układ nastrzykowy składa się zwykle z membrany, którą
nakłuwa się specjalną strzykawką chromatograficzną oraz odparowywacza, w którym
następuje odparowanie wszystkich składników analizowanej próbki. Odparowywacz to krótka
(5-10 cm) rurka metalowa lub szklana otoczona spiralą grzejną, która umożliwia rozgrzanie
rurki do ponad 200°C. W niektórych aparatach odparowywacz pracuje w stale tej samej
temperaturze, zaś w innych istnieje możliwość szerokiego regulowania jego temperatury.
Nastrzyki wykonuje się ręcznie lub automatycznie. Ręczny nastrzyk można wykonać przy
pomocy specjalnej strzykawki. Automatyczne nastrzyki wykonuje się przy pomocy
autosamplera lub też autosamplera typu headspace.
Pierwszy typ autosamplera to sampler w którym wstawia się fiolki w odpowiednich miejscach
a sprzęt automatycznie pobiera do strzykawki odpowiednią objętość analizowanej próbki. W
przypadku autosamplera headspace do analizy pobierana jest próbka gazu znad powierzchni
analizowanej substancji. W przypadku tego rodzaju autosamplera aparaty są często
pozbawione odparowywacza, gdyż nastrzykiwana próbka jest już od razu w formie gazowej.
Najważniejszą częścią układu nastrzykowgo jest układ dozownika do którego trafia próbka po
pobraniu jej przez autosampler lub strzykawkę. Wyróżniamy takie oto dozowniki: dozownik
typu split i dozownik on-column. W dozowniku typu split próbka pobrana do nastrzyku jest
dzielona poprzez dzielenie strumienia gazu trafiającego na kolumnę. Dozownik on-column to
dozownik, w którym cała próbka trafia od razu na kolumnę. W przypadku kolumn
kapilarnych stosuje się najczęściej dozowniki typu split.
Piec. Piec w chromatografie gazowym to szczelny, odizolowany od otoczenia i
wysokowydajny grzejnik z bardzo dokładną kontrolą temperatury. Wewnątrz pieca
umieszczona jest zwinięta w pętlę kolumna. Piece, aby zapewnić możliwość szybkiej zmiany
temperatury w czasie, posiadają zwykle wymuszony obieg powietrza. W większości
współczesnych chromatografów istnieje możliwość liniowej zmiany temperatury w czasie
pomiaru, co pozwala na wykonywanie analiz w tzw. gradiencie, co zwykle ją przyspiesza.
Czasami jednak analizy wykonuje się w tzw. izotermie czyli stałej, ściśle określonej
temperaturze.
Kolumna. Kolumny chromatograficzne występują w trzech rodzajach:
•
Tradycyjne kolumny z wypełnieniem stałym - są to kolumny o długości 1-5 m i średnicy
wewnętrznej ok. 2-3 mm, wykonywane ze specjalnych stopów metali kolorowych.
Wypełnia się je substancjami porowatymi takimi jak mika, pokruszona cegła, rozmaite
kserożele. Rozdział substancji analizowanych odbywa się w nich na granicy gaz-ciało
stałe.
3

•
Tradycyjne kolumny z wypełnieniem stało-ciekłym - są to kolumny o podobnej długości i
średnicy jak kolumny do wypełnienia stałego. Wypełnia się je jednak specjalnymi
porowatymi kserożelami (zwykle silikażelami), które przed napełnieniem nasącza się
roztworami polimerów lub innych nielotnych substancji ciekłych o wysokiej lepkości.
Rozdział substancji analizowanych odbywa się w nich na granicy gaz-ciecz.
•
Kolumny kapilarne - są to kolumny o długości nawet do 20-30 m i średnicy wewnętrznej
rzędu 0,1 mm i mniej. Są one wykonywane ze specjalnych gatunków szkła i z wyglądu
przypominają światłowody. Wypełnia się je roztworami polimerów lub innych nielotnych
substancji ciekłych o wysokiej lepkości. Roztwory te po odparowaniu pozostawiają na
ściankach kolumny cienki film polimeru, który w warunkach analizy jest bardzo lepką
cieczą. Rozdział substancji analizowanych odbywa się w nich na granicy gaz-ciecz.
Najczęściej stosowanymi polimerami w tego rodzaju kolumnach są polisiloksany.
Detektor. Detektor w chromatografie gazowym mierzy stężenie wypływających związków w
eluencie. Idealny detektor powinien być wrażliwy tylko na samo stężenie niezależnie od
struktury chemicznej analizowanego związku. W praktyce jednak detektory mają różną
czułość na różne związki chemiczne, co wymaga ich kalibrowania i ustalania tzw.
współczynników odpowiedzi dla każdego związku chemicznego osobno o ile chce się
mierzyć dokładny skład procentowy związków chemicznych w analizowanej próbce.
Rodzaje detektorów:
•
Katarometr - w którym pomiar stężenia zasadza się na zmianach przewodnictwa
elektrycznego ze zmianą stężenia "obcego związku" chemicznego w gazie nośnym.
•
Detektor płomieniowo-jonizacyjny - który jest specyficznym rodzajem spektrometru
płomieniowo-jonizacyjnego
Jest to jeden z najczęściej stosowanych detektorów w chromatografii gazowej. Jego działanie
polega na jonizacji (rozkład na jony) cząsteczek w płonieniu oraz rejestracji zmian potencjału.
Podstawowym elementem tego detektora jest płomień (najczęściej wodorowo - powietrzny,
wodorowo - tlenowy), płomień otacza elektroda zbiorcza. Podczas pracy, gdy przez detektor
przepływa san gaz nośny (ulegający jonizacji) ustala się stały potencjał między płomieniem, a
elektrodą. W momencie gdy do detektora dotrze oznaczana substancja, także zostanie
zjonizowany w wyniku czego mierzony potencjał zmieni się (wzrośnie) co zostanie
zarejestrowane jako sygnał pomiarowy.
•
Detektor masowy - który jest z kolei specyficznym rodzajem spektrometru masowego.
Tego rodzaju detektor nie pozwala na dokładnie mierzenie stężeń związków w
mieszaninie, ale za to umożliwia jednoznaczą identyfikację struktury chemicznej tych
związków. Aparaty z detektorem masowym są często nazywane GC-MS (Gas
chromatography - mass spectrometry).
•
Detektor płomieniowo fotometryczny - wykorzystujący zjawisko chemiluminescencji.
•
Detektor wychwytu elektronów - którego działanie polega na gwałtownym spadku
natężenia prądu płynącego w komorze jonizacyjnej po wproeadzeniu do niej substancji o
dużym powinowactwie elektronowym.
•
Detektor termojonowy - będący modyfikacją detektora płomieniowo-jonizacyjnego.
Rejestrator.
Niegdyś jako rejestratory stosowano analogowe urządzenia pisakowe, czasami
zaopatrzone w integrator, które po prostu "rysowały" zmiany napięcia elektrycznego
generowanego przez detektor. Wykresy te nazywa się tradycyjnie chromatogramami.
4
Chromatogramy przyjmują zwykle kształt serii ostrych pików, których wysokość odpowiada
stężeniu wychodzącego z kolumny związku chemicznego, a pole pod pikiem można
przeliczyć na całkowite stężenie danego związku chemicznego w całej analizowanej próbce.
Współcześnie jako rejestratory stosuje się komputery, zaopatrzone w odpowiednią kartę i
oprogramowanie umożliwiające zarówno sterowanie parametrami pracy całego aparatu jak i
automatyczne gromadzenie oraz analizowanie chromatogramów. Najczęściej, komputer, karta
i oprogramowanie są dostarczane przez producenta aparatu, choć możliwy jest też zakup
oprogramowania i kart od niezależnych producentów.
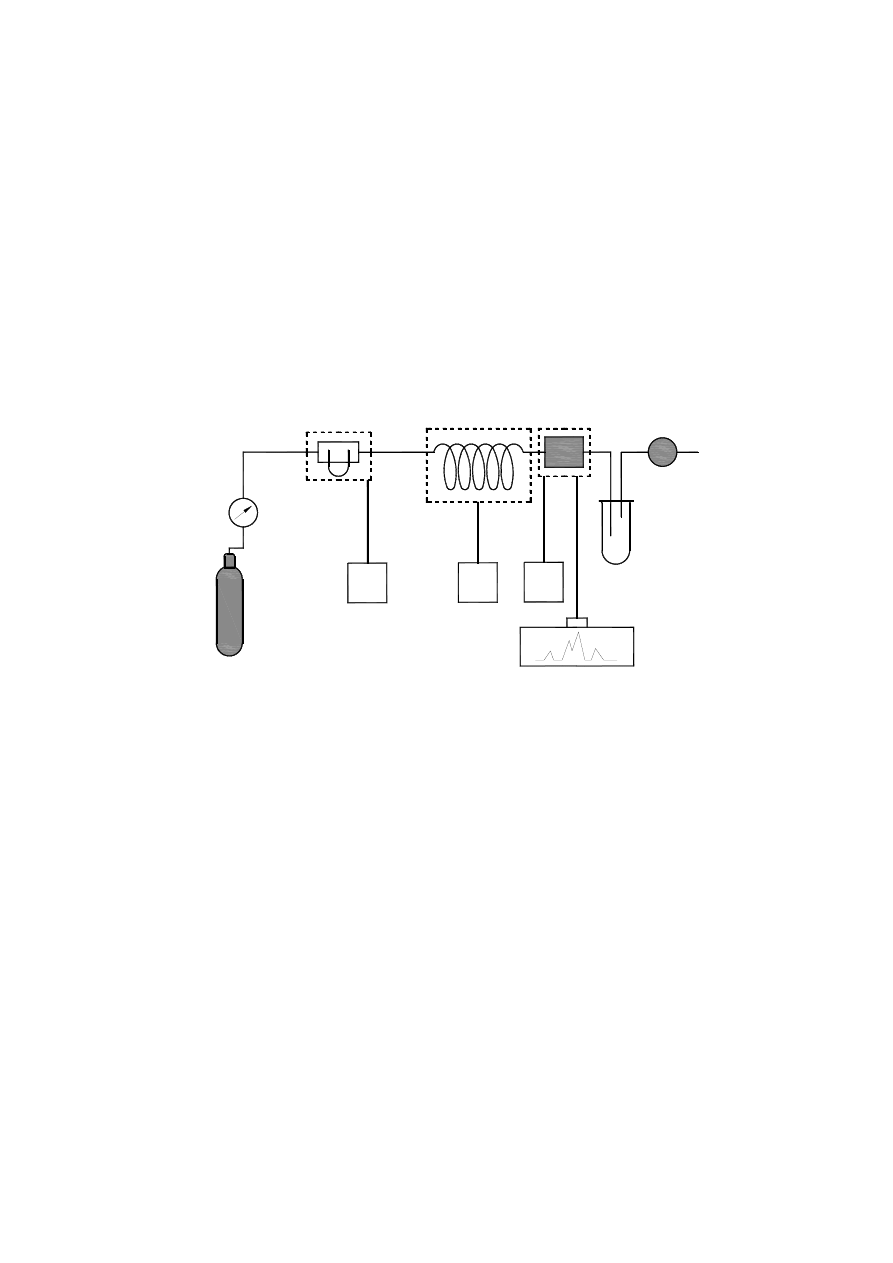
Ogólną budowę chromatografu przedstawiono na rys. 1.
R
R
R
C
D
E
H
G
F
A
B
Rys. 1. Schemat chromatografu
A - zbiornik ze sprężonym gazem, B -kontrola i regulacja ciśnienia, C - dozownik, D - kolumna,
E - detekcja, F - wzmocnienie i rejestracja, G - wyłapywanie frakcji, H - pomiar prędkości
przepływu, R -kontrola i regulacja temperatury
WIELKOŚCI MIERZONE W CHROMATOGRAFACH
Z chromatogramu czystego, pojedynczego składnika uzyskuje się 5 parametrów, za
pośrednictwem których można obliczyć wszystkie wielkości niezbędne do pełnej interpretacji
wyników. W przypadku mieszaniny dla każdego ze składników odczytuje się te same
parametry. Nie zawsze jednak jest możliwe dokładne ich zmierzenie.
Niepoprawiony czas retencji składnika t
R
. Jest to czas, jaki upływa od wprowadzenia
składnika do kolumny do momentu, w którym detektor wskaże maksymalne stężenie tego
składnika w opuszczającym kolumnę gazie nośnym.
Czas retencji powietrza t
M
. Jest to bardzo ważna wielkość, określająca czas przejścia przez
kolumnę i inne elementy aparatu substancji, która nie jest zatrzymywana przez wypełnienie
(powietrze w podziałowej chromatografii gazowej). Czas, jaki spędza w fazie stacjonarnej
substancja zatrzymywana, wynosi zatem t
R
-t
M
.
Szerokość piku składnika. Zwykle stosuje się szerokość podstawy piku. Miarą, jej jest
długość odcinka, jaki odcinają na linii podstawy styczne do boków piku poprowadzone przez
punkty jego przegięcia.
5

Dla pików o kształcie krzywej rozkładu Gaussa można również mierzyć szerokość w połowie
wysokości lub w innym, ale dokładnie określonym miejscu.
Wysokość piku. Wysokość piku jest proporcjonalna do ilości wprowadzonej do kolumny
substancji. Ponieważ jednak wysokość piku zmienia się znacznie nawet przy małych
zmianach warunków doświadczenia (wahania przepływu, temperatury, czasu dozowania) i dla
tej samej wielkości próbki może przybierać różne wartości, lepiej jest w interpretacji
ilościowej posługiwać się powierzchnią piku. Jeśli pik ma kształt krzywej Gaussa, to
powierzchnia pod krzywą jest proporcjonalna do iloczynu wysokości i szerokości podstawy
piku. Najlepiej jest określać pole piku całkując otrzymany sygnał.
Parametry piku można wyrażać albo w takich jednostkach, w jakich odczytuje się
bezpośrednio z chromatogramu, tzn. w jednostkach długości, albo w jednostkach fizycznych,
faktycznie odpowiadających mierzonym wielkościom (czas, sygnał detektora).
1
2
3
6
9
10
11 12
13
14
15
4
5
7
8
Rys. 2. Zestaw do analizy chromatograficznej gazu
1 - kolumny chromatograficzne, 2 - programator temperatury, 3 - regulator temperatury
kolumn chromatograficznych, 4 - pokrętło regulatora temperatury, 5 – lampka kontrolna
regulatora temperatury, 6 - zasilacz, 7 - pokrętła zerowania wskaźnika, 8 - regulator prądu
mostka, 9 - głowica, 10 - przepływomierz banieczkowy, 11- włącznik podaj
nika,
12 - dozowniki, 13 - regulator temperatury dozownika, 14, 15 - regulatory przepływu.
WYKONANIE OZNACZENIA
Oznaczenie wykonywane będzie na chromatografie przedstawionym na rysunku 2. Realizująć
pomiar należy wykonać kolejno następujące czynności. Odkręcić zawór główny gazu
wzorcowego i ustawić ciśnienie robocze na wartość 0,4 MPa. Nastawić ciśnienie wejściowe na
0,3 MPa. Podłączyć przepływomierz banieczkowy (10) i ustawić strumień przepływ na ok.
40 ml/min. Ustawić wymaganą temperaturę kolumn pokrętłem (4) regulatora (3) w zależności
od analizy (60ºC), dozowników i detektora (regulatorem 13) oraz włączyć termostat. Po
uzyskaniu żądanych temperatur dozowników, detektora i kolumn włączyć zasilacz (6) oraz
6
ustawić prąd mostka regulatorem (8). Włączyć rejestrator i wyzerować wskaźnik za pomocą
pokręteł (7). Po uzyskaniu poprawnej linii podstawowej, o czym sygnalizuje świecąca lampka
(5) w kolorze zielonym, przystąpić do dozowania próbki gazu wzorcowego a następnie
badanego.
Za pomocą chromatografu typu ELWRO 504 skład badanego gazu wyznacza się poprzez
analizę powierzchni wykreślonych pików. Analizę powierzchni pików można przeprowadzić
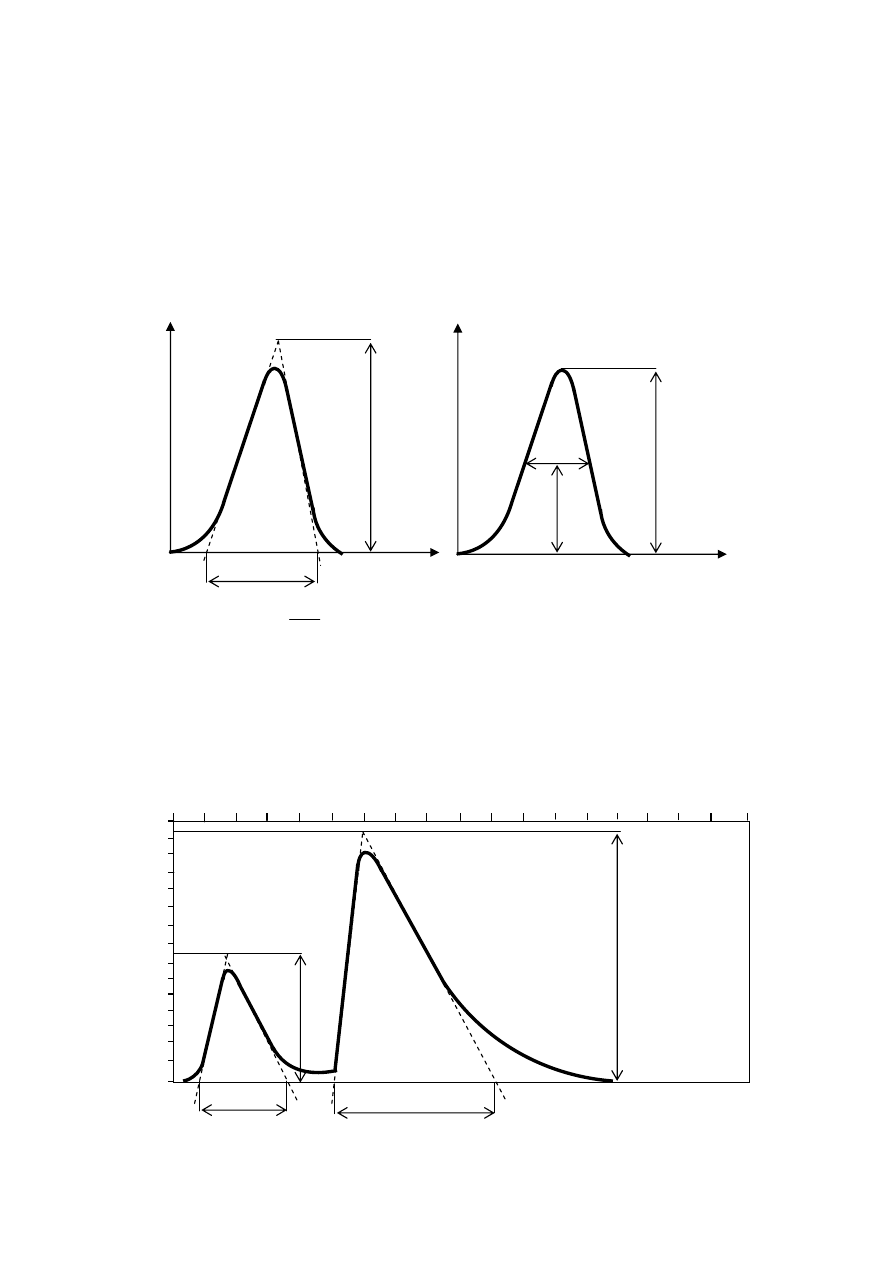
dwoma metodami: trójkąta (rys. 4 a) oraz z wykorzystaniem wysokości piku jego szerokości
w połowie wysokości (rys. 4 b).
a)
b)
Rys. 4. Metody pomiaru powierzchni piku
a – metoda trójkąta
b – metoda z wykorzystaniem wysokości piku i jego szerokości w połowie wysokości
a
a
czas,
czas,
sygna
ł,
sygna
ł,
h
h
05
h
s
mV
,
2
h
a
P
⋅
⋅
=
s
mV
,
a
h
P
0,5h
⋅
⋅
=
Poniżej przedstawiono przykład wyznaczania składu powietrza atmosferycznego
Rys. 5. Przykładowy chromatogram dla powietrza
a
1
czas, s
O
sygna
ł,
μ
V
h
2
50 52 54 56 58 60 62 64 66 68 70 72 74 76 78 80
300
0
280
0
260
0
240
0
220
0
200
0
180
N
h
1
0
a
2
7

Analiza ilościowa oparta jest na liniowej zależności pomiędzy sygnałem detektora
(powierzchnia piku) a stężeniem substancji badanej w gazie nośnym . Powierzchnia piku jest
proporcjonalna do ilości oznaczanej substancji. Można ją wyznaczyć geometrycznie,
planimetrycznie lub przez całkowanie za pomocą integratora. Metoda geometryczna jest
prosta, ale dająca wartości przybliżone. W celu obliczenia powierzchni piku konstruuje się
trójkąt (rys. 5) i oblicza pole P. Metoda ta jest obarczona błędem związanym z wykreśleniem
stycznych w punkcie przegięcia. Wyniki bardziej zbliżone do rzeczywistości uzyskuje się
mnożąc wysokość piku przez szerokość w połowie jego wysokości.
Przykładowe obliczenia dla wyników z rysunku 5:
48
,
1
1
=
h
, mV,
95
,
2
2
=
h
, mV,
6
,
5
9
,
51
5
,
57
1
=
−
=
a
,
s,
0
,
11
5
,
60
5
,
71
2
=
−
=
a
, s,
144
,
4
2
48
,
1
6
,
5
2
1
1
1
=
⋅
=
⋅
=
h
a
P
, mVs,
225
,
16
2
95
,
2
0
,
11
2
2
2
2
=
⋅
=
⋅
=
h
a
P
, mVs,
369
,
20
225
,
16
144
,
4
2
1
=
+
=
+
=
P
P
P
, mVs
34
,
20
100
369
,
20
144
,
4
100
1
2
=
⋅
=
⋅
=
P
P
O
, %
66
,
79
100
369
,
20
225
,
16
100
2
2
=
⋅
=
⋅
=
P
P
N
, %.
OPRACOWANIE WYNIKÓW
Na podstawie otrzymanego chromatogramu określić czasy retencji oraz powierzchnie pików
poszczególnych składników gazu. Na podstawie obliczeń powierzchni pików składników
gazu wzorcowego i badanego, wyznaczyć skład analizowanego gazu.
ZAGADNIENIA DO OPRACOWANIA
a)
Wielkości mierzone w chromatografach.
b)
Gazy nośne i dozowanie.
c)
Typy kolumn chromatograficznych i wypełnienia.
d)
Nośniki, adsorbenty i ciekłe fazy stacjonarne.
e)
Budowa i zasada działania chromatografu.
f)
Metodyka pomiarów.
LITERATURA
1. Bartulewicz J., Gawłowski J., Bartulewicz E.: Zastosowanie chromatografii gazowej i
cieczowej do analizy zanieczyszczeń środowiska , Państwowa Inspekcja Ochrony
Środowiska, Warszawa 1997.
2. Guiochon G., Pommier C.: Chromatografia gazowa w chemii nieorganicznej, PWN,
Warszawa 1979.
3. Kisielew A. W., Jaszin J. I.: Adsorpcyjna chromatografia gazowa, PWN, Warszawa 1969.
4. Kruszyński S.: „Technika cieplna – ćwiczenia laboratoryjne”, Skrypt Politechniki
Częstochowskiej, Częstochowa 1990.
5. Kulesza J.: Pomiary cieplne, WNT, Warszawa 1993.
6. Paryjczyk T.: Chromatografia gazowa w badaniach adsorpcji i katalizy, PWN, Warszawa
1975.
8
Document Outline
- Zasada działania. Metoda ta jest oparta na rozdzielaniu mieszanin na długich i cienkich kolumnach z odpowiednim wypełnieniem stałym lub żelowym, a następnie detekcji stężenia kolejno wychodzących związków na wylocie kolumny. Mechanizm rozdziału oparty jest na występowaniu oddziaływań międzycząsteczkowych między związkami rozdzielanych mieszanin i wypełnieniem kolumn. Oddziaływania te hamują przepływ związków chemicznych przez kolumnę. Czym są one silniejsze, tym czas przejścia związku chemicznego przez kolumnę jest dłuższy. Czas przejścia danego związku chemicznego przez całą kolumnę jest nazywany jego retencją. Przy odpowiednio długiej i cienkiej kolumnie czasy retencji związków są na tyle różne, że wychodzą one z kolumny osobno, przy czym cała objętość związku wychodzi w stosunkowo krótkim czasie.
- KONSTRUKCJA CHROMATOGRAFU GAZOWEGO
- Chromatograf gazowy składa się ogólnie z następujących podstawowych elementów:
- Układ nastrzykowy. Tradycyjny układ nastrzykowy składa się zwykle z membrany, którą nakłuwa się specjalną strzykawką chromatograficzną oraz odparowywacza, w którym następuje odparowanie wszystkich składników analizowanej próbki. Odparowywacz to krótka (5-10 cm) rurka metalowa lub szklana otoczona spiralą grzejną, która umożliwia rozgrzanie rurki do ponad 200°C. W niektórych aparatach odparowywacz pracuje w stale tej samej temperaturze, zaś w innych istnieje możliwość szerokiego regulowania jego temperatury.
- Piec. Piec w chromatografie gazowym to szczelny, odizolowany od otoczenia i wysokowydajny grzejnik z bardzo dokładną kontrolą temperatury. Wewnątrz pieca umieszczona jest zwinięta w pętlę kolumna. Piece, aby zapewnić możliwość szybkiej zmiany temperatury w czasie, posiadają zwykle wymuszony obieg powietrza. W większości współczesnych chromatografów istnieje możliwość liniowej zmiany temperatury w czasie pomiaru, co pozwala na wykonywanie analiz w tzw. gradiencie, co zwykle ją przyspiesza. Czasami jednak analizy wykonuje się w tzw. izotermie czyli stałej, ściśle określonej temperaturze.
- Kolumna. Kolumny chromatograficzne występują w trzech rodzajach:
- Detektor. Detektor w chromatografie gazowym mierzy stężenie wypływających związków w eluencie. Idealny detektor powinien być wrażliwy tylko na samo stężenie niezależnie od struktury chemicznej analizowanego związku. W praktyce jednak detektory mają różną czułość na różne związki chemiczne, co wymaga ich kalibrowania i ustalania tzw. współczynników odpowiedzi dla każdego związku chemicznego osobno o ile chce się mierzyć dokładny skład procentowy związków chemicznych w analizowanej próbce.
- Rejestrator. Niegdyś jako rejestratory stosowano analogowe urządzenia pisakowe, czasami zaopatrzone w integrator, które po prostu "rysowały" zmiany napięcia elektrycznego generowanego przez detektor. Wykresy te nazywa się tradycyjnie chromatogramami. Chromatogramy przyjmują zwykle kształt serii ostrych pików, których wysokość odpowiada stężeniu wychodzącego z kolumny związku chemicznego, a pole pod pikiem można przeliczyć na całkowite stężenie danego związku chemicznego w całej analizowanej próbce.
Wyszukiwarka
Podobne podstrony:
Analiza długich list za pomocą funkcji?zy?nych
Analiza pozycji finansowej za pomocą modelu Du Ponta nowe, studia, finanse przedsiębiorstwa
Analiza zwrotu kosztow za uslug Nieznany (2)
3 ANALIZA SYSTEMOW ZA POMOCA ME Nieznany (2)
06 pomiar mocy za pomoca oscylo Nieznany (2)
Metody organizacji i zarządzania, BCG, Analiza i projektowanie portfela produkcji za pomocą macierzy
Motywowanie za pomoca plac id 3 Nieznany
Kodowanie pilota za pomoca VAG Nieznany
Analiza skladu chemicznego i cz Nieznany
[14.10.2014] Współczynnik wodoprzepuszczalności, ćw[1].3, Wyznaczenie współczynnika wodoprzepuszcza
Wyznaczanie natężenia nieznanego źródła światła za pomocą fotometru, Technologia chemiczna, semestr
06 pomiar mocy za pomoca oscylo Nieznany (2)
Microsoft Excel 2007 PL Analiza danych za pomoca tabel przestawnych Akademia Excela e27aae
Analiza procesu tłoczenia blachy za pomocą elastycznego stempla
więcej podobnych podstron