
Ć
w. audytoryjne nr 2 25.02.2010
1.
Które z następujących związków mają zdelokalizowane elektrony:
a)
CH
2
=CHCH
2
CH=CH
2
b)
c)
d)
e)
f)
g)
h)
i)
2.
Narysuj struktury rezonansowe następujących cząstek i porównaj ich trwałość:
a) CH
3
NO
2
e) 1b i)
b) CH
3
COO
Ө
f) 1c
c) CH
3
SO
3
Ө
g) 1g j)
d) CH
2
=CH-CH
⊕
h) 1h
3.
Rysunek obok przedstawia jedną ze struktur rezonansowych kreatyniny,
ważnego produktu końcowego metabolizmu białek. Narysuj:
a)
strukturę rezonansową kreatyniny, w której nie będzie rozdziału
ładunku,
b)
inne struktury rezonansowe kreatyniny z rozdzielonym ładunkiem,
ale z zapełnionymi powłokami na wszystkich atomach.
4.
W następujących parach struktur rezonansowych wskaż strukturę stabilniejszą:
5.
W oparciu o struktury rezonansowe
wyjaśnij, który z przedstawionych
jonów w parze jest trwalszy?
O
O
C
CH
3
CH
2
CH
3
CH
2
CH
2
NHCH=CH
2
CH
2
NH
2
NH
2
CH
3
C
O
OH
.
CH
3
CH=CHCH=CHCH
2
.
N
N
O
CH
3
H
2
N
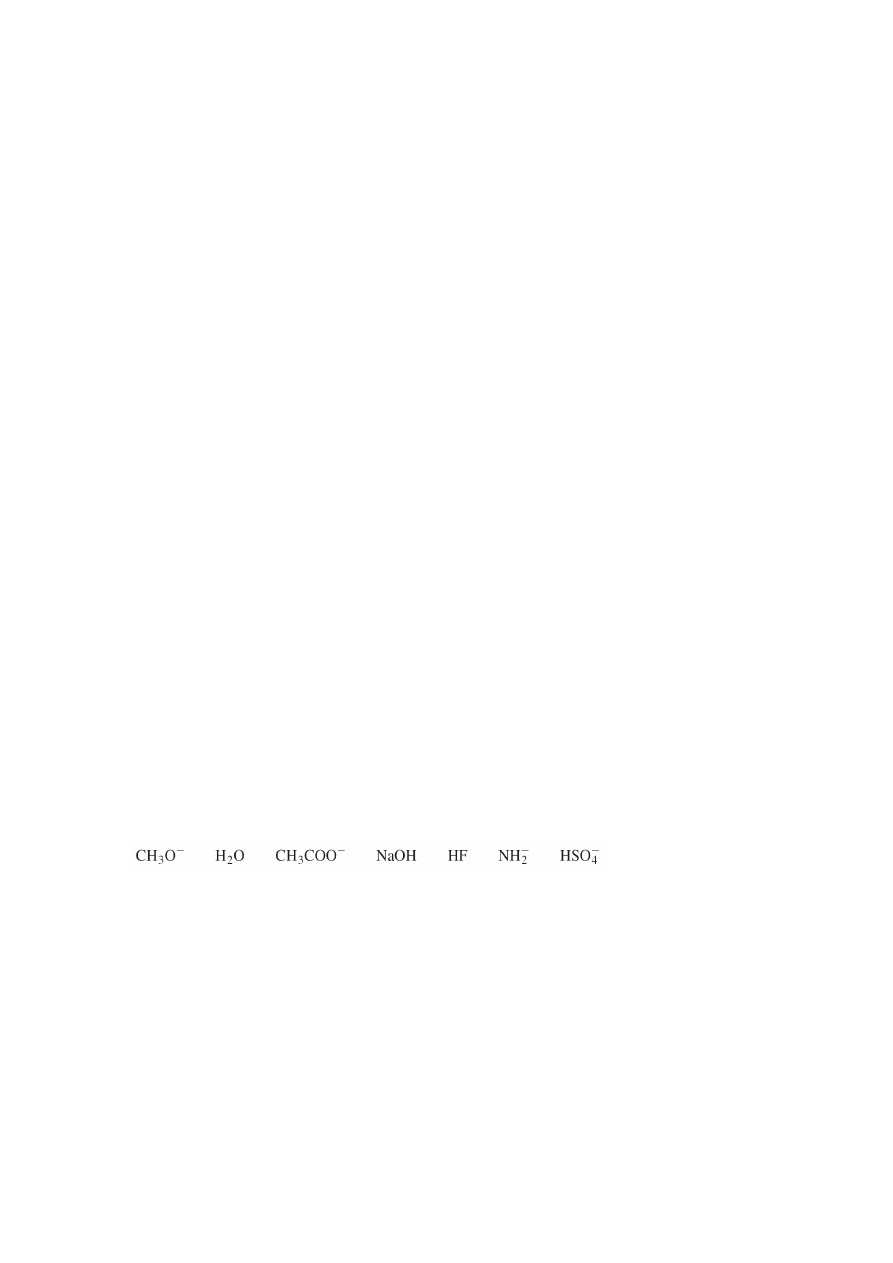
6.
Stała kwasowości alkoholu metylowego wynosi 15.5, a jego stała zasadowości 16.5. Ile
wynoszą pK
a
i pK
b
odpowiednio sprzężonej zasady i kwasu?
7.
Porównaj kwasowość następujących związków:
a) CH
3
CH
3
, CH
3
NH
2
, CH
3
OH
b) HF , HCl , HBr , HI
c) CH
3
OH , CH
3
SH
d) CH
3
CH
2
OH , C
6
H
5
OH , CH
3
COOH
e) CH
3
CH
3
, CH
2
CH
2
, CHCH
f) HCOOH , CH
3
COOH
g) CH
3
COOH , FCH
2
COOH , ICH
2
COOH , BrCH
2
COOH , ClCH
2
COOH
h) CH
3
CH
2
CHBrCH
2
COOH , CH
3
CH
2
CH
2
CHBrCOOH , CH
3
CHBrCH
2
CH
2
COOH
i) CH
3
(CH
2
)
3
OH , (CH
3
)
3
COH
j) CH
3
COOH , CH
3
SO
3
H
k) CH
3
CH
2
CH
2
OH , CH
3
CHCHOH
l) CH
3
CHCHCH
2
OH , CH
3
CHCHOH
8.
Porównaj zasadowość następujących jonów:
c) NH
2
Ө
, I
Ө
, OH
Ө
, C
6
H
5
O
Ө
, Cl
Ө
,
CH
3
COO
Ө
d) CH
3
CH
2
O
Ө
, (CH
3
)
3
CO
Ө
9.
Oceń, w którą stronę przesunięty będzie stan równowagi następujących reakcji kwasowo-
zasadowych:
a) CH
3
OH + H
2
O = CH
3
O
Ө
+
H
3
O
⊕
b) CH
3
OH + OH
Ө
= CH
3
O
Ө
+
H
2
O
c) CH
3
OH + NaH
=
CH
3
ONa
+
H
2
d) C
6
H
5
OH + OH
Ө
= C
6
H
5
O
Ө
+
H
2
O
e) CHC
Ө
Na
⊕
+ CH
3
CH
3
= CHCH
+ CH
3
CH
2
Ө
Na
⊕
10.
W którą stronę przesunięty będzie stan następującej równowagi:
CH
3
CH
2
OH + (CH
3
)
3
C-O
Ө
=
CH
3
CH
2
O
Ө
+ (CH
3
)
3
C-OH
11.
Zapisz reakcję pomiędzy:
a) CH
3
OH + ZnCl
2
b) Br
2
+ FeBr
3
c) CH
3
OCH
3
+ BF
3
12.
Podane poniżej cząstki podziel na nukleofile i elektrofile: H
2
O, NO
2
⊕
, CH
3
CH
2
Ө
,
(CH
3
)
2
CH
⊕
, CH
3
O
Ө
, NH
3
, Br
⊕
, H
⊕
, H
Ө
,
CH
3
CH
2
OH , CH
3
Li , CH
3
Cl, Br
2
, CH
2
=CH
2
13.
Uszereguj następujące związki według rosnącej kwasowości:
CH
3
COOH CH
3
OH CH
3
CH
3
CH
3
SO
3
H CH
3
SH CH
3
C≡CH CH
2
ClCOOH
14.
Uszereguj następujące cząstki w kolejności rosnącej zasadowości:
15.
Metan, będąc alkanem, jest bardzo słabym kwasem o pK
a
~ 50. Z kolei, nitrometan
(CH
3
NO
2
) należy do tzw. C-kwasów i charakteryzuje się wartością pK
a
~ 10. Skąd się
bierze tak ogromna różnica we właściwościach kwasowo-zasadowych tych związków?
16.
Zaproponuj produkty następujących reakcji kwasowo-zasadowych (przekazania protonu
od kwasu do zasady):
a) CH
3
COOH + N(CH
3
)
3
→
b) HCOOH + CH
3
ONa →
c) CH
3
COH + NaOH →
d) CH≡CH + NaNH
2
→
e) CH
3
-Li + H
2
O →
Wyszukiwarka
Podobne podstrony:
BADANIA FIZYKALNE [ćw. + wykłady] - dr Połocka-Molińska, medyczne różne, badania fizykalne
działalność inspektora PP dr Sobolewskiego
ćw.4 - interna od dr Radwińskiej, weterynaria, Choroby wewnętrzne zwierząt gospodarskich
Pytania Czerska, UG Finanse i Rachunkowość LIC, FIR I Sem 2011, Podstawy Zarządzania I sem (W. dr Wo
ćw 1 elektrody węglowe w kondensatorze elektrochemicznym
Sulfonamidy, Farma, Notatki jakies z Kostowskiego i Hermana na zajecia do Dr Kusowsk, Notatki jakies
ćw Strategia BW (dr Stasz )
NLPZ, Farma, Notatki jakies z Kostowskiego i Hermana na zajecia do Dr Kusowsk, Notatki jakies z Kost
rach w2 3 4, UG Finanse i Rachunkowość LIC, FIR I Sem 2011, Podstawy Zarządzania I sem (W. dr Wojcie
Bankowość ĆW dr A Barembruch
zarzadzanie2, UG Finanse i Rachunkowość LIC, FIR I Sem 2011, Podstawy Zarządzania I sem (W. dr Wojci
KPA 2012 13 (ćw dr AK)
reumatologia ćw 8, FIZJOTERAPIA- zaoczne 2007-2010, reumatologia, ćwiczenia dr GregorowiczCieślik
Harm. ćw. dla gr.3.2 03-04, Dr inż
dr Puchalska węglowodany
cw 10 - Wyznaczanie przyspieszenia ziemskiego za pomocą wahadła rewersyjnego, Sprawozdania jakieś, F
więcej podobnych podstron