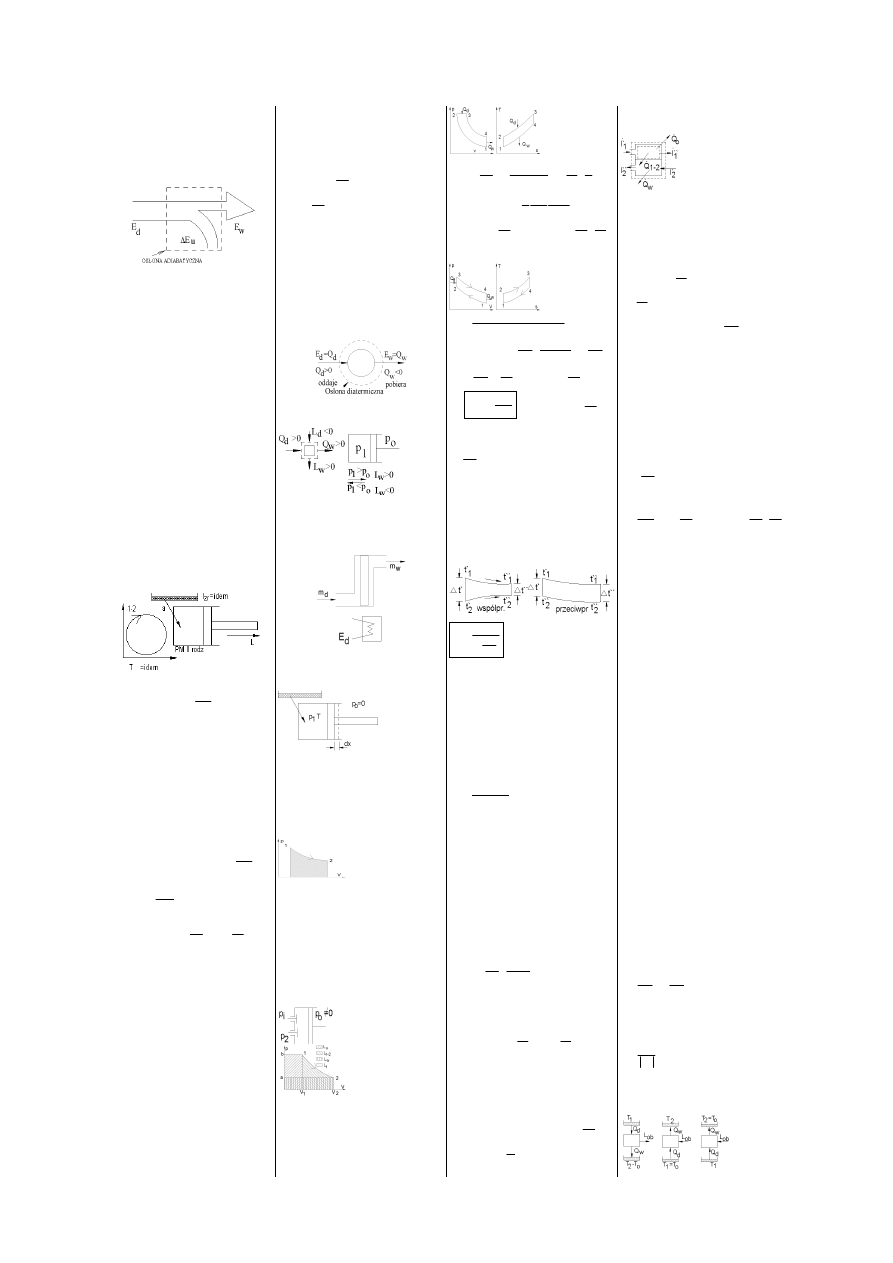
1. I Zasada termodynamiki
W układzie odosobnionym tzn. osłoniętym osłoną
adiabatyczną, ilość energii wewnętrznej układ jest stała
E
d
=
∆
E
u
+E
w
[J] ⇒ równ bilansu energetycznego można
traktować jako I zasadę termodynamiki dot. Układu
zamkniętego. Energia doprowadzona do układu
wyodrębnionego
osłoną
adiabatyczną
pozostaje
częściowo w układzie a część jest wyprowadzona z
układu. Interpretacja graficzna – wykr. Sankeya
Jeżeli układ działa w sposób ustalony (jego energi nie
zmienia się w czasie lub zmienia się w sposób
periodyczny i po skończonej liczbie cykli wraca do
wart. Początkowych) to bilans energetyczny przyjmuje
postać
w
d
E
E
&
&
=
ponieważ
0
>
w
E&
to do czynnego
silnika
⇒
>
0
d
E&
że jest rzeczą niemożliwą
skonstruowanie
perpetum
mobile
pierwszego
rodzaju (silnika pracującego bez zasilania energią z
zewnątrz).
0
,
0
,
>
=
>
=
L
E
E
E
E
w
d
w
d
idem
E
E
u
u
=
=
∆
,
0
2. II Zasada termodynamiki
sformułowanie
a)
Plancka. Jest rzeczą niemożliwą skonstr.
takiego
silnika
(maszyny
działającej
periodycznie), którego działanie polegało by
na podnoszeniu ciężarów i równoczesnym
ochładzaniu jednego źródła ciepła. Silnik taki
nosi nazwę perpetum mobile II rodzaju.
b)
Clausjusa
ciepło
nie
może
przejść
samorzutnie od ciała o temp niższej do ciała o
temp
wyższej.
Aby
spowodować
taki
przepływ ciepła musimy zastosować lewo
bieżną maszynę cieplną i wkładać do niej
energię z zewnątrz, tzn. wywoływać zmiany
w innych ciałach.
•
Samorzutne przejście – zjawisko któremu
nie towarzyszą żadne zmiany w otoczeniu
(otoczenie nie oddziałuje na układ)
c)
Schmidta – nie można całkowicie odwrócić
przemiany, w której występuje tarcie. Pracę w
całości można zmienić na ciepło przez tarcie,
jednak z tego ciepła nie można w całości
odzyskać pracy.
d)
Ostwalda – perpetum mobile II rodzaju jest
niemożliwe – DOWÓD
czyli cykl pracy silnika stąd
∆
S
PM II R
=0 bo entropia jest
wielkością stanu a stan w punkcie 1-2 jest sobie równy
to
∆
=0;
π
=
∆
S
PM II R
+S
ŹR
=0 -
ŹR
T
Q
; Q – ciepło tarcia
π
> 0 sprzeczne z prawem wzrostu entropii
e)
entropia układu zamkniętego i izolowanego
nie może maleć podczas dowolnej przemiany
i
wzrastać
przy
przemianach
nieodwracalnych.
3. Wielkości zastępcze dla roztworów gazowych
Oblicza się w ten sposób, że mnoży się wielkości
indywidualne przez udziały i sumuje się tak obliczone
iloczyny.
a)
udziały gramowe – jeżeli jednostka danej
wielkości zawiera w mianowniku kg np. R
b)
udziały
molowe
(objętościowe)
jeżeli
jednostka
danej
wielkości
zawiera
w
mianowniku kmol np. M [kg/kmol]
c)
objętościowe - jeżeli m
3
lub mm
3
Stałą gazową R obliczamy
∑
=
=
k
1
i
i
i
k
g
R
kgK
J
Masę
drobinową
M
obliczamy
∑
=
=
k
1
i
i
i
M
z
M
kmol
kg
między udz mol z
i
i gram g
i
składnika roztworu
zachodzi zależność
M
M
z
g
i
i
i
=
R
R
g
z
i
i
i
=
4.
Entalpia – sposób obliczania
a)
ciała stałe i ciecze i=u+pv, gdzie v - obj.
właść., p - bezwzględne ciśnienie statyczne, u
– właściwa energia wewnętrzna
b)
gaz doskonały (funkcja tylko temp, nie zależy
od ciśnienia i objętości) i=c
p
T+u
o
, gdzie c
p
–
ciepło wł. przy stałym ciśnieniu, T – temp, u
o
– energia otoczenia
c)
gaz
półdoskonały
(funkcja
tylko
temp)
o
T
0
p
u
T
I
c
i
+
=
; gdzie
T
0
p
I
c
- średnie
ciepło właściwe od 0 doT, T – temp
d)
para nasycona mokra i=i`+x(i``-i`), gdzie i –
entalpia pary nasyc. mokrej, i` - entalpia
cieczy, i`` - ilość pary suchej nasyconej, x –
stopień wilgotności
e)
para przegrzana i=i``q
p
, gdzie q
p
– ciepło
przegrzania pary
f)
para mokra nasycona i=q+r+pr, gdzie r –
entalpia parowania
5. Przejmowanie
jest to wymiana ciepła pomiędzy powierzchnią ciała
stałego a otaczającym ją płynem
z prawa Newtona Q=A-
α
(t
f
-t
w
)
τ
, gdzie t
w
– temp pow
ciała stałego, t
f
- temp opływającego płynu,
α
-
współczynnik,
τ
- czas, A – powierzchnia
α
- ozn. ilość wymienionego podczas przejmowania
przez jednostkę powierzchni w ciągu jednostki czasu
Przewodzenie – polega na przenoszeniu ciepła w
obrębie danego ciała od jednych drobin do drugich,
odbywa się tylko gdy drobiny ciała nie podlegają
przesunięciom makroskopowym. Warunek spełniony
podczas przepływu ciepła przez ciała stałe
Prawo
Fouriera
τ
λ
−
=
du
dV
A
Q
, gdzie
λ
- wsp. przewodz.
materiału,
du
dV
- grzdient temp. A - pole pow
6. Sposoby przekazywania ciepła
a)
przewodzenie ciepła – przenoszenie ciepła w
obrębie danego ciała od jednych drobin do
drugich lub przez dyfuzję
b)
konwekcja – (unoszenie ciepła) ciepło płynie
z cząsteczkami płynu od ściany przegrody do
rdzenia strumienia lub odwrotnie
c)
promieniowanie – ciepło przenosi się od
jednego ciała do drugiego w postaci energii
promienistej
(za
pośrednictwem
fal
elektromagnet)
7 Sposoby doprowadzania energii
a)
na sposób ciepła – wtedy gdy istnieje różnica
temp między ciałem a otoczeniem
b)
na sposób pracy – wtedy gdy między
układem a otoczeniem jest oddziaływanie
różnego rodzaju sił
I – p
1
>p
o
– praca na rzecz otoczenia + L
w
>0
II – p
1
<p
o
– otoczenie na rzecz układu – L
d
<0
c)
ze strumieniem ciepła – wtedy gdy np.
mamy zbiornik i:
-
substancję doprowadzamy M
d
-
substancję wyprowadzamy M
w
przypadki
d)
za pomocą prądu elektrycznego
8. Praca bezwzględna
Jest
to
praca
wykonana
przez
czynnik
termodynamiczny wtedy gdy ciśnienie otoczenia jest
równe zero. Pracę tę można obliczyć rozpatrując układ
cylinder – tłok
Przy
∞
małym dx czynnik wykonuje pracę dl=kdx,
gdzie k – siła, dx droga. Przy pracy bez tarcia siłę k
równoważy ciśnienie działające na tłok. Stąd: k=pA,
gdzie p – ciśnienie, A- przekrój, dl=p A dx ⇒ dl=p dv
p – bezwzględne ciśnienie statyczne wewn. cylindra
dv – przyrost objętości w cylindrze
Praca bezwzględna
∫
=
−
2
1
2
1
pdv
dl
; interpr. graficzna
(założenie – znam zależność p od v)
L
1-2
– zależy od drogi przemiany a nie tylko od stanu
początkowego i końcowego
L
1-2
– dotyczy przemian zachodzących bez strat na
rzecz tarcia (wtedy dl <pdv)
Zastosowanie: w układach otwartych i zamkniętych,
pseudoodwr. dl = p dv - dl
t
= p dv - dQ
f
stąd dl < p dv
dl
t
– praca na rzecz tarcia, dQ
f
– ciepło na rzecz tarcia
9. Sens fizyczny pracy technicznej
Pracę fizyczną rozpatrujemy wg idealnej maszyny
przepływowej tzn.
-
nie występuje tarcie poruszających się
względem siebie powierzchni
-
zawory nie stawiają oporu
-
w wewnętrznym zwrotnym położeniu tłok
dotyka cylindra
Praca techniczna element. dL
t
= -Vdp, L
t
>0 gdy dp<0
Praca skończona L
t 1-2
=
∫
−
2
1
Vdp
dL
t
>0 gdy dp<0; dL
t
<0 gdy dp>0
10. Obieg Diesla
Jest obiegiem porównawczym, silników o zapłonie
samoczynnym i wtryskiem paliwa za pomocą
sprężonego powietrza. Jest to układ otwarty.
Sprawność techniczna
)
T
T
(
c
)
T
T
(
c
1
q
q
1
2
3
p
1
4
v
d
w
tD
−
−
−
=
−
=
η
;
κ
=
1
c
c
p
v
1
1
1
1
1
1
tD
−
ϕ
−
ϕ
ε
κ
−
=
η
κ
−
κ
kompresja
2
1
V
V
=
ε
; st. obciążeni
2
3
2
3
T
T
V
V
=
=
ϕ
Stąd sprawność maleje ze wzrostem obciążenia
11. Obieg Otto.
Obieg porównawczy silnika z ZI
z
ne
doprowadzo
ciepo
ego
porównawcz
obiegu
praca
to
=
η
L
o
=Q
d
-Q
w
;
d
w
d
w
d
w
w
to
Q
Q
1
Q
Q
Q
Q
L
−
=
−
=
=
η
1
1
2
d
w
)
V
V
(
)
Q
Q
(
−
κ
=
;
1
1
2
to
)
V
V
(
1
−
κ
−
=
η
1
to
1
1
−
κ
ε
−
=
η
;
9
5
≤
ε
≤
;
2
1
V
V
=
ε
12. Stopień suchości pary nasyconej mokrej
x – jest to parametr, który stanowi zawartość pary
nasyconej suchej do całkowitej ilości pary mokrej
m
m
x
p
=
-
dla cieczy w punkcie pęcherzyków x = 0
-
dla pary w punkcie rosy x = 1
13. Wymienniki ciepła
Zadaniem ich jest umożliwienie przenikania ciepła z 1
ośrodka do 2. Zależnie od kierunków przepływu obu
czynników mówi się o przepływie współprądowym,
przeciwprądowym lub poprzecznoprądowym.
współpr. – przepływ w którym kierunki przepływu
obu czynników są zgodne
przeciwpr. - ... są skierowane przeciwnie
poprzecznopr. - ...są do siebie prostopadłe
Wartość różnicy temp określana jest równaniem
`
t
``
t
ln
`
t
``
t
tm
∆
∆
∆
−
∆
=
∆
Wnioski: Przy współprądzie temp końcowa płynu
ogrzewanego jest niższa od końcowej temp płynu
ogrzewającego. Przy przeciwprądzie końcowa temp
płynu ogrzewanego może być znacznie wyższa i w
pewnych przypadkach może zbliżyć się do temp
początkowej płynu ogrzewającego.
Przykład: Kocioł
parowy, skraplacz, podgrzewacz,
14. Co to jest entalpia
To wielkość termodynamiczna określająca stan
termodynamiczny układu i równa jest sumie energii
wewnętrznej U układu oraz iloczynowi jego objętości i
ciśnienia. Zmiana entalpii przy stałym ciśnieniu jest
miarą ilości ciepła wymienionego przez układ z
otoczeniem. I – entalpia, U – energia wewnętrzna, p –
ciśnienie statyczne bezwzgl., V – objętość całkowita
ciała. I = U + p V. Entalpia jest funkcją tych samych
parametrów stanu co energia wewnętrzna.
15. Co to jest strumień czynnika termodynamicz.?
Obliczamy za pomocą średniej prędkości przepływu.
Jeżeli na przykład przewodem rurowym o przekroju F
[m
2
] płynie strumień z szybkością
ω
[m/s] to wzór na
strumień objętości wygląda
ω
=
F
V
&
Strumień substancji G
& [kg/s] oblicza się mnożąc
objętość przez gęstość substancji
ωγ
=
F
G
&
gdy G
& =
idem to jest to warunek ciągłości strugi.
16. Gaz doskonały i półdoskonały
gaz doskonały – gaz którego drobiny nie przyciągają
się wzajemnie, są nieskończenie małe i sztywne
(wewnątrz drobin nie występują drgania).
Spełnia on:
- prawo Awogadra – w jednakowych objętościach
znajduje się ta sama ilość cząstek dowolnego gazu
doskonałego, jeżeli ciśnienie i temp obu gazów są
jednakowe.
2
2
1
1
2
1
M
N
M
N
m
m
=
-
równanie stanu – f(p,V,T) =0, gdy znam 2
parametry gazu to mogę obliczyć 3
- równanie stanu gazu doskonałego (Clapeyrona)
pV=RT
-
ciepło właściwe
dt
dq
c
=
; c
p
>c
v
;
k
c
c
v
p
=
; c
p
-c
v
=R
-
zasada ekwipartycji – energia rozkłada się
równomiernie na wszystkie możliwe ruchy cząstek
Gaz półdosk. różni się od gazu doskonałego tym że w
jego drobinach występują drgania. Atomy wchodzące
w skład gazów są powiązane ze sobą sprężyście
17. Co to jest strumień ciepła?
Stosunek elementarnej ilości ciepła dQ do czasu d
τ
trwania wymiany tej ilości ciepła
τ
=
d
dQ
Q
,wzór
osiąga postać
τ
=
Q
Q
przy ustalonej wymianie ciepła
18. Bilans wymiennika ciepła
Wymiennik
przeponowy
to
urządzenie
jest
przekazywanie
ciepła
między
2
czynnikami
oddzielonymi przegrodą
a)
bilans wewnątrz ścianki kanału grzejącego
b)
osłona na zewnątrz wymiennika
o
2
2
1
1
o
2
1
2
1
Q
`
I
``
I
``
I
`
I
Q
``
I
``
I
`
I
`
I
&
&
&
&
&
&
&
&
&
&
+
−
=
−
=
+
=
+
19 Co to jest entropia
Jest to funkcja stanu termodynamicznego, której
zmiana równa się ilorazowi dostarczonego ciepłą i
temperatury
T
dq
dS
=
; S – entropia całkowita
T
dq
ds
=
; s – entropia właściwa w odniesieniu do 1kg
czynnika; dla źródła
∆
S = -
źr
źr
T
Q
źródło oddaje
energię więc przyrost entropii jest ujemny. Entropia
mówi nam o kierunku przemian zachodzących w
przyrodzie.
20. Prawo wzrostu entropii
Jeżeli układ jest jak na rys. i założenie: do tłok +
cylinder możemy doprowadzić ciepło Q ze źródła
ciepłą, przy czym Q = idem. Do cylindra mogę
doprowadzić substancję o ilości dm i entropii
właściwej s.
Wyróżniamy dwa przypadki:
I przemiana odwracalna
a)
T
cz
= T
źr
; b) brak tarcia dQ
t
= 0
przyrost entropii układu odosobnionego
∆
s =
π
,
natomiast elementarny przyrost ozn. d
π
= ds.
u
+ds
ot
sdm
T
dQ
ds
cz
u
+
=
- przyrost entropii układu
zb
źr
ot
ds
ds
ds
+
=
- przyrost entropii otoczenia
−
=
π
⇒
−
−
+
=
π
źr
cz
źr
cz
T
1
T
1
dQ
d
sdm
T
dQ
sdm
dT
dQ
d
0
d
T
T
cz
ź
r
=
π
⇒
=
Wniosek:
W
układzie
odosobnionym sumą przyrostów entropii wszystkich
ciał uczestniczących w zjawisku odwracalnym jest = 0.
Warunek ten jest spełniony nawet w najmniejszej
części zjawiska.
II przemiana nieodwracalna tzn. t
źr
≠
t
cz
21. Co to jest spalanie niezupełne i niecałkowite
niecałkowite - to spalanie kiedy produkty spalania
zawierają stałe składniki palne. Jednym stałym
składnikiem jest C.
niezupełne – gdy w produktach spalania występują
palne gazy (CO, H
2
, CH
4
). Jeżeli do paliwa doprowadzi
się za mało powietrza bądź nie wystąpi jego dokładne
wymieszanie to spalanie nie będzie zupełne i w
spalinach pojawią się produkty niezupełnego spalania.
Najbardziej istotne znaczenie ma CO co połączone jest
ze znaczną stratą.
22. Rodzaje konwekcji
Konwekcja – przenoszenie energii przez przepływ
drobin i mieszanie się strugi o różnej temp. Występuje
tylko w cieczach i gazach.
a) konwekcja wymuszona – występuje gdy prędkość
przepływu strugi płynu może wynikać z działania sił
zewnętrznych (działanie pompy). Wymiana ciepła przy
konwekcji wymuszonej zależy od rodzaju ruchu:
-
laminarny Re<Re
kr
=2300
-
burzliwy Re >10000
-
R
kr
<Re<10
4
(ruch przejściowy, ob. inne zależ)
b) Konwekcja swobodna - występuje wtedy gdy ruch
płynu powstaje samoczynnie na skutek działania sił
wyporu. K. s. najczęściej nakłada się na konw.
wymuszoną, bo siły wyporu powstają zawsze zawsze
gdy gęstość ciężaru płynu jest inna w warstwie
przyściennej niż w rdzeniu strugi
23.
Termiczne
równanie
czynnika
termodynamicznego
Pośród termicznych parametrów stanu czynnika tylko
dwa mogą zmieniać się niezależnie, natomiast trzeci
jest określony przez pozostałe. Zależność F(p, T, V)
nazywamy termicznym równaniem stanu które
obowiązuje zawsze w przyrodzie, podaje się je jako
wzór, zależność między parametrami lub podaje w
postaci tablic.
24. Opisać efekty energetyczne obiegu silnika
cieplnego, ziębiarki, pompy grzejnej
Silnik – pobiera ciepło Qd ze źródła ciepła o temp T
1
,
wykonuje dodatnią pracę i oddaje ciepło Q
w
do źródła
o temp T
2
<T
1
. Sprawność techniczna silnika jest to
stosunek pracy wykonanej przez silnik do ciepła
pochłoniętego przez czynnik obiegowy. L
ob.
=Q
d
-Q
w
d
w
d
ob
t
Q
Q
1
Q
L
−
=
=
η
;
1
t
>
η
Pompa grzejna – pobiera ciepło Q
d
z otoczenia,
pobiera pracę napędową, oddaje ciepło Q
w
do źródła o
temp wyższej od temp otoczenia. Sprawność to
stosunek ciepła Q
w
oddawanego do ogrzewanej
przestrzeni do pracy napędowej. L
ob.
=Q
w
-Q
d
ob
w
g
L
Q
=
ε
;
1
g
>
ε
Ziębiarka – pobiera ciepło Q
d
ze źródła o temp niższej
od temp otoczenia, pobiera pracę L
ob.
i oddaje ciepło
Q
w
do źródła o temp wyższej od temp otoczenia.
Sprawność to stosunek ciepła Q
d
pobranego do
pracypobranej
25,Co to jest skojarzona gospodarka cieplna.
E
w
= L
w
E
d
= E
w
M
d
>M
w
M
d
<M
w
M
d
=M
w
m
d
>m
w
m
d
<m
w
m
d
=m
w
dx – odległość
przesunięcia
tłoka
Jeżeli:
dv>0 to dl>0
dv<0 to dl<0
L
t
=L
n
+L
1-2
+L
w
+L
1-2
+p
1
v
1
-p
2
v
2
L
n
– praca napełniania
L
1-2
– praca przemiany zamknietej
L
w
– praca wytłaczania
zał. p
1
>p
2
a)
w.z.p. – przemiana
napełniania
b)
z.z.p. – ilość czynnika
= const
1-2 sprężanie izentro.
2-3spalanie p=cons
3-4 rozpr. izentropo.
4-1 wydech izochora,
1-2 sprężanie izentro.
2-3 izochora (spal. wyb.)
3-4 rozpr. izentropo.
4-1 wydech
(izochoryczne oddaw.
ciepła)
m
p
– ilość pary suchej
ilość całkowita pary mokrej
i
nosi
nazwę
średniej
logarytmicznej,
gdyż
zawiera
logarytm różnicy temp na końcu i
początku wymiennika
N
1-2
– ilość cząstek gazu
M
1-2
– masy cząsteczkowe
m
1-2
– masa gazu
Oznaczenie:
czynnik grzejący z indeksem 1
czynnik ogrzewany z indeksem 2
czynnik wprowadzany „prim”
czynnik wyprowadzany „bis”
stąd można obliczyć Q
o
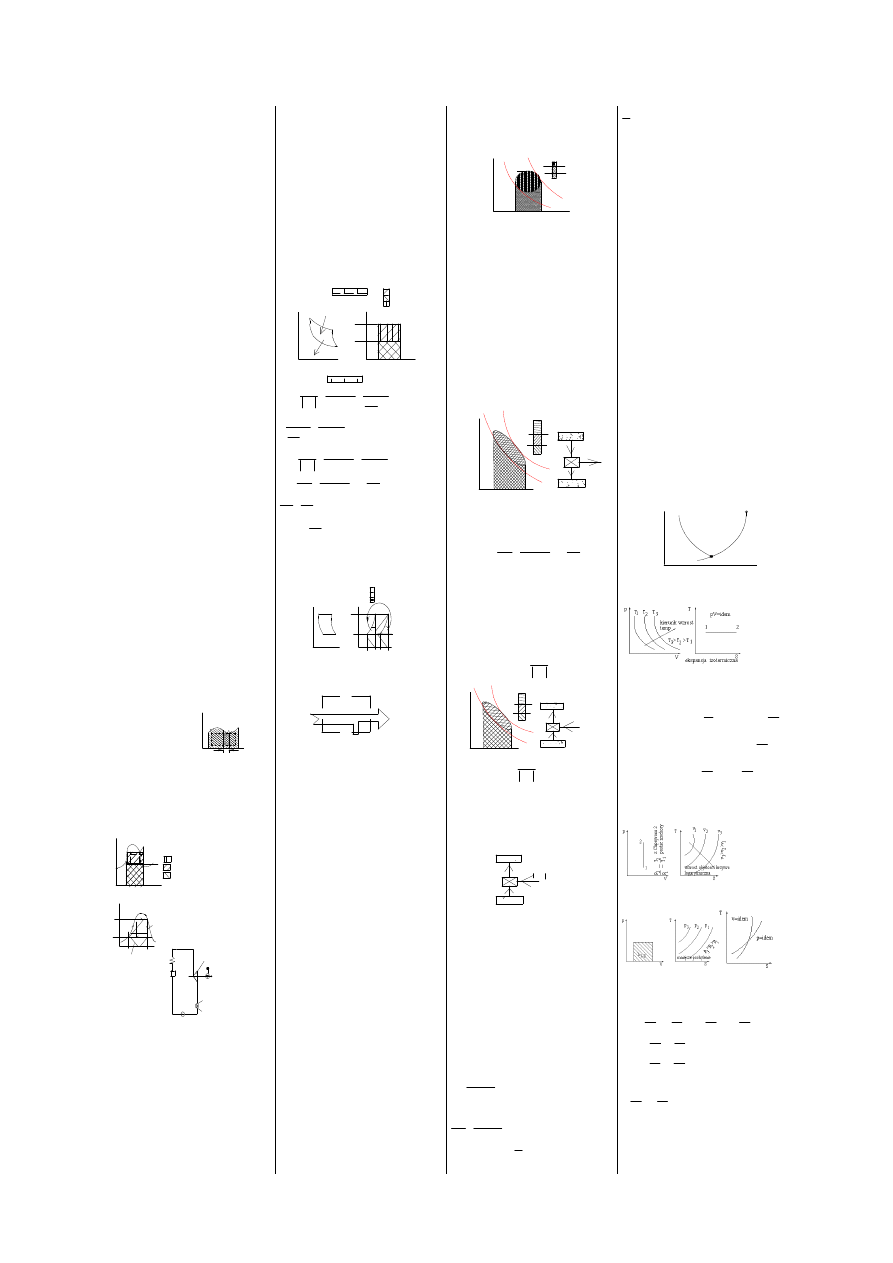
Do ogrzewania pomieszczeń wystarczy czynnik
termodyn o temp 80
0
C , w wielu zaś procesach
przemysłowych potrzebny jest czynnik o temp 150-
200
0
C , taki czynnik a nawet o temp znacznie wyższej
można uzyskać w kotłach parowych. Stosowanie
jednak takiego czynnika do ogrzewania pomieszczeń
powoduje
znaczne
dodatkowe
straty
energii
Unikniemy tego dzięki temu że parę o wysokich
parametrach skieruje się do turbiny przeciwprężnej w
której pary wylotowe mają parametry dogodne do
celów ogrzewczych i jest wykorzystana do pracy. W
ten sposób realizujemy tzw skojarzoną gospodarkę
cieplną. Która polega na równoczesnym wykorzystaniu
pracy (energii elektrycznej) i ciepła grzejnego
doprowadzonego do mieszkań Zakład pracujący w tn
sposób nazywa się elektrociepłownią.
26.Jak oblicza się oszczędność energii uzyskanej w
skojarzonej gospodarce cieplnej.
Sprawność termiczna elektrowni
η
t el
jest to stosunek
wytworzonej mocy elektrycznej do enertgi chemicznej
spalonego paliwa
η
t el
=Nel/(p Wd) Max straty energi
występują w kotle parowym 50%-60% spalonego
paliwa.
27 obieg Braytona.
28. Wady i zalety siłowni turbogazowych
.
ZALETY:
-
możliwość
dobrania
najdogodniejszego
czynnika chłodzącego
-
można zmniejszyć rozmiary agregatu poprzez
zastosowanie podwyższonych ciśnień
-
umożliwia regulację mocy silniki przez
zmianę gęstości czynnika obiegowego
-
ma górną moc graniczną agregatu > niż w
przypadku układu otwartego
-
mogą pracować bez używania wody
WADY
-
konieczność stosowania 2 wymienników
ciepła , zwłaszcza nagrzewnicy narażonej na
wysokie temp
konieczność stosowania sprężarek duże części energii
(aby uzyskać 10 MW musza mieć turbinę 40 Mw gdyż
30 MW na sprężarkę.
29 Zasada zachowania energii
Energia nie może zniknąć nie może powstać z niczego
, lecz może przejść z jednej postaci w drugą i ilość jej
nie może ulec zmianie w układzie zamkniętym i
izolowanym układ jest niezmienny niezależnie od
zmian zachodzących w układzie.
Σ
E=0
30.Co to jest energia wewnętrzna
Energia wewnętrzna U jest to całkowia energia
odniesiona do układu osi współrzędnych mających
początek w środku masy ukł i umieszczonych tak że
energia ruchu obrotowego =0. Z enrgi układu E
u
można wyróznić energię potencjalną Ep + energię
kinetyczna Ek + energię wewnętrzną U
Eu=Ek+Ep+U
Głównymi składnikami U są:
Jest to parametr stanu gdyż zależy od stanu czynnika.
Zawiera w sobie różne rodzaje energii chem, sprężystą
itd.
Energia wewn właściwa u=U/m (intensywny parametr)
31.Przedstawić całkowite ciepło pochłonięte przez
czynnik termodynamiczny w ukł T-S
Całkowite ciepło które zostało pochłonięte przez
czynnik można obliczyć za pomocą wzoru
Qc1-2=
∫
2
1
Tdy
Jnterpretacja graficzna : ciepło pochłonięte w czasie
przemiany odpowiada pole zawarte nad linią
przemianową 1-2 i osią
32 Siłownia parowa
To przede wszystkim turbiny parowe Tłokowe silniki
W których (para jest sprężona do niskiego ciśnienia w
dyszy i uzyskuje Ek Strumień pary o dużej prędkości
skierowany do kanałów łopadkowych wirnika i
przepływa powodując obrót wirnika i wykonuje pracę)
Silnik parowy pracuje w układzie zamkniętym z
innymi urządzeniami tworząc tzw siłownie. W siłowni
nie można zrealizować obiegu Carnota.
3-4 tzw sprężenie wody z ciśnienia za skraplacza do
ciśnienia w kotle
Ciecz podgrzewana izobarycznie w kotle do temp
wrzenia
powstają
pęcherzyki
pary
i
dalsze
podgrzewanie
do
odparowania
cieczy.
Proces
odparowania to proces izobaryczno izotermiczny do
stanu pary nasyconej suchej w turbinie w punkcie 1
Następnie para przepływa do turbiny i rozpręża się w
niej izentropowo do punktu 2 Następnie rozprężona
para trafia do skraplacza w którym przepływająca
woda powoduje skroplenie pary w przemianie
izobarycznej 2s-34.
Jm wyższa temp dolotu i niższa temp wylotu to
sprawność rośnie
Obieg pary przegrzanej kondensacyjnie
η
tCR
=l
CR
/gd
Zpary nasyconej suchej w przegrzewacza pary i
izobary temp rośnie w/g właściwości konstrukcyjnych
elementu.
η
tCR
= lepsze :- rośnie temp i ciśnienie
odtwarzanie obiegu Carnota
stopniowanie turbiny
rozsunięcie T
obniżenie
ciśnienia
końcowego
rozpręzania zależność od wody
chłodzącej skraplak tw1)
33. Obieg Carnota obieg o max sprawności
1-2 izotermiczna ekspansja następuje pobór ciepła
2-3 izentropowa ekspansja
3-4 kompresja izotermiczna następuje oddanie ciepła
4-1 kompresja izentropowa
I
II
TC
I
II
tc
I
II
II
gc
I
II
I
I
II
ZC
T
T
T
T
Qd
Qw
Qd
Qw
Qd
Qw
Qd
Qd
Lob
T
T
T
Qd
Qw
Qw
Lob
Qw
T
T
T
T
T
Qd
Qw
Qd
Qw
Qd
Lob
Qd
−
=
=
−
=
−
=
=
−
=
−
=
=
−
=
−
=
=
−
=
−
=
=
1
1
1
1
1
1
η
η
ε
ε
34. Uogólniony obieg Carnota
Dotyczy siłowni parowych – zamiast przemian
izentropowych zastosowano dwie dowolne przemiany
Równoległe do siebie. Regeneracja ciepła polega na
przekazaniu ciepła między dwoma strumieniami ciepła
tego samego czynnika
η
te
=1-(qk/gc)
35 Co to jest bilans energetyczny
Wypływa
z
zasady
zachowania
energii
Ed=
∆
Eu+Ew[J] dla strumienia wszędzie jest kropka
i[J/s].Energia częściowo doprowadzona do układu Ed
jest częściowo zużyta na zmianę energii układu
∆
Eu
oraz częściowo jest wyprowadzona. Ew.Zas zach
energii wynika z obserwacji zjawisk zachodzących w
przyrodzie i doświadczeń
Energia nie może zniknąć nie może powstać z niczego
, lecz może przejść z jednej postaci w drugą i ilość jej
nie może ulec zmianie w układzie zamkniętym i
izolowanym układ jest niezmienny niezależnie od
zmian zachodzących w układzie.
Σ
E=0
36 Wyjaśnij dlaczego praca i ciepło nie mogą być
traktowane za postaci energii
Praca i ciepło nie są postaciami energii mimo Ze ich
ilość mierzy się tymi samymi metodami jednostkami
co ilość energii. Energia jest bowiem własnością
materii jest funkcją stanu układu. Praca i ciepło
przestają istnieć w chwili zakończenia zjawiska-
wykonania pracy czy przepływu ciepła. Pozostaje po
nich tylko skutek tych zjawisk.
37 Jak określa się skład chem paliw
Skład chem paliw stałych określa się za pom udziałów
gramowych oznaczonych małymi literami:c,h,s
Paliwo składa się z substancji palnej i balastu (w
paliwach stałych i ciekłych – popiół i wilgoć a w
gazowych CO
2
oraz para)
a) paliwa gazowe –za pomocą udziałów molowych
(objętościowych)poszcególnych
składników.Udział
molowy składnika w suchym gazie palnym oznacza się
wprost jego symbolem chem sumą tych udziałów jest 1
Przy spalaniu paliw gazowych za jednostkę ilości
substancji przyjmuje się 1 kmol suchego gazu palnego
b) stałe i ciekłe paliwa – udziały gramowe oznaczając
małymi literami alfabetu. Jednostką ilości paliwa
stałego lub cieklego jest 1kg paliwa wilgotnego. Ilość
substancji poszczególnych składników w jednostce
substancji paliwa wyrażają wzory
n
`
c+s
=c/12+s/32 kmol(c+s)/kgpal
Skład paliwa ciekłego i stałego jest sumą udziałów
gramowych = 1.Określamy 1 min zapotrzebowania na
tlen O
N
min=
c/12+h/4+s/32-0/32 [(kmolO
2
)/(kgpal)]
2 Min powietrza n
lpow
=n
smin
/0.21 [kmol pow/kgpal]
zawsze dajemy więcej n
lpow
λ
=rzeczywista ilość pow(n`l)/teoretyczna ilość
pow(n`lmin)
Wartość opałowa Wd[J/kg]ilość ciepła doprowadzona
z komory spalin po zupełnym i całkowitym spaleniu
jednostki paliwa jeżeli spalenie odbyło się pod stałym
ciśnieniem spaliny zaś zostały ochłodzone do temp
początkowej substratów przy czym para wodna
zawarta w spalinach nie uległa skropleniu.
Ciepło spalania[Wg]- ilość ciepła doprowadzona z
komory spalin po zupełnym i całkowitym spaleniu
jednostki paliwa jeżeli spalenie odbyło się pod stałym
ciśnieniem spaliny zaś zostały ochłodzone do temp
początkowej substratów przy czym para wodna
zawarta w spalinach uległa skropleniu.
Wd=Wg-m``
H2O
*r
H2O
r- ciepło skraplania
pary
38. Jaką przemianę nazywamy obiegiem termod.
Obieg termodynamiczny jest to przemiana w której
stan
końcowy
czynnika
jest
identyczny
z
początkowym. Wykresem (obrazem obiegu) jest
krzywa zamknięta . W każdym wykresie możemy
określić 4 charakterystyczne punkty
a)
dwa punkty zwrotne I II i dzielą one krzywą
na linię ekspansji i kompresji
b)
dwa punkty adiabatyczne i i dzielą one
krzywe na części podczas której czynnik
pochłania ciepło i część podczas której oddaje
ciepło.
Ciepło dostarczane pobrane przez czynnik z zewnątrz
w czasie obiegu ozn Qd, zaś oddawane Qw sa one > 0.
39. Co to jest obieg prawo i lewo bieżny
a)
obieg prawobieżny – jest obiegiem silnika
Qd > Qw
Założenie T I > T II
Silnik pobiera ciepło Qd ze źródła o temp wyższej ,
wykonuje pracę i oddaje ciepło Qw do (otoczenia ) o
temp niższej Sprawność termiczna silnika
Qd
Qw
Qd
Qw
Qd
Qd
Lob
t
−
=
−
=
=
1
η
b)
obieg lewobieżny – jest to obieg ziębiarki lub
pompy grzejnej
sprawność termiczna ogólnie
lewobnieżny
Qw > Qd
η
t
=efekt użyteczny urządzenia/Qd
Chłodnica pobiera ciepło Qd o temp niższej niż temp
otoczenia T II otrzymuje pracę /Lob/ i oddaje ciepło
Qw do źródła o temperaturze wyższej(otoczeniu)
Lob=Qw-Qd
Sprawność ziębiatrki
1
≥≤
=
Lob
Qw
L
ε
Spraw termiczna
1
≥
=
Lob
Qw
g
ε
Pompa grzejna pobiera ciepło z otoczenia Qd
otrzymuje pracę i dostarcza ciepło Qw do żródeł o
temperaturze wyższej od temp otoczenia
Obiegi odwracalne składają się tylko z przemian
odwracalnych . Równanie bilansu (czy obieg jest czy
nie jest odwracalny ) ma postać Qd-Qw=Lob
40.
Definicje
Clausiusa,
Plancka,
Smitcha,
Ostwalda, Entropia
Patrz punkt drugi
41. Prawa dla gazu doskonałego
1)
Boylea Mariottea
Jeżeli w
τ
=idem to p*V=idem
2)
GayLussaca- Charlesa
Jeżeli p= idem to objętość właściwa to objętość
właściwa V=V
0
(1+T
α
);V/T=idem
V
0
-obj.wł gazu w temp 0
0
C
α
-termiczny wsp rozszerzalności objętości gazu
odniesiony do obj V
0
jest ustalony eksperymentalnie
(1/273,15) *(1/K)
Założymy że t=idem
( )
( )
)
1
(
)
0
(
)
(
)
1
(
0
0
0
0
0
0
0
0
0
0
0
t
C
f
t
f
t
p
C
f
p
t
f
idem
p
p
C
f
V
C
f
V
p
C
dla
t
f
V
p
+
•
•
=
+
•
=
=
=
=
•
=
•
α
α
α
)
(
*
*
*
)
0
(
*
)
(
)
15
,
273
(
1
0
Clapeyrona
anu
równaniest
Ttermiczne
R
V
p
C
f
R
T
R
t
f
T
t
=
=
=
≡
+
=
α
α
p-stałe ciśnienie bezwzgl [N/m
2
]
V- objętość właściwa [m
3
/kg]
R-indywidualna stała gazowa [Nm/kgK]
T-temp benzyny
3)
Awogadra
liczba
drobin
zawartych
w
jednakowej
objętości
różnych
gazów
doskonałych w tych samych warunkach
termicznych (temp i ciśnienie gazów jest takie
same)
(MR) jedn indywidualnej stałej gazowej 8314
[J/kmolK]
R=(MR)/M
M
1
*R
1
= M
2
*R
2=
M*R
P*V=R*T⇒p(MV)=MR*T
P*V=m*R*T⇒p*V=n(MR)*T
MV;(MR)
≡
(B)nie zależy od rodzaju gazu
n,m- masy
42. Co to jest punkt krytyczny i potrójny
Jest to punkt równowagi trzech faz (stałej, ciekłej,
gazowej)substancji.
Podczas przejścia cieczy ze stanu ciekłego w
parowy.Zakładając że mamy zamknięte naczynie
(cylindr tłok)z cieczą dostarczając temperaturę przy
p=idem ciecz uzyskuje coraz wyższą temperaturę aż do
momentu osiągnięcia tzw zmiany stanu skupienia
polegającym na powstaniu fazy gazowej w całej
objętości cieczy w postaci pęcherzyków parowych
(wrzenie)- zależy dla określonej cieczy wyłącznie od
ciśnienia. Jeżeli dalej będziemy dostarczać ciepło to
temp będzie się utrzymywać na stałej wartości,
natomiast będzie coraz więcej pary, gdy ciecz
całkowicie odparuje to nastąpi wzrost temp pary.Faza
gazowa mająca kontakt z wrzącą cieczą (temp wrzenia)
to tak zwana para nasycona-para nasycona i ciecz są w
tak zwanym w stanie równowagi trwałej i dla danej
cieczy jest funkcją ciśnienia.Stąd mamy krzywą
nasycenia Zależność ciśnienia nasycenia p od temp
nasycenia.
43.
Przemiany
(gazów
doskonałych
i
pół
doskonałych)
a) izotermiczny- jest przemianą, w której stała jest
temperatura czynnika
*
∫
=
−
2
1
2
1
pdv
L
- praca bezwzględna
mając funkcję p od V p
1
v
1
=p
2
v
2
⇒ p=p
1
v
1
/v ponieważ
p
1
v
1
jest stałe
1
2
1
1
2
1
2
1
dt
dv
1
1
2
1
v
v
ln
p
v
L
v
p
L
=
⇒
∫
=
−
−
robimy podst. V
2
/V
1
=p
1
/p
2
2
1
1
1
2
1
p
p
ln
v
p
L
=
⇒
−
*
2
1
1
1
2
1
p
2
1
1
1
2
1
t
p
p
ln
v
p
p
d
v
p
vdp
L
=
∫
∫
−
=
−
=
−
L
t1-2
=L
1-2
ciepło Q
1-2
=L
1-2
=L
t1-2
jeżeli dv>0 rozprężanie
L
1-2
>0 ; Q
1-2
>0 jeżeli dv<0 sprężanie L
1-2
<0 ; Q
1-2
<0
b)izochoryczny V=idem
p=idem ; v=idem
* L
1-2
=0 * l
t1-2
=V(p
1
p
2
) chcąc sprężyć trzeba
doprowadzić pracę z wewnątrz która jest ujemna
Ciepło Q
1-2
=V
2
-V
1
=m(u
2
-u
1
)=mc
v
(T
2
-T
1
)
c) izobaryczna p=idem
* L
t1-2
=0
* L
1-2
=p(v
2
-v
1
)
*Q
1-2
=I
2
-I
1
=m(i
2
-i
1
)=mc
p
(T
2
-T
1
)
d) adiabatyczna odwracalna – dQ=0 bez wymiany
ciepła z otoczeniem jest przemianą izentropową
*
p
d
R
c
d
R
c
d
v
v
ln
c
p
p
ln
c
c
p
d
cv
s
p
v
v
d
p
s
v
v
d
T
T
d
v
s
1
2
p
1
2
v
v
v
d
p
p
+
=
+
=
+
≡
+
=
jeżeli dQ=0 ⇒ d
s
=0 bo d
s
=d
q
/
τ
0
c
p
d
cv
v
v
d
p
p
=
+
równ. różniczk. adiab. odwrac.
χ
=c
p
/cv ;
χ
=d
v
/v+d
p
/p=0 ⇒
χ
lnv+lnp=0 ;ln(pv
χ
)=0
χ
-wykładn. adiabaty
ds
T
1
dQc
S
2
1 gw
2 Lob=L
CR
3
gd
T1
T2
T
1
1
kociol
turbina
2s
34
λ=0
S
λ=1
2
3
skraplacz
obieg RANKINEA
pompa
kociol
generator
T
Ne
energii
elektr
skraplacz
tw2
tw1
Ni
turbina
silownia parowa
x=0
T
1
x=1
s
2
Lcr
gw
gd
3
T2-idem
V
S
T1=idem
T
1
2
3
4
Qd
Qw
Lob
p
1
Qd
4
Qw
2
V
S
T
Qd
Qw
p
1
2
3
4
3
T1
T2
1
2
4
gr cieplo regen
g regeneracji
os lona jes t w s polna dla
s ubs tancji i energii
Ed
∆
Eu
Ew
A 2
A !
V
p
I
L obiegu
L kompresji
II
Lexp-
p
I
Q w
T II
A I
V
Lob
T I
A II
II
Lk
Lex
Lob
Q d
T I
T I < T II
V
p
I
Lob
A II
A I
II
Lex
Lk
T II=T0
Qd
Qw
Lob
Qd
T I<T II
TI=T0
T II
Qw
Lob
CIECZ
CIA£O
STA£E
p
PARA
T
K
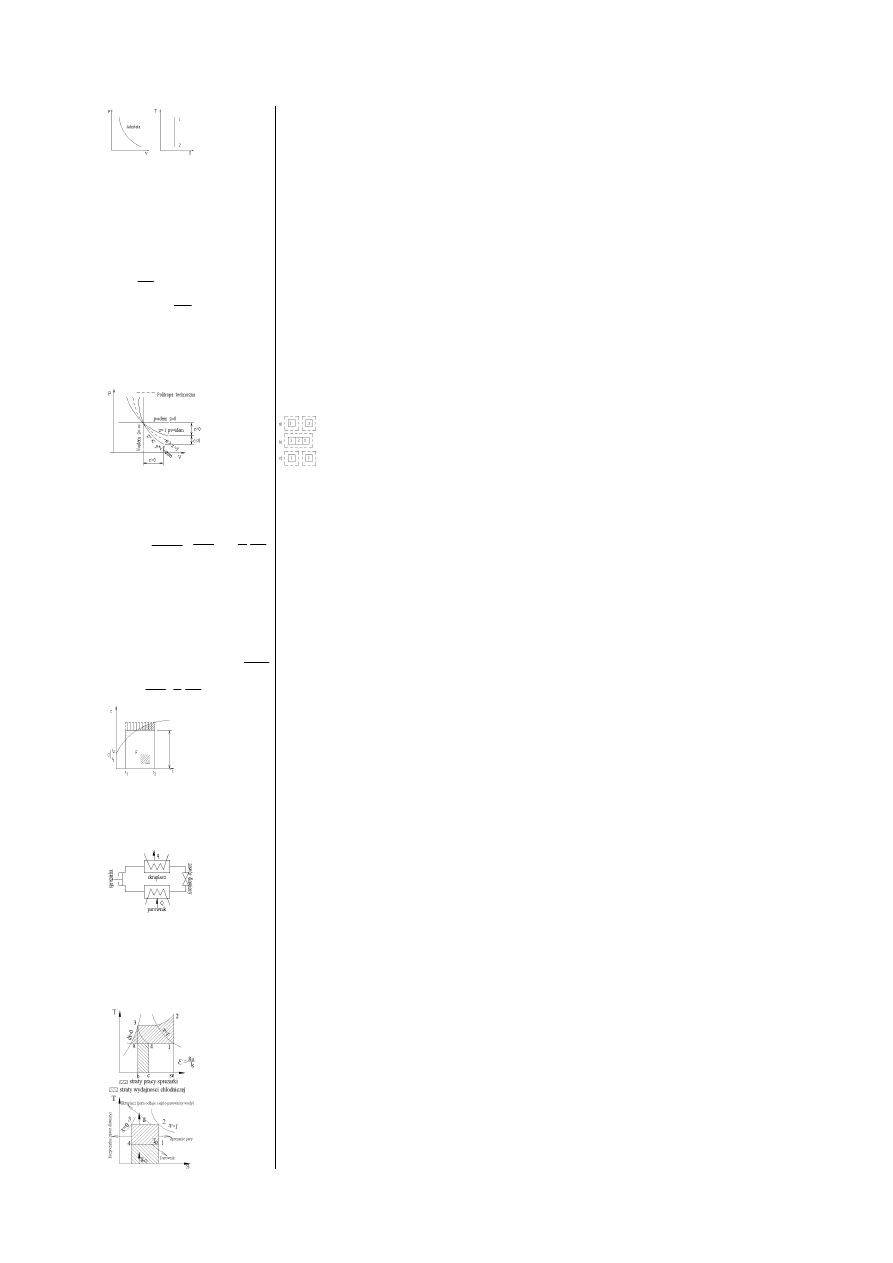
* L
1-2
=c
v
(T
1
-T
2
) ; * L
t1-2
=
χ
L
1-2
e) Politropa- przemiana w której ciepło właściwe jest
równe c=d
q
/d
τ
=idem ; z- wykładnik politropy
44. Co to jest równowaga termodynamiczna?
Jest to taki stan, który ustala się samorzutnie w
układzie
odizolowanym
od
oddziaływań
sił
zewnętrznych i pozostaje niezmienny w czasie czyli
gdy parametry stanu tego układu nie ulegają zmianie w
czasie. Spełnione są trzy warunki równowagi:
a) równowaga termiczna
b) równowaga chemiczna
c)równowaga mechaniczna
45.Ciepło właściwe politropy
1
z
R
C
C
v
−
−
=
natomiast z Capeyrona i równ.
χ
otrzymujemy
1
z
z
C
C
v
−
χ
−
=
Ciepło właściwe politrpy
może mieć wartość zarówno dodatnią jak i ujemną
Przy 1<z<
χ
to C<0
Sens fizyczny C<0; mimo doprowadzono ciepła temp.
czynnika obniża się lub mimo odprowadzonego ciepła
temp. czynnika podwyższa się. Przemiany gdy C<0
często zachodzą w praktyce np. przy sprężaniu
czynnika w sprężarce, przy rozprężaniu adiabatycznym
odwracalnym
46. Co to jest ciepło właściwe i od czego zależy?
Całkowite ciepło przejęte przez ciało o masie m
podczas podgrzewania od T
1
do T
2
jest równe ciepłu
dostarczonemu z zewnątrz i ciepłu tarcia (ciepło
wewnątrz ciał) Q
c 1-2
=Q
1-2
+Q
f
przy czym
)
t
t
(
CI
m
Q
1
2
2
t
1
t
2
1
c
−
⋅
=
−
przekształcając
wg.
)
t
t
(
m
Q
CI
CI
1
2
2
1
c
2
t
1
t
2
t
1
t
−
=
⇒
−
K
kg
J
⋅
)
dt
dQ
(
m
1
C
c
=
α
Średnie ciepło właściwe
2
t
1
t
CI
jest to ilość ciepła jaką
należy dostarczyć jednej jednostce ilości substancji,
aby
zmienić
temperaturę
o
1K
w
całym
rozpatrywanym okresie temp. Zależy od:
a)
rodzaju ciała
b)
temperatury t
1
t
2
c)
warunków ogrzewania ciał
Stosunek C
p
/C
v
=
χ
Jeżeli mam ciało masie m i
podgrzewam od t do
∆
t+t to nastąpi przyrost ciepła
∆
Q
c
)
t
(
m
Q
CI
c
t
t
t
∆
⋅
∆
=
∆
+
dt
dQ
t
m
Q
)
t
(
C
c
m
1
c
lim
0
t
⋅
=
∆
⋅
∆
=
→
∆
2
t
1
t
CI
-rośnie wraz ze wzrostem t i jest wysokością
prostokąta o szerokości (t
2
-t
1
). F pole figury
nieregularnej równe polu prostokąta o wysokości.
Wielkości ciepła właściwego C i szerokości t
2
-t
1
.
Pole
figury F=(t
2
-t
1
)*c
47. Wpływ zaworu dławiącego na pracę ziembiarki
Ziembiarka z zaworem dławiącym- schemat
Zawór dławiący- jest urządzeniem stosowanym w
ziębiarce umożliwiającym spadek ciśnienia od wartości
panującej w skraplaczu do wartości panującej w
parowniku (skroplona ciecz zostaje zdławiona do
odpowiedniego
ciśnienia).
Przemiana
dławienia
odbywa się przy stałej 3-4 entalpi, ponadto obieg z
zaworem dławiącym jest nie odwracalny ze względu
na nie odwracalność przemiany dławienia. Ponadto
również występują straty energetyczne (nie odbiera się
pracy sprężarki oraz zmniejsza się wartość wydajności
chłodniczej g
0
.
Obieg suchy-
∆
od Carnotta ⇒ sprężanie zachodzi e
obszarze pary przegrzanej dzięki (osuszaniu między
parownikiem a sprężarką ⇒ para sucha nasycona)
(osuszacz odbiera krople cieczy od pary suchej
nasyconej)
48. Co to jest dławienie?
Jest to przemiana w której czynnik termodynamiczny
ekspanduje dv (wzrasta) i rozpręża się d
p
(maleje), nie
wykorzystując przy tym pracy. Przemiana ta ma
miejsce gdy czynnik natrafia na przegrodę w postaci
zmieniającego
się
przekroju,
zmiany
kierunku
przepływu, zmianę prędkości.
49. Co to jest równanie przemiany?
Jest to zależność pomiędzy parametrem stanu. Dla
każdej przemiany można podać 3 równania.
Przemiany mogą być odwracalne lub nieodwracalne
Przemiany mogą być zamknięte lub otwarte
Otwarta przebiega przy zmiennej ilości substancji
50. Podać równowagę stanu gazu doskonałego i
półdoskonałego?
pV= RT- równanie stanu gazów doskonałych
pV= mRT ; p [N/m
2
] ; V [m
3
/kg] ; R [Nm/kgK] ; T [K]
51. Zerowa zasada termodynamiki
Jeżeli dwa ciała 1 i 2 są w stanie równowagi termicznej
z 3 są one także w równowadze między sobą.
52. Zdefiniować i podać zast. i sposób oblicze. straty
wylot i napełnienia sprężarki
?
Strata wylotowa- temp. spalin wypływających do
otoczenia jest większa niż temp. otoczenia. Ciepło
unoszone do otoczenia przez spaliny q
w
.
w
*
w
*
s
t
o
t
2
puO
2
s
t
o
t
2
puCO
2
s
t
o
t
pui
ri
s
t
o
t
puss
n
V
`
ss
``
ss
o
s
s
t
o
t
O
2
puH
``
O
2
H
o
s
s
t
o
t
puss
``
ss
w
o
s
s
t
o
t
puss
``
s
w
q
B
Q
...
I
C
]
O
[
I
C
]
CO
[
I
C
I
C
)
H
(
n
V
)
t
t
(
I
C
V
)
t
t
(
I
C
V
q
)
t
t
(
I
C
V
q
⋅
=
+
+
⋅
=
∑
=
=
−
⋅
+
−
⋅
=
−
⋅
=
B
*
- ilość spalonego paliwa
Równanie Pecleta
.
(
)
2
1
f
f
t
t
k
A
Q
−
⋅
=
•
k- współczynnik przenikania ciepła [ W / m
2
K ]
straty wydajności
chłodniczej l
t
=l
s
-l
r
s- sprężanie
r- rozprężanie
Parownik (skropiony
czynnik odparowuje
pobierając
ciepło
osiąga stan określony
punktem 1)
a)t
1
różne od t
2
b) t
1
=t
2
=t
3
c)t
1
=t
3
d
v
=0, d
p
=0
E
v
=m(i+w
2
/2)
i
1
+w
1
2
/2=i
2
+w
2
2
/2
w<40 m/s
2
przyjmujemy
E
k
strugi i
1
=i
2
Wyszukiwarka
Podobne podstrony:
prezentacja dobra id 390418 Nieznany
(Sciaga silniki dobra)id 733 Nieznany
ABC dla dobra dziecka id 50115 Nieznany (2)
dobra praktyka hig obozy id 138 Nieznany
Abolicja podatkowa id 50334 Nieznany (2)
4 LIDER MENEDZER id 37733 Nieznany (2)
katechezy MB id 233498 Nieznany
metro sciaga id 296943 Nieznany
perf id 354744 Nieznany
interbase id 92028 Nieznany
Mbaku id 289860 Nieznany
Probiotyki antybiotyki id 66316 Nieznany
miedziowanie cz 2 id 113259 Nieznany
LTC1729 id 273494 Nieznany
D11B7AOver0400 id 130434 Nieznany
analiza ryzyka bio id 61320 Nieznany
pedagogika ogolna id 353595 Nieznany
więcej podobnych podstron