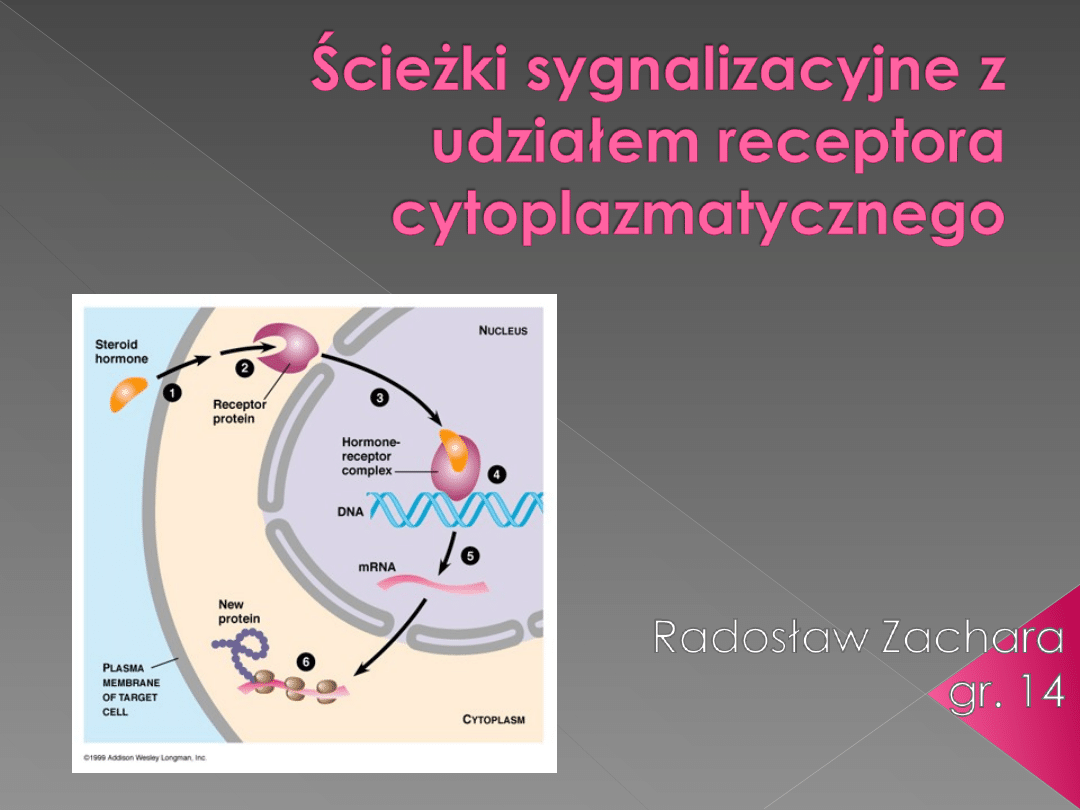
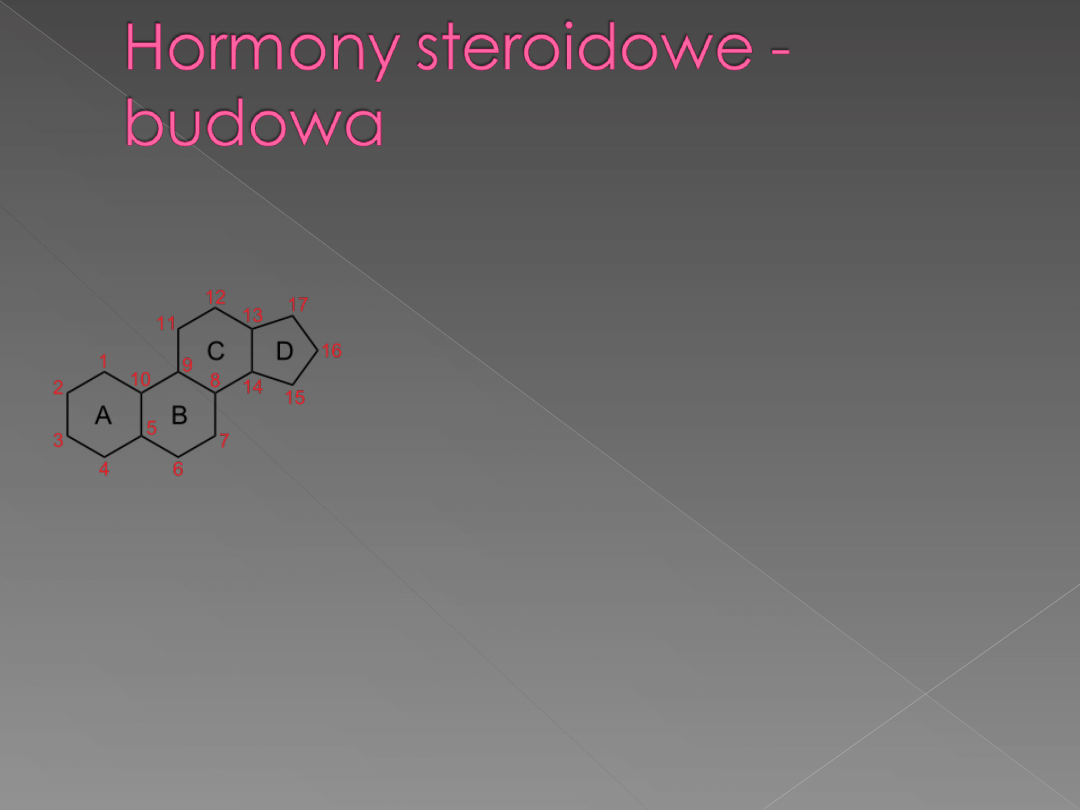
Budowa
hormonów
steroidowych oparta jest na
szkielecie węglowym w
formie czterech sprzężonych
pierścieni, czyli na steranie.
Hormony
sterydowe
są
małocząsteczkowymi
hormonami, które bez trudu
przenikają
przez błonę
komórkową i
dla
których receptory znajdują
się w jądrze komórek, na
które oddziałują.
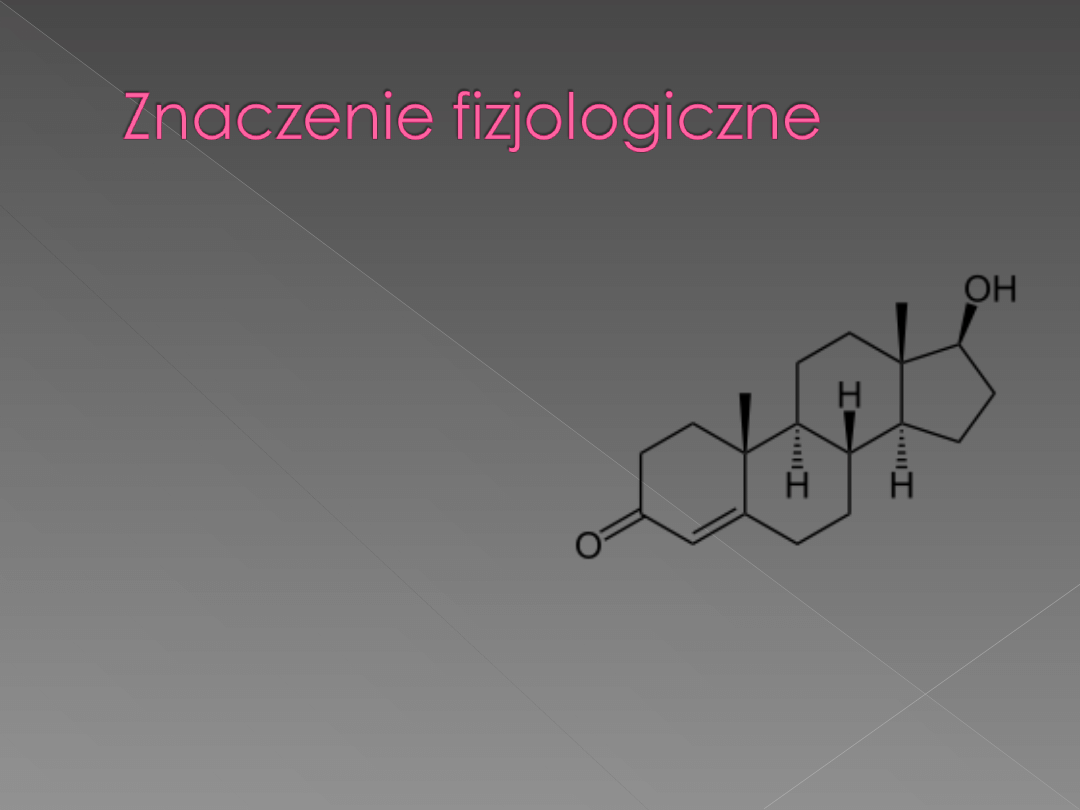
Androgeny – działanie
maskulinizujące:
kształtowanie się
męskich narządów
płciowych w życiu
płodowym
wykształcanie się
wtórnych cech
płciowych
wpływ
na spermatogenezę
wpływ anaboliczny
(zwiększenie masy
mięśniowej itp.)

Estrogeny - nazywane hormonami żeńskimi i
najważniejszą rolę odgrywają
w organizmie kobiet, ale są też niezbędne
dla mężczyzn - ich niedobór w jądrach może
powodować bezpłodność. Regulują gospodarkę
lipidową, wapniową. U kobiet regulują również
cykl miesiączkowy (estradiol).
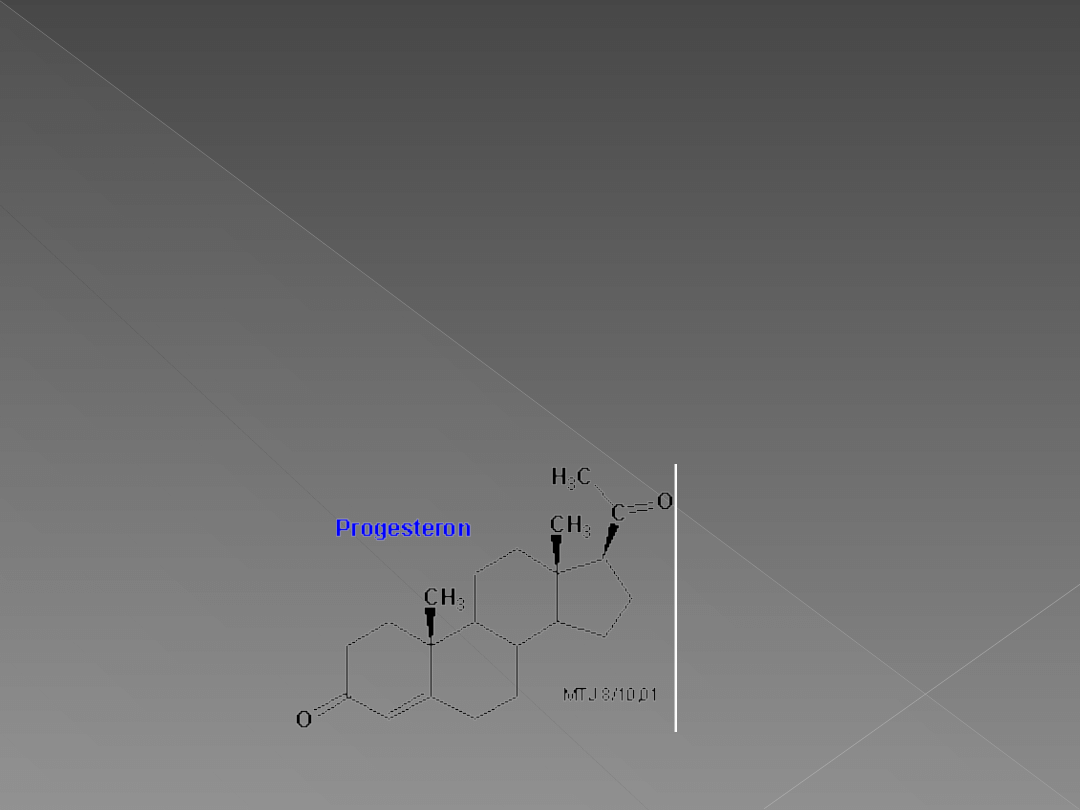
Gestageny – grupa hormonów
steroidowych, które służą
przygotowaniu organizmu do zajścia a
następnie utrzymania ciąży. Głównym
przedstawicielem gestagenów jest
progesteron

Mineralokortykoidy -
hormony wytwarzane w organizmie
człowieka przez warstwę
kłębkowatą kory nadnerczy. Wpływają
na nieorganiczną przemianę materii i
zachowanie równowagi elektrolitowej
ustroju.

Glikokortykoidy – hormony produkowane
w warstwach pasmowatej i
siatkowatej kory nadnerczy pod
wpływem ACTH, które regulują
przemiany białek, węglowodanów i
tłuszczów.
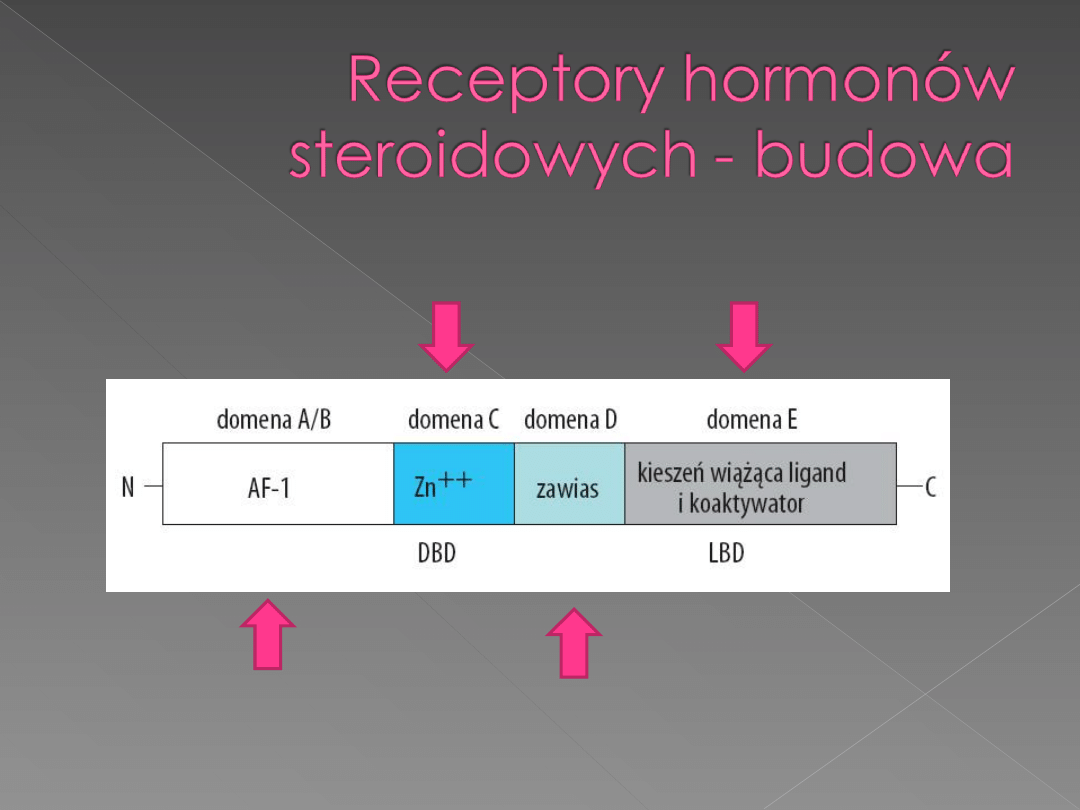
Wysoce zmienna domena
aktywacyjna, koniec NH2
Konserwatywna domena,
oddziałuje z DNA, motyw
palców cynkowych
Domena wiążąca
hormon
Region niekonserwatywny o
zmiennej długości

Zaktywowane receptory hormonów
steroidowych wiążą się ze
specyficznymi sekwencjami DNA, tzw.
elementami odpowiedzi
hormonalnej (HRE). Elementy
odpowiedzi na hormon regulują
ekspresję sąsiadujących genów oraz
inne miejsca kontroli transkrypcji.

HRE dzieli się na 4 klasy:
- GRE - element odpowiedzi
glikokortykoidów, wiąże on też receptory
AR, PR, MR;
- ERE - element odpowiedzi estradiolu;
- TRE - element odpowiedzi hormonu
tarczycy, do którego przyłącza się również
receptor RAR;
- D R E - ostatnią grupę stanowi sekwencja,
która wiąże „receptory sieroce” (receptory
białek o nieznanej funkcji i ligandach).

Podczas nieobecności liganda większość
receptorów ER, PR, AR zlokalizowanych
jest w cytoplazmie, a kompleks
receptor-hormon migruje do jądra
komórkowego, aby modulować
ekspresję genów. Są to receptory
klasy I, w których białko HSP zakrywa
domenę NLS (Nuclear Localization
Signals)
Receptory klasy II: GR, MR, TR, RAR
występują w jądrze niezależnie od
obecności liganda, nie posiadają białek
opiekuńczych.
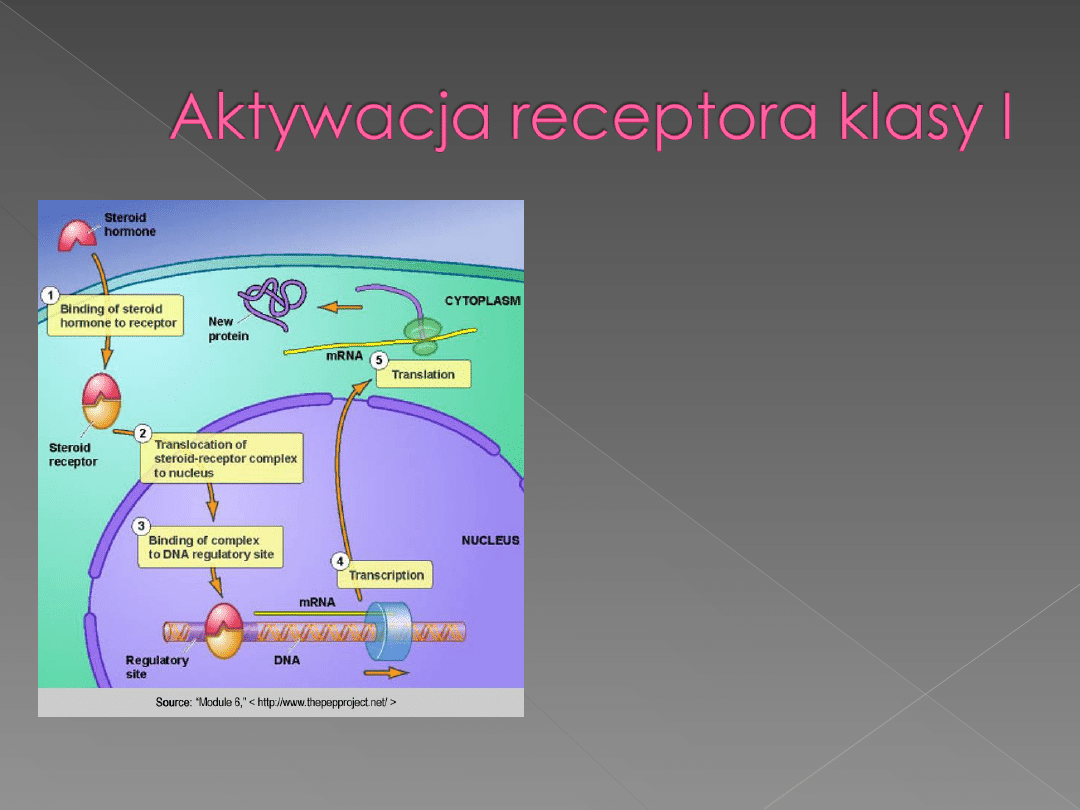
Związanie liganda przez
receptor skutkuję
zmianą jego
konformacji
przestrzennej (często
dimeryzację
receptora) i
oddysocjowanie od
HSP90 w cytoplazmie.
Kompleks receptor-
ligand jest
translokowany do
jądra stymulując
transkrypcję.

Receptory te (np. GR, MR, TR, RAR) są
zlokalizowane w jądrze komórkowym i
nie posiadają białek HSP. Aktywacja ich
przez ligand stymuluje proces
transkrypcji tak jak w przypadku
receptorów klasy I.

Receptory jądrowe hormonów
steroidowych są przykładem białek
transregulatorowych transkrypcji.
Wchodzą one w interakcję z czynnikami
transkrypcyjnymi (z polimerazą RNA II)
i stabilizują czynniki wiążące w pobliżu
promotora. Ten sposóbinterakcji
cząsteczek steroidowych receptorów
jądrowych nazywa się transaktywacją
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
Wyszukiwarka
Podobne podstrony:
prezentacja ścieżki sygnalizacyjne z udziałem receptora błonowego
prezentacja ścieżki sygnalizacyjne z udziałem receptora błonowego
przesyłanie sygnału przez receptory fcgamma
Receptory klasyfikacja, budowa i szlaki tworzenia sygnałów ( 10 2010
Polimorfizm enzymów, receptorów i innych białek biorących udział w mechanizmie działania leków
Zamiana sygnału chemicznego na elektryczny w błonie postsynaptycznej
Sygnały klasyfikacja
Receptura zbiorczy GWSH 2
Antagoniści receptora histaminowego H1
Agoni Ťci receptor w alfa i beta adrenergicznych
mam Udzial w zapobieganiu chorobom
2010 05 Kombajn sygnałowy DDS
C Receptury Wydanie II cshre2
więcej podobnych podstron