
• Druga po urazach przyczyna
zgonów wśród dzieci do 14 roku
życia
• 105-130 nowych zachorowań na 1
mln. dzieci
• W Polsce ponad 1000 nowych
zachorowań rocznie

Przyczyny zgonów wśród dzieci do 14
roku życia
Wypadki 44%
Nowotwory 10%
Wady wrodzodzone 8%
Choroby serca 4%
Zapaleniah płuc 2%
Zapalenia opon 1%

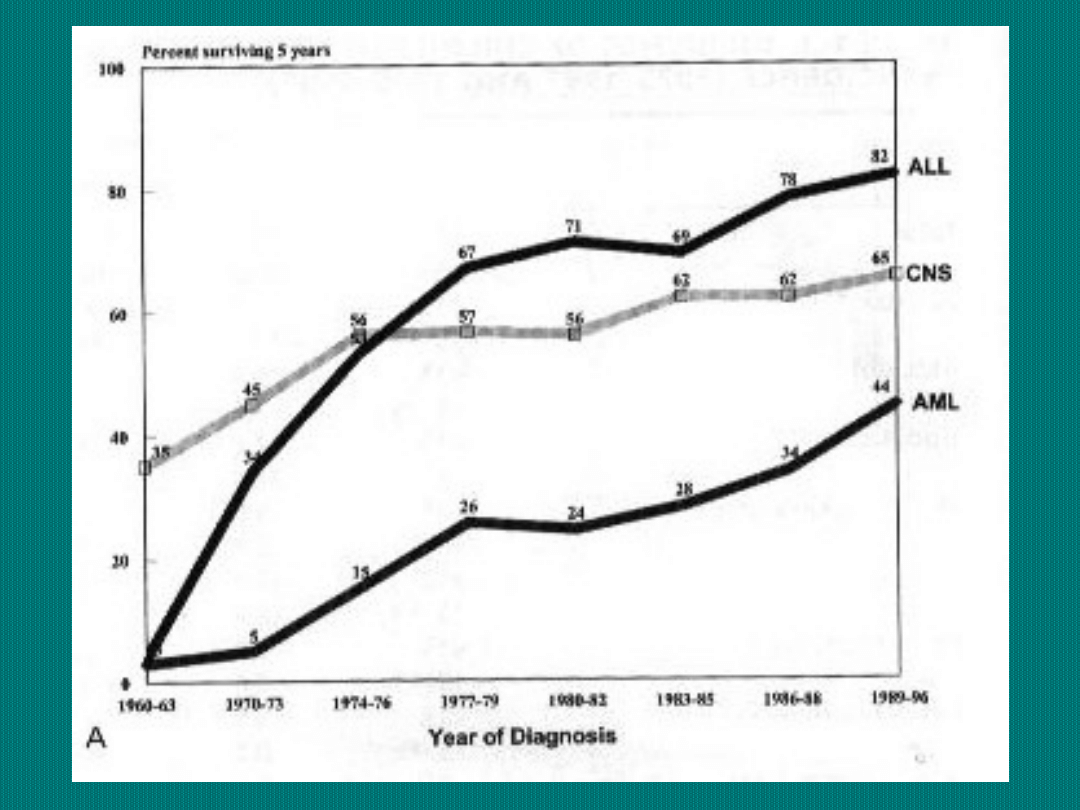
Odsetki 5-cio letnich przeżyć wśród dzieci
chorych na nowotwory
1960
1970
1980
1990
HD
57%
65%
80%
90%
ALL
3%
15%
63%
70%
Chłoniaki
20%
25%
50%
62%
AML
0%
0%
18%
38%
Guz Wilmsa
33%
65%
78%
82%
RMS
18%
33%
62%
65%
Guzy mózgu
10%
45%
53%
55%
Mięsak Ewinga 10%
20%
42%
55%
Osteosarcoma
20%
25%
38%
55%
Retinoblastoma 78%
81%
86%
86%

Częstość występowania poszczególnych
nowotworów dziecięcych w Polsce
Nowotwór
%
Białaczki
28
Chłoniaki
14
Guzy mózgu
18
Nowotwory układu nerwowego współczulnego
7
Nowotwory nerek
7
Nowotwory kości
8
Nowotwory tkanek miękkich
7
Nowotwory gonad i zarodkowe
5
Siatkówczak
2
Nowotwory wątroby
1.5
Nowotwory nabłonkowe
1.5
Inne
<1
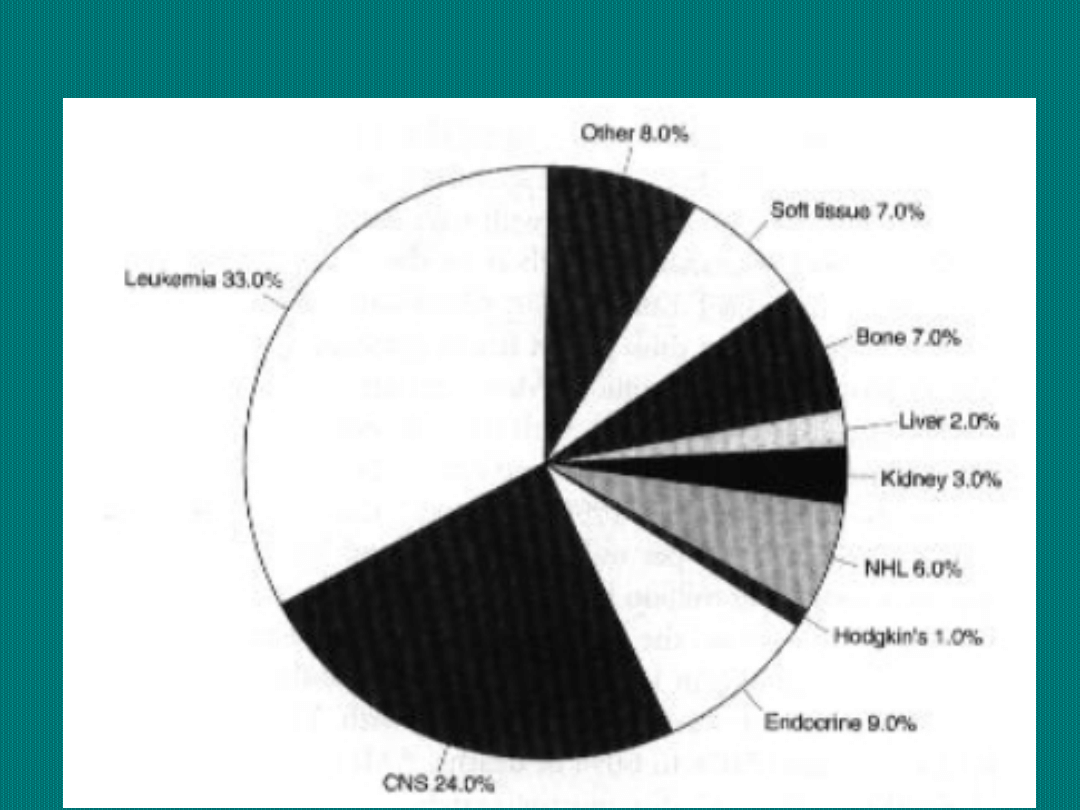
Częstość występowania poszczególnych nowotworów
dziecięcych w USA
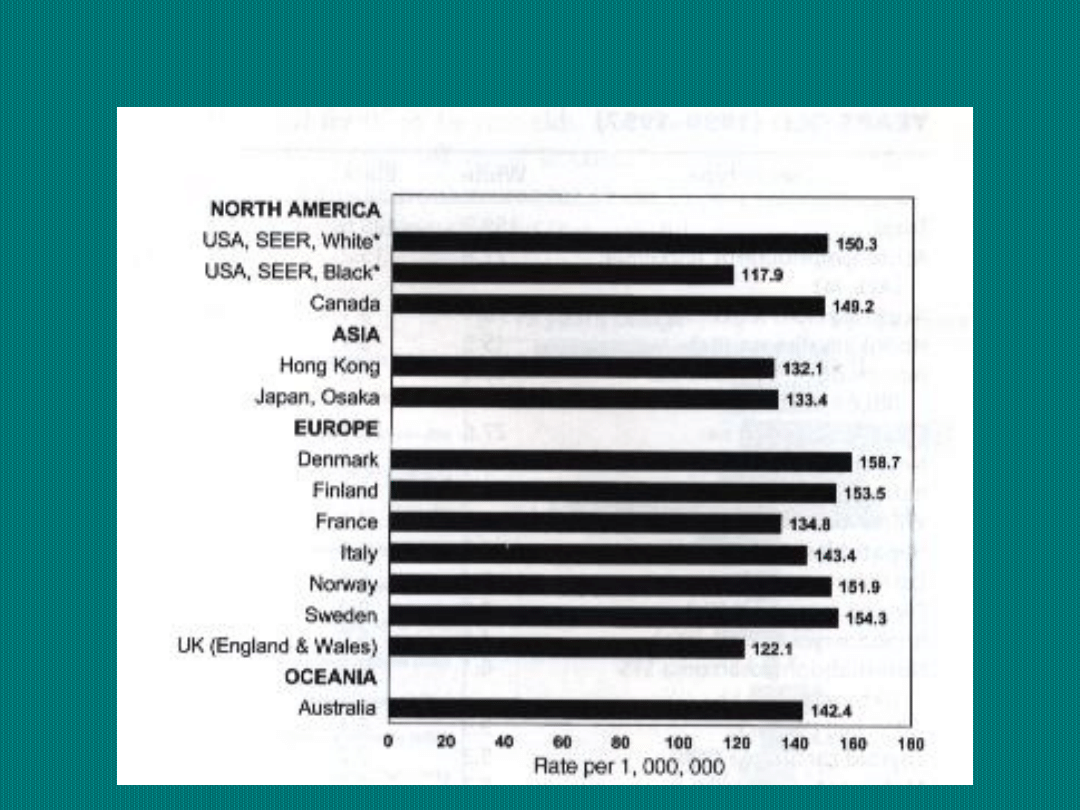
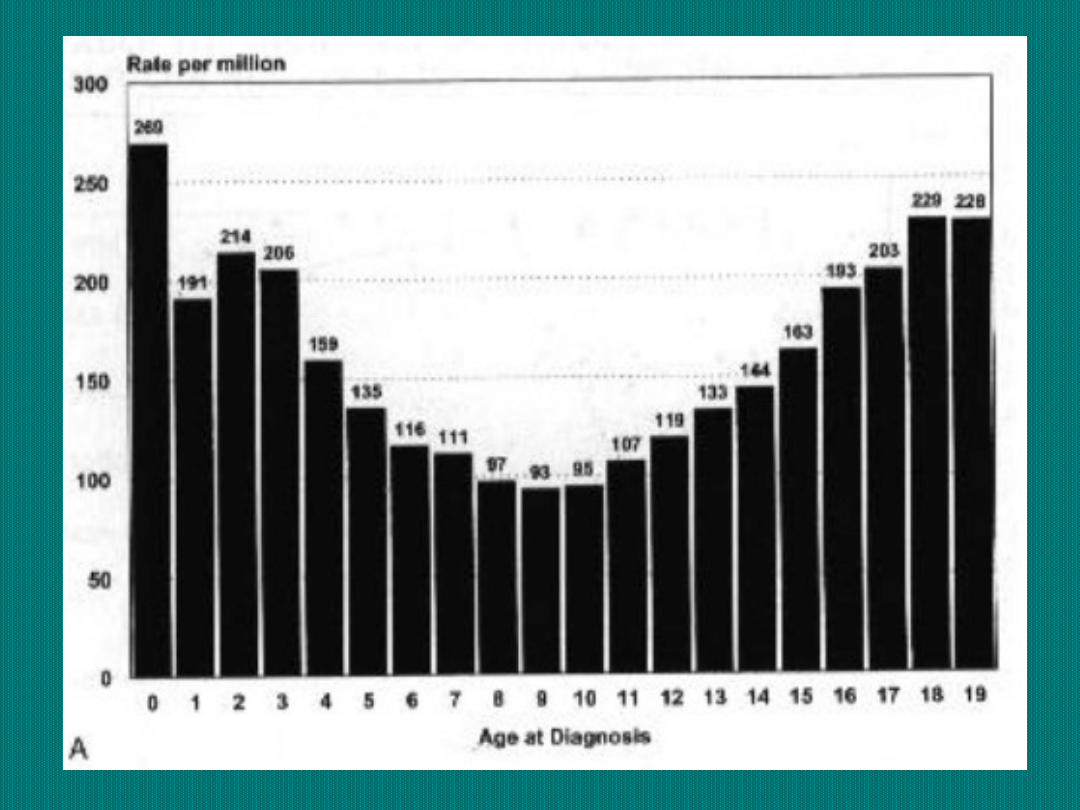
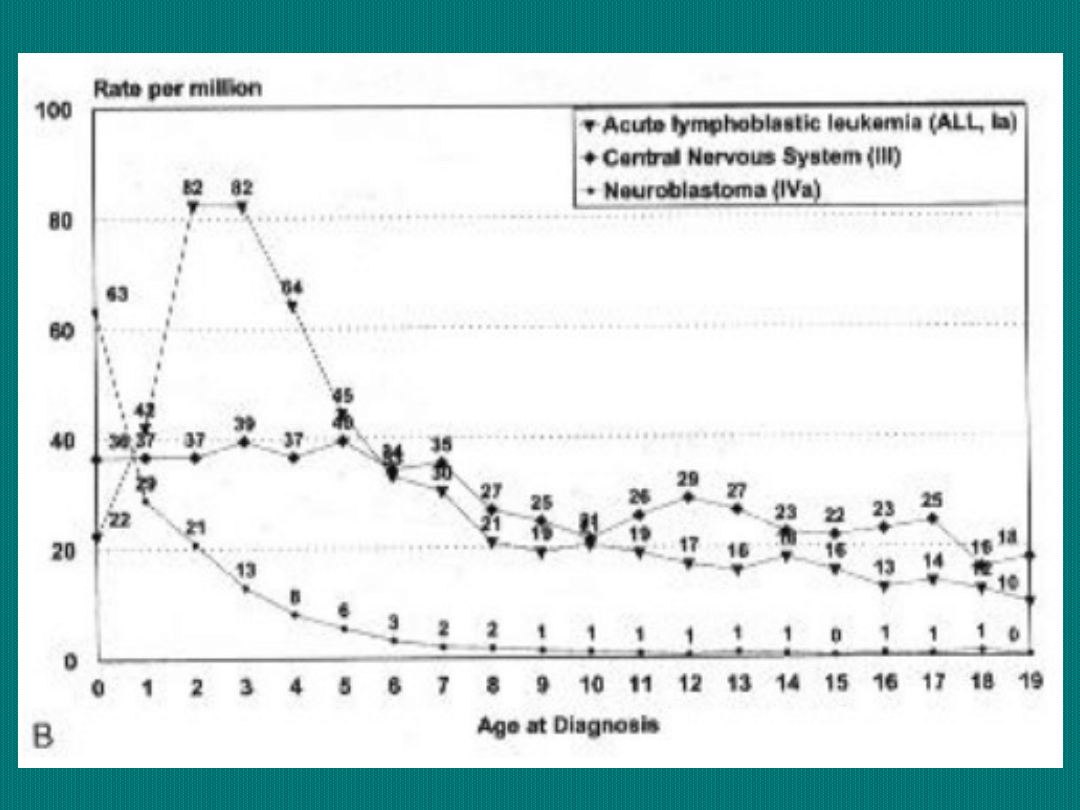
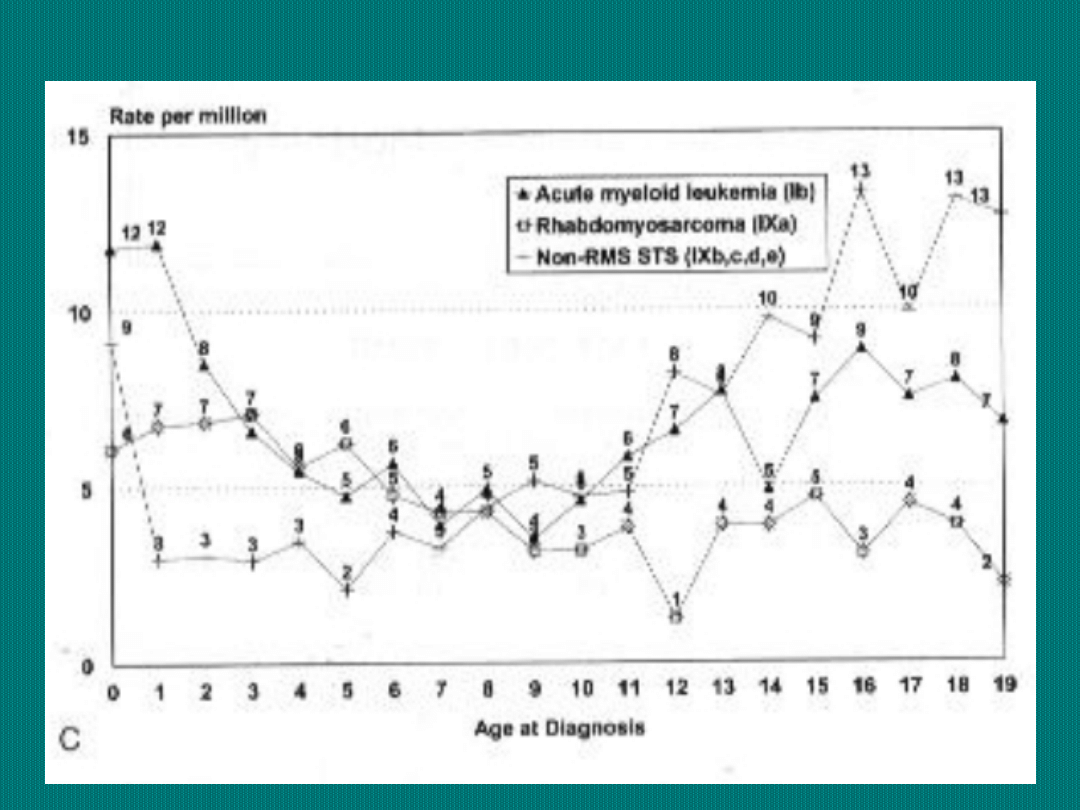
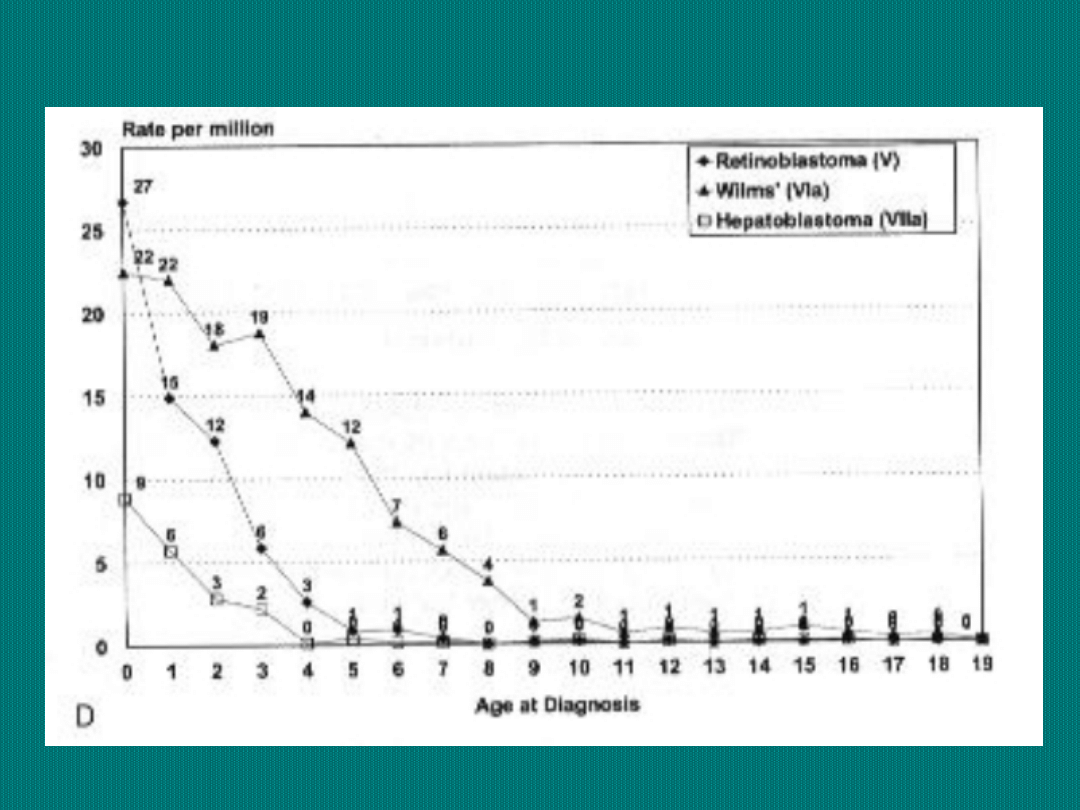
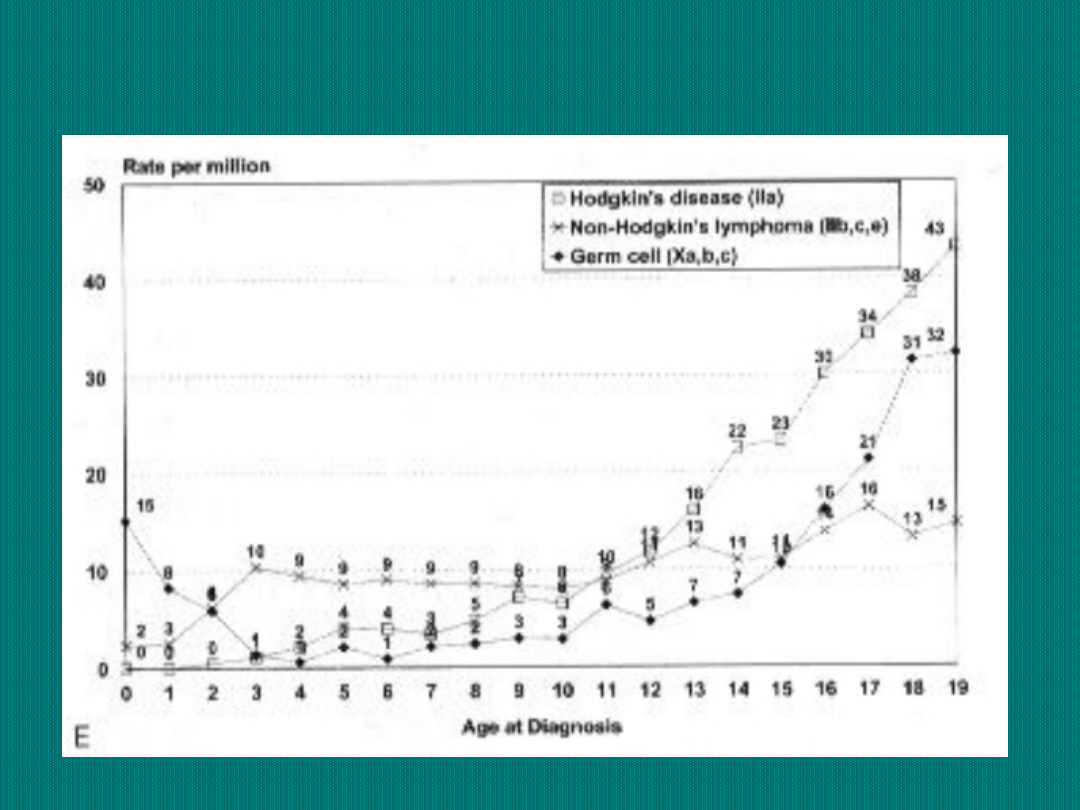
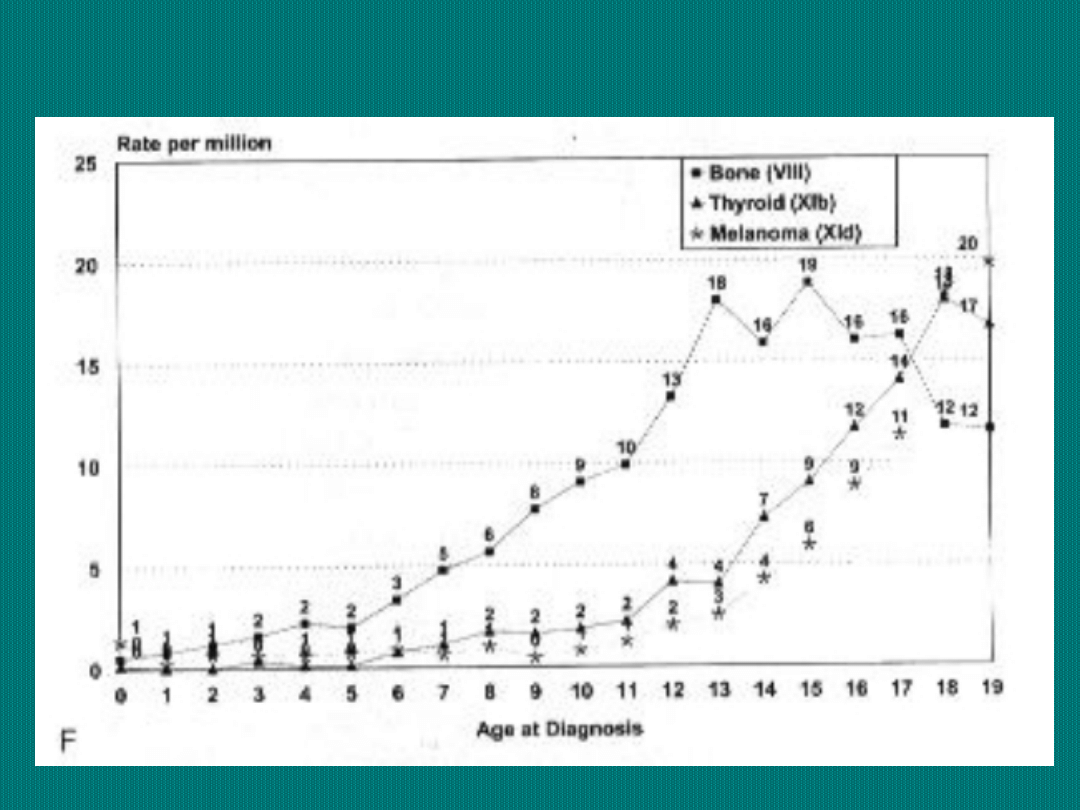
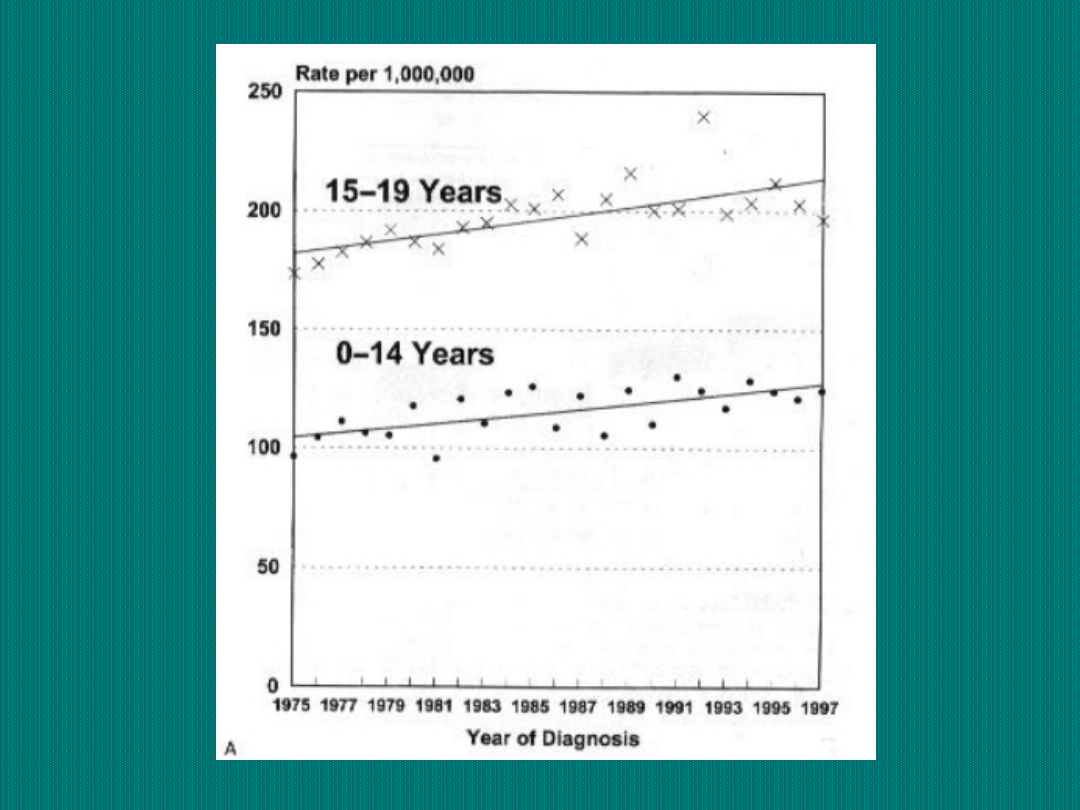
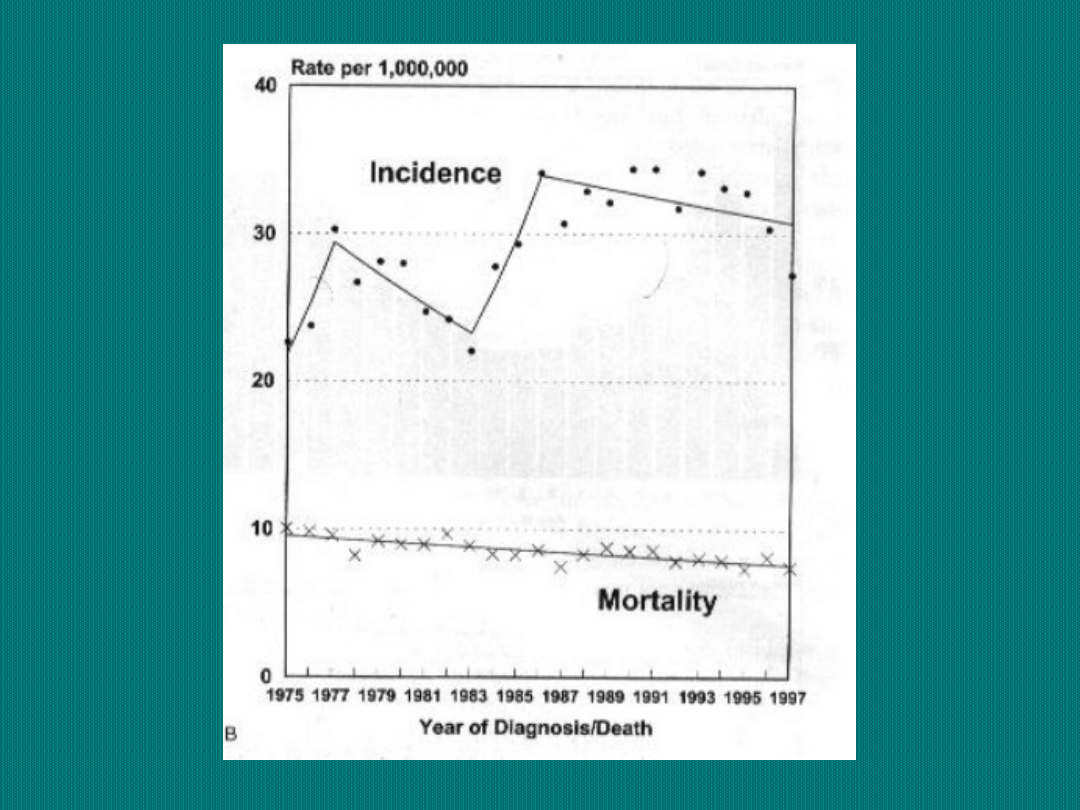
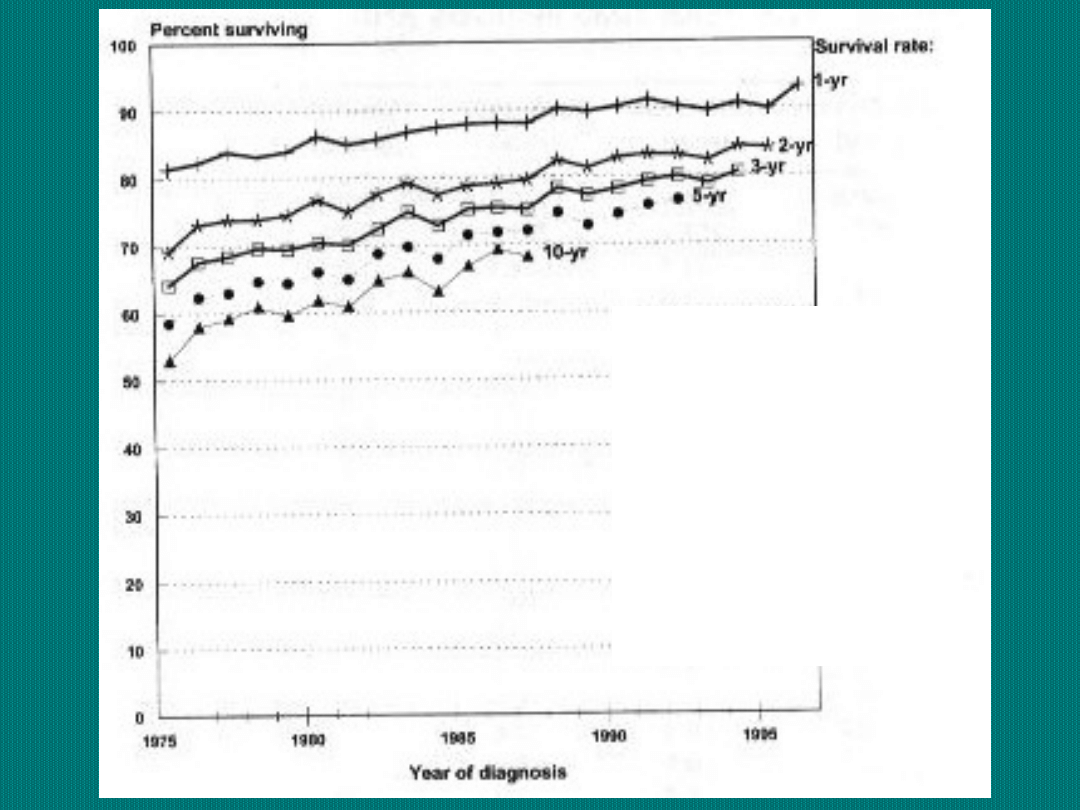
Odsetki 1, 2, 3, 5
i 10-cio letnich
przeżyć wśród
dzieci chorych na
nowotwory
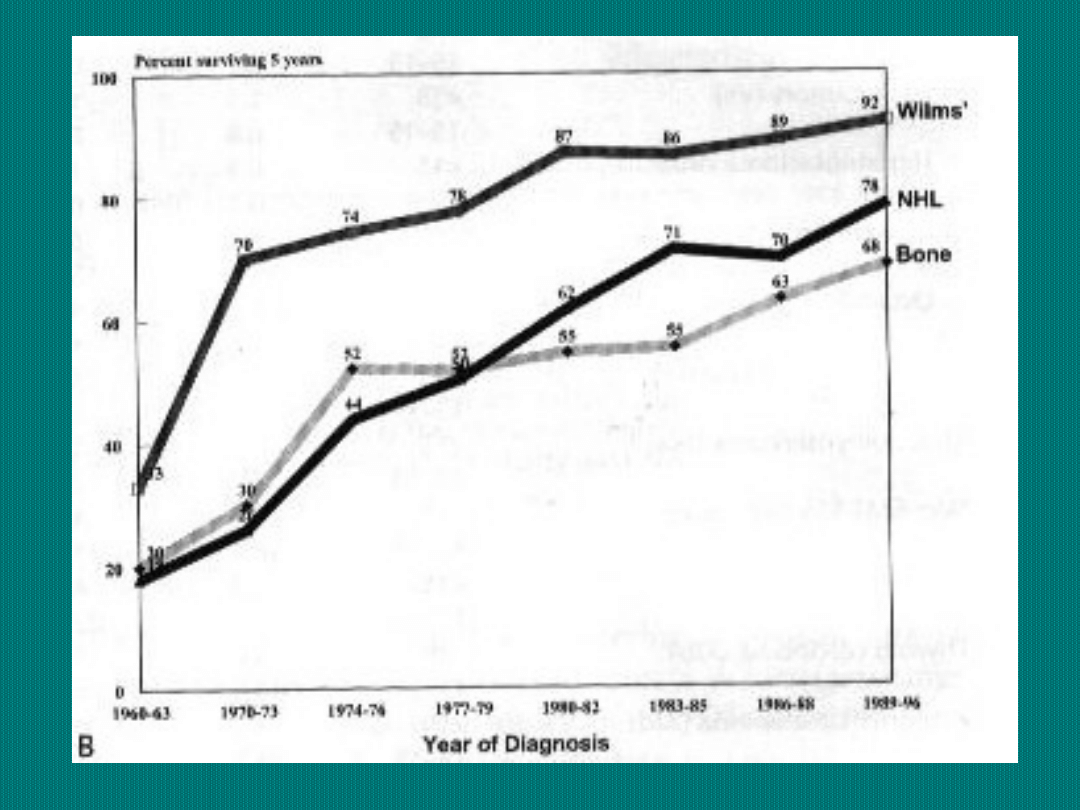
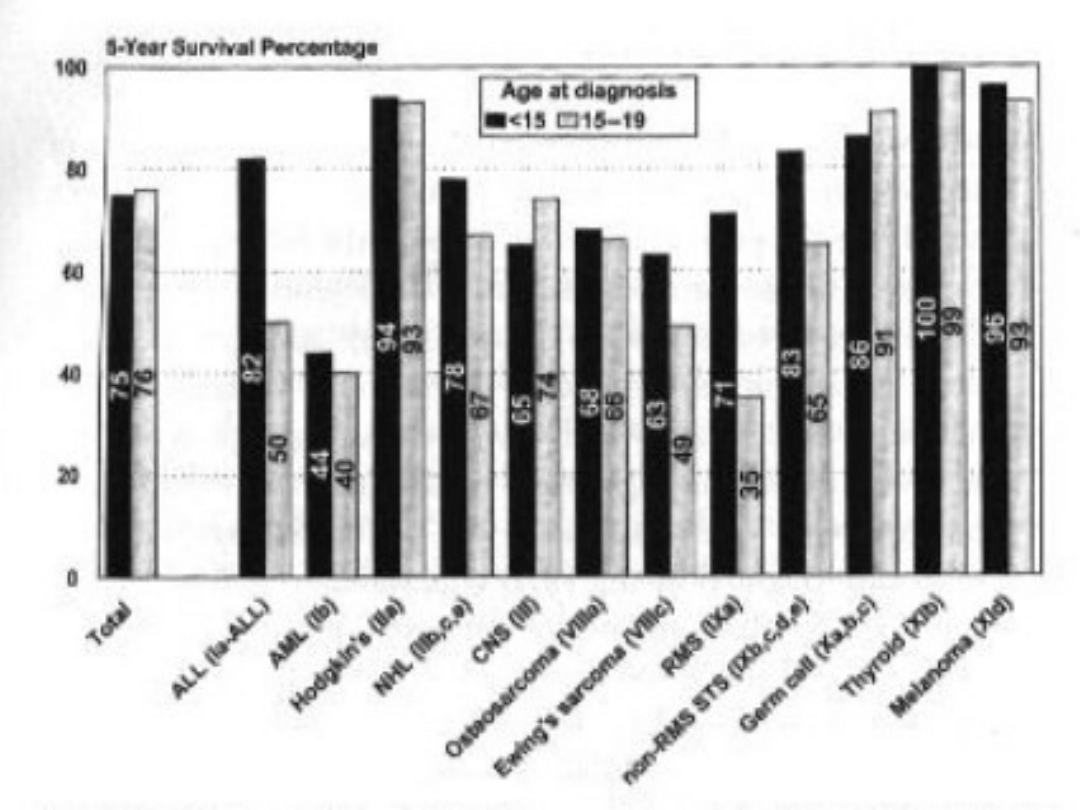
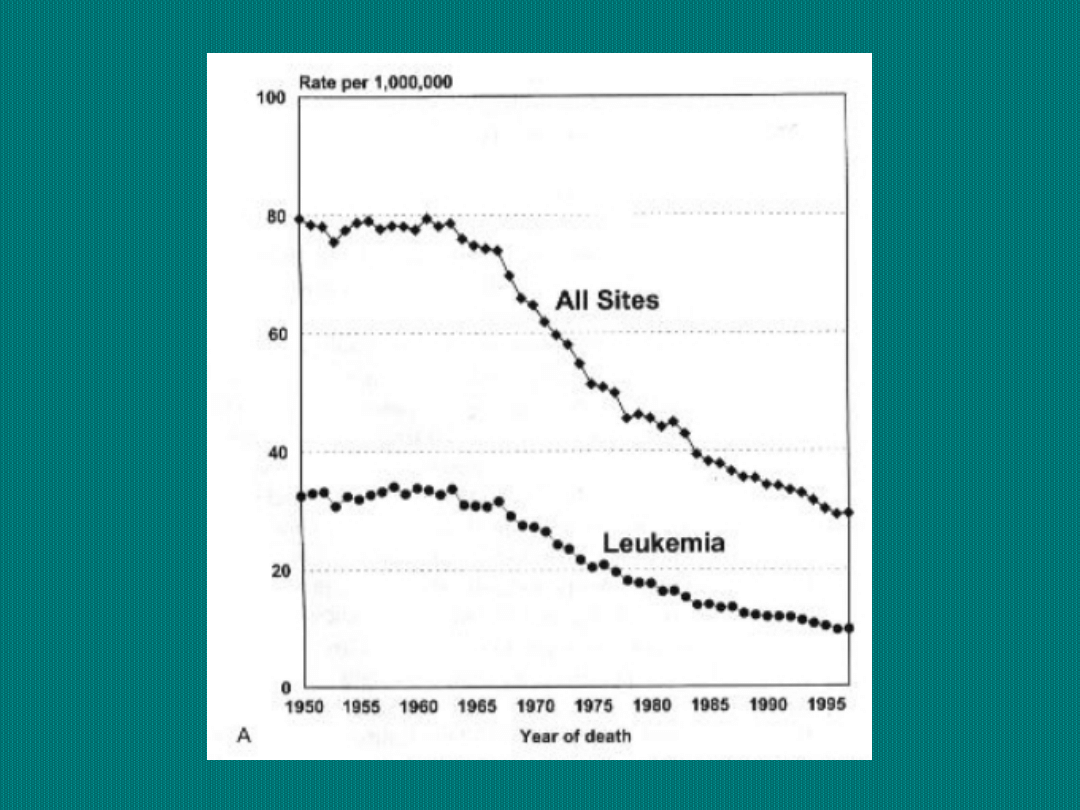
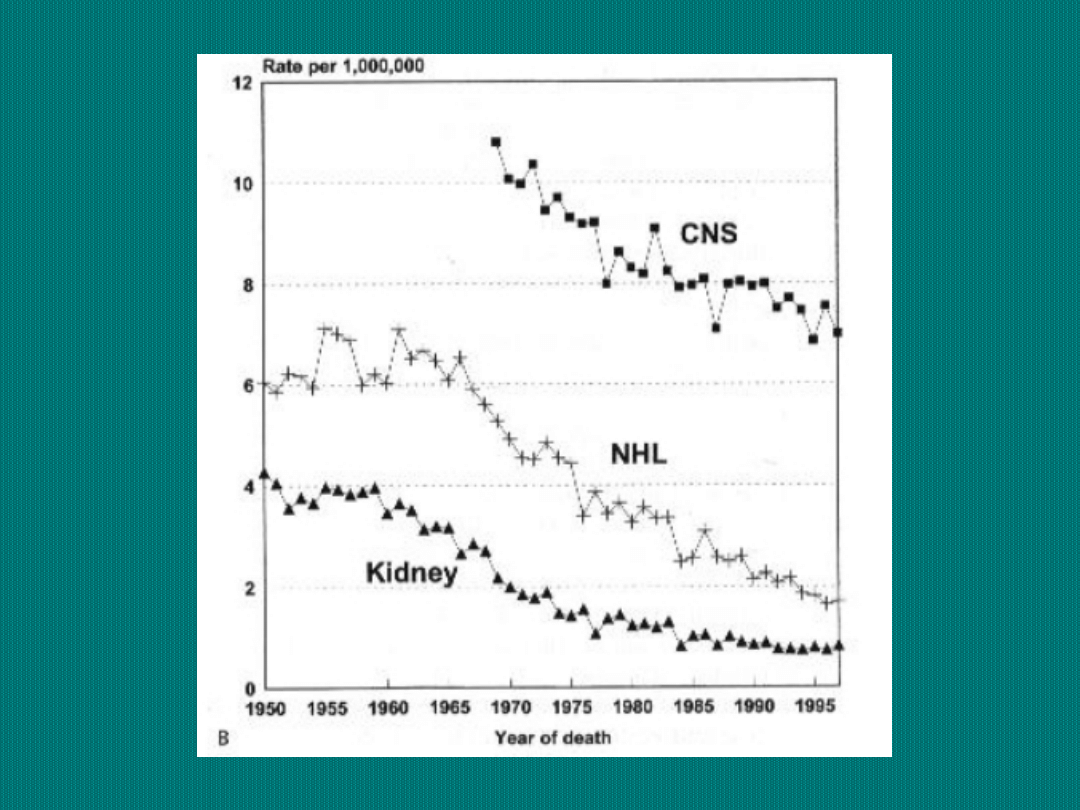

Odsetek zachorowań dziedzicznych
Glejaki nerwu wzrokowego 45%
Retinoblastoma 40%
Pheochromocytoma 25%
Guz Wilmsa 3%
Nowotwory OUN 1%
Białaczki 2.5-5.0%

ALL
• Promieniowanie jonizujące
• Rasa biała
• Czynniki genetyczne
- zespół Downa
- zespół Blooma
- ataxia telangiectasia
Czynniki ryzyka

AML
• Cytostatyki (leki alkilujące, epidophyllotoxyny)
• Czynniki genetyczne:
- zespół Downa
- NF1
- rodzinna monosomia 7
Czynniki ryzyka

Guzy mózgu
• Radioterapia
• Czynniki genetyczne:
- NF1
- TS
Czynniki ryzyka

osteosarcoma
• Radioterapia
• Chemioterapia – leki alkilujące
• Czynniki genetyczne
- zespół Li-Fraumeni
- dziedziczna postać retinoblastoma
Czynniki ryzyka

NHL – wrodzone i nabyte niedobory odporności
HD - bliźnięta, infekcje EBV
RMS – Li-Fraumeni, NF1
Mięsak Ewinga – rasa biała choruje 9x częściej
niż czarna
Guzy jąder - wnętrostwo
Czynniki ryzyka

Zespół Downa
20 x wyższe ryzyko zachorowania na
białaczkę
1 na 100
40% AML, 60% ALL
Często ostra białaczka megakariocytowa

Guz Wilmsa
WAGR
delecja 11p13
Zespół Denis-Drash
autosomalnie dominująca
mutacja typu missense w WT1
Autosomalnie dominujący guz Wilmsa
gen nieznany
Hemihipertrofia i zespół Beckwith-Wiedemann 11p15

Nieprawidłowości chromosomów
płciowych
• Fenotyp żeński z obecnością Y
- Zespół niewrażliwości na androgeny
- Zespół Turnera z mozaicyzmem 45X,
46XY
• Zespół Klinefeltera

Cechy autosomalnie dominujących zespołów
rodzinnego występowania nowotworów
• Nowotwory występują w wielu pokoleniach
• Przekazywane przez matki i ojców
• Wcześniejsze niż w populacji ogólnej występowanie
nowotworów
• Częstsze występowanie nowotworów mnogich i
obustronnych
• Zwiększone ryzyko występowania jednego lub kilku
typów nowotworów w jednej rodzinie
• Zmienna penetracja genów powoduje, że w rodzinie
mogą występować nosiciele, którzy nie zachorują na
nowotwór

Autosomalne dominujące
• Retinoblastoma
• Dziedziczne mutacje P53 – zespół Li-Fraumeni
• FAP/APC
• HNPCC
• Zespół Turcota
• MEN2
• Fakomatozy
- NF1, NF2, TS, VHL

retinoblastoma
• Utrata obu kopii genu RB1
• Postać rodzinna: komórki zawierają 1 kopię
genu
Autosomalne dominujące

Zespół
Li-Fraumeni
Mutacja p53
Występowanie nowotworów przed 45. r.ż.
Rak piersi przed menopauzą, białaczki,
mięsaki, guzy mózgu, rak kory nadnerczy,
żołądka, chłoniaki, rak płuca, rak splotu
naczyniówkowego, rak jelita grubego
Prawdopodobieństwo zachorowania na drugi
nowotwór – 57%
Autosomalne dominujące

MEN
• MEN1
przytarczyce, wyspy trzustki, przysadka
chromosom 11
28% zachoruje przed 15. r.ż.
• MEN2
onkogen RET, chromosom 10q11
• MEN2A
rak rdzeniasty tarczycy, gruczolaki przytarczyc, guz
chromochłonny nadnerczy
• MEN2B
występowanie nowotworów w okresie niemowlęcym,
ganglioneuroma w przewodzie pokarmowym,
deformacje kośćca
Autosomalne dominujące

FAP
• Gen supresorowy APC
• Rozwój polipowatości w drugiej, trzeciej dekadzie życia
• 90% powstaje rak jelita grubego
• Zwiększone ryzyko zachorowania na nowotwory
górnego odcinka przewodu pokarmowego, raka
tarczycy(1:100) oraz hepatoblastoma (1:250)
• Sigmoidoskopia od 8 rż
• Profilaktyczna colectomia z usunięciem błony śluzowej
odbytnicy
• Sulindac
Autosomalne dominujące

HNPCC
• Niestabilność mikrosatelitarna, do której
prowadzi brak funkcji genów hMSH2, pML1 i
MSH6
• Nowotwory macicy, jajników, górnego odcinka
przewodu pokarmowego
• Kolonoskopia co 6 miesięcy po 25 rż
Autosomalne dominujące

Zespół Turcota
• APC i HNPCC
• Medulloblastoma 92xczęściej niż w
ogólnej populacji, glioblastoma
Autosomalne dominujące

fakomatozy
• NF1
1:2500
Plamy cafe-au-lait
Nerwiakowłókniaki
Przebarwienia pach i pachwin
Hamartomy tęczówki
Glejaki nerwu II (15%)
Inne glejaki o niskim stopniu złośliwości
Pheochromocytoma
MPNST, RMS, AML,
Autosomalne dominujące

Autosomalne recesywne
• Xeroderma pigmentosum
• Zespół Cockayne
• Trichothiodystrophy
• AT

Diagnostyka
• Wywiad z szczegółowym wywiadem
rodzinnym
• Badanie fizykalne
• Badania laboratoryjne (biochemiczne,
hormonalne, immunologiczne,
genetyczne
• Badania obrazowe

Leczenie skojarzone
• Chemioterapia
• Postępowanie chirurgiczne
• Radioterapia
• Rehabilitacja
• Opieka paliatywna

Radioterapia
• Unieruchomienie pacjenta
- wykonanie masek z orfitu na podstawce węglowej lub
pleksiglasowej
• Planowanie leczenia
- pozycjonowanie na symulatorze
- zebranie skanów TK i przesłanie do systemu planowania
- wrysowanie obszarów do planowania GTV, CTV, PTV
- zaplanowanie leczenia w systemie planowania

nowotwory ośrodkowego układu
nerwowego
• Wysokozróżnicowane gwiaździaki
• Rdzeniak płodowy
• Wyściółczak
• Czaszkogardlak
• Złośliwe glejaki

• >50% podnamiotowo
• 40% nadnamiotowo
• Około 5% guzy rdzenia
nowotwory ośrodkowego układu
nerwowego

Gwiaździaki łagodne
• 50% guzów mózgu u dzieci
• 10 OS 80%
• Móżdżek>półkule>śródmózgowie,
wzgórze>drogi wzrokowe
• Włosowatokomórkowe – małe dzieci,
móżdżek, drogi wzrokowe
• Włókienkowe – dzieci starsze, pień,
półkule, progresja złośliwości

Rdzeniaki płodowe
85% przypadków przed 15 rokiem życia
Należy napromieniać oś mózgowo-rdzeniową do 36 Gy
Niekorzystne czynniki prognostyczne:
zakres resekcji guza <75%
rozsiew do płynu m-r
obecność przerzutów odległych
zajęcie pnia mózgu
wiek poniżej 4 lat
są wskazaniami do leczenia cytostatycznego
Przeżycie 5-letnie od 40% do 80%

Guzy pnia mózgu
• 10%
• 5 OS 20-30%
• Egzofityczne, endofityczne

czaszkogardlak
• Chirurgia - wyleczenie 60-80%
• Radioterapia po operacji nawrotu
lub nieradykalnym zabiegu
chirurgicznym
• 5 OS 80%

Mięsaki tkanek miękkich
70 nowych zachorowań rocznie
70% RMS
10% sarcoma neurogenes
10% synovioma malignum
5% pozakostny Ewing i PNET
5% fibrosarcoma
Chorzy z licznymi wadami wrodzonymi
Występowanie rodzinne – zespół Li Fraumeni
Postaci histologiczne RMS:
Zarodkowa
Pęcherzykowa
Wielopostaciowa
Niesklasyfikowane

RMS - lokalizacja
Głowa i szyja 43%
Oczodół 4%
Okolica okołooponowa
26%
Okolica nieokołooponowa 13%
Układ moczowy
9%
Narząd rodny 7%
Kończyny 18%
Inne 23%

Mięsaki – stopień zaawansowania
klinicznego
• I (16%) guz usunięty w granicach
tkanek zdrowych, węzły chłonne (-)
• II (28%) resekcja mikroskopowo
nieradykalna, węzły chłonne (+) lub (-)
usunięte
• III (36%) częściowa resekcja guza, węzły
chłonne (+) lub (-)
• IV (20%) przerzuty odległe

Mięsaki – leczenie
• I – uzupełniająca chemioterapia
• II – uzupełniająca chemioterapia i
radioterapia
• III – wstępna chemioterapia, chirurgia
i/lub radioterapia, chemioterapia
pooperacyjna
• IV – chemioterapia, chirurgia i/lub
radioterapia, chemioterapia
pooperacyjna

• Pięcioletnie przeżycia:
I i II – 75 – 80%
III – 40 - 50%
IV – 20%
Oczodół – 90%
Pęcherz moczowy – 80%
RMS – rokowanie

• W lokalizacji okołooponowej:
• Objęcie guza pierwotnego z 2-5 cm
marginesem tkanek zdrowych w oparciu o
badanie CT lub MRI wykonane przed
rozpoczęciem leczenia
• objęcie maginesem 2-3 cm powyżej podstawy
czaszki
• W pozostałych lokalizacjach zmiana resztkowa
z 2 cm marginesem
• Dawki 40-55 Gy
mięsaki – radioterapia

• Vinkrystyna
• Adriamycyna
• Cyklofosfamid
• Aktynomycyn
a
• Etopozyd
• Ifosfamid
• Cisplatyna
• DTIC
mięsaki – chemioterapia
Zastosowanie chemioterapii wielolekowej
zwiększyło prawdopodobieństwo
wieloletniego przeżycia z 10-40% do 60-80%

Białaczki
• 80% ALL
• 17% AML
• 2-5% CML
Często w skojarzeniu z dziedzicznymi
anomaliami: zespół Downa, anemia
Fanconiego, NF1
Diagnostyka – zakwalifikowanie do grup ryzyka
Chemioterapia: indukcja, konsolidacja,
podtrzymanie remisji

• Napromienianie OUN
• Profilaktyczne - całe mózgowie z rdzeniem
przedłużonym do C2-C3, 12-18 Gy po1,8 Gy
• Lecznicze – napromienianie całego OUN
18 Gy po1,8 Gy
napromienianie jąder 20-24 Gy po 2 Gy
Białaczki - rola radioterapii

Chłoniaki nieziarnicze
• Chłoniaki o wysokim stopniu złośliwości,
wysoka wrażliwość na cytostatyki
• NHL z kom B guz w jamie brzusznej, guzy kości,
twarzoczaszki, zajęcie szpiku
• NHL z kom T – najczęściej zajęcie śródpiersia
• Leczenie: chemioterapia wielolekowa
radioterapia profilaktyczna lub lecznicza
OUN
raditerapia paliatywna:SVCS, ucisk
rdzenia

Ziarnica złośliwa
• LP 5-15%, NS 40-60%, MC 15-30%,
LD<5%
• Leczenie: chemioterapia wielolekowa +
radioterapia
• Dawki niższe niż u dorosłych
• Wyleczenia > 90%

Guz Wilmsa
• Najczęściej 3-4 rż
• 95% zachorowań przed 7 rż
• Wstępna chemioterapia bez weryfikacji
histopatologicznej
• Radykalny zabieg operacyjny
• Chemioterapia pooperacyjna
• Radioterapia
- stopień III i IV o histologii korzystnej i standardowej
- stopień II i III o histologii niekorzystnej
- w stopniu II i III napromieniamy lożę po guzie i
okoliczne węzły chłonne
- napromienianie całej jamy brzusznej i całych płuc

neuroblastoma
• Szczyt zachorowań 1-2 rż
• 90% zachorowań przed 5 rż
• 30% chorych ma nieprawidłowości cytogenetyczne
delecja ramienia chromosomu 1, hiperploidia DNA,
amplifikacja onkogenu N-myc
Najczęściej okolica zaotrzewnowa 60-80%
Śródpiersie 15%
Miednica 2-5%
W chwili rozpoznania 60-70% chorych ma przerzuty
odległe
90% ma podwyższone stężenie katecholamin w moczu
Postać występująca u niemowląt IV S z przerzutami do
wątroby, szpiku i tkanki podskórnej

- I i II stopień – guz ograniczony do narządu, nie
przekracza linii środkowej ciała, zabieg operacyjny
radykalny lub nieradykalny mikroskopowo
leczenie wyłącznie chirurgiczne lub z uzupełniającą
chemioterapią
- III stopień – guz przekracza linię środkową
chemioterapia indukcyjna, zabieg operacyjny,
chemioterapia, radioterapia
IV stopień – przerzuty odległe, chemioterapia,
megachemioterapia z przeszczepieniem szpiku,
chirurgia, radioterapia
IVS – jeśli brak objawów – bez leczenia
neuroblastoma

Mięsaki kości 5-7%
• W Polsce około100 zachorowań rocznie
• 70% mięsaki kościopochodne
• Rozpoznanie na podstawie biopsji operacyjnej
• Osteosarcoma - 50% w okolicy stawu
kolanowego
• Mięsak Ewinga – 40% ma objawy stanu
zapalnego

Osteosarcoma
1. Chemioterapia
2. Zabieg operacyjny
3. Chemioterapia
75% długoletnich przeżyć

Mięsak Ewinga
• Chemioterapia
• Chirurgia
• Radioterapia
• Napromieniamy objętość guza sprzed
zabiegu z marginesem
• 50% wyleczeń w postaci zlokalizowanej,
• 20% 5-letnich przeżyć w postaci
rozsianej

Guzy zarodkowe
• 2-3%
• Gruczoły płciowe, okolica krzyżowo guziczna,
okolica zaotrzewnowa, śródpiersie, OUN
• Rozrodczaki, potworniaki, rak zarodkowy, guz
pęcherzyka żółtkowego, kosmówczak
• Chemioterapia
• Chirurgia
• Radioterapia
• 70-90% wyleczeń w postaciach zlokalizowanych
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
- Slide 34
- Slide 35
- Slide 36
- Slide 37
- Slide 38
- Slide 39
- Slide 40
- Slide 41
- Slide 42
- Slide 43
- Slide 44
- Slide 45
- Slide 46
- Slide 47
- Slide 48
- Slide 49
- Slide 50
- Slide 51
- Slide 52
- Slide 53
- Slide 54
- Slide 55
- Slide 56
- Slide 57
- Slide 58
- Slide 59
- Slide 60
- Slide 61
- Slide 62
- Slide 63
- Slide 64
- Slide 65
- Slide 66
Wyszukiwarka
Podobne podstrony:
2014 09 30 nowotwory wieku dziecięcego
Nowotwory wieku dziecięcego 2
nowotwory wieku dzieciecego 1
Nowotwory wieku dziecięcego, nowotwory-onkologia
nowotwory wieku dzieciecego - seminarium dr sujkowska, IV rok, IV rok CM UMK, Patomorfologia, Sujko
nowotwory wieku dziecięcego 3
nowotwory wieku dziecięcego, Medycyna, Onkologia
Nowotwory wieku dziecięcego
2014 09 30 nowotwory wieku dziecięcego
Nowotworem charakterystycznym dla wieku dziecięcego NIE jes1
S1 Choroby zakaz¦üne wieku dziecie¦Ęcego b
NIEWYDOLNOŚĆ ODDECHOWA W WIEKU DZIECIĘCYM
Choroby zakazne wieku dzieciecego do druku
więcej podobnych podstron