
Równowaga
kwasowo -
zasadowa

Równowaga kwasowo-
zasadowa
Jest to zdolność organizmu do
utrzymywania stałego stężenia
(aktywności) jonów wodorowych
w środowisku wewnętrznym.
Naruszenie równowagi kwasowo-zasadowej
prowadzi do kwasicy
(oddechowej/metabolicznej) lub zasadowicy
(oddechowej/metabolicznej).

Laboratoryjna ocena równowagi
kwasowo-zasadowej polega na
analizie następujących
parametrów krwi tętniczej:
- pH: 7,35 – 7,45
- pCO
2
: 35 – 45 mmHg
(pCO
2
wzrasta w
kwasicach oddechowych, a maleje w zasadowicach
oddechowych)
- stężenia jonów wodorowęglanowych:
22 – 27 nmol/l
(HCO
3
‾ wzrasta w zasadowicach
metabolicznych i kwasicach oddechowych, a maleje w
kwasicach metabolicznych)
- nadmiaru lub niedoboru zasad
buforujących
(BE): -2,5 do +2,5

W wyniku przemian biochemicznych
dochodzi
w organizmie do ↑ stężenia jonów
wodorowych, które zakwaszają środowisko.
W związku z tym istnieje konieczność
zobojętniania tych substancji.
Za utrzymanie stałego pH krwi (7,35 –
7,45) odpowiadają układy buforowe.

Bufory są to roztwory, które nie
zmieniają pH pomimo wprowadzenia
do nich pewnych ilości jonów H+ lub
OH‾ (roztwór buforowy może być
mieszaniną słabego kwasu
z mocną zasadą lub mocnego kwasu
ze słabą zasadą).

Składniki równowagi kwasowo-
zasadowej
Zgodnie z teorią Brönsteda kwasem jest
związek, który w roztworze wodnym
oddysocjowuje jon H+ (jest donorem
jonów wodoru), zasadą natomiast jest
związek, który przyłącza jony wodoru (jest
ich akceptorem).
H
2
CO
3
↔ H+ + HCO
3
‾
kwas zasada
protonodawca protonobiorca

W utrzymaniu stałego pH krwi
i płynów ustrojowych biorą
udział:
- układy buforowe krwi i tkanek
- płuca
- nerki
- przewód pokarmowy
- kości

Układy buforowe organizmu
człowieka
• wodorowęglanowy (70%) –
składa się z kwasu węglowego i
soli tego kwasu z mocną zasadą HCO
3
‾/H
2
CO
3
=20/1
• hemoglobinowy (20%) –
składa się z hemoglobiny i
hemoglobiny utlenowanej
• fosforanowy (3%) –
składa się z fosforanu I i II rzędowego
• białczanowy (6%) –
składa się z białka i jego anionu

Regulacja równowagi kwasowo-
zasadowej jest ściśle związana z
regeneracją zasad buforujących oraz
transportem gazów przez krew. W
utrzymaniu tej równowagi
zaangażowane są głównie płuca i
nerki.

Regulacja oddechowa równowagi
kwasowo-zasadowej
Płuca wydalają CO
2
na zasadzie biernej dyfuzji (zgodnie z
gradientem stężeń). Ilość wydalanego CO
2
zależy od
wentylacji płuc regulowanej przez ośrodek oddechowy
znajdujący się na dnie komory IV mózgu (w rdzeniu
przedłużonym). Stan napięcia tego ośrodka zależy od
chemoreceptorów centralnych (dno komory IV blisko
ośrodka oddechowego) i obwodowych (kłębki szyjne,
łuk aorty). Pobudzenie osmoreceptorów obwodowych
jest zależne od pCO
2
w osoczu i stężenia jonów H+
(↑pCO
2
i ↑H+ pobudza, a ↓pCO
2
i ↓H+ hamuje osmoreceptory i zwalnia
rytm oddechowy).
Osmoreceptory centralne reagują tylko na
stężenie jonów H+ (
↑H+ w płynie mózgowo-rdzeniowym pobudza
je, a ↓H+ hamuje).

Regulacja oddechowa
równowagi kwasowo-
zasadowej
W płucach krew ulega utlenowaniu.
pCO
2
we krwi żylnej wynosi 45mmHg, a pO
2
40mmHg.
pCO
2
we krwi tętniczej w wyniku dyfuzji do pęcherzyków płucnych
zmniejsza się do 40mmHg, zaś pO
2
(wskutek utlenowania) z 40
wzrasta do 100mmHg.
98% tlenu jest transportowane z płuc w postaci oksyhemoglobiny, a 2%
w postaci rozpuszczonej w osoczu.
CO
2
we krwi jest transportowany w 5% w postaci rozpuszczonej w
osoczu,
w 15% wiąże się z hemoglobiną tworząc połączenie karbaminianowe,
a w 80% w reakcji katalizowanej przez dehydratazę węglanową
tworzy kwas węglowy dysocjujący na H+ i HCO
3
‾. Jon H+ ulega
następnie zbuforowaniu przez odtlenowaną hemoglobinę, a jon HCO
3
‾
jest wymieniany na pozakomórkowy jon Cl‾.

Przyczyną oddechowych zaburzeń
równowagi kwasowo-zasadowej są
głównie zmiany wentylacji
pęcherzyków płucnych:
hipowentylacja powoduje
kwasicę,
a hiperwentylacja zasadowicę.

Regulacja metaboliczna
równowagi kwasowo-
zasadowej
Sprowadza się głównie do nerkowej
eliminacji H+ oraz do zapewnienia
prawidłowego zasobu podstawowej
zasady buforującej HCO
3
‾.

Regulacja metaboliczna
równowagi kwasowo-
zasadowej
Zachodzące w kanalikach nerkowych wchłanianie wodorowęglanów
przesączalnych do moczu pierwotnego chroni przed ich utratą
z moczem i zachodzi w dwojaki sposób:
1.
ok. 20% HCO
3
‾ ultraprzesączu osocza wchłania się w kanaliku
proksymalnym łącznie z jonem Na+
2.
pozostałe wodorowęglany z jonem H+, wymienianym na jon Na+,
tworzą H
2
CO
3
, rozkładany następnie przy udziale anhydrazy
węglanowej na CO
2
i H
2
O (w kanaliku dystalnym reakcja ta
zachodzi samorzutnie
w wyniku niskiego pH moczu). CO
2
zgodnie z gradientem stężeń,
swobodnie dyfunduje do komórek kanalikowych, gdzie pod
wpływem anhydrazy węglanowej odtwarza kwas węglowy,
dysocjujący następnie do H+ i HCO
3
‾. Jon H+ wraca ponownie do
światła kanalika, a jon HCO
3
‾ (w równowadze z jonem Na+)
dyfunduje do płynu pozakomórkowego.
Mechanizm ten sprawia, że mocz prawidłowy nie zawiera
wodorowęglanów.

Regulacja metaboliczna
równowagi kwasowo-
zasadowej
Jony H+ na tym etapie są wykorzystywane
w procesie wchłaniania HCO
3
‾. Z chwilą, gdy
stężenie HCO
3
‾ ↓ w płynie cewkowym (w
wyniku ich całkowitego wchłonięcia), jony H+
są wydzielane do światła cewki, aby następnie
zostać związane przez bufor fosforanowy lub
w procesie amoniogenezy z jonem NH
4
+
(w kanaliku dalszym) i usunięte z organizmu.

Rola wątroby w równowadze
kwasowo-zasadowej
W katabolizmie białek powstają
równoważne ilości NH
4
+ i HCO
3
‾,
które ulegają przekształceniu w
mocznik. W zależności od nasilenia
wytwarzania mocznika przemiana
aminokwasów może być źródłem
HCO
3
‾.

Rola kości w równowadze
kwasowo-zasadowej
W układzie kostnym dorosłego
człowieka jest zdeponowane 7 - 8
moli zasad pod postacią węglanów i
fosforanów wapnia. Uruchomienie
tych zasad zachodzi
z reguły tylko w przewlekłych
kwasicach.

Rola przewodu pokarmowego
w równowadze kwasowo-
zasadowej
W stanach fizjologicznych przewód pokarmowy
nie odgrywa istotnej roli w bilansie jonów H+.
W stanach chorobowych, w następstwie np.
utraty soku żołądkowego przez wymioty
mogą rozwinąć się ciężkie zaburzenia
równowagi kwasowo-zasadowej pod postacią
zasadowicy metabolicznej (u wymiotujących)
lub kwasicy metabolicznej (przy biegunce).
Spożywane w ciągu doby pokarmy zawierają
ok. 35 mmoli zasad, które w tych
okolicznościach mają istotny wpływ na
przebieg zaburzeń.

Podział zaburzeń równowagi
kwasowo-zasadowej
Zmiana H+ uwarunkowana pierwotną zmianą pCO
2
:
- Kwasica oddechowa - ↑pCO
2
,↑H+, ↓pH
- Zasadowica oddechowa - ↓pCO
2
, ↓H+, ↑pH
Zmiana H+ uwarunkowana pierwotną zmianą HCO
3
‾:
- Kwasica metaboliczna - ↑H+, ↓pH, ↓HCO
3
‾
- Zasadowica metaboliczna - ↓H+, ↑pH, ↑HCO
3
‾
Zmiana H+ uwarunkowana zarówno zmianą pCO
2
, jak
i HCO
3
‾:
- Zaburzenie mieszane

Kwasica metaboliczna
• addycyjna –
nadmierne wytwarzanie nielotnych kwasów
(np.
kwasica ketonowa w cukrzycy, głodzeniu)
• subtrakcyjna –
utrata zasad buforujących
(np. biegunki,
niedrożność jelit)
• retencyjna –
zaburzenia nerkowych mechanizmów regulacji
gospodarki kwasowo-zasadowej
(np. kwasica kanalikowa, ciężkie
postacie niewydolności nerek)
Objawy: ↑H+, ↓pH, ↓HCO
3
‾, pCO
2
N/↓
W wyrównaniu kwasicy metabolicznej bierze udział:
- kompensacja oddechowa - hiperwentylacja
- kompensacja komórkowa
- kompensacja nerkowa

Kwasica oddechowa
Powodowana jest przez wszystkie stany upośledzające
wymianę gazową (zaburzenia wentylacji, dyfuzji,
perfuzji).
Objawy: ↑H+, ↓pH, ↑ pCO
2
,↑HCO
3
‾
W wyrównaniu kwasicy oddechowej bierze udział:
- kompensacja nerkowa
- kompensacja komórkowa

Zasadowica metaboliczna
• addycyjna –
nadmierna kumulacja zasad buforujących
(np.
zwykle jatrogenna – podawanie nadmiernej ilości wodorowęglanów
)
• subtrakcyjna –
utrata nielotnych kwasów
(np. wymioty,
podawanie diuretyków)
• dystrybucyjna –
przesunięcie H+ pomiędzy płynem
pozakomórkowym
a wewnątrzkomórkowym
(np. hipokaliemia)
Objawy: ↓ H+, ↑pH, ↑ HCO
3
‾
Wyrównanie zasadowicy metabolicznej jest bardzo trudne, bo:
- kompensacja oddechowa – ograniczona
- kompensacja komórkowa prowadzi do hiperkaliemii
- kompensacja nerkowa – zależy od przesączania kłębuszkowego i
stężenia Cl‾

Zasadowica oddechowa
Przyczyny:
• bezpośrednie,
np. hiperwentylacja emocjonalna, zapalenie
mózgu
• odruchowe,
np. odma, rozedma, zwłóknienie płuc
• mechaniczne,
np. niewłaściwe stosowanie respiratorów
Objawy: ↓pCO
2
, ↓H+, ↑pH, ↓HCO
3
‾
W wyrównaniu zasadowicy oddechowej bierze udział:
- kompensacja nerkowa
- kompensacja komórkowa
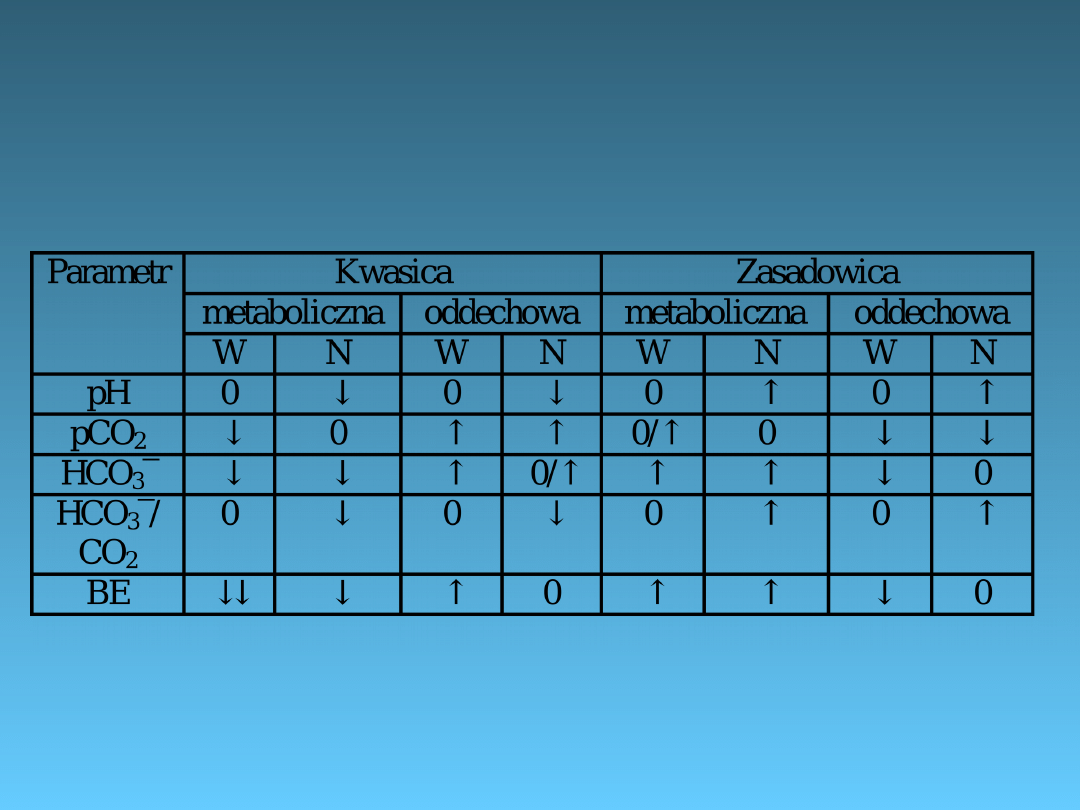
Wskaźniki laboratoryjne w
zaburzeniach równowagi kwasowo-
zasadowej

Pytanie 1
Który z poniższych stanów jest charakterystyczny
dla kwasicy metabolicznej?
a) ↑ HCO
3
‾, norma pCO
2
b) ↑ HCO
3
‾, ↑ pCO
2
c) ↓ HCO
3
‾, ↓ pCO
2
d) ↑ HCO
3
‾, ↓ pCO
2
e) ↓ HCO
3
‾, norma pCO
2
Pytanie 2
Który zestaw charakteryzuje
skompensowaną
zasadowicę metaboliczną?
HCO
3
‾
pCO
2
pH
a.
20
25
7,5
b.
40
46 7,56
c.
17
30
7,3
d.
34
10
7,7
e.
17
19
7,9
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
Wyszukiwarka
Podobne podstrony:
stała równowagi kw zas
Kw zas
Gosp kw zas pol
ZABURZENIA RoWNOWAGI KWAS-ZAS, fizjologia
równowaga kwas zas
EGZ 2009 hip nerka kw-zas, Patofizjologia
g wod el i kw zas
Moduł III cz 1 Równowaga, Kw, pH rozwiazania zadań
Gospodarka wodno elektrolitowe, kw zas, ketoza, cukrzyca
4 zas stw kw
Równowaga kwasowo zasadowa fizjot3
GOSPODARKA KWAS ZAS
kw żółciowe
APARATURA DO OCENY RÓWNOWAGI STATYCZNEJ
więcej podobnych podstron