
CHOROBY WIRUSOWE I
BAKTERYJNE
PRZEWODU
POKARMOWEGO
BYDŁA
Sandra Sieracka
Anna Głuszyńska
2a

CZYNNIKI
ETIOLOGICZNE
Rotawirusy
Koronawirusy
Kolibakterioza
Salmonella
Zakażenia beztlenowcami
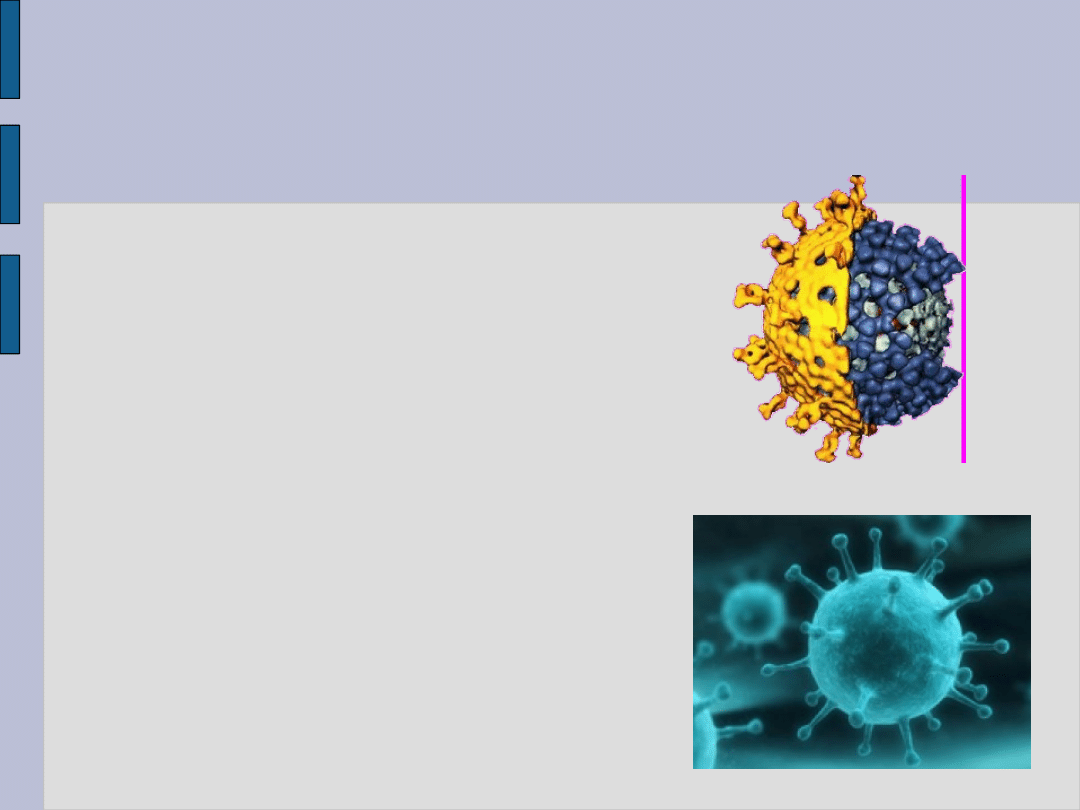
ROTAWIRUSY
-Rodzina Reoviridae
-dsRNA
-Brak otoczki
-Są oporne na zamrażanie oraz
inkubację przez godzinę w temp.
56°C. Zakaźność wirusów
zmniejsza alkohol etylowy i
podchloryn sodu.

ROTAWIRUSY
NAJCZĘSTSZA PRZYCZYNA ROZWOJU BIEGUNKI
NOWONARODZONYCH CIELĄT (40%)
-Głównie Rotawirusy z grupy serologicznej A,
podgrupy I i II
-Szeroko rozpowszechnione w populacji Bo
-Oporne na czynniki środowiskowe – zachowują
zdolność do infekcji do 6 msc
-Wysoka zaraźliwość
-Krótki okres inkubacji 13h-2 dni
-Intensywne wydalanie wirusa z kałem

PATOGENEZA
Zakażenie rotawirusowe charakteryzuje się występowaniem
ostrych biegunek u cieląt do 14 dnia życia. Do zakażenia
dochodzi drogą pokarmową, a wirus wykazuje powinowactwo z
komórkami jelit cienkich, gdzie namnaża się, powodując
atrofię kosmków i hiperplazję krypt jelitowych.
Zmiany te charakteryzują się zniszczeniem enterocytów
kosmków jelitowych oraz następowym, stopniowym
zastępowaniem komórek walcowatych przez nowe, bardziej
sześcienne komórki nabłonka pochodzące z krypt jelitowych.
Dotyczą one przede wszystkim górnej połowy kosmków w
obszarze jelita biodrowego i częściowo czczego.
Młodociane komórki są niewrażliwe na zakażenie, jednak nie
wykazują zdolności do pełnienia funkcji trawiennych i absorpcji
substancji pokarmowych charakterystycznych dla enterocytów
kosmków jelitowych ze względu na niedobór disacharydazy i
aktywności ATPazy sodowo-potasowej.

Z tego też względu w zakażeniach tego typu mamy do czynienia z
upośledzeniem funkcji trawiennych i zmniejszenia wchłaniania. Dalsze
konsekwencje zakażenia rotawirusowego wynikają z funkcjonowania
komórek krypt, które to nadal zdolne są do pełnienia funkcji
wydzielniczych, jednak nie są one równoważone przez procesy
wchłaniania treści przez kosmki jelitowe. Sytuacja ta prowadzi do
zachwiania równowagi we wchłanianiu, co przyczynia się do
wystąpienia biegunki osmotycznej.
Ponadto, w zakażonych rotawirusem komórkach obecne jest
niestrukturalne białko NSP4. Podczas uszkodzenia komórki jest ono
uwalniane i powoduje zależną od jonów wapnia transepitelialną
sekrecję chloru w sąsiadujących enterocytach.Wzrastające nadmiernie
ciśnienie osmotyczne również prowadzi do przechodzenia wody do
światła jelit, podczas gdy niestrawione składniki pokarmowe, jak
laktoza, przechodzą przez jelita do okrężnicy, gdzie fermentują do LKT,
co prowadzi do powstania form D i L kwasu mlekowego.
Forma D jest wolno rozkładana, przez co przechodzi ona do krwi i gromadzi
się w krwiobiegu, prowadząc ostatecznie do kwasicy metabolicznej.

DROGI SZERZENIA
ROTAWIRUSÓW
-intensywne siewstwo wirusa z kałem przez:
klinicznie bezobjawowi nosiciele
chore cielęta wraz z kałem biegunkowym.
-do zakażenia cieląt dochodzi podczas porodu lub krótko po
nim.
-biegunka może ujawnić się już w pierwszych dniach życia,
najczęściej jednak w 5 – 14 dniu a w stadach, w których
zaopatrzenie cieląt w siarę jest bardzo dobre, objawy
pojawiają się dopiero w 3. lub 4. tygodniu życia.

Przebieg choroby zależy od :
-zjadliwości szczepu
-odporności zwierząt
-zagęszczenia zwierząt
-zakażenie innymi enteropatogenami

-Wysokie stężenie wirusa w środowisku
-Infekcje mieszane
-Niedostateczna podaż składników odżywczych
-Równoległe infekcje
-Zaburzenia pracy rynienki przełykowej
CZYNNIKI
KOMPLIKUJĄCE
ZAKAŻENIE

ROTAWIRUSY
OBJAWY
-biegunki mniej lub bardziej rzadkie, jasnożółte, mlecznoszare,
zielonkawe (zaawansowana choroba-domieszki barwników
żółciowych i biliwerdyny), ślady krwi (nietypowe)
-apatia, obniżone pragnienie
-podwyższona do 40°C temperatura ciała → potem spada
-UTRATA PŁYNÓW I ELEKTROLITÓW!!!!!
-obniżone napięcie skóry
-zapadnięcie gałek ocznych
-zaleganie
-zimne dystalne części kończyn
-blado-sine błony śluzowe
-pogłębione i częste oddechy
-niewydolność krążenia, spadek filtracji kłębuszkowej,
mocznica przednerkowa
-wzrost Ht, mocznika i kreatyniny, ciężaru moczu
-możliwy wstrząs hypoglikemiczny

OBJAWY KLINICZNE
Przebieg lekki:
kał ma konsystencję półstałą,
dzienna ilość kału nie przekracza 1000 g.
Przebieg ciężki:
silne, wodniste biegunki,
duża częstotliwość oddawania kału
biegunkowego,
dzienna jego ilość może przekraczać nawet
7000 g

Diagnostyka
Próbki kału pobieramy od cieląt nieleczonych
antybiotykami.
Do badania na obecność wirusów wykorzystuje się:
techniki immunologiczne – ELISA, IF
potwierdzenie fragmentu genomu za pomocą PCR

Zmiany Ap
W badaniu sekcyjnym stwierdza się:
silne odwodnienie zwierzęcia wywołane dużą utratą
płynów,
jelita wypełnione płynną treścią,
wychudzenie zwierzęcia, atrofia tkanki tłuszczowej.

Leczenie
-Leczenie objawowe tj. zapobieganie odwodnieniu – cielętom podajemy 3 razy
dziennie po 1-2l dostępnego komercyjnie roztworu glukozowo-elektrolitowego jako
„pojenie dodatkowe” – pomiędzy normalnymi posiłkami mlecznymi.
-U wszystkich silnie odwodnionych i objętych kwasicą metaboliczną cieląt
wdrażamy nawadnianie parenteralne:
w odwodnieniu lekkiego stopnia – podskórnie,
w odwodnieniu ciężkiego stopnia – dożylnie w ilości do 10 l płynów / dobę.
W przypadku rozwinięcia się hipoglikemii wynikającej z niechęci do przyjmowania
płynów, pacjentowi podajemy dodatkowo glukozę.
-Leczenie antybiotykowe w celu leczenia biegunek jest niezalecane, gdyż
negatywnie wpływa na funkcjonowanie jelit:
hamowanie działania flory jelitowej,
zwiększone ryzyko rozwoju grzybicy,
możliwy rozwój lekooporności.
-Antybiotykoterapia uzasadniona jest jedynie w przypadkach potwierdzenia, że
czynnikiem etiologicznym biegunki jest infekcja bakteryjna.
-U zwierząt rzeźnych nie dopuszcza się stosowania leków o działaniu
antysekrecyjnym oraz hamującym motorykę jelit, typu loperamid.

Zapobieganie
Zapobieganie rozwojowi biegunek cieląt powinno
obejmować:
poprawę warunków zoohigienicznych odnośnie
utrzymania, a także pojenia zwierząt,
wycielenie powinno mieć miejsce w pomieszczeniach
czystych
prawidłowe pojenie cieląt siarą.
Istnieje szczepionka z zabitymi wirusami:
szczepienie zasuszonych krów na 6 i 3 tygodnie przed
wycieleniem,
powtarza się co roku na 4 tygodnie przed
wycieleniem.
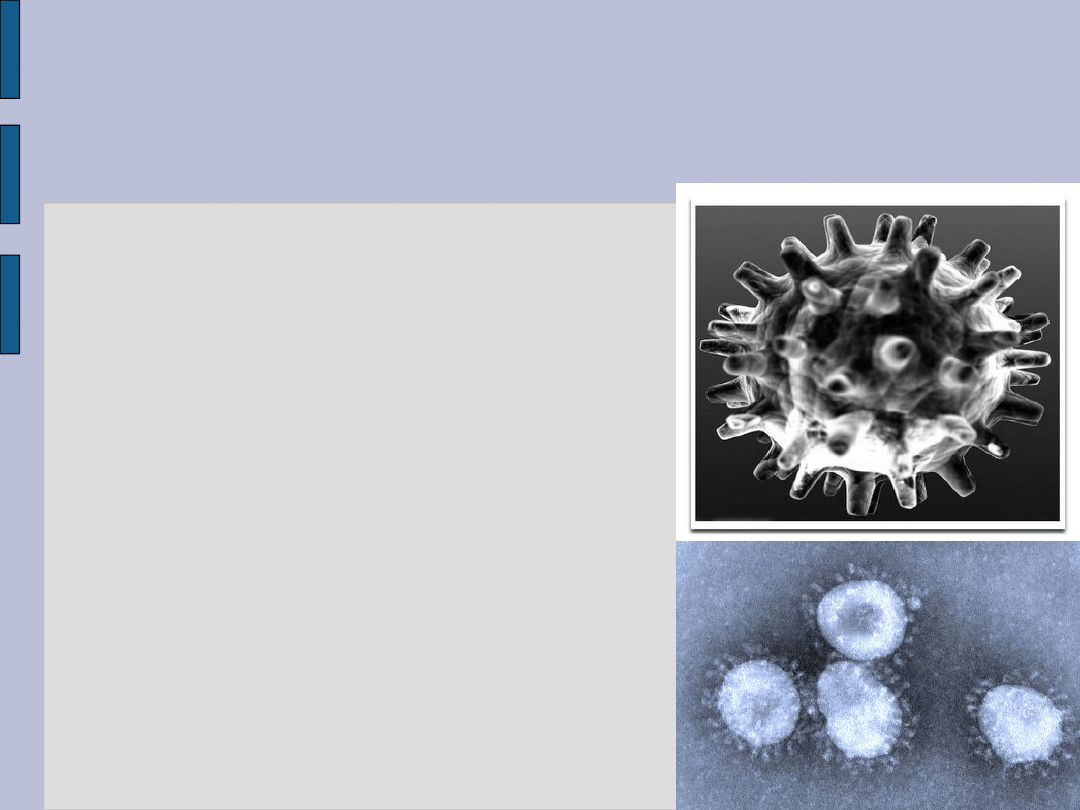
KORONAWIRUSY
-Rodzina Coronaviridae
- Jednoniciowy niesegmentowany
RNA
-Otoczka
-Wiriony są mniej odporne niż
wiriony rotawirusów
-O. inkubacji 20-36 h
-Wirus wydalany jest tylko przez 3
dni
Tropizm
-do układu oddechowego
-do układu pokarmowego
-jednoczesne wystąpienie
zapalenia jelit i płuc !!!

KORONAWIRUSY U
CIELĄT
-zakażenia rzadsze od rotawirusowych
-zakażenia alimentarne
-wirusy wydalane z kałem
- chorują cielęta do 3 tyg. życia
(U dorosłego bydła stany podkliniczne)
Zapalenie jelit cienkich i grubych dużego stopnia
(śluz w kale), przez co przebieg kliniczny jest
cięższy niż przy rotawirusach

Patogeneza:
Wirus ten wykazuje tropizm do enterocytów kosmków jelit cienkich
oraz do krypt jelita grubego, wywołując ciężkie zapaleni jelit
/enterocolitis/. Charakteryzuje się ono zniszczeniem komórek
epitelialnych kosmków jelitowych środkowej i tylnej części jelita
cienkiego, a także szczytów i krypt wszystkich regionów jelita
grubego. Zmiany obejmują więc nie tylko kosmki lub też
powierzchniowe warstwy nabłonka, lecz również wnętrze krypt.
Nasilenie opisanych zmian powoduje, iż w odróżnieniu od zakażeń
rotawirusowych, koronawirusy mogą prowadzić nawet do śmierci
zwierząt z jałowym przewodem pokarmowym. Z tego względu
naturalne zakażenia koronawirusowe wywołują silną biegunkę, a
śmiertelność w przypadku zakażeń mieszanych może wynieść
nawet 50%.Czynniki warunkujące biegunkę osmotyczną, jak
wzrost ciśnienia osmotycznego w świetle jelit, czy kwasica
metaboliczna powodowana powstawaniem LKT w okrężnicy, są
tożsame z zakażeniem rotawirusowym.

PATOGENEZA-
PORÓWNANIE
ROTAWIRUSY
-Zmiany dotyczą głównie górnej
połowy kosmków w jelicie
biodrowym i części jelita
czczego
-Śmiertelność zróżnicowana,
zachorowalność 50-100%
-Nowo narodzone cielęta (<14
dnia życia) są szczególnie
wrażliwe na zakażenia
-Największa liczba przypadków
zakażeń jest w pierwszych
tygodniach życia
KORONAWIRUSY
-Ciężkie zap. jelit - enterocolitis
-Zmiany w środkowej i tylnej
części jelita cienkiego i we
wszystkich regionach jelita
grubego – tam jest całkowite
zniszczenie nabłonka
-Niszczenie nie tylko komórek
nabłonka kosmków, ale również
krypt j. grubych
-B. silna biegunka, śmiertelność
przekracza 50% przy zakażeniach
naturalnych
-Do zakażeń dochodzi najczęściej w
7-10 dniu życia
-Okres podatności może sięgać 3
tygodnia życia

KORONAWIRUSY U
BYDŁA DOROSŁEGO
Biegunka zimowa bydła
-w ciągu kilku dni obejmuje całe stado
-biegunka obfita, ciemna, niecuchnąca
-często surowiczy/śluzowy wyciek z nosa i kaszel

Dignostyka:
MATERIAŁ DO BADAŃ:
a) Przyżyciowo
Próbki kału w pierwszych 24 godzin trwania
biegunki
-Mikroskop elektronowy- wykazanie obecności cząstek
wirusa
-Test ELISA
-PCR

Diagnostyka:
b) Pośmiertnie
Materiał do badań: próbki tkanek pobrane od
martwych cieląt (j. cienkie, j. grube)- test
immunofluorescencji bezpośredniej
Ze względu na cytolityczne oddziaływanie wirusa
może on zniknąć z tkanek, dlatego cielęta z
przebiegiem przewlekłym nie są dobrym źródłem
materiału do badań

Zmiany Ap:
-Silne odwodnienie
-Jelita wypełnione płynną treścią
-Wychudzenie
-Uszkodzenie błony śluzowej jelita, atrofia kosmków,
zapalenie nieżytowe

LECZENIE
-Uzupełnienie traconych z wodnistym kałem płynów i
elektrolitów (doustnie, gdy cielęta są zainteresowane
pokarmem i wodą)
-Przy podawaniu wyłącznie mleka ilość dostarczanych
elektrolitów i substancji buforujących jest zbyt mała,
żeby zrównoważyć straty jelitowe
-Gdy cielę nie pije – infuzja płynów podskórnie
(odwodnienie lekkiego stopnia) lub dożylnie
(odwodnienie ciężkie z objawami wstrząsu
hipowolemicznego i/lub silnej kwasicy metabolicznej)

ŚRODKI
PRZECIWBAKTERYJNE
-W łagodnym przebiegu nie ma potrzeby stosowania
antybiotyków
-W ciężkim przebiegu, gdy jest duże ryzyko wystąpienia
zakażeń mieszanych powinno się stosować
antybiotykoterapię (uszkodzenie enterocytów sprzyja
przyleganiu bakterii)
-Jednakże może to mieć zły wpływ na funkcjonowanie
jelit (hamowanie resorpcji, hamowanie działania flory
sacharolitycznej, zwiększone ryzyko rozwoju grzybicy i
lekooporności)

ZAPOBIEGANIE
-Czyszczenie boksów porodowych po każdym
rozwiązaniu
-Ograniczenie kontaktu cielęcia z matką (i ekspozycji na
jej odchody) przez jak najszybsze odseparowanie od niej
-Umieszczenie cielęcia w indywidualnym czystym boksie
-Karmienie indywidualnym smoczkiem, unikanie
karmienia zbiorowego
-Siara powinna być podawana przez pierwsze 30 dni
życia

SZCZEPIENIA
-Szczepionki z zabitymi wirusami – szczepienie
zasuszonych krów na 6 i 3 tyg. przed wycieleniem i
powtarzać co roku na 4 tygodnie przed wycieleniem

Kolibakterioza-
zakaźna, zaraźliwa
choroba cieląt
-Czynnik etiologiczny : Escherichia coli
-Rodzina Enterobacteriaceae
-Pałeczka Gram „-”,
-Tlenowa lub względnie beztlenowa,
-Nie wytwarza przetrwalników,
-Wytwarza liczne fimbrie,
-Stanowi ona składnik fizjologicznej flory jelitowej w dystalnym odcinki jelita
cienkiego i w jelicie grubym. Jedynie niektóre szczepy mają obligatoryjne
patogenne działanie na układ pokarmowy.
-Zwykle nie patogenna, może wywoływać w sprzyjających warunkach:
mastitis, metritis i enteritis
-Występuje powszechnie w środowisku
Gleba
Woda
Na roślinach
Jako saprofit układu pokarmowego zwierząt

PATOGENNE SZCZEPY
ETEC – enterotoksyczne (głównie kolibakteriozy
noworodków),
EAEC – enteroadherentne (niszczą mikrokosmki),
EIEC – enteroinwazyjne (atakują enterocyty i
głębsze warstwy śluzówki, powodują
kolisepticemię),
EHEC – enterokrwotoczne (produkują werotoksynę,
niszczą mikrokosmki),
EPEC – enteropatogenna (głównie enteritis u kociąt i
szczeniąt)

GATUNKI WRAŻLIWE –
WSZYSTKIE GATUNKI
ZWIERZĄT
Szczególnie narażone są:
-Drób,
-Króliki,
-Świnie, głównie prosięta,
-Bydło, głównie cielęta,
-Psy,
-Koty,
-Człowiek.

Czynniki zjadliwości:
1. Polisacharydy otoczkowe (antygeny K),
2. Lipopolisacharydy (LPS) – czynnik wirulencji,
3. Adhezyny,
4. Enterotoksyny, siderofory, werotoksyny, czynniki
nekrotyzujące CNF-1, CNF-2, hemolizyny,
5. Fimbrie

Do zakażenia dochodzi drogą pokarmową
Kontakt bezpośredni
Drogą pośrednią ( sprzęt oborowy)
Źródłem zakażenia są:
Kał bezobjawowych nosicieli ( dorosłe
bydło)
Kał osobników chorych ( siewstwo ok 7
dni)
Okres inkubacji: kilka godzin

ETEC
- Biegunki występują najczęściej w pierwszych 3-4
dniach życia do 14 dnia
-Szczepy te charakteryzują się obecnością fimbrii
oraz zdolnością do produkcji enterotoksyn
-Fimbrie umożliwiają kolonizacje jelit poprzez
adhezje do enterocytów
-Enterotoksyny:
*ciepłostała
*ciepłochwiejna

Mechanizm działania enterotoksyn polega na wnikaniu ich do
wnętrza enterocytów i aktywacji cyklazy
guanylowej/adenylowej, są to enzymy aktywujących produkcję
cAMP, cGMP i stymulację kinazy proteinowej oraz wzrost
stężenia jonów Ca w enterocytach.
Prowadzi to do wzrostu wydzielania chloru i sodu, a w
konsekwencji do napływania wody i dwuwęglanów do światła
jelita. Powoduje to powstawanie biegunki sekrecyjnej a w
konsekwencji utrate wody i i elektrolitów z organizmu.
Działanie enterotoksyn STa nie powoduje jednak powstania
zmian morfologicznych w enterocytach!
Sporadycznie może być izolowany szczep E.coli produkujący
enterotoksyne ciepłochwiejną LT. Mechanizm jej działania
powoduje wzrost cAMP w enterocytach, co powoduje przejście
dużej ilości płynów do światła jelit i wystąpienie biegunki.
ETEC- Enterotoksyczne

EHEC
Szczepy werotoksyczne E. coli są często izolowane od dorosłego bydła
Kiedy dojdzie do zakażenia szczepami werotoksycznymi, najważniejszą rolę
odgrywają czynniki zjadliwości, takie jak:
-zdolność do produkcji Shiga-like toksyny,
-adhezja do komórek nabłonka jelit
-powodowanie „Zjawisko przylegania i zacierania struktury kosmków
jelitowych” W wyniku tego zjawiska dochodzi do niszczenia rąbka
szczoteczkowego nabłonka jelitowego oraz zaburzenia funkcji enterocytów i
ich destrukcji.
Okres inkubacji ok 18 godzin od momentu zakarzenia.

Podatność cieląt na biegunki wywołane E.coli zależą od:
1)statusu immunologicznego – prawidłowe odpojenie siarą
zapewnia odpowiedni poziom w jelicie przeciwciał
skierowanych przeciwko antygenom fimbrialnym i / lub
otoczkowym E.coli
2)wieku – wraz z wiekiem spada podatność na zakarzenia.
Ważną role odgrywa tu pH trawieńca. Trawieniec
noworotków produkuje niewielką ilość soków trawiennych
o obojętnym pH ( ma to na celu ochrone IG ) od 2 dnia
życia pH trawieńca osiąga wartośc poniżej 3 – co
zabezpiecza przez zakażeniamiE.coli

Biegunka wywołana ETEC ma postać luźną do wodnistej, koloru
białawego do żółtego ( niekiedy może zawierać niewielkie
ilości krwi, najczęściej w postaci smużek)
Szybko doprowadza do utraty płynów z przestrzeni
międzykomórkowej oraz utraty elektrolitów czego skutkiem
jest postępujące odwodnienie oraz kwasica.
Dochodzi do wyraźnego osłabienia, spadku ilości pobieranej
karmy oraz utraty mięśniowej.
W przypadku ostrych biegunek w przeciągu 6-8 godzin może
dojść do utraty płynów sięgających nawet 10% masy ciała
Około 15-30% cieląt może wykazywać objawy.
Chociaż zachorowalność może sięgać 50% w przypadku ras
mięsnych i 75% ras mlecznych

W przypadku infekcji szczepami shigatoksycznymi,
objawy kliniczne dotyczą cieląt starszych (2-8
tygodniowe). Ważne są indywidualne
predyspozycje, biegunka często rozwija się u kilku
osobników w stadzie.
Objawy różnie nasilone- od słabej, wodnistej
biegunki do intensywnej i krwawej.
Pojawiają się objawy odwodnienia, ale słabiej
wyrażone niż w postacie enterotoksycznej. Mogą
wystąpić objawy neurologiczne (neurotoksyczne
działanie toksyn shiga)

Zmiany AP
-Nasilenie zmian zależy od stadium i formy choroby
-Biegunka: zwłoki odwodnione, okolice odbytu
zabrudzone kałem
-J. cienkie- zapalenie nieżytowe/ krwotoczne (lub brak
widocznego stanu zapalnego)
-Histologicznie uszkodzenie enterocytów w przypadku
infekcji szczepami shigatoksycznymi
-Posocznica: wybroczyny na powierzchni worka
osierdziowego, powiekszenie śledziony, obrzęk płuc
-Postać przewlekła- obecność włóknika w stawach

Diagnostyka
Do badań mikrobiologicznych pobieramy
wymazy kałowe lub próbki kału od
chorych, nieleczonych zwierząt.
Pośmiertnie pobieramy wycinki lub
wymazy z jelit
PCR

Leczenie
-ze względu na szybko postępujące odwodnienie należy
niezwłocznie uzupełnic płyny i eletrolity.( w zależności od
stopnia odwodnienia 2-10 l / dz)
iv- stany bardzo ciężkie
per os- stany lekkiej biegunki
-monitorowanie występowania kwasicy poprzez podawanie
kwaśnego węglanu sodu ( 1.3% iv)
-należy zapewnić też substancje odżywcze w postaci
świerzego mleka lub preparatu mlekozastępczego
-zaleca się stosowanie chemioterapeutyków tylko w stanach
bardzo ciężkich lub przy równoczesnym wystąpieniu
zapaleń dr. oddechowych

Profilaktyka:
W profilaktyce najważniejsze jest prawidłowe
odpojenie siarą o wysokiej jakości
można wprowadzić program szczepień,
którym objęte będą krowy cielne i jałówki (
pozwala to na uzyskanie siary o wysokiej
jakości)
najcześciej stosowane są szczepionki
poliwalentne ( np. rota i koronawirusy)

Szczepionka KOLIBIN
RC NEO
Roztwór do wstrzykiwań dla
bydła
Skład:
-Rotawirus bydlęcy inaktywowany
-Koronawirus bydlęcy inaktywowany
-3 inaktywowane enteropatogenne
szczepy E. Coli
-adiuwant: Montanide JSA70
Docelowe gatunki zwierząt: ZDROWE
bydło (ciężarne jałówki i krowy)

WSKAZANIA
Czynne uodparnianie ciężarnych jałówek i
krów przeciw chorobom przewodu
pokarmowego wywołanym przez
rotawirusy, koronawirusy oraz
enteropatogenne szczepy E. Coli.
Wytworzone przeciwciała pobrane przez
cielęta z siarą chronią je przed
infekcjami powodowanymi przez te
patogeny.

pojawienie się odporności:
u cieląt karmionych mlekiem matki oraz u cieląt
karmionych siarą pochodzącą od szczepionych
krów, odporność bierna pojawia się wraz z
rozpoczęciem karmienia.
Czas trwania odporności:
• odporność bierna utrzymuje się do momentu
zakończenia karmienia siarą.
• Cielęta karmione mlekiem matki są odporne
na infekcje dzięki odporności nabytej z siary
oraz mleka przez pierwsze 2-4 tygodnie życia.

DAWKOWANIE
Podanie szczepionki: podawać domięśniowo, najlepiej w okolice
zadu. Ciężarnym jałówką lub krowom szczepionym po raz
pierwszy, szczepionkę należy podawać dwukrotnie w
odstępie 21 dni, w schemacie 7-5 tygodni oraz 4-2 tygodnie
przed spodziewanym ocieleniem.
Następne szczepienia przeprowadzone są pojedyncza dawką na
4-2 tyg. przed każdym ocieleniem.
Karmienie siarą: W celu zapewnienia efektywnej ochrony cieląt
przez infekcją, układ pokarmowy cieląt powinien być
nasycony siarą szczepionych krów w ciągu pierwszych 2-3
tygodnia życia cieląt.
Dla cieląt które nie są karmione przez matki, siara oraz
późniejsze mleko powinny być zebrane od szczepionych
krów w ciągu pierwszych 6-8 udojów. Siara oraz mleko
powinny być przechowywane zamrożone lub schłodzone do
temperatury 2-8 C. Dzienna dawka siary dla cielęcia wynosi
2,5-3,5l dziennie przez minimum 2 pierwsze tygodnie życia.

Salmonella
Rodzina:
Enterobacteriaceae
Rodzaj:
Salmonella
Do rodzaju
Salmonella
należą dwa gatunki:
- S. enterica (podzielony na setki serotypów)
S. enterica ssp. enterica .
S. enterica ssp. salamae,
S. enterica ssp. arizonae,
S. enterica ssp. diarizonae,
S. enterica ssp. houtenae,
S. enterica ssp. indica
S. Bongori
Większość serowarów patogennych
dla człowieka i zwierząt stałocieplnych
należy do podgatunku S. enterica subsp.
enterica. Natomiast gatunek
S. bongori stanowi homogenną grupę
bakterii bez większego znaczenia epidemiologicznego

Salmonella
-Rodzaj Salmonella, ze względu na duże zróżnicowanie podzielony
został na grupy oraz typy serologiczne. Podstawą do podziału jest
zróżnicowanie antygenów somatycznych (antygen O) i rzęskowych
(antygen H).
-Pałeczki Salmonella występują w około 2500 typach serologicznych.
-Salmonella enterica spp. enterica ser. Enteritidis rozumiany, jako
rodzaj: Salmonella, gatunek enterica podgatunek enterica typ
serologiczny Enteritidis, można skrócić do formy: Salmonella
Enteritidis.
Morfologia:
-urzęsione (
peritricha
)
-pałeczki gram „–”
-3 – 4 x 0,4 – 0,6 μm

Salmonelloza bydła
(Salmonellosis bovum)
Chorobę wywołują głównie:
- S. Dublin,
-S. Typhimurium DT 104 („definitive type”) - wariant oporny na antybiotyki mający coraz
większe znaczenie u bydła,
- S. Newport.
Inne to:
S. Enteritidis,
S. Agona,
S. Anatum,
S. Virchov,
S. Choleraesuis,
S. Montevideo
Serowarami najczęściej izolowanymi
od bydła są S. Typhimurium i S. Dublin.
Jednak częstotliwość zakażeń tymi
drobnoustrojami znacznie różni się
w poszczególnych krajach.

Źródła i drogi zakażenia:
-Chorzy ludzie i zwierzęta, będący potem bezobjawowymi siewcami (siewstwo z
kałem do kilku lat, a nawet całe życie- S. Dublin, a S. Typhimurium kilka tyg. do
kilku m-cy)
-Zwierzęta innych gatunków utrzymywane w tym samym obiekcie
-Zanieczyszczone bakteriami woda, mleko, pokarm, pasza
-Główną drogą zakażenia u bydła jest droga pokarmowa, u cieląt możliwa
aerogenna
Czynnikami chorobotwórczymi rodzaju Salmonella są:
-antygeny (polisacharydy znajdujące się w ścianie komórkowej):
- somatyczny (antygen O) – będący endotoksyną
- wirulencyjny (antygen Vi) – właściwości antyfagocytarne, który jest specjalnym
otoczkowym polisacharydem S. Typhi
- inwazyny – białka powodujące przyleganie i penetrację komórek nabłonkowych
jelita
-czynniki uodparniające bakterie na fagocytozę (neutralizujące aktywne rodniki tlenowe
- katalaza
- dysmutaza ponadtlenkowa

Epizootiologia:
-Wrażliwe głównie cielęta i młode bydło w wieku 2 – 6 tygodni
(gospodarstwa łączące zwierzęta różnego pochodzenia).
-Bydło mleczne – endemicznie na obszarach objętych inwazją
motylicy wątrobowej
-Szerzenie się choroby:
-Szybkie – chów wolno-wybiegowy,
-Wolne – boksy.

Przewlekłe zakażenie gruczołu
mlekowego S.Dublin może być
przyczyną siewstwa drobnoustrojów
zarówno z mlekiem jak i kałem. Mleko
może być przyczyną zakażenia cieląt.
Możliwe jest też lokalizowanie się
drognoustroju w węzłach chłonnych i
migdałkach.

Stres zwiększa podatność na zakażenie ale też
uaktywnia zakażenia u cieląt nosicieli (krowy
zakażone S. Dublin często rodzą cielęta zakażone
które stają się źródłem zakażenia lub stałymi
nosicielami)
U krów ciężarnych może dojść do poronień oraz
wydalania salmonelli z dróg rodnych, z moczem
oraz z mlekiem
S. Typhimurium- zakażenia 1-3 tyg życia
S. Dublin- zakażenia w 4-5 tyg życia
Choroba u dorosłych krów mlecznych zazwyczaj
pojawia się w okresie okołoporodowym (zmiany w
diecie)

Zasiedlenie organizmu zwierzęcia przez
salmonellę zależy od szeregu czynników:
takich jak ilość patogenów,
ich wirulencja,
wiek zwierzęcia,
kondycja
status immunologiczny organizmu.

PATOGENEZA
Najłagodniejszą konsekwencją, a zarazem
najprawdopodobniej najczęstszą, kontaktu z
salmonellą jest przedostanie się bakterii do żwacza i
trawieńca, które stanowią naturalną barierę
ochronną organizmu. Jeśli bakteriom uda się
przeniknąć dalej, to do wywołania choroby konieczna
jest pewna ilość zarazków oraz ich wniknięcie do
błony śluzowej jelit. Dlatego gdy dostanie się tam
mało salmonelli, muszą one wpierw namnożyć się w
ich świetle, co nie jest konieczne przy dużej ich ilości
w materiale zakaźnym.

Adherencja i penetracja do komórek nabłonka jelitowego,
w tym przede wszystkim do komórek M są cechami
szczepów zjadliwych i mają charakter procesów
czynnych, ponieważ tylko żywe, metabolicznie aktywne
pałeczki przylegają do powierzchni komórek
gospodarza i do nich wnikają. Odpowiedzią na
przesłany sygnał jest pofałdowanie błony komórkowej i
miejscowa agregacja powierzchniowych białek.
Zachodzi miejscowa rearanżacja białek cytoszkieletu
enterocytów, połączona z akumulacją aktyny,
alfaatyniny, tropomiozyny i taliny, a następnie
dochodzi do wniknięcia pałeczek na drodze
mikropinocytozy i uszkodzenia komórek.

Wystąpienie biegunki jest skutkiem zapalenia i zmian
martwiczych błony śluzowej jelit, oraz wynikiem zmniejszonej
resorpcji sodu i zwiększonej sekrecji płynów i chlorków. Jest to
powodowane bądź przez enterotoksyny, bądź przez wzrost
zawartości w błonie śluzowej cyklicznego
adenozynomonofosforanu (cAMP), prawdopodobnie pod
wpływem stymulacji przez endotoksynę neutrofilii do
uwalniania prostaglandyn uczynniających enzym cyklazę
adenylową.
Bakterie są następnie pochłaniane przez granulocyty
obojętnochłonne i makrofagi i wraz z nimi przenoszone do
regionalnych węzłów chłonnych. Gdy bakteriom uda się
przełamać system retikuloendotelialny wątroby i przedostaną
się do krwi, dochodzi do rozwoju posocznicy, która przy
równoczesnej obecności endotoksyn może spowodować
wstrząs. Proces ten przebiega, szczególnie w przypadku
młodych zwierząt, bardzo szybko i kończy się najczęściej
śmiercią.

Endotoksyna salmonelli porównywalna jest w sile swego
działania do toksyny cholery. Prowadzi do wzrostu
wydzielania chlorków przez enterocyty i hamuje
resorpcję sodu, z czego wynika pojawienie się silnej
hiponatremii. Dodatkowo, wraz z płynami i elektrolitami
organizm w ostrej fazie choroby traci duże ilości białek,
w wyniku czego dochodzi do utraty masy ciała,
wynikającej ze wzmożonych reakcji katabolicznych.
Pojawia się również znaczna utrata krwi i spada
hematokryt.
Jeśli zwierzę przeżyje manifestującą się klinicznie chorobę,
staje się długotrwałym nosicielem drobnoustrojów, które
lokalizują się najczęściej w migdałkach, węzłach
chłonnych i pęcherzyku żółciowym.

Objawy kliniczne
Zależą one głównie od serotypu
wywołującego zakażenie i związanej z nim postaci
choroby oraz od drogi wniknięcia zarazka. U bydła
okres inkubacji wynosi od 2-8 dni do kilku tygodni.
Chorują zwykle cielęta w wieku 2-6 tyg.

Przy nadostrej i ostrej postaci posocznicowej
objawy ogólne (gorączka, apatia, utrata apetytu) są bardzo
ciężkie , kał może być konsystencji wodnistej i zawierać śluz,
krew lub włóknik. Cielne krowy mogą ronić . Gorączka
utrzymuje się zwykle kilka dni. Upadki notowane są najczęściej
między 4-7 dniem od pojawienia się pierwszych objawów
klinicznych. Śmiertelnośc może sięgać 75%
Przy postaci podostrej przebieg jest mniej
gwałtowny, chodź podobny do ostrego, rokowanie jest raczej
pomyślne. Powrót do zdrowia może trwać ok 2 miesięcy
Postać przewlekłą cechuje długotrwała biegunka
oraz objawy zapalenia płuc i stawów, doprowadzające do
znacznego wychudzenia zwierzęcia.
Postać posocznicowa występuje stosunkowo
rzadko. Charakteryzuje się nagłymi upadkami bez biegunki.
Chore zwierzeta wykazują szybko postępującą depresje,
połączoną z wysoką gorączką. Śmierć następuje zwykle po 24-
48 godzinach.
Zakażenie może także przebiegać w postaci zapalenia płuc, z
objawami nerwowymi jako wynik zapalenia mózgu, w postaci
zapalenia stawów, martwicy końcówek uszu i ogona
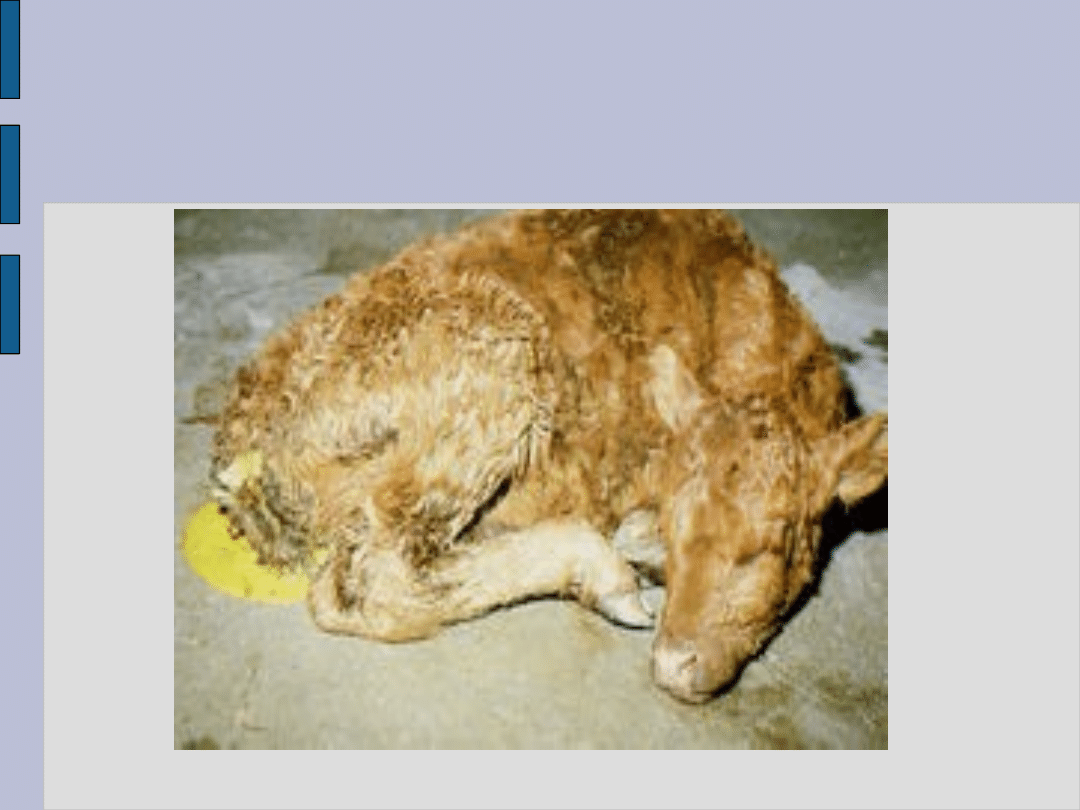
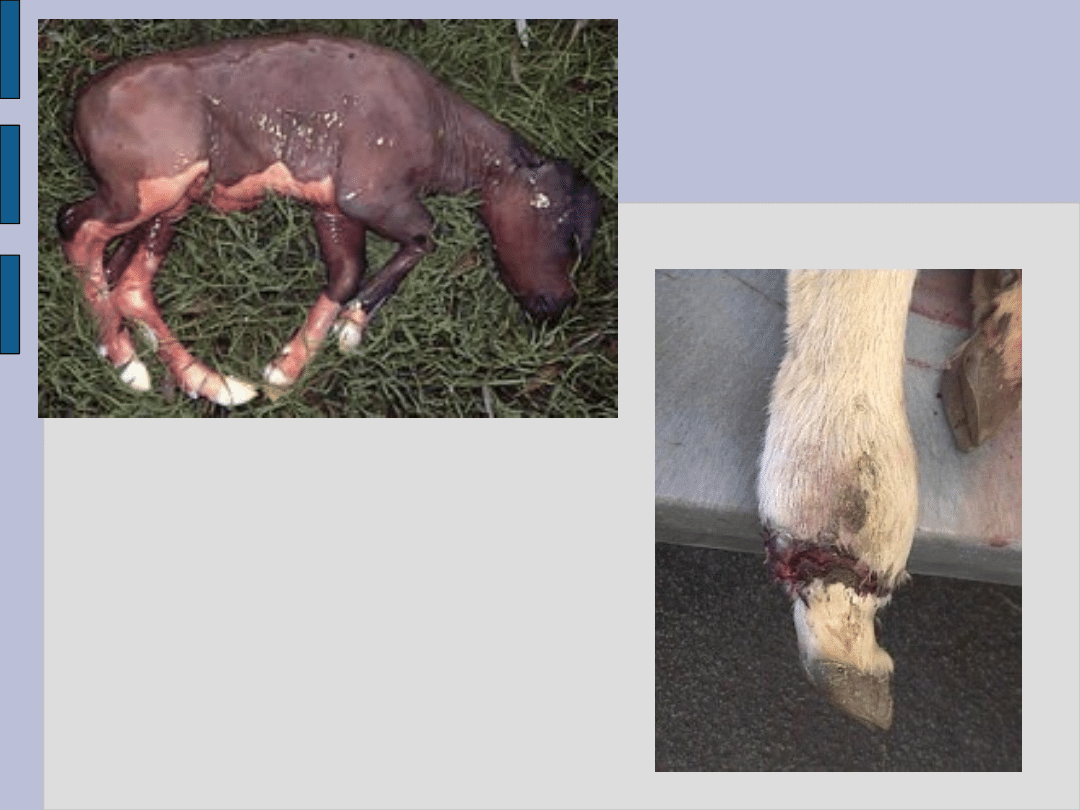
Poroniony płód
Zgorzel i martwica dystalnej
części kończyny u krowy
zainfekowanej S. Dublin

Zmiany AP
Nadostra i ostra:
Obrzęk i zwyrodnienie narządów miąższowych,
Wybroczynowość nasierdzia, opłucnej i torebki wątroby, nerek, pęcherza
moczowego, przewodu pokarmowego,
Obrzęk przerostowy śledziony (tumor lienis hiperplasticus) gumiasta,
ciemnoczerwona, napięta torebka, wybroczynowość,
Obrzęk i przekrwienie śluzówki trawieńca i jelit cienkich,
Jelita cienkie wzdęte gazowo, płynna treść, zapalenie
nieżytowe/nieżytowo-krwotoczne,
Jelito biodrowe - zapalenie dyfteroidalne,
Węzły chłonne krezkowe obrzękłe, przekrwione, marmurkowate
(ziarniniaki z serowaciejącym centrum)
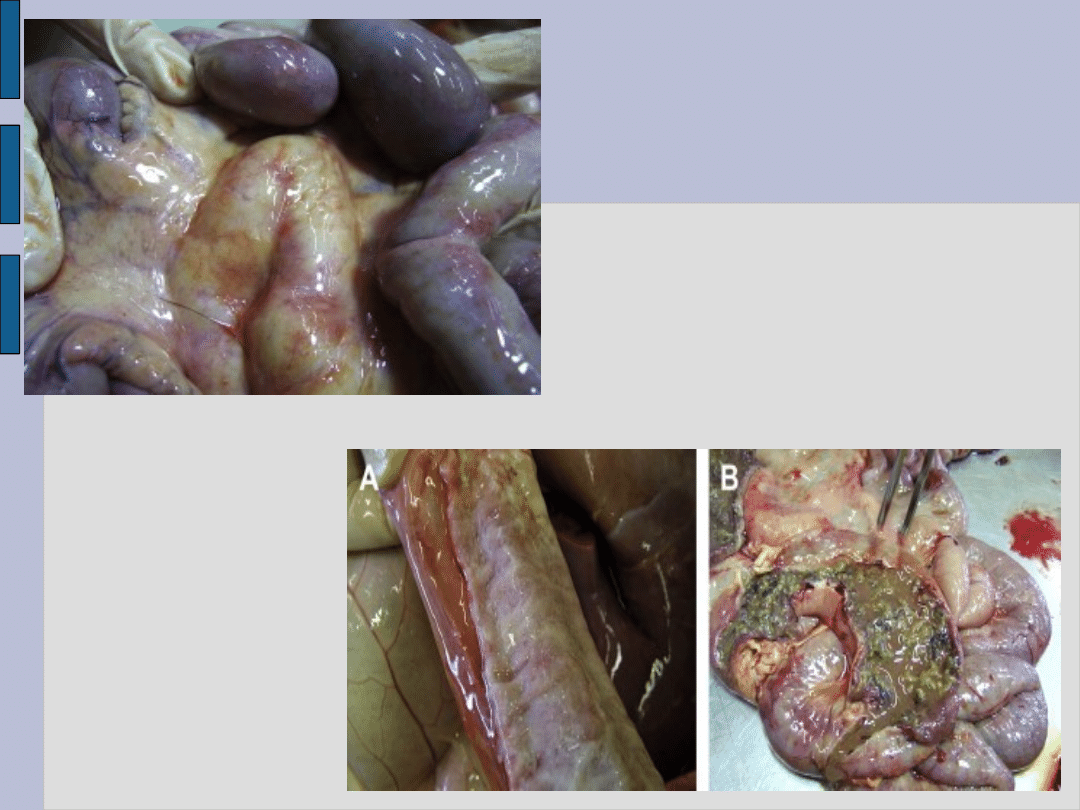
Powiększone krezkowe
węzły chłonne u cielęcia
z uogólnioną infekcją.
Złogi włóknika i
krwotoczne zapalenie
jelit

Zmiany AP
Podostra i przewlekła:
-Zmiany w płucach u 50% padłych zwierząt,
-Żółty/Żółtoczerwony wysięk w klatce piersiowej z
domieszką włóknika,
-Płuca – zapalenie doczaszkowych i dolnych partii płatów
środkowych, zapalenie nieżytowo-ropne, włóknikowe
zapalenie opłucnej i osierdzia,
-Zwyrodnienie mięśnia sercowego – matowy, wiotki, z
wybroczynami pod nasierdziem,
-Stawy i pochewki ścięgniste – obrzęk, zgrubienie torebki
stawowej, zmętnienie i wzrost ilości płynu stawowego,
- Zapalenie opon mózgowych (rzadko)

ROZPOZNANIE
-Badanie bakteriologiczne
-Próbki pobieramy od zwierząt nieleczonych
Przyżyciowo:
- Kał, wymazy z odbytu
Pobieramy pośmiertnie:
-Wycinki śledziony i wątroby w postaci ostrej
-Migdałki i pęcherzyk żółciowy w postaci przewlekłej
-Liścienie, błony płodowe, zawartość żołądka płodów
Kilkanaście posiewów w ciągu 3-6 mc by odróżnić zwierzęta w
okresie rekonwalescencji od nosicieli zakażonych przewlekle i
nosicieli biernych.
Testy serologiczne- ELISA (Ag płytkowy LPS) - U cieląt jednak do
12 tyg życia, reakcja na LPS jest słaba, co ogranicza użycie testu
ELISA u tych zwierząt.

Diagnostyka
różnicowa:
Biegunka nowo narodzonych cieląt,
Posocznica wywołana przez E. coli,
BVD/MD,
Zimowa dyzenteria,
Motyliczność,
Ostertagioza,
Kokcydioza,
Niestrawność pokarmowa,
Enterotoksemia,
Zatrucie orlicą pospolitą, ołowiem, arsenem,
Zapalenie płuc,
Zapalenie wielostawowe.

LECZENIE
-Izolacja chorych zwierząt,
-Antybiotykoterapia według antybiogramu
(enrofloksacyna, apramycyna, gentamecyna,
neomycyna),
-Leczenie objawowe (płynoterapia, probiotyki,
zakwaszacze, leki nasercowe, witaminy),
-Cielęta zamiast mleka ciepła herbatka/wywar z owsa lub
lnu

SALMONELLOZA – jest chorobą podlegającą obowiązkowi
monitorowania, mówi o tym punkt 8 „Salmonelloza i jej
czynniki chorobotwórcze” z Załącznika nr 5 „O ochronie
zdrowia zwierząt oraz zwalczaniu chorób zakaźnych zwierząt”
Dz. U. 2004 Nr 69 poz. 625.a
Także podlega rejestracji o czym mówi punkt 15
,,Salmonellozy bydła i świń" z Załącznika nr 3 „O ochronie
zdrowia zwierząt oraz zwalczaniu chorób zakaźnych zwierząt”
Dz. U. 2004 Nr 69 poz. 625.

Zakażenia
beztlenowcami
Enerotoksemia bydła
-Wywoływane przez różne typy Clostridium
perfringens.
-Bakterie produkują 4 toksyny główne i wiele toksyn
pobocznych oznaczanych literami greckimi.
-Podstawową role w chorobotwórczości u bydła
odgrywa toksyna α.
-Wrażliwe są cielęta do 10. dnia życia i cielęta ras
mięsnych od 1. do 4. m-ca życia

Patogeneza
-Pobierana siara zawiera inhibitory trypsyny.
-W skutek inhibicji toksyna β nie ulega
inaktywacji.
-Toksyna ta uszkadza kosmki jelitowe dzięki
czemu bakterie mogą przylepiać się i namnażać
-Powstają obszary martwicy i krwawień.
-Przez uszkodzona bł. śluz. Jelita toksyny mogą
przedostawać się w większej ilości do
krwioobiegu – enterotoksemia.
-Prowadzi to do szybkiej śmierci zwierzęcia.

Objawy
Postać nadostra – śmierć bez uprzednich objawów
klinicznych
Postać ostra:
Wzdęcia
Kolka
Krwista biegunka
Objawy z OUN (pobudzenie, ślepota, zaburzenia
koordynacji, skurcze, opisthotonus) – zwykle poprzedzają
zgon
Postać łagodna:
Wzdęcie żwacza i trawieńca
Zapalenie trawieńca
Owrzodzenia błon śluzowych przedżołądków i trawieńca

Zmiany sekcyjne
-Szybko postępujący rozpad tkanek
-Wybroczyny podwsierdziowe
-Jelita cienkie wypełnione krwią/skrzepami
-Badanie HP – Martwica nabłonka śluzówki jelit i
liczne bakterie

Diagnostyka
Ze względu na szybki przebieg choroby i rozpad
toksyn β diagnostyka jest utrudniona.
Pobieramy fragmenty zmienionych chorobowo błon
śluzowych.
W materiale wykrywamy toksyny za pomocą:
-Test ELISA
-PCR

Diagnostyka różnicowa
-Posocznica E. coli/Salmonella
-Kokcydioza – starsze zwierzęta

Leczenie
Antybiotykoterapia:
Betalaktamazy
Cefalosporyny
Tetracykliny
Makrolidy
Bakterie oporne są na aminoglikozydy!

Zapobieganie
-Stopniowe wprowadzanie nowej paszy
-Unikanie wahań w ilościach podawanego pokarmu i
wody
-W przypadku zagrożonych stad zaleca się podwójne
szczepienie wysokociężarnych krów w odstępie 4
tyg. i powtarzanie szczepienia co roku.
-Choroba nie podlega obowiązkowi zgłaszania ani
zwalczania z urzędu.

Diagnostyka:Od czego
zacząć
1. Wywiad epizootiologiczny:
-Wiek cieląt chorych
-Zachorowalność i śmiertelność
-Rasa
-Pochodzenie cieląt
-Sposób karmienia (mleko/preparat mlekozastępczy)
-Liczba chorych
-Podjęte lecznie

Ustalenie wieku zwierząt jest istotne ze względu na
preferencje czynników zakaźnych w zależności od
wiek:
-ETEC 0-16 dni
-rotawirus, konorawirus 5-21 dni
-EPEC, EHEC od 4 dni
-Eimeria sp. od 15 dni
-Salmonella od 7 dni
-Clostridium perfringens 7-25 dni
-BVD od 28 dni
-Cryptosporidum sp. 7-21 dni

2. Badanie kliniczne
-Ocena stopnia odwodnienia
-Zaburzeń wodno-elektrolitowych
-Zawansowania kwasicy metabolicznej
3.Badanie laboratoryjne
-Próbki świeżego kału
-Materiał wiarygodny powinien pochodzić od jak
największej liczby zwierząt
-Przy podejrzeniu zakażenia wirusowego należy pobrać
kał w pierwszych 24 godzinach choroby
-Wykazanie obecności chorobotwórczych szczepów E.coli
w wymazach z odbytu, w kale, w wycinkach jelit,
narządów wewnętrznych (posocznica)
-W postaci biegunkowej określa się obecność fimbrii przy
użyciu testu aglutynacji z przeciwciałami
mono/poliklonalnymi
-Obecność toksyn shiga- PCR,

4.Badanie sekcyjne
-W pierwszej kolejności pobieramy wycinki wątroby,
śledziony, serca, płuca a na końcu przewodu
pokarmowego
-Każdą próbkę należy pakować do osobnego
sterylnego pojemnika
5. Badanie bakteriologiczne
-Wykonujemy badania w kierunku obecności
pałeczek salmonella oraz patogennych szczepów
E.coli
-Do identyfikacji możemy użyć testów np. API firmy
bioMerieux

PROFILAKTYKA
Cielę powinno otrzymać z siarą - w ciągu kilku
pierwszych godzin życia - około 100 g
immunoglobulin, czyli 1 litr siary zawierającej
100 g immunoglobulin/ l albo 2 litry, jeśli
koncentracja immunoglobulin siary wy nosi ok.
50 g/l.
W oborze powinien więc znajdować się siaromierz
(kolostrometr) pozwalający oszacować w
przybliżeniu zawartość immunoglobulin w siarze
na podstawie jej ciężaru właściwego.
W praktyce, co najmniej 20-40 proc. cieląt cierpi
na niedobór immunologiczny wywołany
niedoborem zabezpieczenia matczynego

PROFILAKTYKA
Zwiększanie odporności swoistej to przede wszystkim
wszystkim:
-szczepienie krów przeciw Escherichia coli K99 (u krów nie
szczepionych koncentracja przeciwciał jest zwykle zbyt niska).
Pierwsze szczepienie jałówek zaleca się przeprowadzić w wieku 6-
12 mies., kolejne w późnym okresie ciąży nie później, niż 2
tygodnie przed porodem;
-szczepienia przeciw rota i coronawirusom;
-szczepionki wieloważne (zdarza się jednak, że ich skuteczność jest
poniżej oczekiwań, co wynika z różnicy pomiędzy szczepami
obecnymi w szczepionce i w obiekcie, w którym przebywają
zwierzęta);
-w przypadku zakażeń na tle drobnoustrojów, wobec których brak
szczepionek komercjalnych, proponowane jest wykorzystanie
autoszczepionek;
-szczepienia doustne cieląt noworodków nie sprawdzają się w
warunkach terenowych.

PROFILAKTYKA
Zwiększanie odporności cieląt-noworodków powinno
polegać na immunizacji ich matek szczepionkami
skierowanymi przeciw drobnoustrojom obecnym w
stadzie, co jest możliwe do zrobienia na podstawie
wcześniejszego rozpoznania bakteriologicznego i
wirusologicznego.
Warunkiem powodzenia szczepień jest jednak prawidłowy
system podawania siary noworodkom, gwarantujący
prawidłowe zabezpieczenie większości cieląt. Jeśli nie
jesteśmy w stanie prawidłowo napoić cielęta siarą
(można to sprawdzić badając poziomy immunoglobulin
w krwi cieląt w wieku 48 godzin), nie warto inwestować
w szczepionki.

PROFILAKTYKA
Wskazane jest także podawanie witaminy A przy
podejrzeniu jej niedoboru i obecności
kryptosporidiów.
Niektórzy zagrożonym cielętom podają doustnie
antybiotyki, co doraźnie zmniejsza zachorowalność,
ale indukuje narastanie antybiotykooporności
bakterii w stadzie, a ponadto zaburza tworzenie się
prawidłowej mikroflory przedżołądków. W skrajnych
przypadkach takie postępowanie może doprowadzić
nawet do awitaminozy B.

PROFILAKTYKA
Od pewnego czasu pojawiła się możliwość
dodatkowego zabezpieczania cieląt przeciwciałami
obcogatunkowymi. Szczególnie atrakcyjne jest
zastosowanie immunoglobulin żółtka jaj, uzyskanych
od kur szczepionych antygenami drobnoustrojów
powodujących biegunki u cieląt.
Najłatwiej podawać takie przeciwciała z preparatami
mlekozastępczymi w okresach największego
zagrożenia biegunkami, czyli po okresie podawania
siary matki do ok. 14 dnia życia, a następnie przez
pierwsze dwa tygodnie po przeniesieniu cieląt z
obory lub profilaktorium do cielętnika.

ZAPOBIEGANIE
- prawidłowe czyszczenie i dezynfekcja pomieszczeń
usuwa ok. 90 proc. bakterii
- mycie pod wysokim ciśnieniem usuwa 99,98 proc.
bakterii
- dobór środków wg wrażliwości czynników
biegunkotwórczych - dezynfekcja jest zwykle skuteczna
po wcześniejszym, dokładnym umyciu powierzchni
- okres odpoczynku pomieszczeń, wietrzenie po środkach
dezynfekcyjnych, likwidacja wektorów zakażenia, a
tam, gdzie to możliwe - stosowanie zasady "wszystko
pełne wszystko puste"
- dbanie o higienę stanowisk porodowych, tak aby nie
dochodziło do zakażeń bezpośrednio po urodzeniu
-izolacja i stosowne leczenie zwierząt chorych.
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
- Slide 34
- Slide 35
- Slide 36
- Slide 37
- Slide 38
- Slide 39
- Slide 40
- Slide 41
- Slide 42
- Slide 43
- Slide 44
- Slide 45
- Slide 46
- Slide 47
- Slide 48
- Slide 49
- Slide 50
- Slide 51
- Slide 52
- Slide 53
- Slide 54
- Slide 55
- Slide 56
- Slide 57
- Slide 58
- Slide 59
- Slide 60
- Slide 61
- Slide 62
- Slide 63
- Slide 64
- Slide 65
- Slide 66
- Slide 67
- Slide 68
- Slide 69
- Slide 70
- Slide 71
- Slide 72
- Slide 73
- Slide 74
- Slide 75
- Slide 76
- Slide 77
- Slide 78
- Slide 79
- Slide 80
- Slide 81
- Slide 82
- Slide 83
- Slide 84
- Slide 85
- Slide 86
- Slide 87
Wyszukiwarka
Podobne podstrony:
kolo metodologia sandra i ania
ania
PowikT ania oczne w cukrzycy
Ania Klimaszewska
Ania
ustawa zakazy, Weterynaria, Choroby zakaźne koni
zakazy u p.Profesor2, 5 ROK, CHOROBY ZAKAŹNE
Pytania Ania Woźnialis i Wojtek Zduńczyk, gik, semestr 7, seminarium, Seminarium
odpowiedzi ania
sprawozdanie Ania
Konspekt lekcji do lektury ania z Zielonego Wzgórza
Ania z Zielonego Wzgórza opracowanie
zakazy bydło I koło
zakazy
CISS - handout, praca ania
więcej podobnych podstron