
Ekstrakcja w układzie
ciecz - ciecz

Techniki ekstrakcyjne
Wśród metod przygotowania próbek techniki
ekstrakcyjne stanowią dominującą grupę.
Opierają się one na procesach przebiegających na
granicy faz :
• Gaz – ciecz czy gaz – ciało stałe ( HS )
• Ciecz – ciecz ( LLE )
• Ciecz – ciało stałe ( SPE )

Przed przystąpieniem do analizy materiału
biologicznego należy wykonać szereg czynności
wstępnych. Polegają one na :
• Przygotowaniu materiału biologicznego do
ekstrakcji
• Ekstrakcji trucizn organicznych rozpuszczalnikami
organicznymi lub innymi metodami
• oczyszczeniu

Przygotowanie materiału biologicznego
do ekstrakcji :
*Odbiałczanie
- metoda siarczanowo – amonowa
- wolframowa
* Odtłuszczanie
* Hydroliza

Odbiałczanie
Stosuje się różne substancje :
-
kw. wolframowy
-
kw. nadchlorowy
-
kw. trichlorooctowy
-
alkohol etylowy
-
mieszaninę alkoholu etylowego i kw. winowego
-
Siarczan amonowy
-
Alkaliczny roztwór siarczanu cynku
* Temp 60 – 100 C

Metoda siarczanowo - amonowa
• W temp. wrzenia wody
• 50 g próbki + siarczan amonowy i za pomocą 1 M kw.
siarkowego do ph 4
• Mieszaninę ogrzewa się do wrzenia i w tej temp utrzymuje
przez 3 min, sączy na gorąco
• Osad na sączku przemywa się wrzącą wodą do uzyskania
ok. 500 ml przesączu

Metoda wolframowa
• do odbiałczania materiału biologicznego, zawierającego
trucizny o charakterze kwaśnym i obojętnym
• 1 część materiału biologicznego homogenizuje się z 1
częścią 25% roztworu wolframianu sodowego i 1 częścią
wody
• Mieszaninę przenosi się do kolby, homogenizator
przepłukuję się 4 częściami wody
• Po podaniu 1 części 50% roztw. disiarczanu sodowego
ogrzewa się ją na łaźni wodnej, aż przestanie ciemnieć,
sączy lub wiruje
• przesącz ekstrahuje się rozp. org. - chloroform, eter , octan
etylu

Hydroliza
* Przeprowadza się w celu rozbicia połączeń z kwasem
glukuronowym oraz siarkowym
* Połączenia z kwasem siarkowym hydrolizowane są już w czasie
kilkunastominutowego ogrzewania z rozcieńczonymi kwasami
* Glukuroniany hydrolizują po ogrzaniu ze stężonymi kwasami w
proporcji 1:1 w temperaturze powyżej 100°C
* Glukuroniany mogą też ulec rozłożeniu pod wpływem
glukuronidazy. Metodę tę stosuje się do oznaczania środków
uzależniających, np.: morfiny, pochodnych benzodiazepiny,
metakwalonu, trójpierścieniowych leków przeciwdepresyjnych,
salicylanów
* W stosunku do leków zasadowych, takich jak amitryptylina,
chloropromazyna, pochodnych benzodiazepin, można używać też
enzymu bakteryjnego - proteazy alkalicznej

Ekstrakcja w układzie ciecz -
ciecz
Proces przenoszenia subst. rozpuszczonej w jednej fazie ciekłej do drugiej,
nie mieszającej się z pierwszą. Jedną fazą ciekłą jest na ogół roztwór
wodny, drugą odpowiedni rozpuszczalnik organiczny, trudno mieszający się
z wodą. W celu względnie szybkiego osiągnięcia stanu równowagi między
fazami należy zwiększyć i odnawiać powierzchnię zetknięcia faz przez
ręczne lub mechaniczne wytrząsanie całości
• Zależność tę określa prawo podziału Nernsta, zgodnie z którym substancja
wprowadzona do dwu nie mieszających się cieczy dzieli się między nie w
ten sposób, że w stanie równowagi stosunek stężeń substancji
rozpuszczonej w tych dwu cieczach jest stały w stałej temp. I nie zależy od
ogólnego stężenia tej substancji.
• Stosunek ten wyraża współczynnik podziału
K = C
0
/ C
w
• Jeżeli K > 1 to jednorazowe wykłócenie
• Jeżeli K < 1 to kilkakrotne

Wydajność ekstrakcji zależna jest od:
* współczynnika podziału substancji pomiędzy fazą
wodną (analizowany materiał) a fazę organiczną
(rozpuszczalnik użyty do ekstrakcji)
* stanu elektrochemicznego izolowanych związków

Techniki ekstrakcji:
-prosta
• Wydzielenie zw org z jego roztworu lub zawiesiny w wodzie, przez
wytrząsanie z rozpuszczalnikiem org. , w którym dany związek jest
rozpuszczalny i który nie miesza się z wodą
• W rozdzielaczu kulistym lub gruszkowym ( poj rozdzielacza powinna być
dwukrotnie większa ), który umieszcza się w pierścieniu na statywie
• Do rozdzielacza wprowadza się roztwór przeznaczony do ekstrakcji i
rozpuszczalnik (1/3 objętości roztworu ekstrahowanego )
• Wytrząsa się
• Po dokładnym wytrząśnięciu umieszcza się rozdzielacz w pierścieniu, aby
mieszanina się rozdzieliła
• Dolną warstwę wodną spuszcza się , a eterową wylewa się górnym
otworem
• Wodny roztwór zawraca się
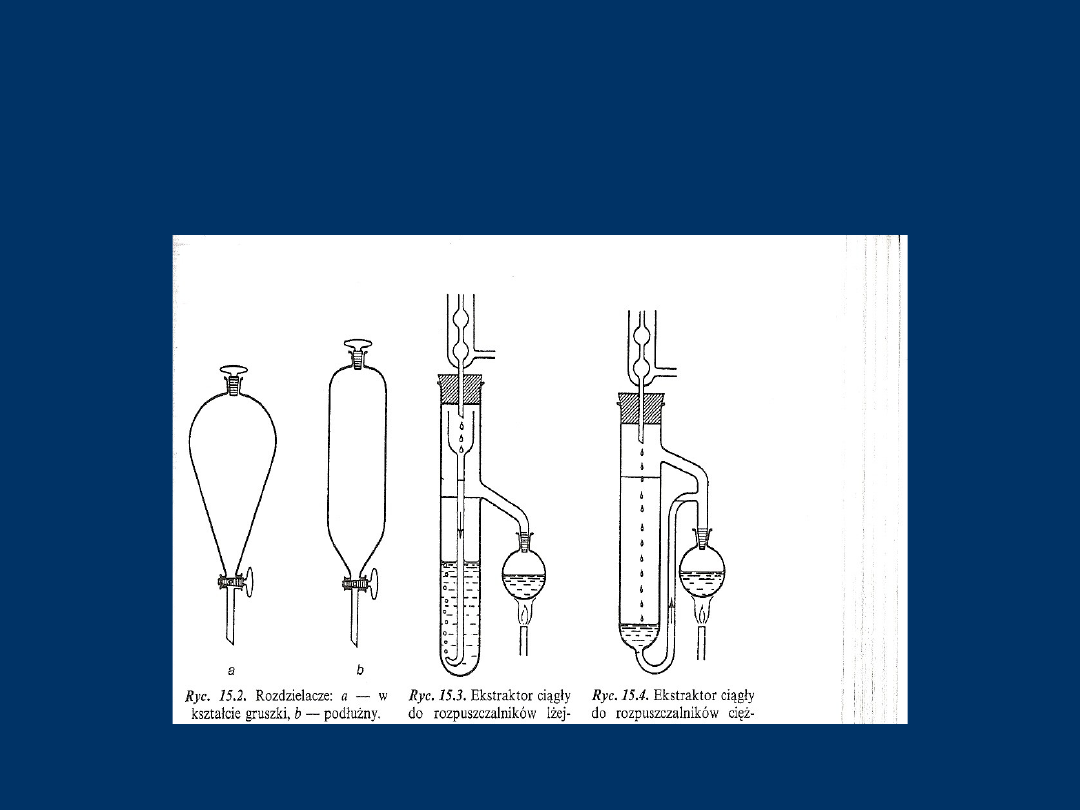
- Ciągła cieczy
• Stosowana w przypadku układów o małych współczynnikach
podziału, umożliwiając użycie małej ilości rozpuszczalnika

Ogólna zasada :
• Subst, w których przeważają gr hydrofobowe ( np. łańcuchy
alifatyczne, pierścienie benzenowe ) lepiej rozp się w rozp o
małej stałej dielektrycznej
• Subst z gr hydrofilowymi ( np. gr hydroksylowe,
karboksylowe, sulfonowe ) lepiej rozp się w rozp o dużej
stałej dielektrycznej
• Dobiera się rozp o odpowiedniej polarności, korzystając z
szeregu eluotropowego w myśl zasady „ podobne
rozpuszcza się w podobnym „

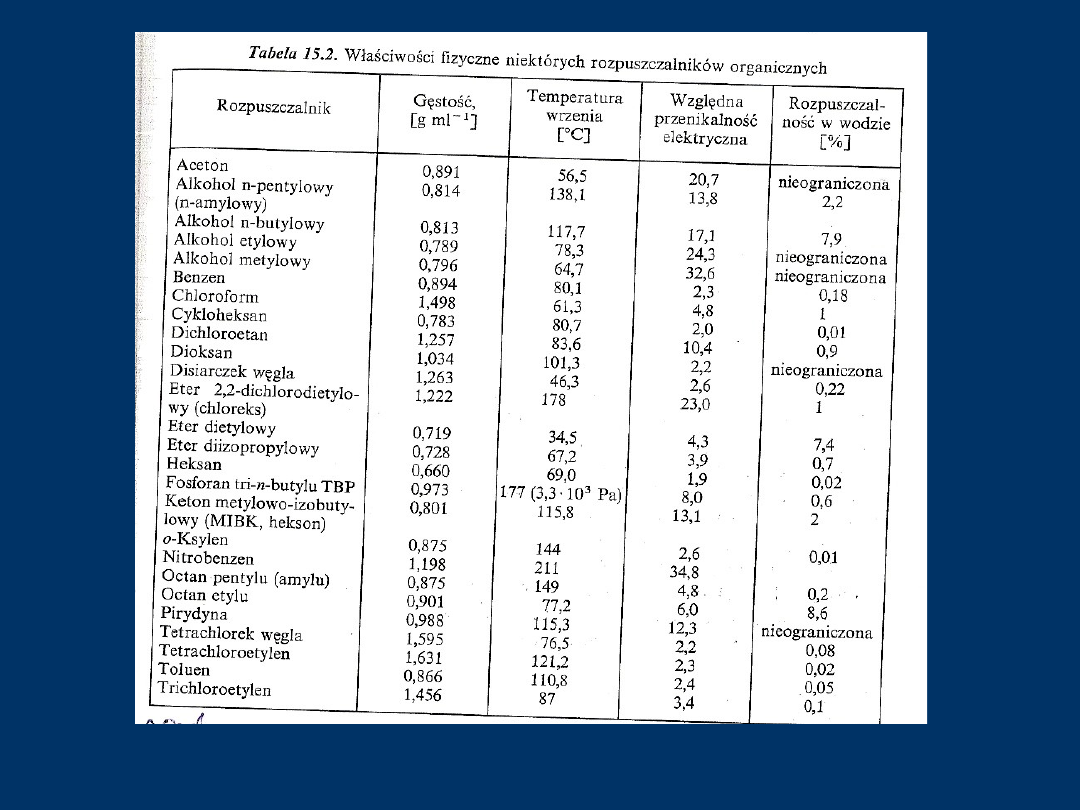
Rozpuszczalniki stosowane w
ekstrakcji :
• Najczęściej stosuje się :
- eter dietylowy
- eter diizopropylowy
- toluen
- dichlorometan
- benzynę lekką
• Przy wyborze rozpuszczalnika bierze się pod uwagę rozpuszczalność w nim
substancji ekstrahowanej oraz łatwość usunięcia go z ekstraktu. Najszersze
zastosowanie znajduje eter dietylowy
• Najlepiej rozpuszczalniki mało rozp w wodzie
• Zwraca się uwagę na gęstość rozp, temp wrzenia i palność
• Stosuje się również mieszaniny dwóch rozp lżejszych od wody np.. Eteru
dietylowego i alk pentylowego
• Dogodniejsze są mniej lotne

• Do rozpuszczalników organicznych przechodzą w trakcie ekstrakcji
substancje:
* obojętne
* kwasowe
*zasadowe
w formie niezdysocjowanej, bowiem nierozpuszczalne w wodzie,
lepiej rozpuszczają się w rozpuszczalnikach organicznych, dzięki
czemu mogą być łatwiej ekstrahowane.
Związki organiczne – leki o charakterze słabych kwasów
lub zasad występują w fazie wodnej częściowo w formie
niezjonizowanej, częściowo zjonizowanej.

• Zmiana pH (alkalizacja bądź zakwaszanie) poddawanej ekstrakcji
fazy wodnej powoduje przeprowadzenie poszukiwanej trucizny w postać
niezdysocjowaną i zależnie od charakteru chemicznego umożliwia jej
wydajną ekstrakcję z odpowiednio dobranego środowiska.
* związki o charakterze kwasowym przeprowadza się w postać
niezdysocjowaną przez zakwaszenie kwasami : winowym, solnym,
fosforowym lub siarkowym
* związki o charakterze zasadowym przez alkalizację roztworami
NaOH, KOH, Na
2
CO
3
, NH
4
OH.
Lipofilowe substancje o charakterze obojętnym
występuje w fazie wodnej w formie niezjonizowanej
mogą być izolowane ze środowisk o różnym pH (jeśli nie
ulegają rozkładowi pod wpływem kwasów lub alkaliów).
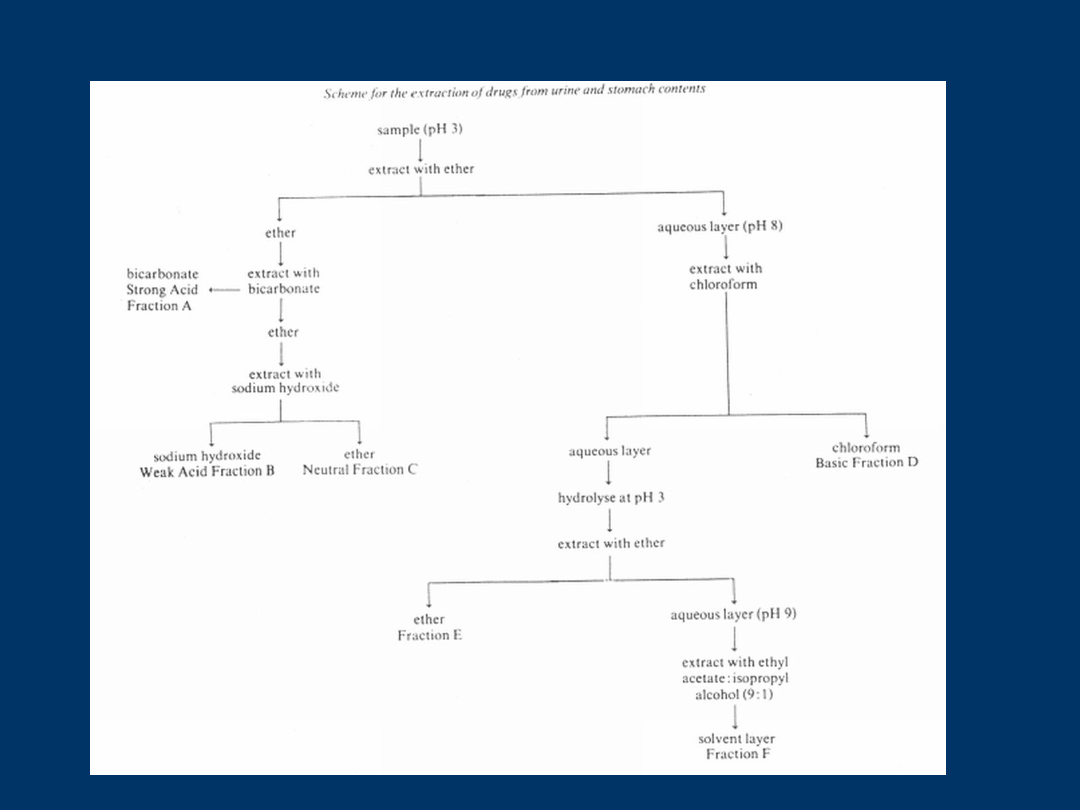
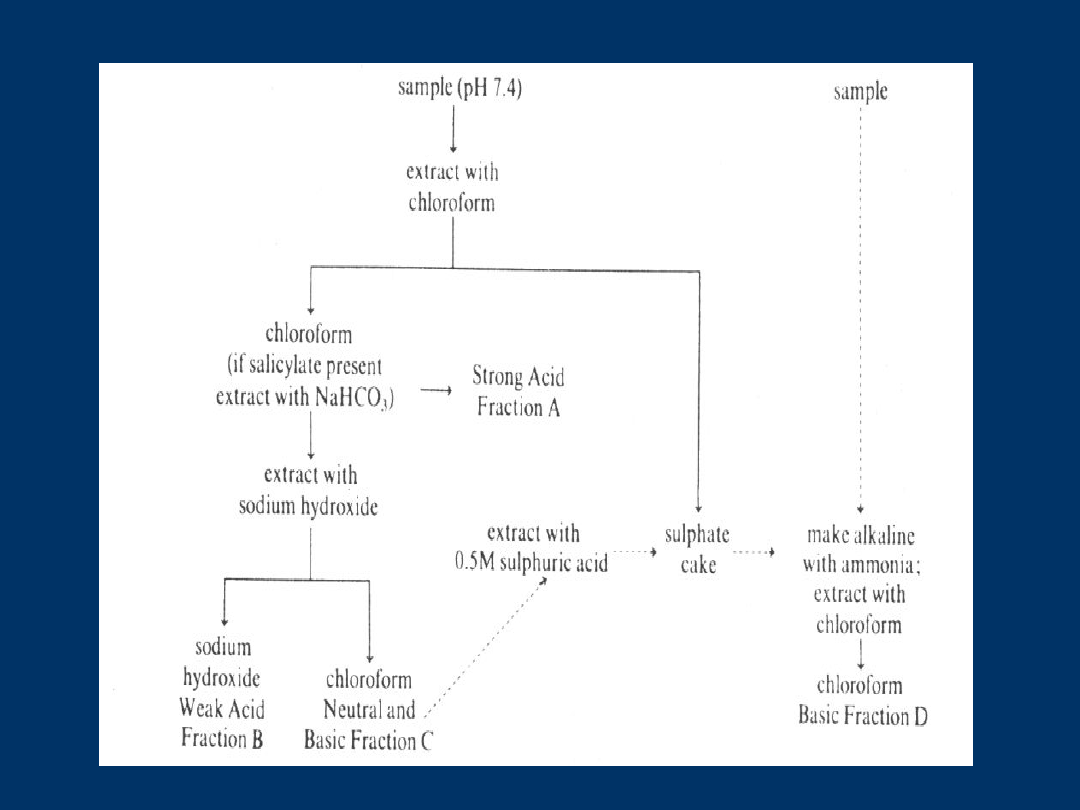
Metoda Stass – Otto
według Stass – Otto próbę poddaje się kolejnym ekstrakcjom różnymi rozp org
zmieniając ph próby
I gr
Subst eksrahuje się eterem z roztworu
kwaśnego ( ph 3-4 )
Np. kw salicylowy, aspiryna,
fenacetyna, barbiturowce, pestycydy
chloro- i fosfoorganiczne
II gr
Subst ekstrahuje się eterem ze
środowiska alkalicznego (NaOH ; ph 9
– 10 )
Większość alkaloidów i zw
syntetycznych o char. Zasadowym :
np.. Strychnina, papaweryna,
atropina, chinina, kokaina, poch
fenotiazyny
III gr
Trucizny ekstrahuje się eterem ze
środ. Amoniakalnego ( NH
4
OH ; ph 9 –
10 )
apomorfina
IV gr
Subst dające się ekstrahować
chloroformem z roztw amoniakalnego
( NH
4
OH ; ph 9 – 10 )
morfina
V gr
Subst pozostałe w roztw wodnym, nie
eksteahuje się wymienionymi rozp org

Wady metody :
*
długotrwały tok wyosabniania trucizny;
* mała wydajność uniemożliwiająca
niekiedy ilościowo oznaczenie
trucizny w badanym materiale;
* uzyskiwanie ekstraktów
zanieczyszczonych ciałami balastowymi;
* konieczność użycia dużej ilości
materiału;
* zużycie znacznych ilości odczynników
do ekstrakcji;
* powstawanie emulsji w toku ekstrakcji;
* niewystarczająca wykrywalność
.
Przykłady leków
Salicylany – char kwaśny
Kw salicylowy – ph przesączu po wytrząśnięciu
0,5 g subst z 50 ml wody – 2 – 3
Kw acetylosalicylowy – ph ,,, 1 g subst z 10 ml
wody 2,5 – 3,5
Salicylamid – ph roztw nasyconego 4,5 – 5,5
Salicylan sodu – ph 10 % roztw 5 - 7
Rozp w etanolu 95 ‘ i wodzie, nierozp w
chloroformie i eterze
Rozp w etanolu i 1M NaOH, chloroformie, eterze,
trudno w wodzie
Rozp w KOH, NaOH, NH
4
OH, roztw węglanów
alkalicznych, etanolu 95, słabo w chloroformie i
eterze, b.trudno w wodzie
Paracetamol
Ph roztw 20 mg subst w 1 ml wody 5,5 – 6,5
Rozp w etanolu 95, trudno w wodzie, nierozp w
eterze
Barbiturany
Kw barbiturowy – char mocnego kw
5,5- dipodstawione – b słabe kw
Rozp w etanolu 95, KOH, eterze, wrzącej wodzie,
słabo w chloroformie, trudno w zimnej wodzie
Sole Na – łatwo w wodzie, trudno w etanolu,
nierozp w chloroformie i eterze
Poch fenotiazyny –w postaci soliHCl,maleinianów
HCl promazyny – ph 4,2 – 5,4
HCl chlorpromazyny- ph 4 – 5,5
HCl tiorydazyny – ph 3,5 – 4,5
Rozp w wodzie, etanolu, chloroformie, nierozp w
eterze
Poch benzodiazepiny – 1,4 ph 9 – 10
( chlordiazepoksyd w postaci HCl ph 2 – 3 )
Chlordiazepoksyd – rozp w wodzie i etanolu,
nierozp w eterze i chloroformie
Diazepam – łatwo w eterze, rozp w chloroformie,
etanolu, nierozp w wodzie
Oksazepam – słabo w etanolu, eterze i
cloroformie, nierozp w wodzie


Dziękuję za uwagę
D.M.
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
Wyszukiwarka
Podobne podstrony:
Ekstrakcja ciecz ciecz4 ppt
Ekstrakcja ciecz ciecz3 ppt
Ekstrakcja ciecz ciecz ppt
Stopień wyekstrahowania w układzie ciecz – ciecz2
Ekstrakcja ciecz ciecz4 ppt
12a Równowaga ciecz para w układach dwuskładnikowych (a)id 14224 ppt
Focus Ekstra 2 2008
Focus Ekstra 7 2008
poprawa druk, Uczelnia, sem I, fiza, LABORATORIUM, Nowe laborki, Ciecz
Ekstrakcja
Ekstrakt z pestek grejpfruta i jego kosmetyczne właściwości
biochemia ekstrakcja dna ĆWICZENIA PYTANIA
ekstrakcja zęba w znieczuleniu
EKSTRAKCJA OLEJKÓW ETERYCZNYCH Z MATERIAŁU ROSLINNEGO
Izolacja ekstraktów z roślin i ziół
Odpowiedzialność ekstraneusa w świetle art 21 § 2 k k opracowanie
Wpływ energii mieszania na współczynnik wnikania w układzie ciało stałe - ciecz, pwr biotechnologia(
więcej podobnych podstron