
Georg Wittig, 1897
- 1987
niemiecki chemik,
Nagroda Nobla
1979
Georg Wittig, Ulrich
Schöllkopf
Über Triphenyl-phosphin-
methylene
als olefinbildende
Reagenzien.
Berichte der Deutschen
Chem. Ges. 87 (9), 1318–
1330, 1954.
2
J. Wilamowski 2011 - Reakcja
Wittiga
1. YLIDY – struktura i otrzymywanie
1. YLIDY – struktura i otrzymywanie
Dygresja – jaka jest hybrydyzacja
atomu azotu w amoniaku?
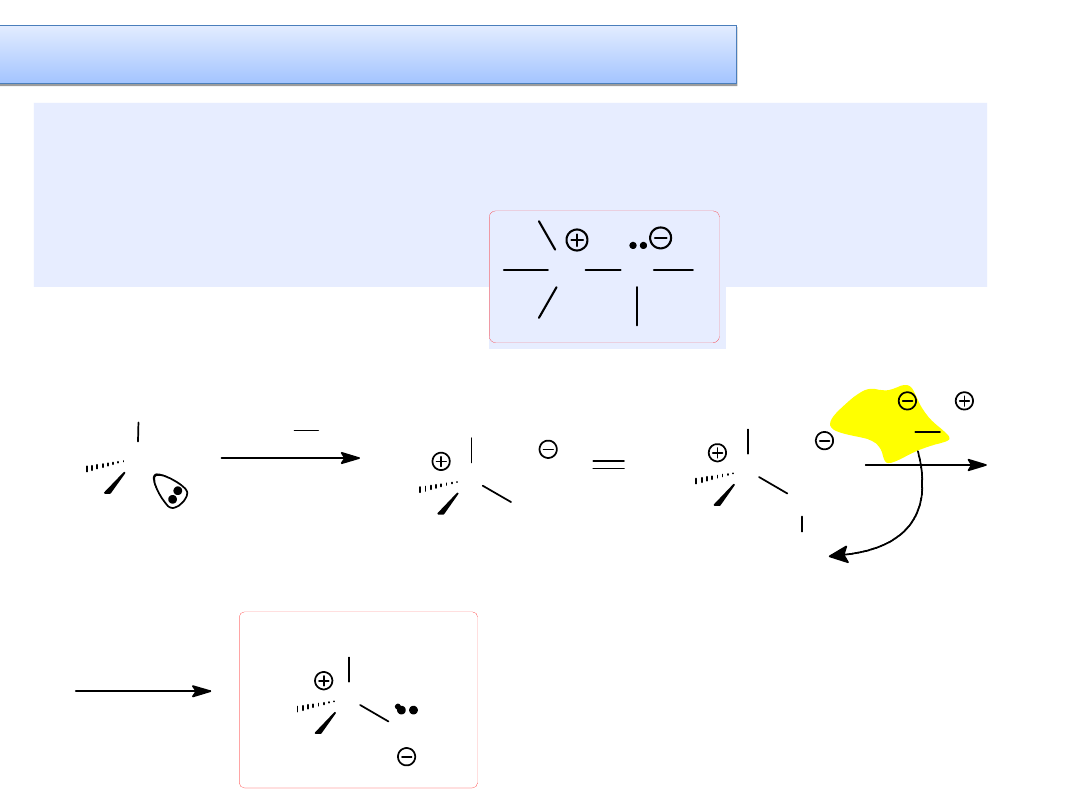
YLIDY
- związki posiadające
na sąsiadujących
atomach ładunek dodatni oraz z ujemny
, przy
czym atom z ładunkiem dodatnim posiada
oktet elektronowy
+CH
3
Br
N
CH
3
H
3
C
H
3
C
CH
3
N
CH
3
H
3
C
H
3
C
Br
Ph Li
N
CH
3
H
3
C
H
3
C
CH
2
H
Br
S
N
2
bardzo mocna
zasada
N
CH
3
H
3
C
H
3
C
CH
2
halogenek metylu
lub 1
o
alkilu
- Ph-H, - LiBr
Ylid azotowy
karboanion stabilizowany wyłącznie indukcyjnie
niezwykle reaktywny!
X
Y
JAK OTRZYMUJE SIĘ
YLIDY?
a) Ylidy azotowe
3
J. Wilamowski 2011 - Reakcja
Wittiga
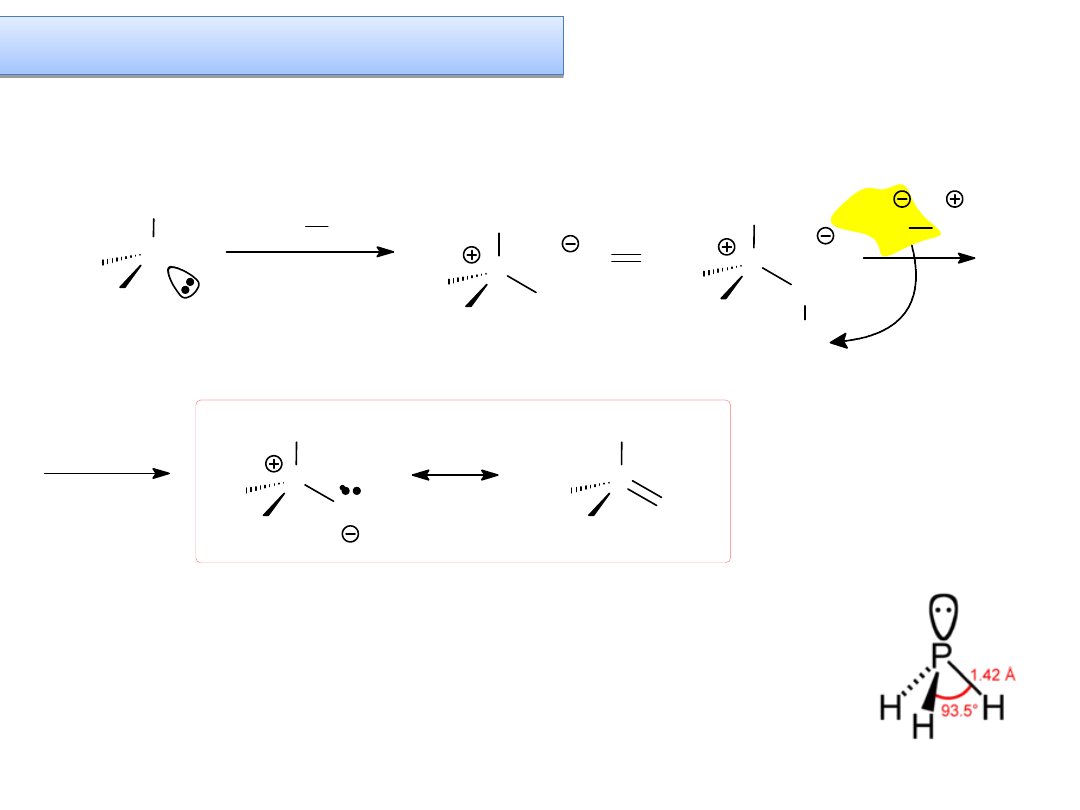
YLIDY cd. – ylidy fosforowe
YLIDY cd. – ylidy fosforowe
Dygresja – jaka jest hybrydyzacja atomu
fosforu w fosfanie (fosfinie, fosforowodorze)?
+CH
3
Br
P
Ph
Ph
CH
3
Ph
P
Ph
Ph
Ph
Br
Ph Li
P
Ph
Ph
CH
2
H
Ph
Br
S
N
2
bardzo mocna
zasada
P
Ph
Ph
CH
2
Ph
halogenek metylu
lub 1
o
alkilu
- Ph-H, - LiBr
Ylid fosforanowy
karboanion stabilizowany indukcyjnie i rezonansowo
reaktywny
P
Ph
Ph
CH
2
Ph
sól fosfoniowa
(bromek trifenylo-
metylofosfoniowy)
trifenylometylenofosforan
trifenylofosfina
Dlaczego w ylidach
fosforanowych możliwa jest
stabilizacja rezonansowa,
a w ylidach azotowych nie?
b) Ylidy fosforowe
4
J. Wilamowski 2011 - Reakcja
Wittiga
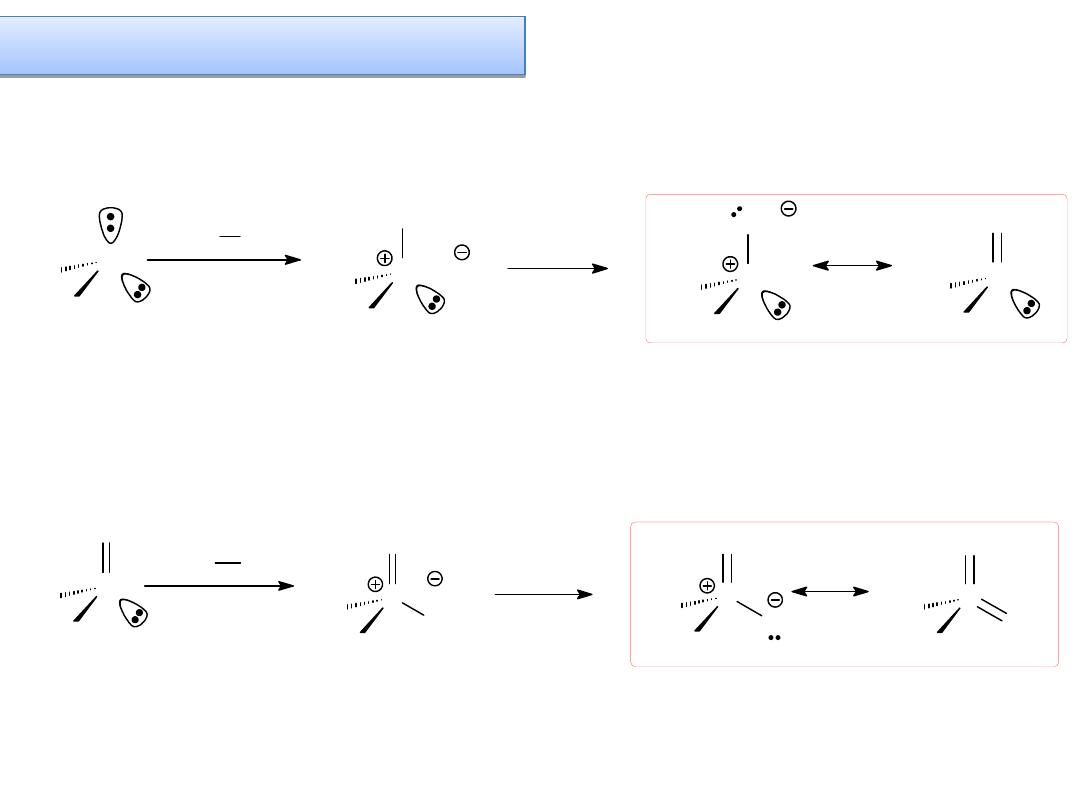
YLIDY cd. – ylidy siarkowe
YLIDY cd. – ylidy siarkowe
c) Ylidy siarkowe
+CH
3
I
S
CH
3
CH
3
O
I
S
N
2
bardzo mocna
zasada
halogenek metylu
lub 1
o
alkilu
Ylid sulfoksoniowy
trwalszy i mniej reaktywny niż sulfoniowy
(dlaczego???)
sól sulfoksoniowa
NaH
-H
2
-NaI
S
CH
3
CH
3
O
CH
3
S
CH
3
CH
3
O
CH
2
S
CH
3
CH
3
O
CH
2
+CH
3
Br
S
CH
3
CH
3
Br
S
N
2
bardzo mocna
zasada
halogenek metylu
lub 1
o
alkilu
Ylid sulfoniowy
bardzo reaktywny!
sól sulfoniowa
S
CH
3
CH
3
CH
3
S
CH
3
CH
3
CH
2
S
CH
3
CH
3
CH
2
5
J. Wilamowski 2011 - Reakcja
Wittiga
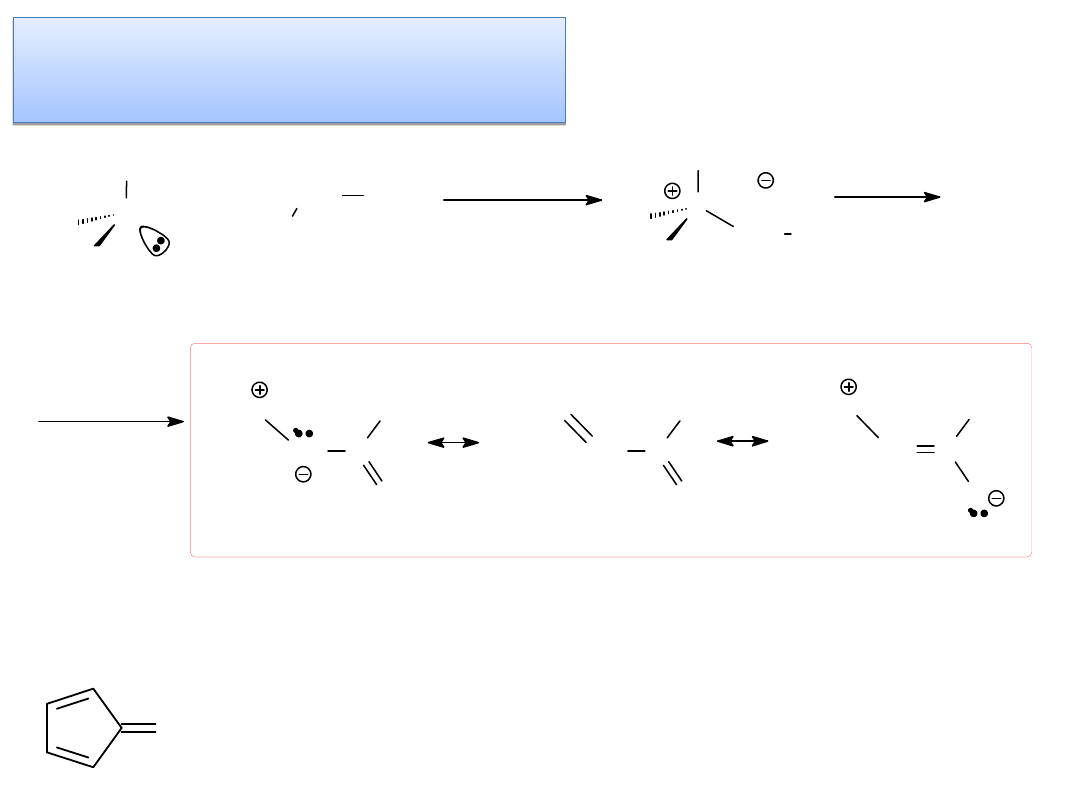
YLIDY – cd. - ylidy
stabilizowane
YLIDY – cd. - ylidy
stabilizowane
PPh
3
Ten ylid też jest niezwykle trwały – dlaczego?
+
CH
2
Br
EtOOC
P
Ph
Ph
CH
2
Ph
COOEt
P
Ph
Ph
Ph
Br
S
N
2
Ph
3
P
CH C
O
OEt
halogenek alkilu
z grupą EWG
- H
2
O, - NaBr
- CO
2
tzw. ylid fosforanowy STABILIZOWANY
dodatkowa stabilizacja rezonansowo w wyniku sprzężenia z grupą EWG
mało reaktywny
trifenylofosfina
(lub inna grupa elektronoakceptorowa,
tzw. EWG: np. -COR, -CN)
NaHCO
3
słaba zasada
Ph
3
P
CH C
O
OEt
Ph
3
P
CH C
O
OEt
6
J. Wilamowski 2011 - Reakcja
Wittiga
2. Reakcje ylidów fosforowych - ogólny schemat reakcji Wittiga:
2. Reakcje ylidów fosforowych - ogólny schemat reakcji Wittiga:
CH
PPh
3
G
+
R
1
C
R
2
O
C
C
PPh
3
O
R
1
G
H
R
2
C
C
G
H
R
1
R
2
P
O
Ph
Ph
Ph
+
tlenek
trifenylofosfiny
(czasem trudno go
oddzielić od alkenu)
YLID
- optymalnie: aldehyd
- ketony nie reagują ani ze stabilizowanymi ylidami,
ani z ylidami otrzymywanymi z halogenków alkilu
- związki karbonylowe mogą być sprzężone z C=C,
mogą zawierać podstawniki np.:
estrowe, OR, OH, NR
2,
NO
2
OKSAFOSFETAN
- wiazanie podwójne w ściśle z
definiowanej pozycji
- alken nie może być tetrapodstawiony
(dlaczego?)
CH
2
X
G
+ PPh
3
CH
2
PPh
3
G
X
zasada
CH
PPh
3
G
halogenek alkilu - optymalnie 1
o
(dla 2
o
- zwykle niskie wydajności)
G = H, alkil, aryl, EWG: -COR, CN itp.
YLID
sól fosfoniowa
„siła napędowa” rozpadu:
tworzenie trwałego wiązania P=O
(529 kJ/mol w Ph
3
P=O)
„siła napędowa” rozpadu:
tworzenie trwałego wiązania P=O
(529 kJ/mol w Ph
3
P=O)
7
J. Wilamowski 2011 - Reakcja
Wittiga
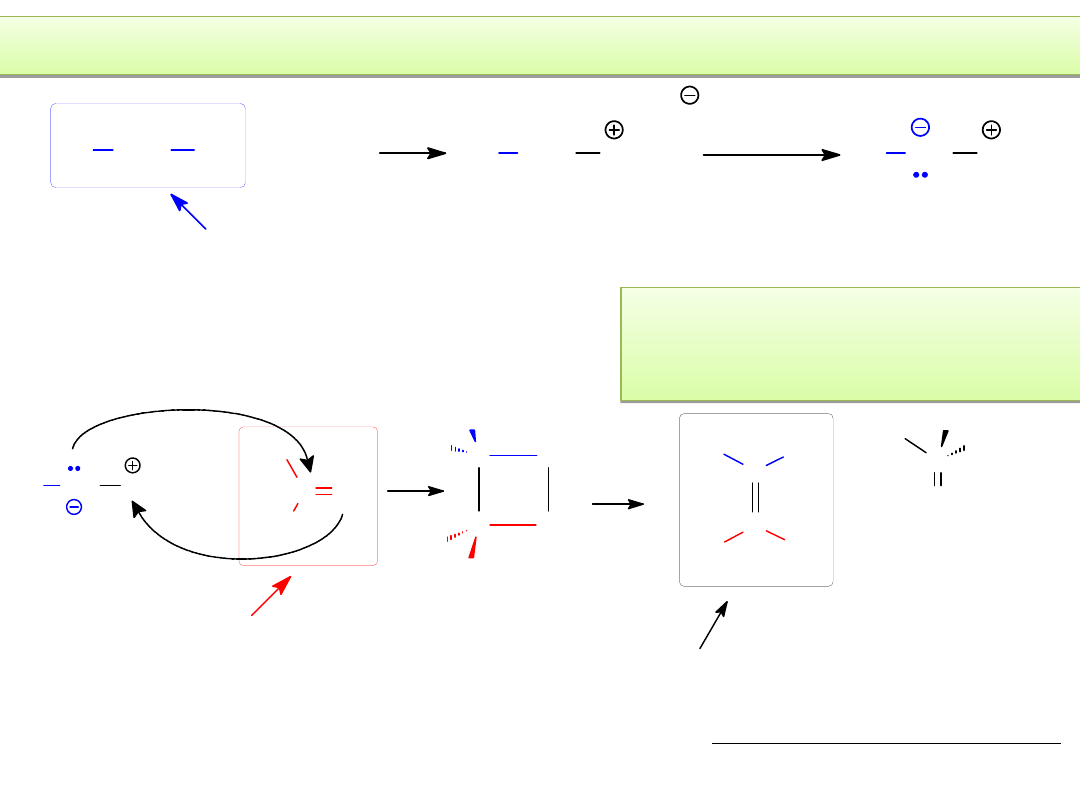
3. Mechanizm reakcji Wittiga i stereochemia procesu
3. Mechanizm reakcji Wittiga i stereochemia procesu
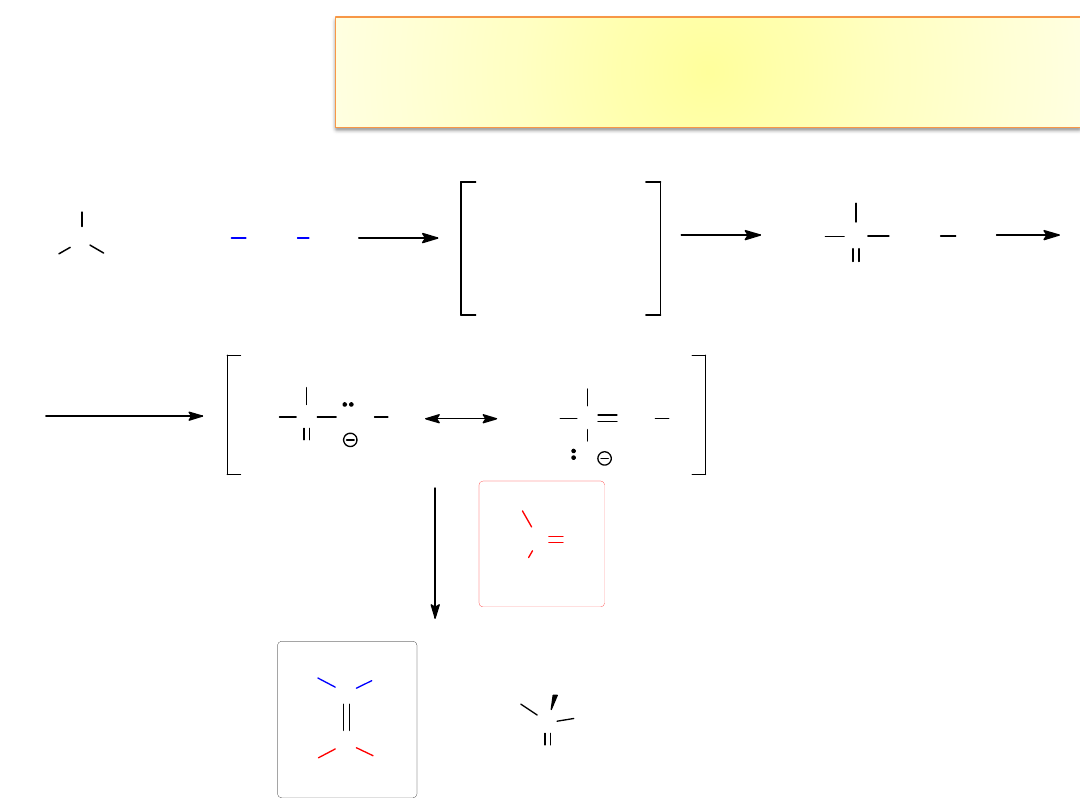
PROBLEM 1:
W wyniku reakcji Wittiga z udziałem niestabilizowanych ylidów powstają
zwykle alkeny o konfiguracji (Z) – dlaczego?
A) Wyjaśnienie w oparciu o (
BŁĘDNY!
) mechanizm klasyczny:
O
R
H
PPh
3
H
R'
O
R
H
PPh
3
H
R'
PPh
3
H
R'
O
H
R
BETAINA
(w rzeczywistości nie tworzy się)
PPh
3
H
R'
O
H
R
- Ph
3
P=O
H
H
R'
R
Z-alken
8
J. Wilamowski 2011 - Reakcja
Wittiga
Mechanizm reakcji Wittiga i stereochemia procesu – cd.
Mechanizm reakcji Wittiga i stereochemia procesu – cd.
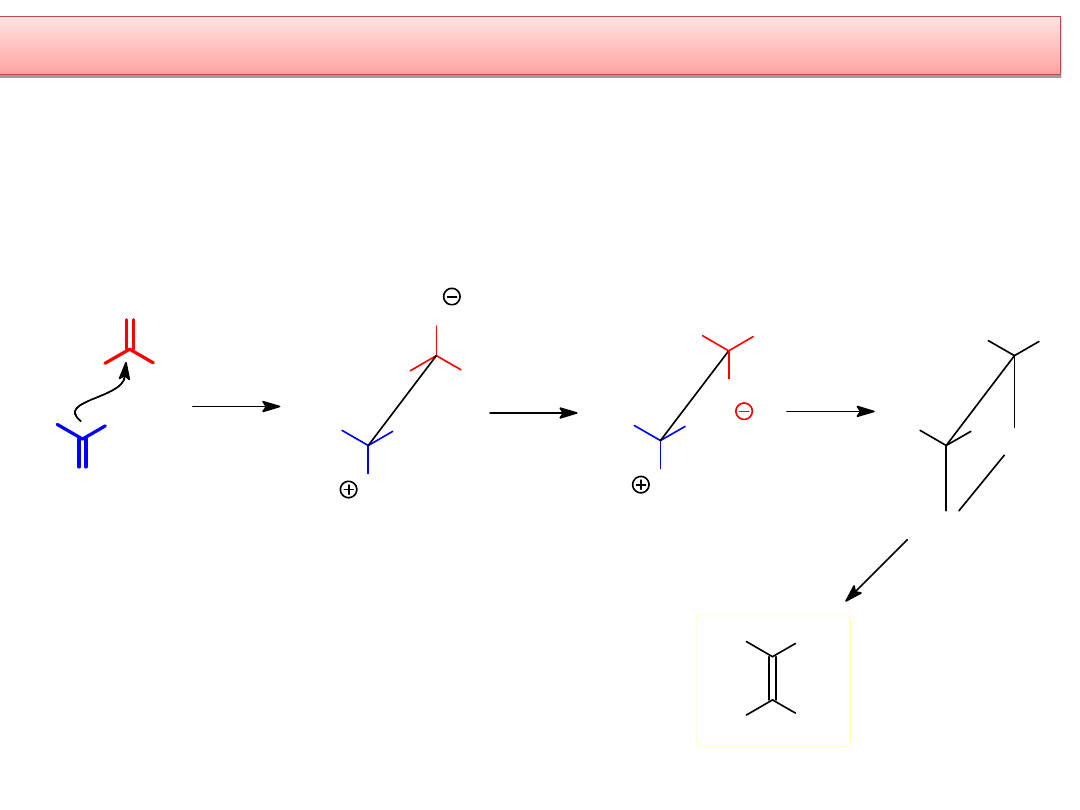
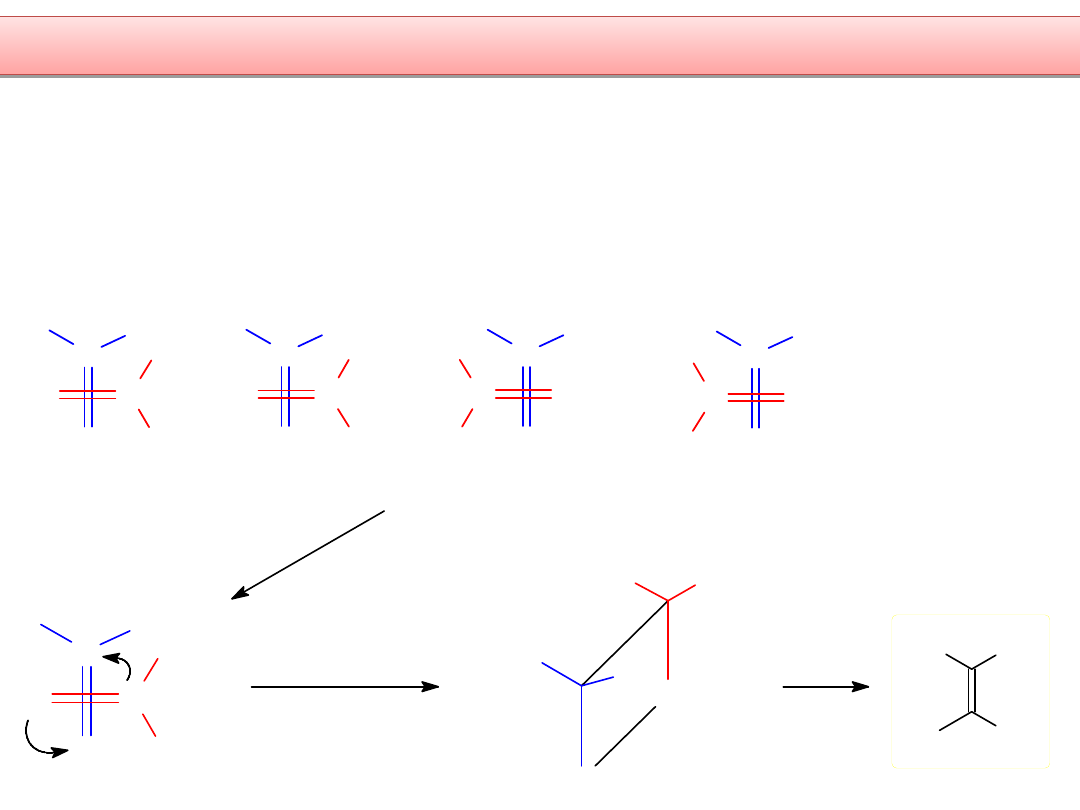
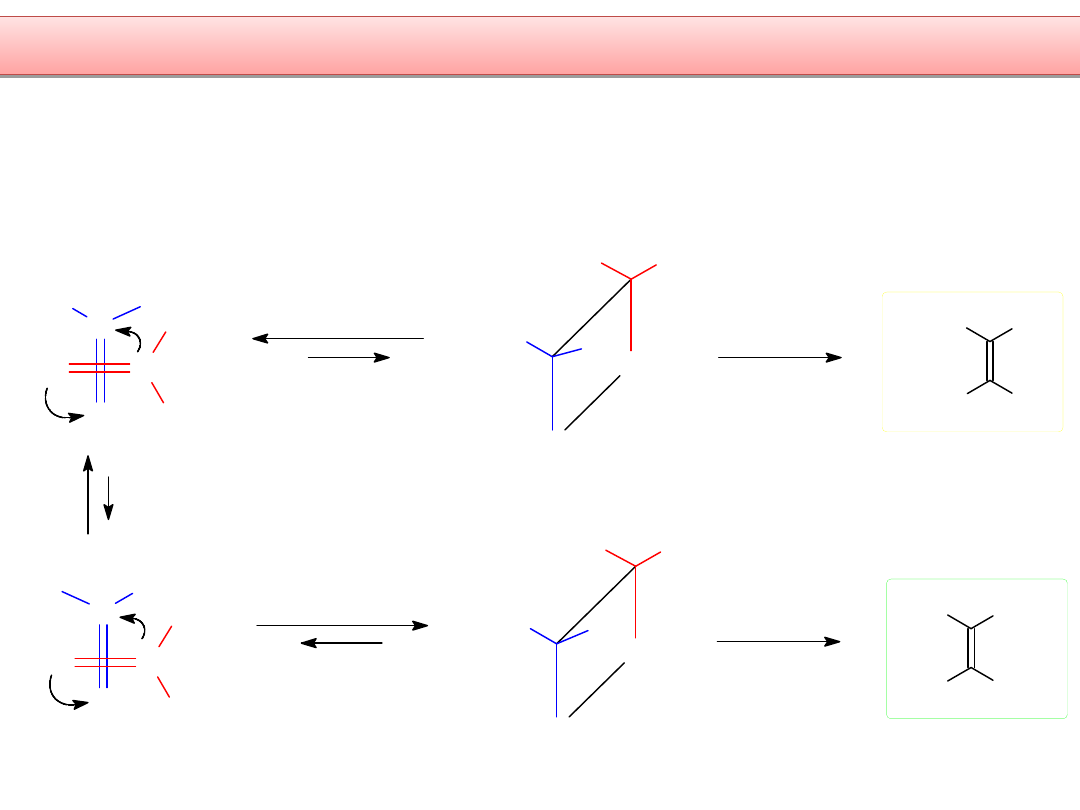
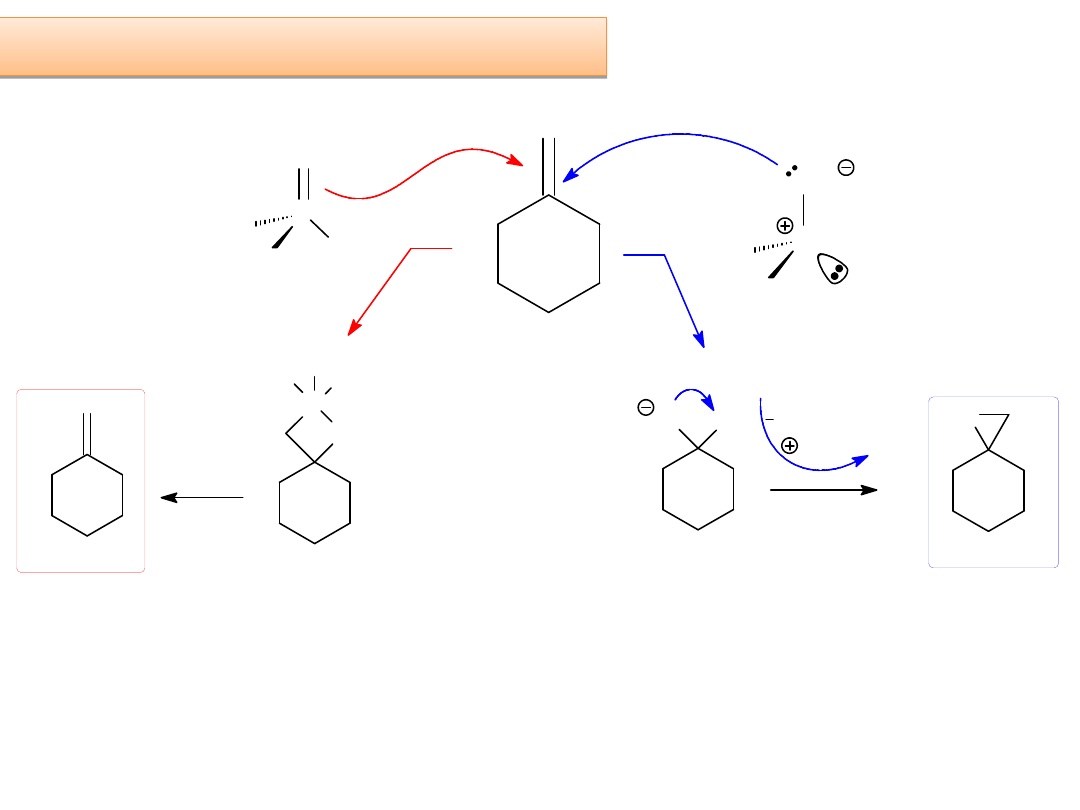
B) Wyjaśnienie w oparciu o współcześnie akceptowany mechanizm
Wittiga jako addycji uzgodnionej [2 + 2] z udziałem orbtali d-LUMO
Który ze stanów
przejściowych
jest najtrwalszy?
W stanie przejściowym cząsteczki układają się tak, że wiązania podwójne są
względem siebie pod kątem prostym
C
PPh
3
R'
H
C
O
R
H
C
PPh
3
R'
H
C
O
R
H
C
PPh
3
R'
H
C
O
R
H
C
PPh
3
R'
H
C
O
R
H
C
PPh
3
R'
H
C
O
R
H
O
PPh
3
R'
H
R
H
R
R'
H
H
- Ph
3
P=O
nieodwracalnie!
9
J. Wilamowski 2011 - Reakcja
Wittiga
PROBLEM 1:
W wyniku reakcji Wittiga z udziałem STABILIZOWANYCH ylidów powstają
zwykle alkeny o konfiguracji (E) – dlaczego?
Mechanizm reakcji Wittiga i stereochemia procesu – cd.
Mechanizm reakcji Wittiga i stereochemia procesu – cd.
C
PPh
3
EWG
H
C
O
R
H
O
PPh
3
EWG
H
R
H
R
EWG
H
H
- Ph
3
P=O
odwracalnie!
wolniej niż
odtworzenie
substratów
C
PPh
3
EWG
H
C
O
R
H
O
PPh
3
H
EWG
R
H
R
H
H
EWG
- P h
3
P=O
syzbciej niż
odtworzenie
substratów
DOMINUJ E
10
J. Wilamowski 2011 - Reakcja
Wittiga
4. Modyfikacje reakcji Wittiga
– reakcja
Hornera-Wadswortha-Emmonsa
OEt
P
EtO
OEt
+
G CH
2
X
OEt
P
EtO
CH
2
O
G
?
reakcja
Arbuzowa
alkilofosfonian dietylu
- optymalnie 1
o
- G = H, alkil, aryl,
EWG: -COR, CN itp.
mocna zasada
(np. Ph-Li)
OEt
P
EtO
CH
O
G
OEt
P
EtO
CH
O
G
YLID FOSFONIANOWY
- bardziej reaktywny niż
ylid fosoforanowy (Wittiga)
- gdy G = EWG może reagować
z aldehydami i ketonami
reakcja
HORNERA
C
C
G
H
R
1
R
2
P
O
O
-
OEt
EtO
+
sól diestru kwasu fosforowego
(łatwo oddzielić od alkenu)
aldehyd lub keton
+
R
1
C
R
2
O
alken
o konfiguracji (E)
(UWAGA : zad. 2F!]
11
J. Wilamowski 2011 - Reakcja
Wittiga
5. Reakcje ylidów siarkowych
5. Reakcje ylidów siarkowych
S
CH
3
CH
3
CH
2
O
P
Ph
Ph
CH
2
Ph
P
O
Ph PhPh
- O=PPh
3
O
CH
2
S(CH
3
)
2
- S(CH
3
)
2
O
Dlaczego???
(dwie przyczyny…)
12
J. Wilamowski 2011 - Reakcja
Wittiga
Reakcje ylidów siarkowych – cd.
Reakcje ylidów siarkowych – cd.
- Porównanie reaktywności ylidów suloniowych i sulfoksoniowych
– aspekt stereochemiczny:
O
OH
+H
2
C=S(CH
3
)
2
+H
2
C=SO(CH
3
)
2
O
OH
O
OH
13
J. Wilamowski 2011 - Reakcja
Wittiga
ZADANIA:
1) Zaproponuj optymalną metodę syntezy poniższych związków
z wykorzystaniem reakcji Wittiga. Jeśli nie jest to możliwe, zaproponuj
metodę alternatywną metodę, w której tworzy się wiązanie węgiel-węgiel
C
A
B
D
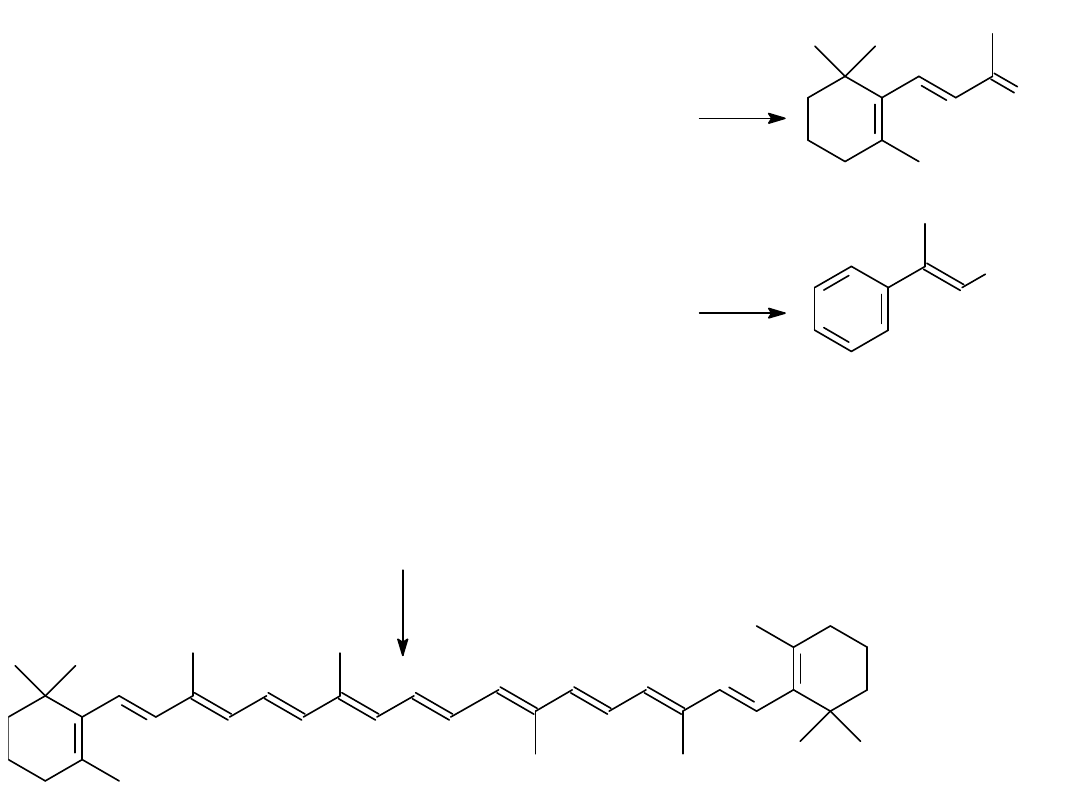
14
J. Wilamowski 2011 - Reakcja
Wittiga
ZAD. 1. cd.
E
O
-jonon
COOEt
F
G
15
J. Wilamowski 2011 - Reakcja
Wittiga
2) Podaj wzory produktów poniższych reakcji. W reakcji A
pamiętaj o stereochemii procesu!
O
H
3
C
CH
3
H
H
+ PPh
3
A)
O
Ph
H
H
H
+ Ph
3
P-CH-COOEt
B)
+ Ph
3
P-CH-O-CH
3
C)
O
H
3
O
+
16
J. Wilamowski 2011 - Reakcja
Wittiga
3) Jakich produktów można oczekiwać w reakcji karwonu
z podanymi ylidami?
O
H
2
C=S(CH
3
)
2
H
2
C=PPh
3
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
Wyszukiwarka
Podobne podstrony:
1431 W3 Reakcje 2012
Czynności obronne i reakcje stresowe
CZLOWIEK I CHOROBA – PODSTAWOWE REAKCJE NA
Fizyka 0 wyklad organizacyjny Informatyka Wrzesien 30 2012
pmp wykład podmioty 2011 2012
Cukrzyca ciężarnych 2012 spec anestetyczki
KOMPLEKSY POLAKOW wykl 29 03 2012
Biotechnologia zamkniete użycie (2012 13)
W15 reakcje utlenienia redukcji
Alergeny ukryte Sytuacja prawna w Polsce i na Świecie E Gawrońska Ukleja 2012
psychologiczna reakcja na katastrofy
NIEDOKRWISTOŚCI SEM 2011 2012
więcej podobnych podstron