
Wtórne niedobory
Wtórne niedobory
odporności -AIDS
odporności -AIDS
Dr med. Mariusz Skiba

Definicje
Definicje
Wtórne niedobory odporności obejmują
stany, w których zmniejszenie
odporności jest spowodowane inną
chorobą lub czynnikami zewnętrznymi
–
Znacznie częstsze niż pierwotne N.O.
–
Bardzo zróżnicowana etiopatogeneza
Najbardziej znany jest zespół AIDS, chociaż
najwięcej ludzi cierpi na WNO spowodowane
niedożywieniem, chorobami metabolicznymi,
immunosupresją, chorobami nowotworowymi
i in.

Definicje
Definicje
Zespół nabytego niedoboru odporności jest
przewlekłą chorobą charakteryzującą się
głębokim upośledzeniem czynności układu
immunologicznego i różnorodnym obrazem
klinicznym.
–
Początek choroby niecharakterystyczny (czas trwania do kilku
tygodni)
–
Okres utajenia, klinicznie bezobjawowy (kilka, kilkanaście lat)
–
ARC – AIDS Related Complex – znaczna wiremia i limfopenia
z objawami klinicznymi pod postacią limfadenopatii, gorączki,
biegunki, utrata masy ciała, ale NIE WYSTĘPUJĄ
charakterystyczne nowotwory i zakażenia oportunistyczne
–
Pełnoobjawowy AIDS – końcowa faza choroby
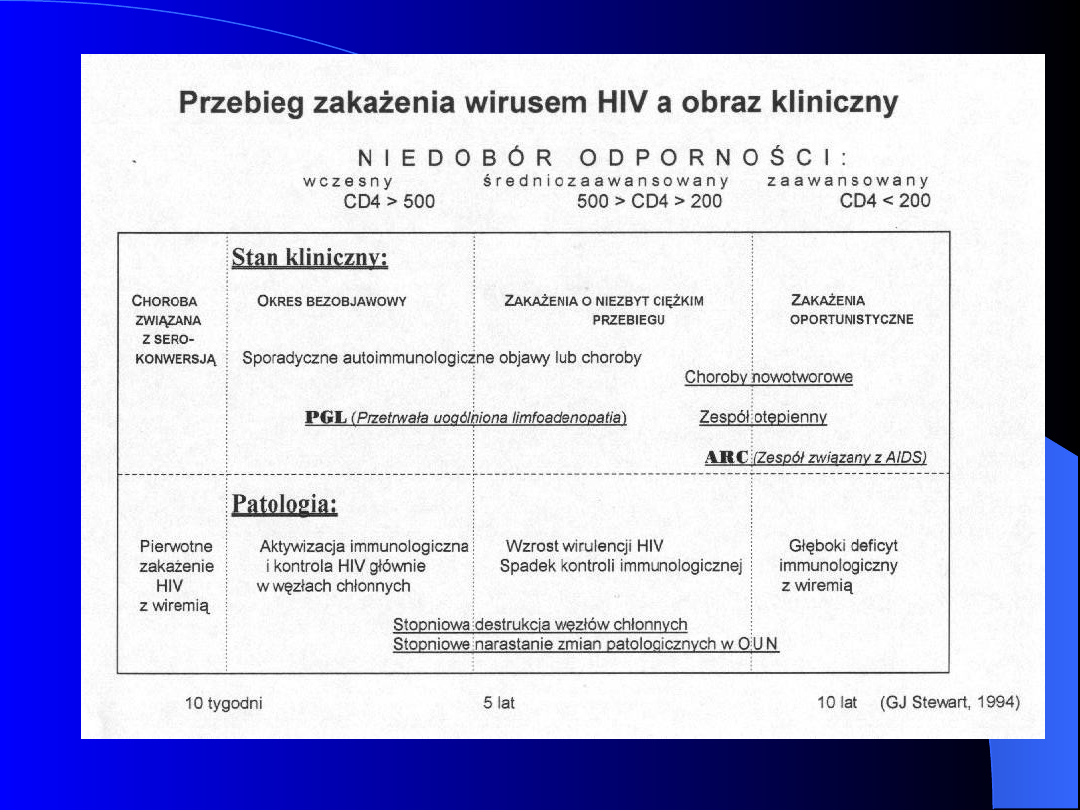
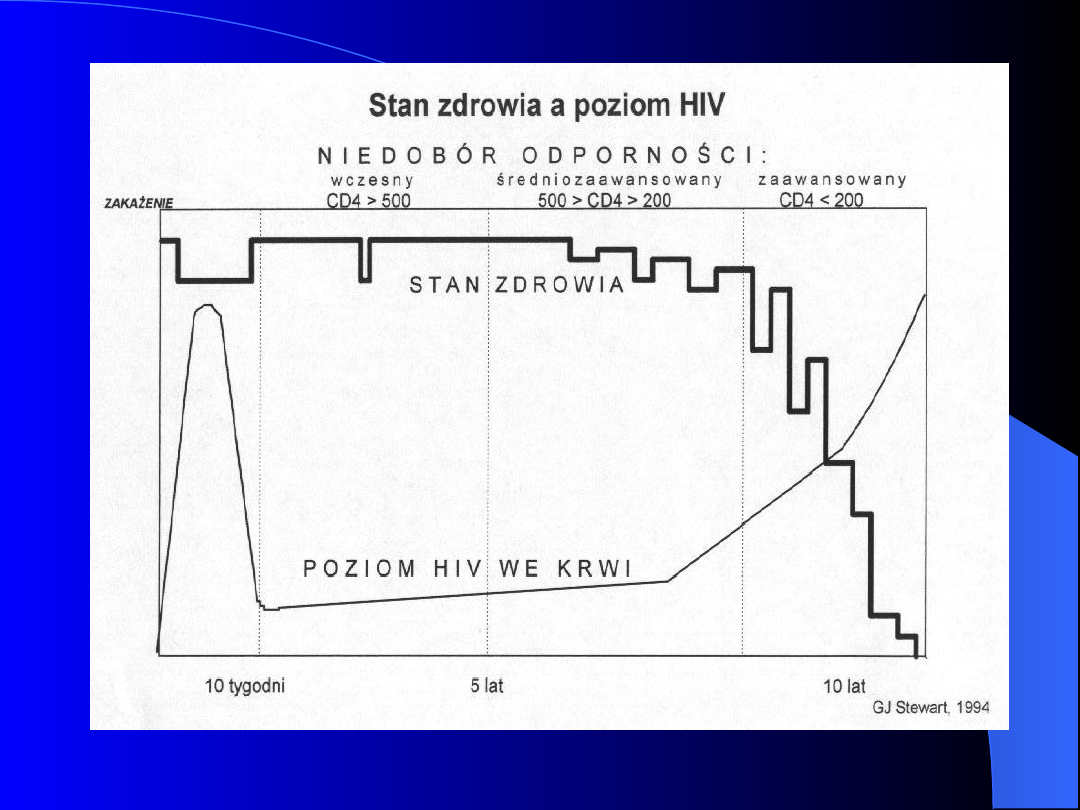
Kliniczny przebieg
Kliniczny przebieg
zakażenia HIV
zakażenia HIV
Kontakt z
wirusem
HIV
Brak
zakaże
nia
Ostra
infekcja
pierwotna
Okres
zakażenia
bezobjawoweg
o
Uogólniona
limfadenopatia
ARC
AIDS
pełnoobjawo
wy
S
ch
o
rz
e
n
i
a
n
e
u
r
o
lo
g
i
cz
n
e

Historia
Historia
LAV - wyizolowany w 1983 roku z węzłów
chłonnych pacjentów z tzw. limfadenopatią
(Luca Montagnier – Instytut Pasteura)
HTLV III – wyizolowany w 1984 roku (Robert
Gallo – Narodowy Instytut Badania nad
Rakiem, Bethesda)
ARV – wyizolowany w 1984 roku (zespół Jay’a
Levy, U. Kalifornijski)
LAV 2-HTLV IV – 1986 rok
HIV 1 i HIV 2 – 1986 rok – Międzynarodowy
Komitet Taksonomii Wirusów

Kilka danych liczbowych
Kilka danych liczbowych
Na początku XXI wieku - epidemia
obejmie 1 na 100 mieszkańców globu
Liczbę zakażonych osób obecnie szacuje
się na 50 milionów
Wprowadzenie wielolekowej terapii z
użyciem HAART (swoiste inhibitory
enzymów wirusowych) znacznie obniżyło
śmiertelność, ale wciąż nie wyeliminowało
wirusa – koszt takiej terapii to około 10
tys. Dolarów rocznie na pacjenta

Retrowirusy
Retrowirusy
Lentiviridae
–
HIV 1 i HIV 2
–
SIV
–
VISNA,
–
CAEV,
–
BIV,
–
FIV,
Oncoviridae
–
HTLV 1(białaczka z kom. T, chłoniak kom. B,
tropikalne porażenie spastyczne, mielopatia)
–
HTLV 2 (białaczka włochatokomórkowa, przewlekły
chłoniak T4, przewlekła białaczka limfatyczna T)
Spumaviridae

Podtypy HIV 1
Podtypy HIV 1
Gag - 8 genotypów wirusa HIV 1
(A-H) oraz szczep 0 i Y
–
Przyczyny – liczne mutacje
–
Skutek – możliwość zakażenia
wieloma typami, trudności w
opracowaniu poliwalentnej
szczepionki indukującej adekwatną
odpowiedź immunologiczną
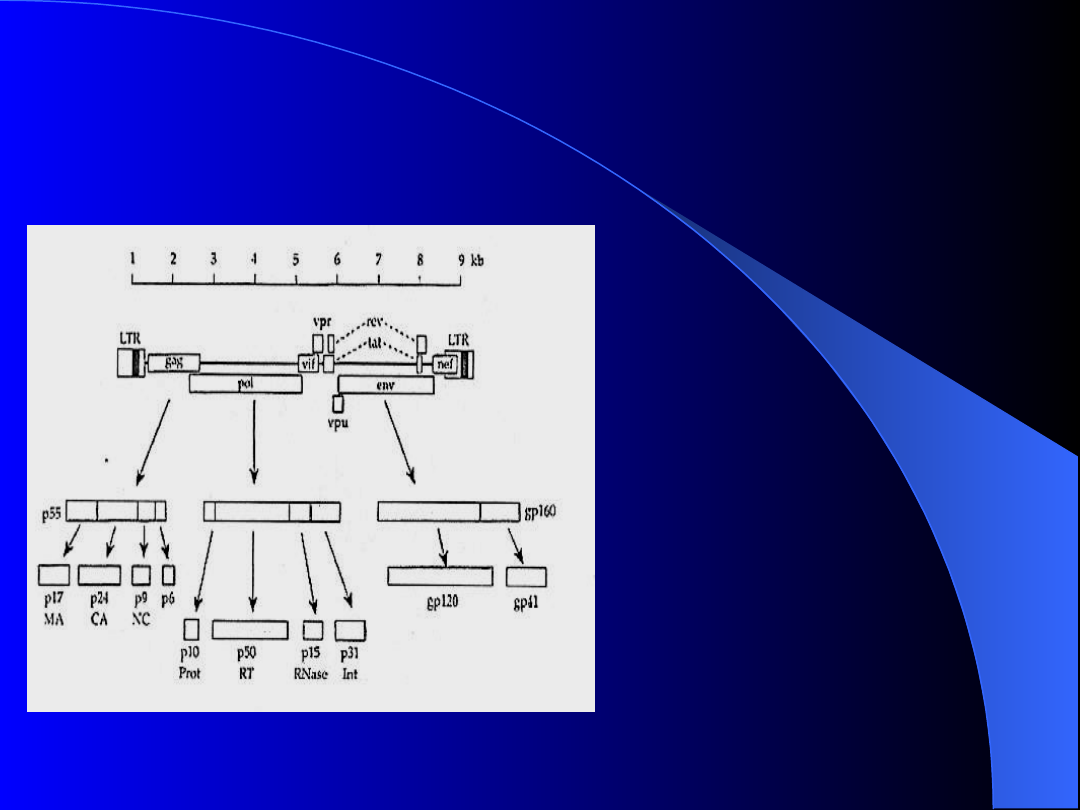
Budowa wirusa
Budowa wirusa
•Dwudziestościan, 80-100nm
•Rdzeń z podwójną błoną
lipidową, białka kodowane
przez gen env (gp 120, gp 41)
•W rdzeniu - Podwójny
genomowy RNA wraz z
towarzyszącymi cząsteczkami
tRNA, produkty genów gag i
pol, otoczone białkiem
strukturalnym p24
•Ponadto białko Nef i
cyklofilina A – znaczenie w
skutecznej replikacji

Wirus HIV 2
Wirus HIV 2
Znacznie rzadszy – ok.. 10% zakażeń
Występuje w Afryce Zachodniej
Nie zawiera genu Vpu i Vpx,
kodującego białko o nieznanej funkcji
Charakterystyczna jest insercja w
genie Rev ( nie ma jej HIV 1)
Posiada odmienną strukturę genu Env

Komórki wrażliwe na
Komórki wrażliwe na
zakażenie HIV
zakażenie HIV
Komórki posiadające receptor CD 4
–
Limfocyty CD4,
–
monocyty, makrofagi
–
Komórki Langerhansa
–
Folikularne komórki dendrytyczne w ww.
chłonnych
–
Makrofagi płucne
–
Kom. Siatkówki
–
Kom. Szyjki macicy, jelita grubego
Możliwe jest zakażenie także innych komórek nie
posiadających CD 4

Tropizm wirusa
Tropizm wirusa
HIV wykorzystuje przede
wszystkim receptor CD4 ale także
koreceptory (receptory dla
chemokin) – dlatego zakaża różne
populacje limfocytów, makrofagów
i kom. Dendrytycznych. Jest to
przykład molekularnej mimikry

Tropizm wirusa
Tropizm wirusa
Szczepy M-tropowe wykazują tropizm do
makrofagów i limfocytów krwi obwodowej
(główny koreceptor to CCR5) – są
odpowiedzialne za zakażenie drogą seksualną.
1% populacji kaukaskiej nie ma funkcjonalnego
receptora CCR5 dlatego jest ona oporna na
zakażenie wirusem tą drogą.
Wirusy T-tropowe – tropizm do limfocytów krwi
obwodowej wykorzystujący koreceptor CXCR4.
Nasilają niszczenie limfocytów Ti przyśpieszają
rozwój pełnoobjawowego AIDS
Szczepy R5X4 – wykorzystują oba koreceptory
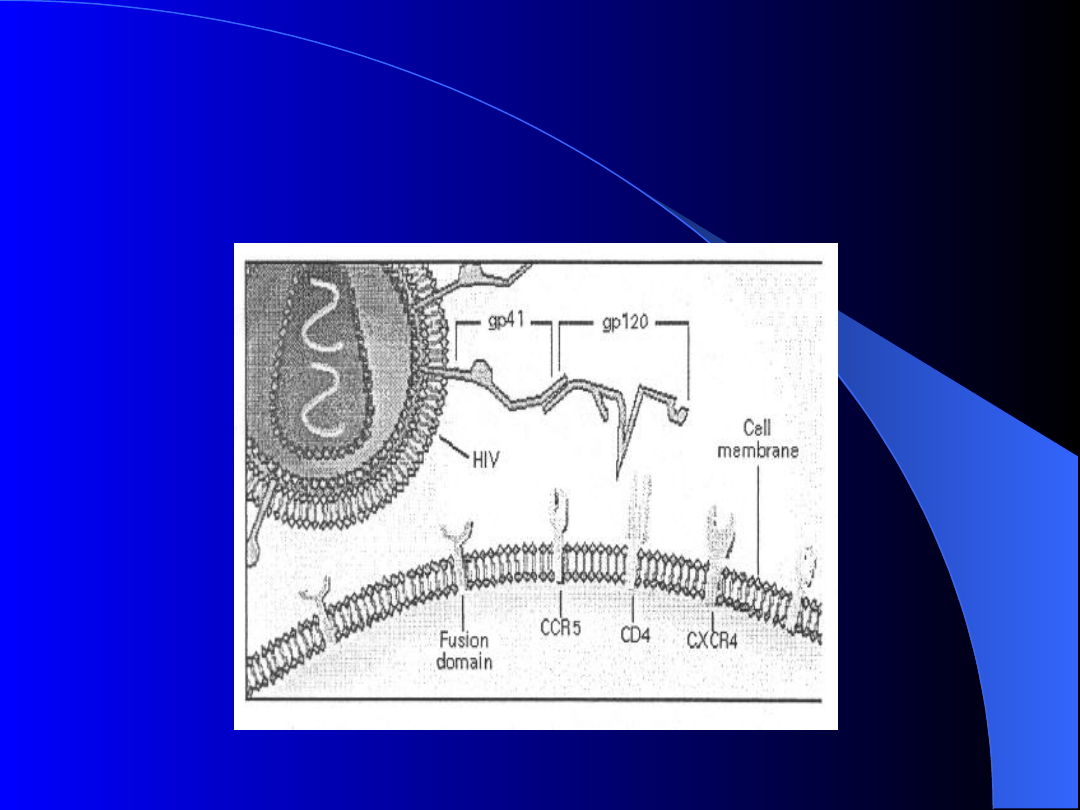
Wiązanie i internalizacja
Wiązanie i internalizacja
wirusa
wirusa

Etapy zakażenia
Etapy zakażenia
Połączenie się wirusa z błoną komórki
permisywnej za pomocą receptorów
Internalizacja wirusa
Replikacja
Działanie cytopatyczne
Mutacje wirusa
Synteza bialek i formowanie
potomnych wirionów
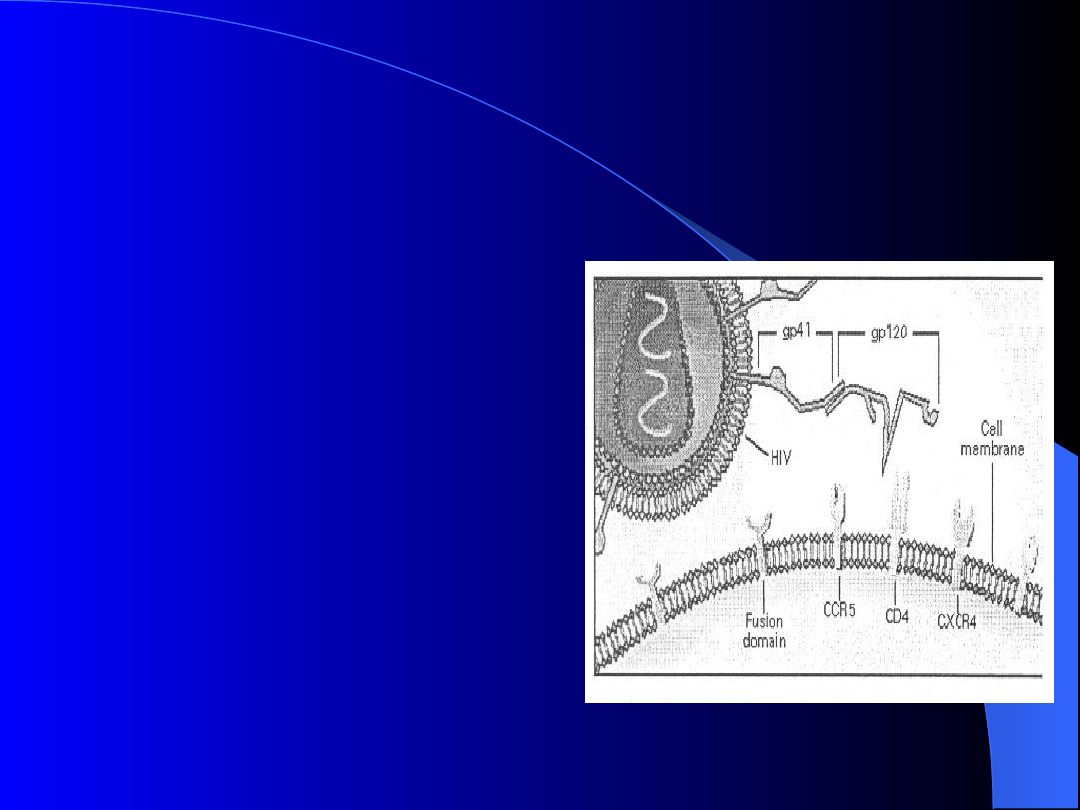
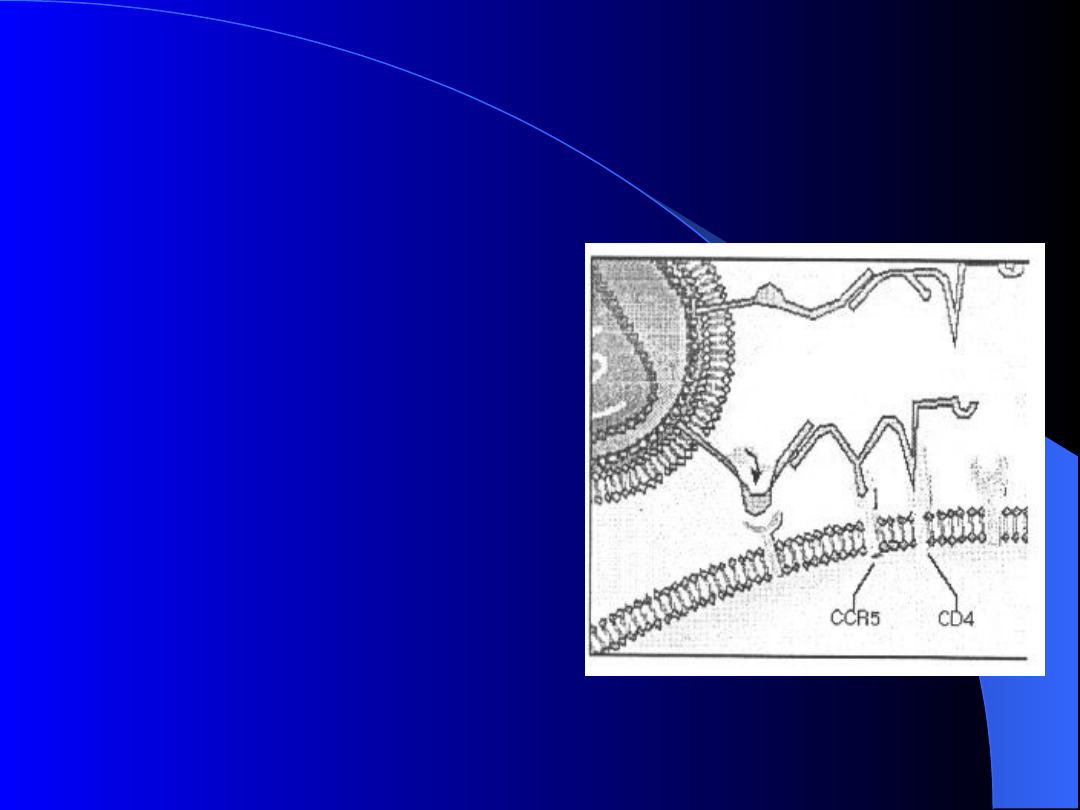
Interakcje HIV z powierzchnią
Interakcje HIV z powierzchnią
komórki – pierwszy etap
komórki – pierwszy etap
HIV wzajemnie
oddziałuje z CD4, to
powoduje zmiany
konformacyjne zbliżające
go do koreceptorów
chemokinowych (CXCR4
i CCR5), dzięki temu
może silniej związać się z
powierzchnią
HIV 2 może wiązać się z
CXCR4 bezpośrednio
Interakcje HIV z powierzchnią
Interakcje HIV z powierzchnią
komórki – drugi etap
komórki – drugi etap
Wzajemne oddziaływanie
miejsca wiązania CD4 na
gp120 wirusa HIV-1 z
cząsteczką CD4 na
powierzchni komórki
Następują zmiany
konformacyjne w otoczce
wirusa jak i w receptorze
CD4 – umożliwia to
przyłączenie gp120 do
następnego receptora
powierzchniowego np.. CCR5

Interakcje HIV z powierzchnią
Interakcje HIV z powierzchnią
komórki – trzeci etap
komórki – trzeci etap
Zbliżenie otoczki wirusa do
powierzchni komórki
umożliwia wzajemne
oddzialywanie pomiędzy
gp41 otoczki a domeną
fuzyjną na powierzchni
komorki
W ten sposób HIV łączy się
z komórką
W rezultacie rdzeń wirusa
wnika do komórki. Po
zakończeniu tego etapu
rozpoczyna się replikacja.

Replikacja
Replikacja
Replikację rozpoczyna wytworzenie kopii RNA
na podstawie prowirusowego DNA. Część
nowych kopii stanowi materiał genetyczny
nowych cząstek wirusa, inne kodują białka
strukturalne i regulacyjne
Formowanie nowej cząstki rozpoczyna
ponowna fuzja z błoną komórki gospodarza,
powstaje kulista struktura „wciągająca” 2 nici
wirusowego RNA
Nowa cząsteczka opuszcza komórkę na drodze
procesu przypominającego pączkowanie

Regulacja replikacji
Regulacja replikacji
Własności pobudzające replikację
posiadają:
–
Sekwencje 5’’ końcowe DNA wirusowego
–
Gen tat – kontrolujący transkrypcję i translację
bialek
–
Gen rev – regulator ekspresji wirusowego RNA
–
Gen nev – podtrzymuje stan przewleklego
zakażenia
–
Gen vpr – stymuluje transkrypcję przez LTR
–
Gen vpn – zwiększa syntezę bialek kapsydu

Regulacja replikacji
Regulacja replikacji
Działanie hamujące posiadają:
–
NRE – negative regulatory element –
zlokalizowany we fragmencie LTR
końca 5’
–
nef – w początkowej fazie transkrypcji
może hamować replikację HIV
–
vpu – oddziałuje na tworzenie
glikoprotein otoczki

Efekt cytopatyczny
Efekt cytopatyczny
W miarę postępu replikacji dochodzi do
stopniowego zmniejszania się liczby limfocytów
CD4.
Prawdopodobne przyczyny to:
–
Nagromadzenie znacznych ilości niezintegrowanego DNA
–
Wirusowego RNA
–
Kompleksów CD4/gp120
–
Nieodwracalne zmiany przepuszczalności błony komórkowej
spowodowane pączkowaniem wirusów potomnych
–
Tworzenie syncytiów komórek niezakażonych i zakażonych poprzez
kompleksy CD4/gp120
–
Zakażone komórki „prezentują” antygen gp120 – są więc atakowane
przez CD8
–
CD8 powodują lizę niezakażonych CD4 na drodze mechanizmów
autoimmunologicznych

Mutacje wirusa
Mutacje wirusa
HIV charakteryzuje bardzo wysoka
częstość mutacji
Mają one miejsce w czasie odwrotnej
transkrypcji
Częstość wynosi 1 mutacja na 1
genom na 1 cykl replikacyjny
Jest to główny mechanizm ucieczki
przed ukladem odpornościowym
gospodarza

HIV a układ odpornościowy
HIV a układ odpornościowy
Najistotniejsze patogenetycznie jest zjawisko
ciągłego namnażania wirusa w komórkach krwi
obwodowej nawet w okresie bezobjawowym
doprowadzające do stałego spadku ilości i
aktywności limfocytów CD4+
Pierwszym celem dla wirusa HIV są śluzówkowe
komórki dendrytyczne i limfocyty T pomocnicze
Komórki dendrytyczne spełniają rolę konia
trojańskiego przenosząc wirusa ze śluzówek do
okolicznych węzłów chłonnych
HIV wymaga receptora CCR5 do zakażenia (jego
brak powoduje oporność na zakażenie)

HIV a układ odpornościowy
HIV a układ odpornościowy
W węzlach chłonnych do transmisji wirusa
dochodzi podczas prezentacji antygenu
wirusowego przez kom. Dendrytyczne
Jedna komórka dendrytyczna zakaża w ciągu
godziny kilkadziesiąt limfocytow T
Dlatego relatywnie niewielka ilość wirionów
w krótkim czasie doprowadza do masywnego
wytwarzania wirusów w węzlach chłonnych
Ostra infekcja pierwotna przebiega z
niecharakterystycznymi objawami
przypominającymi mononukleozę zakaźną

HIV a układ odpornościowy
HIV a układ odpornościowy
Limfocyty CD4+ są komórkami
aktywnie wytwarzającymi wirusa
w związku z tym dochodzi do:
–
Ich niszczenia bezpośrednio przez
HIV
–
Niszczenia przez limfocyty CD8

HIV a układ odpornościowy
HIV a układ odpornościowy
Początkowo odpowiedź immunologiczna
redukuje wiremię , ale jednocześnie
przemieszcza wirusa do obwodowych narządów
limfatycznych gdzie kontynuuje replikację i
destrukcję ukladu chłonnego
W efekcie po kilku latach środowisko
limfatyczne jest na tyle zniszczone, że
niemożliwa jest skuteczna prezentacja
antygenów i odpowiedź immunologiczna
Cechą charakterystyczną jest stan przewlekłej
aktywacji ukladu odpornościowego ( z powodu
samego wirusa, indukowanych cytokin.

HIV a układ odpornościowy
HIV a układ odpornościowy
Istotnym mechanizmem eliminacji limfocytów jest
indukcja apoptozy zarówno komórek zakażonych
jak i nie zakażonych
HIV pobudza proliferację limfocytów, ale z
drugiej strony niszczy miejsca dojrzewania
komórek układu odpornościowego czyli centralne
narządy limfatyczne.
HIV atakuje również makrofagi
Makrofagi z kolei rozprzestrzeniają wirusa,
aktywują apoptozę komórek niezakażonych,
indukują zmiany patologiczne w OUN (AIDS
dementia complex)

Odpowiedź
Odpowiedź
immunologiczna przeciw
immunologiczna przeciw
HIV
HIV
Odp. Immunologiczna jest silnie indukowana ale nie jest
w stanie zwalczyć infekcji
Podstawowe znaczenie mają mechanizmy komórkowe
Masywna replikacja wirusa indukuje silną odpowiedź
limfocytów CD8 (CTL)
Odpowiedź CTL ma charakter oligoklonalny
CTL mogą zabijać komórki zakażone zanim one uwolnią
potomne wirusy
CTL wydzielają chemokiny konkurujące o receptor z
HIV
Niepowodzenie tego mechanizmu spowodowane jest
pojawianiem się wariantów wirusa nierozpoznawanych
przez CTL

Mechanizmy utraty
Mechanizmy utraty
kontroli CTL nad replikacją
kontroli CTL nad replikacją
HIV
HIV
Sekwestracja wirusa w komórkach
niedostępnych dla ukł.
Odpornościowego
Zmniejszenie ekspresji MHC klasy I
Nadmiar antygenu doprowadzający
do delecji klonalnej czy anergii
Ekspresja FasL na zakażonych
komórkach indukowana przez Nef

Odpowiedź humoralna w
Odpowiedź humoralna w
zakażeniach HIV
zakażeniach HIV
Ma ograniczone znaczenie
Przeciwciała neutralizujące pojawiają się
tylko u niektórych osób
Szybko dochodzi wtedy do selekcji
opornych wirusów
Początkowo pojawiają się IgM swoiste dla
p24 i gp41
Po kilku tygodniach pojawia się wysokie
miano IgG przeciw p24 i, gp41, gp 120
(na tych Ig opierają się testy ELISA)
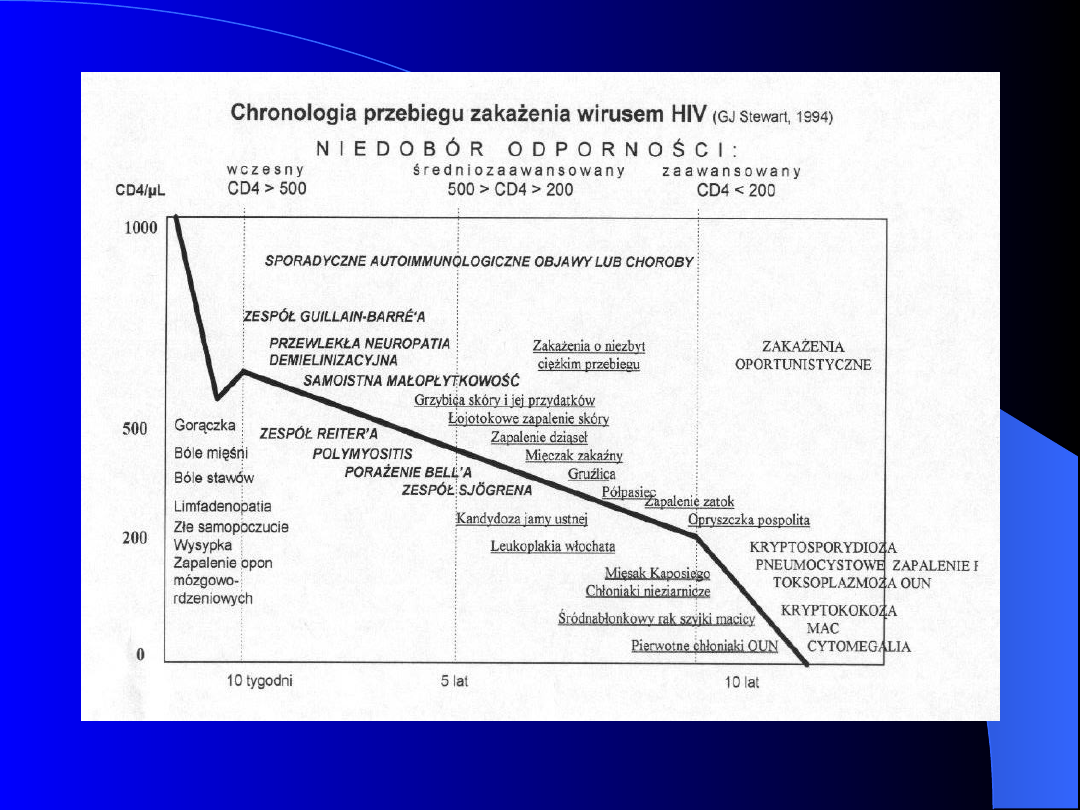

Zakażenia oportunistyczne
Zakażenia oportunistyczne
w AIDS
w AIDS
Cytomegalia- lokalizacja
inna niż wątroba, ww
chłonne, śledziona
Zapalenie siatkówki
wywołane CMV
HSV – zapalenie
oskrzeli, płuc,
przewlekłe owrzodzenia
Histoplazmoza rozsiana
lub pozapłucna
Kandydoza przełyku,
oskrzeli, płuc
Kokcidioidiomykoza
Kryptokokoza rozsiana,
jelitowa
Gruźlica płuc a także
pozapłucna
Pneumocystozowe
zapalenie płuc
Posocznice pałkami G-
Postępująca
wieloogniskowa
leukoencefalopatia
Toksoplazmoza mózgu

Inne współistniejące
Inne współistniejące
„wskaźnikowe” schorzenia
„wskaźnikowe” schorzenia
Chłoniak Burkitta
Chłoniak immunoblastyczny
Chłoniak pierwotny mózgu
Encefalopatia związana z HIV
Mięsak Kaposiego
Inwazyjny rak szyjki macicy
Zespół wyniszczenia związanego z HIV
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
- Slide 34
- Slide 35
- Slide 36
Wyszukiwarka
Podobne podstrony:
Imm Cw 3 Wt rne niedobory odpornosci
Imm Cw 3 Wt rne niedobory odpornosci
Immunologia nowotworoTŽ w, niedobory odpornosTŽ ci, psychoneuroimmunologia
Niedobory odpornosci wersja dluzsza
00 Niedobory odpornoscioweid 1 Nieznany (2)
03 0000 014 02 Leczenie pierwotnych niedoborow odpornosci u dzieci immunoglobulinami
3 WtË rne
Niedobory odporności
09 pierwotne niedobory odporności
Niedobory odporności
więcej podobnych podstron