ANALIZA KATIONÓW III GRUPY ANALITYCZNEJ
GRUPA III
Do III grupy kationów zalicza się jony: Hg2+, Bi3+ , Cu2+ , As3+, As5+, Sb3+, Sb5+, Sn2+, Sn4+
Odczynnikiem grupowym dla III grupy kationów jest H2S.
Siarczki grupy III dzielą się na siarczki metali o właściwościach: zasadowych i amfoterycznych.
Właściwości te pozwalają rozdzielić siarczki grupy III na dwie podgrupy:
Podgrupa A:
Hg2+, Bi3+, Cu2+, Cd2+ - daje siarczki o charakterze zasadowym
Podgrupa B:
As3+, As5+, Sb3+, Sb5+, Sn2+, Sn4+ - daje siarczki amfoteryczne o przeważającym charakterze kwasowym.
PODGRUPA IIIA:
Do podgrupy IIIA należą kationy: Hg2+, Bi3+ , Cu2+
Bizmut, Bi
Bizmut w związkach występuje na +3 i +5 stopniu utlenienia.
1. Siarkowodór H2S.
Siarkowodór wytrąca z roztworu zawierającego jony Bi3+ ciemnobrunatny siarczek bizmutu (III) Bi2S3.
2Bi3+ + 3H2S Bi2S3
2. Wodorotlenek sodu, potasu i amoniak, NaOH, KOH i NH3·H2O
Jony OH- wytrącają z roztworów zawierających jony Bi3+ biały osad wodorotlenku bizmutu (III) Bi(OH)3
Bi3+ + 3OH- Bi(OH)3
3. Jodek potasu KI.
Wytrąca z roztworów zawierających jony Bi3+ brunatnoczarny osad jodku bizmutu (III) BiI3.
Bi3+ +3I- BiI3
4. Wodoroortofosforan (V) sodu Na2HPO4
Wytrąca biały osad BiPO4.
Bi3+ + HPO42- BiPO4 + H+
5. Chromian (VI) i dwuchromian (VI) potasu K2CrO4 i K2CrO7
Wytrącają ze słabo kwaśnych roztworów żółty osad soli tlenku bizmutu (III)
(BiO)2CrO4 i (BiO)2CrO7.
6. Heksatiocyjanianochromian (III) amonu lub potasu (NH4)3[Cr(SCN)6] lub K3[Cr(SCN)6]
Wytrącają z jonami bizmutu (III) Bi3+ czerwonoceglasty osad Bi[Cr(SCN)6]
Bi3+ + [Cr(SCN)6]3- Bi[Cr(SCN)6]
Podobne osady żółte do czerwonoróżwych dają sole srebra, rtęci i ołowiu
Miedź, Cu
Miedź nie roztwarza się w HCl i w rozcieńczonym H2SO4 oraz nie wypiera wodoru z kwasów. Najlepiej roztwarza się w rozcieńczonym HNO3.
3Cu + 8HNO3 3Cu(NO3)2 + 2NO + 4H2O
Cu + 2H2SO4 →CuSO4 + SO2 + 2H2O
Miedź w związkach może występować na +1 i +2 stopniu utlenienia.
1. Siarkowodór H2S.
Wytrąca z roztworu zawierającego jony Cu2+ w środowisku obojętnym czarny osad siarczku miedzi (II) CuS.
Cu2+ + H2S CuS +2H+
2. Wodorotlenek sodu, potasu i amoniak, NaOH, KOH i NH3·H2O
Jony OH- wytrącają na zimno z roztworów zawierających jony Cu2+ niebieski osad wodorotlenku miedzi (II) Cu(OH)2. Podczas gotowania Cu(OH)2 przechodzi w ciemnoszary osad CuO.
Cu2+ + 2OH- Cu(OH)2 → CuO + H2O
3. Jodek potasu KI.
Jony I- wytrącają z roztworów zawierających jony Cu2+ czarny osad CuI2.
2Cu2+ + 4I- 2CuI2
4. Heksacyjanożelazian (II) potasu K4[Fe(CN)6]
Odczynnik ten wytrąca czerwonobrunatny osad heksacyjanożelazianu (II) miedzi (II).
2Cu2+ + [Fe(CN)6]4- Cu2[Fe(CN)6]
5. Wodoroortofosforan (V) sodu Na2HPO4
Wytrąca z jonami Cu2+ jasnoniebieski osad.
3Cu2+ + 2HPO42- → Cu3(PO4)2 + 2H+
Kadm, Cd
Kadm występuje na +2 stopniu utlenienia. Wszystkie proste sole kadmu są bezbarwne, wyjątek stanowi intensywnie żółty CdS.
1. Siarkowodór H2S.
Wytrąca jasnożółty osad siarczku kadmu.
Cd2+ + H2S CdS + 2H+
2. Wodorotlenek sodu lub potasu, NaOH, KOH.
Jony OH- z roztworów zawierających jony Cd2+ wytrącają biały bezpostaciowy osad wodorotlenku kadmu Cd(OH)2.
Cd2+ + 2OH- Cd(OH)2
3. Amoniak NH3 · H2O
Wytrąca z roztworów zawierających jony Cd2+ biały osad wodorotlenku kadmu Cd(OH)2.
Przegląd reakcji chemicznych kationów podgrupy IIIA
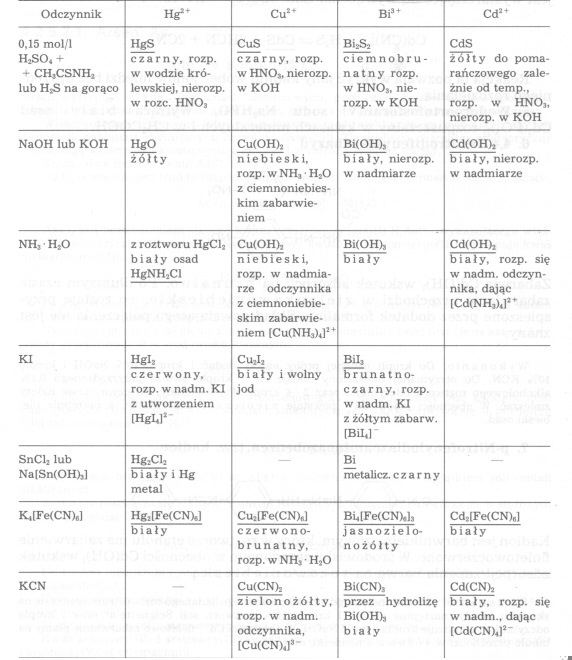
PODGRUPA IIIB:
Do podgrupy IIIB należą kationy: As3+, As5+, Sb3+, Sb5+, Sn2+, Sn4+
Cyna, Sn
Reakcje jonu Sn2+
1. NaOH, KOH, NH3 · H2O
wytrącają z roztworów zawierających jony Sn2+ biały osad wodorotlenku cyny (II).
Sn2+ + 2OH- Sn(OH)2
2. Chlorek żelaza (III) FeCl3
Utlenia Sn2+ do Sn4+
Sn2+ + 2Fe3+ + 6Cl- SnCl62- + 2Fe2+
Po dodaniu do roztworu chlorku żelaza (III) kropli HCl, roztwór K3[Fe(CN)6] i kroplę badanej substancji powstaje ciemnobłękitny osad błękitu Turnbulla.
Reakcje jonu Sn4+
1. NaOH, KOH, NH3 · H2O
wytrącają ze związków Sn(IV) biały, galaretowaty osad wodorotlenku cyny (IV) Sn(OH)4.
[SnCl6]2- + 4OH- Sn(OH)4 + 6Cl-
4
Wyszukiwarka
Podobne podstrony:
ANALIZA KATIONÓW IV i V GRUPY ANALITYCZNEJ, Studia, Chemia
Sprawozdanie chemia 6 Reakcje dla poszczególnych kationów III grupy analitycznej
ANALIZA KATIONÓW I i II GRUPY ANALITYCZNEJ
ANALIZA KATIONÓW I,II,III GRUPY ANALITYCZNEJ
3 Analiza jakościowa III grupy kationów
AJ Identyfikacja kationów III grupy, ~FARMACJA, I rok, chemia (ciul wie co), Semestr I
Podział kationów na grupy analityczne i ich ogólna charakterystyka
analiza kationów III gr (2)
Podział kationów na grupy analityczne
podział kationów na grupy analityczne, STUDIA (ochrona), ROK I, chemia, laboratoria
ANALIZA ANIONÓW I VII GRUPY ANALITYCZNEJ
5 Analiza jakościowa III grupy anionów
Kationy III A, Analiza Leków
Kationy III B, Analiza Leków
Rozdzielanie kationów IV grupy w toku analizy chemicznej
Analiza kationów na przykładzie V grupy
analiza kationów i anionów III, IV i V grupa
analiza wody sprawozdanie chemia analityczna analiza wody teoria
analiza kationów I V (2)
więcej podobnych podstron
