WYŻSZA SZKOŁA MORSKA W SZCZECINIE WYDZIAŁ MECHANICZNY
|
LABORATORIUM- ITESO
|
|
|||
|
Nr 5 |
Temat ćwiczenia:EMISJA SPALIN |
|
||
Data wyk .ćw 22.02.99
|
Data oddania ćw: |
Ocena:
|
Podpis asystenta |
Podpis Kier.Zakł. |
|
WSTĘP
Za podstawowe składniki spalin zanieczyszczające atmosferę, emitowane przez silniki spalinowe tłokowe; uważa się:
tlenki azotu NOx- określeniem tym obejmuje się głównie tlenek azotu wywiązujący się w komorze spalania przy wysokich temperaturach oraz dwutlenek azotu, powstający w wyniku utleniania tlenku azotu;
tlenki siarki SOx;
niespalone węglowodory CnHm - których zidentyfikowana liczba w spalinach sięga około dwóch tysięcy;
cząstki stałe TPM - cała materia stała lub ciekła (organiczna i nieorganiczna) zawarta w spalinach;
tlenek węgla CO;
aldechydy RCOHO - największe stężenia osiąga formaldehyd z grupy aldehydów nasyconych i akroleina z grupy aldehydów nienasyconych;
dwutlenek węgla CO2, który jako naturalny składnik atmosfery nie stanowin bezpośredniego zagrożenia dla organizmów żywych, więc nie jest traktowany jako zanieczyszczenie, ale jest przyczyną tak zwanego „efektu cieplarnianego”. Wzrastające stężenie tego składnika w atmosferze stanowi duże zagrożenie o działaniu długofalowym.
Substancje zanieczyszczające atmosferę emitowane w spalinach mają w średniej temperaturze otoczenia postać:
gazową- tlenek i dwutlenek węgla, tlenki azotu, część węglowodorów i aldehydów, dwutlenek siarki
ciekłą - niektóre węglowodory i aldehydy,
stałą - sadza, związki metali i ciężkie węglowodory.
1. Reakcja spalania paliwa węglowodorowego w powietrzu może być zapisana następująco:
HCx+ A(O2+3,7274 N2+0,0444 Ar+0,0014 CO2)+ B H2O⇒ a CO+ b CO2+c O2+d H2O+e HCx+f H2+ g N2+h NO+ j Ar
Równania bilansu dla składników palnych paliwa i tlenu :
Węgla(C); 1 = a+b+e
Wodoru(H); x+ 2B + 2d+xe+2f
Tlenu(O); 2A+B + 2b+2c+d+h
2. Skład 1 kg paliwa o udziałach masowych: Cp, Hp, Sp, Np, Op, Wp, Ap.
Cp [kg]+ Hp[kg]+ Sp[kg]+ Np[kg]+ Op[kg]+ Wp[kg]+ Ap[kg] = 1[kg]
3. liczby znamienne (Moliera0 określające skład paliwa:
δ= 1+ 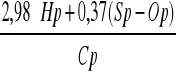
δ = 1,438436781
υ = 0,429 ![]()
υ = 0
4. Teoretyczne zapotrzebowanie powietrza.
Ilość powietrza lub tlenu niezbędna do spalenia zupełnego 1 kg paliwa określonego składem masowym Cp, Hp, Sp, Op, Np, Wp, Ap.
5. Teoretyczne kilomolowe zapotrzebowanie powietrza:
LTk = 0,3974 Cp + 0,1491 Sp + 1,1839 [ Hp - ![]()
] [kmol/kgpal]
LTk = 0,4972772
6. Teoretyczne masowe zapotrzebowanie powietrza :
LTm = 11,5102 Cp + 4,31117 Sp + 34,2290 [Hp - ![]()
] [ kg/kgpal]
LTm = 14,3946994
7. Teoretyczne objętościowe zapotrzebowanie powietrza :
LTv = 8,9075 Cp + 3,3366 Sp + 26,5362 [ Hp - ![]()
] [ Nm3/kgpal]
LTv = 11,1461586
8. Współczynnik nadmiaru powietrza (tlenu) :
![]()
λ = ![]()
= ![]()
Skład powietrza reagującego z 1 kg paliwa przy spalaniu
stechiometrycznym
9. Ilość azotu N2:
∑N2 = 0,3103 Cp + 0,1162 Sp + 0,9245 [ Hp- ![]()
] [kmol]
∑N2 = 0,388297
∑N2 = 8,6934 Cp + 3,2565 Sp + 25,8374 [Hp - ![]()
] [kg]
∑N2 = 10,8704452
∑N2 = 6,9559 Cp + 2,6056 Sp + 20,7222 [ Hp- 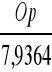
] [Nm3]
∑N2 = 8,7040746
10. Ilość tlenu O2:
∑O2 = 0,0832 Cp + 0,0312 Sp + 0,248 [ Hp - ![]()
] [ kmol]
∑O2 = 0,104128
∑O2 = 2,6640 Cp + 0,9979 Sp + 7,9364 [ Hp - ![]()
] [kg]
∑Op = 3,3335392
∑Op = 1,8662 Cp + 0,6990 Sp + 5,5594 [ Hp - ![]()
] [Nm3]
∑O2 = 2,3351972
11. Ilość argonu Ar:
∑Ar = 0,0037 Cp + 0,0014 Sp + 0,0110 [ Hp - ![]()
] [kmol]
∑Ar = 4,627 10-3
∑Ar = 0,1476 Cp + 0,0553 Sp + 0,4399 [ Hp - ![]()
] [kg]
∑Ar = 0,1847192
∑Ar =0,0828 Cp + 0,0310 Sp + 0,2468 [ Hp - ![]()
] [Nm3]
∑Ar =0,1036264
12. Ilość dwutlenku węgla CO2:
∑CO2 = 0,0001 Cp + 0,0003 Sp + 0,0003 [ Hp - ![]()
] [kmol]
∑CO2 =1,254 10-4
∑CO2 = 0,0052 Cp +0,0020 Sp + 0,0015 [ Hp - ![]()
] [kg]
∑CO2 =4,716 10-3
∑CO2 = 0,0026 Cp +0,0010 Sp + 0,0078[ Hp - ![]()
] [Nm3]
∑CO2 = 3,2604 10-3
Skład spalin wilgotnych otrzymanych w wyniku spalenia stechiometrycznego 1 kg paliwa
13. Ilość dwutlenku węgla CO2:
CO2 = 0,0835 Cp + 0,0003 Sp + 0,0003 [ Hp - ![]()
] [kmol]
CO2 =0,0726834
CO2 = 3,6744 Cp +0,0020 Sp + 0,0015 [ Hp - ![]()
] [kg]
CO2 =3,19692
CO2 = 1,8714 Cp +0,0010 Sp + 0,0078[ Hp - ![]()
] [Nm3]
CO2 = 1,6291164
Ilość dwutlenku siarki SO2:
SO2 = 0,0312 Sp [kmol]
SO2 = 0
15. Ilość azotu N2 :
N2 = 0,3103 Cp + 0,1162 Sp + 0,9245 [ Hp- ![]()
] [kmol]
N2 = 0,388297
N2 = 8,6934 Cp + 3,2565 Sp + 25,8374 [Hp - ![]()
] [kg]
N2 = 10,8704452
N2 = 6,9559 Cp + 2,6056 Sp + 20,7222 [ Hp- 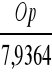
] [Nm3]
N2 = 8,7040746
16. Ilość argonu Ar :
Ar = 0,0037 Cp + 0,0014 Sp + 0,0110 [ Hp - ![]()
] [kmol]
Ar = 4,627 10-3
Ar = 0,1476 Cp + 0,0553 Sp + 0,4399 [ Hp - ![]()
] [kg]
Ar = 0,1847192
Ar =0,0828 Cp + 0,0310 Sp + 0,2468 [ Hp - ![]()
] [Nm3]
Ar =0,1036264
17. Ilość wody H2O :
H2O = 0,4960 [ Hp - ![]()
] + ![]()
+ ![]()
[kmol]
H2O = 0,063488
H2O = 0,4960 Hp + 0,0005 Op + ![]()
[kmol]
H2O = 0,063488
H2O = 8,9364 [ Hp - ![]()
] + 1,1260 Op + Wp [kg]
H2O = 1,1438592
H2O = 8,9364 [ Hp - ![]()
] + 1,1260 Op + Wp [kg]
H2O = 1,1438592
H2O = 11,1176 [ Hp - ![]()
] + 1,4318 Op + 1,25 Wp [Nm3]
H2O = 1,4230528
H2O = 11,1176 Hp + 1,25 Wp[Nm3]
H2O = 1,4230528
Skład spalin na podstawie pomiaru
18. Objętościowy udział procentowy składników spalin:
(CO2) + (CO) + (H2) + ( Cx Hy) + (SO2) + (O2) + (NOx) + (N2) + (Ar) = 100
19. Korekcja emisji tlenków azotu polega na uwzględnieniu wilgotności i temperatury powietrza dolotowego. Emisja tlenków azotu jest zależna od parametrów powietrza otoczenia, stad pomierzona wartość stężenia tego składnika w spalinach powinna być skorygowana do warunków standartowych według następujących zasad:
silniki o zapłonie samoczynnym ogólnie :
KH = ![]()
A = 0,309 ![]()
- 0,0266
B = - 0,209 ![]()
- 0,00954
Wyszukiwarka
Podobne podstrony:
emisja spalin
Emisja spalin
CAT Niska emisja spalin
Emisja spalin
Gnieźnieńska Wyższa Szkoła
Sesja poprawkowa II rok SUM SP, WSB ( WYŻSZA SZKOŁA BANKOWA)
Anatomia 5 cwiczenia, kosmetologia-wyższa szkoła fizjoterapii-wrocław
Zagadnienia na Egzamin z Demografii, Wyższa Szkoła Biznesu w Dąbrowie Górniczej, Demografia spoleczn
LISTA 2 zaoczne, WSB ( WYŻSZA SZKOŁA BANKOWA)
Pytania do testu 2013, WSZOP- Wyższa Szkoła Zarządzania Ochroną Pracy, Choroby zawodowe
WYŻSZA SZKOŁA PRAWA I?MINISTRACJI
WYŻSZA SZKOŁA ZARZĄDZANIA I?NKOWOŚCI W POZNANI1
2011 09 19 Wyzsza Szkola Policj Nieznany (2)
Wyższa Szkoła Społeczno(1), Studia
Rynki Finansowe 2, Wyższa Szkoła Bankowa w Poznaniu, Studia licencjackie - Zarządzanie - Zarządzanie
Wyższa Szkoła Społeczn1, Studia
Państwowa Wyższa Szkoła Zawodowa
więcej podobnych podstron