
CHEMIA
ANALITYCZNA
Zadanie dla analityka:
Podniesienie jakości
smaku ciasteczek
Pewnego dnia firma cukiernicza
postanowiła zmienić dotychczasową
formułę produkcji ciasteczek
polewanych czekoladą. Niestety po tej
zmianie, w trakcie specjalistycznych
testów smaku eksperci stwierdzili
obecność nieprzyjemnego posmaku,
który psuje jakość produktu.
Co można zrobić?

Analiza chemiczna ciasteczka
1) Ekstrakcja chloroformowa ciasteczka
–
przeprowadzenie do roztworu substancji celem
dalszej analizy. Przeanalizowano ciasteczko
wyprodukowane według tradycyjnego przepisu
oraz według nowej receptury.
2)
Analiza jakościowa –
zastosowanie technik analityczne celem ustalenia
składu chemicznego mieszaniny
3)
Analiza ilościowa –
zastosowanie technik analityczne celem ustalenia
składu zawartości poszczególnych produktów
Zadanie dla analityka: Podniesienie jakości smaku ciasteczek
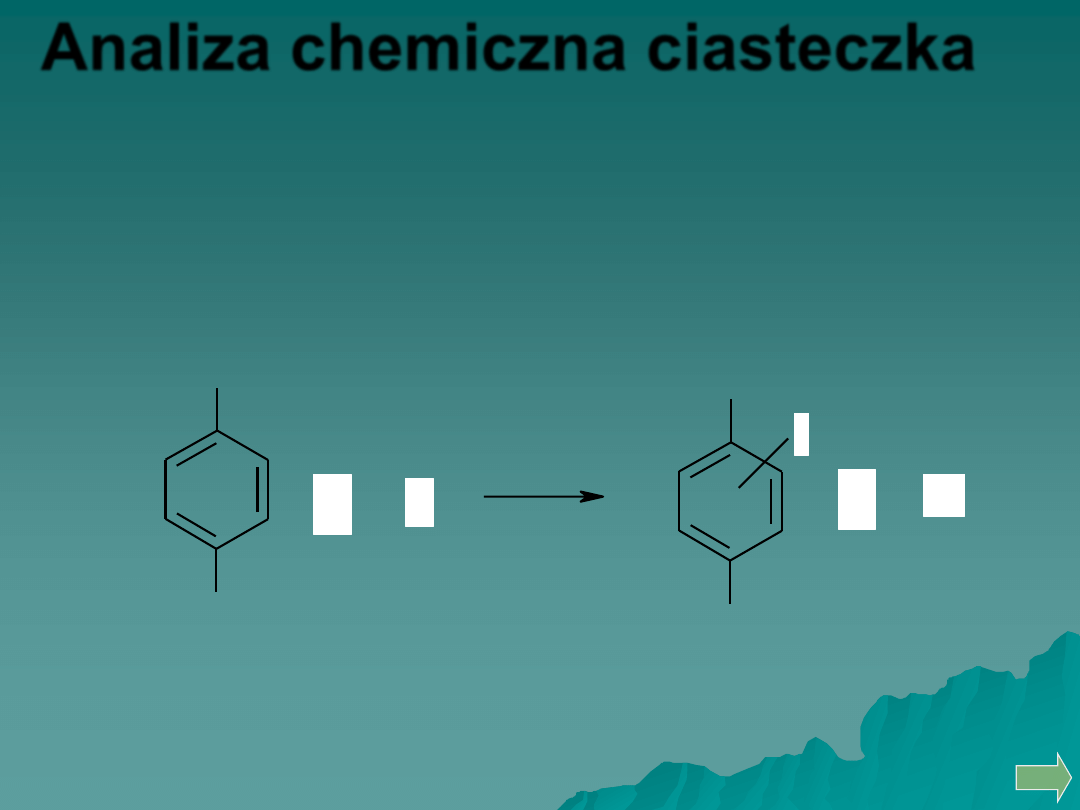
Okazuje się, że nowa wersja ciasteczek, w
przeciwieństwie do tradycyjnej formuły, zawiera
produkt reakcji jodu z krezolem
– jodokrezol.
OH
CH
3
OH
CH
3
+
I
2
I
HI
+
Analiza chemiczna ciasteczka

Doświadczalnie potwierdzono, że jodokrezol tworzony
jest in situ
jako produkt bezpośredniego zmieszania
jodu z krezolem
– składnikiem występującym w
aromacie
jodokrezol
Mieszanina z solą jodowaną
Mi
eszanina z sola pozbawioną jodu
2.4 ppb
0.1 ppb
Rozwiązanie:
nie używać jodowanej soli w
trakcie produkcji ciasteczek!
Analiza chemiczna ciasteczka
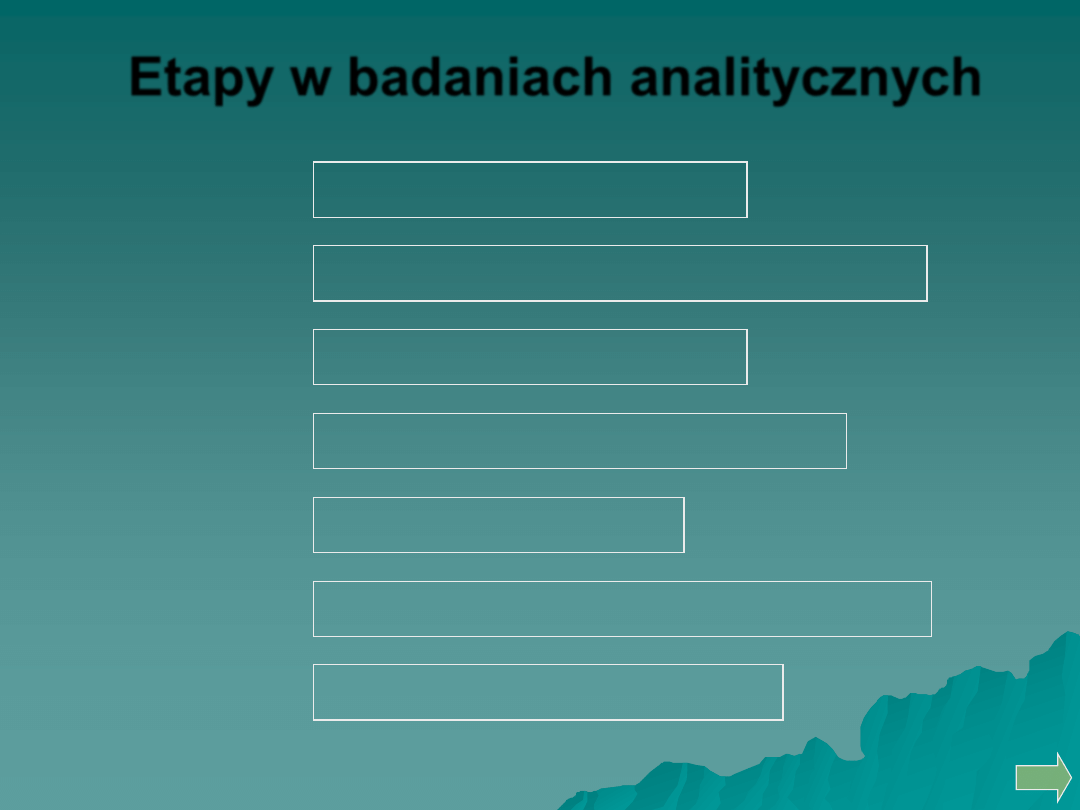
Etapy w badaniach analitycznych
1. Sytuacja problemowa
2.
Dobór procedury analitycznej
3.
Próbkowanie
4.
Obróbka wstępna próbki
5. Analiza
6. Raport
i prezentacja wyników
7. Wnioski analityczne

Przedmiot i zadania chemii analitycznej
Chemia analityczna jest to:
• nauka stosowaną zajmującą się odkrywaniem i
formułowaniem praw, kryteriów i metod prowadzących do
ustalenia z określoną precyzją i dokładnością skład
jakościowy i ilościowy
• zajmuje się analizą wszelkiego rodzaju materiałów
spotykanych w przyrodzie lub wytwarzanych przez człowieka
• ustala skład jakościowy i ilościowy badanych substancji
• strukturę i budowę przestrzenną cząsteczek i ciał stałych
• przemiany zachodzące w czasie i (lub) przestrzeni w
obrębie badanych cząsteczek
• interdyscyplinarna nauka, łączącą i wykorzystującą wiedzę z
różnych dziedzin chemii, fizyki, biologii i matematyki oraz
nowoczesnej techniki, elektroniki, automatyki i informatyki.

Przedmiot i zadania chemii analitycznej
Niektóre dziedziny zastosowań chemii analitycznej
:
Przemysł metalurgiczny, geologia, ceramiczny analiza rud i
innych minerałów, nawozów sztucznych oznaczanie m.in.
azotu, fosforu i potasu.
Przemysł elektroniczny oznaczanie śladowych ilości
zanieczyszczeń oraz śladowych ilości pierwiastków celowo
wprowadzonych do .materiałów półprzewodnikowych.
materiałów budowlanych - analiza surowców i produktów
końcowych.
Różne gałęzie przemysłu organicznego:
a) koksownictwo - analiza produktów suchej destylacji węgla,
b) przemysł gumowy i mas plastycznych analiza
półproduktów i produktów finalnych,
c) przemysł farb i lakierów - ocena jakości produktów;
badanie zawartości składników szczególnie szkodliwych dla
środowiska,
d) przemysł petrochemiczny ocena jakości produktów
naftowych,

Przedmiot i zadania chemii analitycznej
Niektóre dziedziny zastosowań chemii analitycznej
:
Przemysł farmaceutyczny - analiza półproduktów syntezy
leków, analiza produktu (leku), oznaczanie głównego
składnika oraz zanieczyszczeń.
Przemysł tłuszczowy - analiza surowców (np. oznaczanie
liczby kwasowej olejów) lub produktów (np. oznaczanie
zawartości niklu w utwardzonych tłuszczach).
Przemysł zielarski - analiza substancji czynnych w ziołach,
mieszankach ziołowych i różnych produktach przemysłu
zielarskiego stosowanych jako leki. Oznaczanie substancji
szkodliwych (środki ochrony roślin, metale ciężkie Pb, Cd, Hg,
Ni, Cr) w ziołach, mieszankach ziołowych i preparatach
przemysłu zielarskiego.
Przemysł spożywczy oznacza nie tylko substancje decydujące
o wartości danego produktu (np. zawartość kwasów
nienasyconych w olejach lub zawartość witamin w owocach,
przetworach owocowych i warzywach), ale także substancje
szkodliwe, m.in. środki ochrony roślin, metale ciężkie, środki
konserwujące, barwniki syntetyczne, azotany (III) i azotany
(V) itd.

Przedmiot i zadania chemii analitycznej
Niektóre dziedziny zastosowań chemii analitycznej
:
Lecznictwo
Laboratoria kontroli leków (m.in. Instytut Leków w
Warszawie). Każdy lek (produkcji krajowej lub z importu)
przed wprowadzeniem do obrotu jest poddawany analizie,
przy czym oznacza się nie tylko zawartość głównych
składników leku, ale także zanieczyszczenia - m.in.
półprodukty syntezy.
Laboratoria analizy klinicznej oznacza się nie tylko stężenie
cukru, cholesterolu, acetonu, jonów sodu, potasu i innych
substancji w płynach ustrojowych (mocz, krew), ale także
stężenie leku i jego metabolitów w moczu lub krwi podczas
terapii. Tego typu analizy nie tylko ułatwiają lub umożliwiają
lekarzowi postawienie odpowiedniej diagnozy, ale także przy
tzw. terapii monitorowanej zastosowanie odpowiednich
dawek leków, które często mają mniejsze lub większe
działanie niepożądane.

Przedmiot i zadania chemii analitycznej
Niektóre dziedziny zastosowań chemii analitycznej
:
Analiza substancji szkodliwych:
Powietrze - oznacza się m.in. zawartość SO
2
i tlenków azotu,
węglowodorów aromatycznych o skondensowanych
pierścieniach, mających właściwości kancerogenne, zawartość
metali ciężkich i różnych innych związków organicznych
występujących w powietrzu, w zakładach przemysłowych i w ich
otoczeniu.
Woda i ścieki oznacza się m.in. zawartość metali ciężkich,
azotanów (III) i azotanów (V), środków ochrony roślin oraz
różnych innych substancji organicznych.
Kryminalistyka i medycyna sądowa oznacza się m.in. zawartość
różnych trucizn, narkotyków, środków psychotropowych.
Sport oznacza się zawartość środków dopingujących i anabolików
(m.in. steroidów) w moczu sportowców. Analizy takie wykonują
specjalistyczne laboratoria, mogące oznaczać kilkaset różnych
związków tego typu m.in. półprodukty syntezy.

Spis zagadnień
chemia analityczna
I. Analiza jakościowa
I.1. Analiza kationów
Pierwsza grupa kationów: Ag, Pb, Hg
Druga grupa kationów
Podgrupa II A Hg, Bi, Cu, Cd
Podgrupa II B As, Sb, Sn
Trzecia grupa kationów Al, Cr, Fe, Ni, Co, Mn, Zn
Czwarta grupa kationów Ba, Ca, Sr
Piąta grupa kationów NH
4
+
, K, Na, Mg

I.2. Analiza anionów .
Pierwsza grupa anionów
Jony: Cl
-
Br
-
I
-
CN
-
Jon tiocyjanianowy (rodankowy), SCN
-
Jon heksacyjanożelazianowy (II), [Fe(CN)
6
]
4-
Jon heksacyjanożelazianowy (III), [Fe(CN)
6
]
3-
Jon chloranowy (I), Cl0
-
Druga grupa anionów
S2- ., CH3C00- , NO3- .
Trzecia grupa anionów
CO
3
2-
, SO
3
2-
, C
2
O
4-
Jon winianowy: C
4
H
4
0
6
-
BO
2-
Czwarta grupa anionów
S
2
0
3
2-
Cr0
4
2-
Cr
2
O
7
2-
PO
4
3-
AsO
4
3-
(III) AsO
3
3-
Piąta grupa anionów
NO
3
-
, ClO
3
-
ClO
4
-
MnO
4
-
Szósta grupa anionów
SO
4
2-
F
-
SiF
6
2-
Siódma grupa anionów
SiO
3
2-
I.3. Analiza substancji prostych i mieszanin

II. Analiza ilościowa
II.1. Analiza wagowa
Oznaczanie jonów baru
Oznaczanie jonów żelaza III
Oznaczanie jonów magnezu obok jonów wapnia
Oznaczanie jonów glinu obok jonów żelaza (III)
Oznaczanie jonów miedzi (II) obok jonów żelaza (III)
Oznaczanie jonów żelaza (III) obok jonów siarczanowych (VI)
Oznaczanie zawartości wody
II.2. Analiza objętościowa
II.2.A. Alkacymetria
II.2.B. Redoksymetria.
II.2.C. Miareczkowe metody wytrąceniowe (precypitometria)
II.2.D. Kompleksonometria

Podstawowe pojęcia
Próbka
podzbiór populacji podlegający bezpośrednio badaniu ze względu
na daną cechę w celu wyciągnięcia wniosków o kształtowaniu się
wartości tej cechy w populacji.
Próbka laboratoryjna
próbka przygotowana z próbki ogólnej, reprezentująca właściwości
partii produktu, przeznaczona do prowadzenia analiz.
Próbka analityczna
część produktu z próbki laboratoryjnej przeznaczona w całości do
jednego oznaczenia lub wykorzystywana bezpośrednio do badania
lub obserwacji.
Próba ślepa (zerowa)
próba (badanie) wykonana w warunkach identycznych jak analiza
badanej próbki, ale bez dodania substancji oznaczanej.
Próbka:

Podstawowe pojęcia
Wykrywanie
czynność mająca na celu stwierdzenie obecności lub nieobecności
określonego jonu lub związku (jonów lub związków) w badanej próbce.
Wykrywalność
najmniejsze stężenie lub ilość wykrywanego składnika w badanej
próbce, przy których można go jeszcze wykryć daną metodą z
określonym prawdopodobieństwem. Wielkość tę określano jako granicę
wykrywalności lub limit detekcji.
Metoda analityczna:
sposób wykrywania lub oznaczania składnika próbki.
Oznaczanie
określenie ilościowej zawartości danego składnika w badanej próbce.
Oznaczalność
najmniejsze stężenie lub ilość oznaczanego składnika w badanej
próbce, przy których można jeszcze ten składnik oznaczyć daną
metodą. Wielkość tę określano także jako granica oznaczalności.

Podstawowe pojęcia
Czułość metody analitycznej
stosunek przyrostu sygnału analitycznego do odpowiadającemu mu
przyrostu stężenia (lub zawartości) oznaczanego składnika.
Dokładność metody analitycznej
stopień zgodności między wynikiem pomiaru (oznaczenia) lub średnią z
serii a wartością prawdziwą mierzonej (oznaczanej) wielkości.
Precyzja metody analitycznej
wielkość charakteryzująca rozrzut wyników uzyskiwanych przy
wielokrotnym oznaczaniu danego składnika daną metodą; określana
odchyleniem standardowym i rozstępem wyników uzyskiwanych w
warunkach powtarzalności lub odtwarzalności.
Selektywność metody
możliwość jej zastosowania do wykrywania lub oznaczania tylko
pewnej niewielkiej liczby składników.
Metoda analityczna:
sposób wykrywania lub oznaczania składnika próbki.

Preparatyka analityczna
Preparatyka osadów
Preparatyka lotnych produktów
Preparatyka roztworów
Preparatyka roztworów
Rozpuszczanie i roztwarzanie próbek nieorganicznych.
Rozpuszczanie
Rozpuszczanie zachodzi wtedy, gdy energia solwatacji jest większa niż
energia sieci krystalicznej. W ten sposób rozpuszczają się w wodzie
związki jonowe, a więc sole, kwasy, zasady oraz niepolarne związki
organiczne w niepolarnych rozpuszczalnikach organicznych.
Roztwarzanie
Bardzo wiele oznaczanych ilościowo substancji, takich jak: metale,
stopy, minerały, gleba, próbki biologiczne, jest nierozpuszczalnych w
wodzie albo rozpuszczają się tylko w sposób ograniczony.
Próbki o charakterze nieorganicznym roztwarza się najczęściej w
kwasach nieutleniających: HCl, HBr, HF, rozcieńczonych H2SO4 i H
3
PO
4
.
W kwasach utleniających: HNO
3
, stężony H
2
SO
4
, stężony HClO
4
, albo w
mieszaninach tych kwasów roztwarza się wiele metali ulegając w
pierwszym etapie utleniania.

Preparatyka analityczna
Przyspieszenie rozpuszczania lub roztwarzania
Rozdrobnienie
- roztwarzanie, jak i rozpuszczanie można przyspieszyć przez
rozdrobnienie próbki (co powoduje zwiększenie powierzchni
zetknięcia między dwiema fazami),
Mieszanie
Wzrost temperatury
Próbki nieorganiczne nierozpuszczalne w kwasach lub alkaliach
stapia się odpowiednio dobranymi topnikami. Stosuje się topniki
alkaliczne (Na
2
CO
3
, K
2
CO
3
, NaOH i Na
2
O
2
), kwasowe (KHSO
4
,
KHF, K
2
S
2
O
7
, B
2
O
3
) i utleniające (Na
2
O
2
, Na
2
CO
3
+ Na
2
O
2
).
Dobór środowiska

Roztwarzanie próbek organicznych
(mineralizacja sucha i mokra).
Podłoże organiczne (materiały roślinne, żywność oraz materiały
biologiczne) - mineralizacja – przeprowadzenie do roztworu z
całkowitym rozkładem matrycy organicznej.
Mineralizacja
sucha – spopielanie, polega na spalaniu próbki w
piecu muflowym w temperaturze 300-500
o
C lub w specjalnie
skonstruowanej rurze kwarcowej. Pozostałość po spaleniu rozpuszcza
się w kwasach i dopiero w tym roztworze oznacza się pierwiastki
nielotne, najczęściej metale.
Mineralizacja mokra
– polega na ogrzewaniu próbki z kwasami lub
ich mieszaninami. w zlewce, parownicy, albo w systemie
zamkniętym: w kolbach z chłodnicą zwrotną.
Preparatyka analityczna

Inne metody mineralizacji.
Mineralizacja ciśnieniowa
– (w bombie teflonowej), to
mineralizacja na drodze mokrej w systemie zamkniętym. Próbkę z
kwasami utleniającymi umieszcza się w pojemniku teflonowym w
obudowie stalowej, szczelnie zamkniętej. Całość ogrzewa się w
temperaturze 180
o
C.
Mineralizacja mikrofalami
– metoda stosowana do
przeprowadzania do roztworu zarówno materiałów organicznych, jak
i nieorganicznych. Jest to pewna odmiana mineralizacji mokrej, która
przebiega kilkakrotnie szybciej pod wpływem ogrzewania w układzie
mikrofalowym. Niekiedy przeprowadza się ją pod ciśnieniem, w
specjalnie do tego celu skonstruowanych naczyniach.
Mineralizacja w strumieniu wzbudzonego tlenu
– tą metodą
można mineralizować tylko bardzo małe próbki. Łódeczkę z bardzo
małym materiałem umieszcza się w rurze kwarcowej w atmosferze
O
2
.
Mineralizacja przez naświetlanie promieniami UV
–
mineralizowaną próbkę w roztworze umieszcza się w tyglu
kwarcowym i przykrywa kwarcowym szkiełkiem zegarowym,
następnie naświetla lampą rtęciową nisko- lub wysokociśnieniową.
Preparatyka analityczna

Ocena jakości oznaczeń analitycznych
Ocena i interpretacja
wyników analizy chemicznej
•Każdy wynik analizy chemicznej, nawet wykonanej zupełnie
prawidłowo, jest obciążony mniejszym lub większym błędem.
•Błędy te mają zróżnicowany charakter
•mogą wynikać z niedoskonałości samej metody pomiarowej
•niedoskonałości przyrządów stosowanych w laboratorium
•istnieniu w analizowanej mieszaninie innych substancji, które
zniekształcają wyniki pomiarów,
•mogą być związane z niedoświadczeniem lub niesumiennością
osoby wykonującej analizę.
Rodzaje błędów
Błąd gruby
Błędem systematycznym
błędy metodyczne, aparaturowe, indywidualne.
Błąd przypadkowy.

Czułość metody
, zwana również limitem oznaczalności (detekcji),
określa najmniejszą ilość substancji lub jej stężenie, jakie można realnie
zmierzyć metodą analityczną. Najlepsze metody analizy klasycznej
charakteryzują się czułością rzędu 10
-5
g, metody analizy instrumentalnej
często pozwalają oznaczać mniejsze ilości. Często dla obniżenia limitu
oznaczalności stosuje się zwłaszcza w metodach instrumentalnych wstępne
zagęszczanie analizowanego składnika, dzięki czemu można oznaczać
niektóre substancje na poziomie 10-15.
Dokładność metody
polega na zgodności otrzymanych wyników z
wartością rzeczywistą. Ilościowo miarą dokładności jest wielkość błędu,
czyli różnica między otrzymanym wynikiem a wartością rzeczywistą; im
mniejszy błąd, tym większa dokładność.
Precyzja metody
analitycznej jest to zgodność kolejnych otrzymywanych
wyników między sobą. Im mniejsze są różnice miedzy wynikami
poszczególnych oznaczeń, tym precyzja jest większa. Osiągnięcie dużej
dokładności jest niemożliwe bez dużej precyzji pomiarów, jednakże sama
precyzja, choćby bardzo znaczna, nie wystarcza do uzyskania wyników
dokładnych.
Czułość, dokładność i precyzja metod analitycznych
Ocena jakości oznaczeń analitycznych

Powtarzalność
metody rozumie się zgodność wyników uzyskiwanych
tą samą metodą i za pomocą tej samej aparatury podczas
wielokrotnego analizowania tych samych próbek przez jedną osobę.
Odtwarzalność
to zgodność wyników uzyskiwanych podczas
analizowania tą samą metodą identycznych próbek, ale przez różnych
wykonawców, pracujących w różnych laboratoriach, lub w tym samym
laboratorium, lecz w innym czasie.
Miarą dokładności metody analitycznej jest błąd systematyczny
popełniany w trakcie analizy. Błąd ten można wyrazić na dwa sposoby:
Błąd bezwzględny
jest to różnica między wynikiem analizy a wartością rzeczywistą.
Błąd względny
to stosunek błędu bezwzględnego do wartości rzeczywistej;
najczęściej błąd względny wyraża się w procentach.
Ocena jakości oznaczeń analitycznych
Ocena statystyczna wyników pomiarów
jest poza zakresem merytorycznym niniejszego wykładu:
Powtórzyć samodzielnie!
Wyszukiwarka
Podobne podstrony:
Prezentacja 2 analiza akcji zadania dla studentow
Zadanie 4 CHEMIA ANALITYCZNA
zadania chrom, Analityka semestr IV, Analiza Instumentalna
2015 Zadania dla lekarskiego
zadania dla dzieci
plytoteka, Zadania dla uczniów, Bazy danych, płytoteka 3 VI 2014
Zadania dla maturzystów na dzień 28 marca 2010, matematyka, LICEUM, arkusze maturalne, Nowy folder (
Zadania dla klasy 2 Zjawisko fotoelektryczne,?le? Broglie’a
Zadania 15X2013, Zadania dla uczniów, Programowanie
Zadanie Wypadki dodatkowe, Zadania dla uczniów, Bazy danych, zadanie dodatkowe 1
zadania dla studentów
Zadania dla klas 5 6
Zadania dla 6-7 latków nr 2
zacznik nr 2 zadania dla grup
zadania dla wszop Liczby zespolone
lipoproteiny dla analityki
Zadania dla studentów MSSF 5 i MSR 2, STUDIA UE Katowice, semestr I mgr, materiały od gr. 7, Standa
Zadania dla studentów instrumenty finansowe, STUDIA UE Katowice, semestr I mgr, materiały od gr. 7,
więcej podobnych podstron