
1
11.
REAKCJE
CHARAKTERYSTYCZNE
AMINOKWASÓW
1. Deaminacja aminokwasów kwasem azotowym (III)
Zasada:
Aminokwasy pod wpływem kwasu azotowego (III), tworzącego się wg reakcji
pierwszej, ulegają reakcji deaminacji, której produktami są: azot cząsteczkowy
(wydzielający się w formie gazowej) oraz odpowiedni hydroksykwas. Deami-
nacja
α
-aminokwasu przebiega zgodnie z drugą reakcją przedstawioną poniżej:
Reakcja ta jest podstawą w gazometrycznej metodzie ilościowego oznaczania
α
-aminokwasów metodą van Slyke’a.
Wykonanie:
•
W probówce zmieszać:
– 1 ml 10% roztworu NaNO
2
(azotanu (III) sodowego),
– 1 ml 2 M roztworu CH
3
COOH – odczekać, aż zmniejszy się wydzielanie
gazu o żółtej barwie i ostrej woni (tlenki azotu), po czym dopiero dodać do
probówki:
– 2 ml 1% roztworu glicyny lub innego
α
-aminokwasu i obserwować wydziela-
nie się produktu gazowego reakcji deaminacji.
H
C
H
NH
2
COOH
HNO
2
H
C
H
OH
COOH
N
2
H
2
O
+
+
+
NaNO
2
CH
3
COOH
HNO
2
CH
3
COONa
+
+
Reakcja 1
Reakcja 2
2
2. Wykrywanie aminokwasów aromatycznych,
reakcja ksantoproteinowa
Zasada:
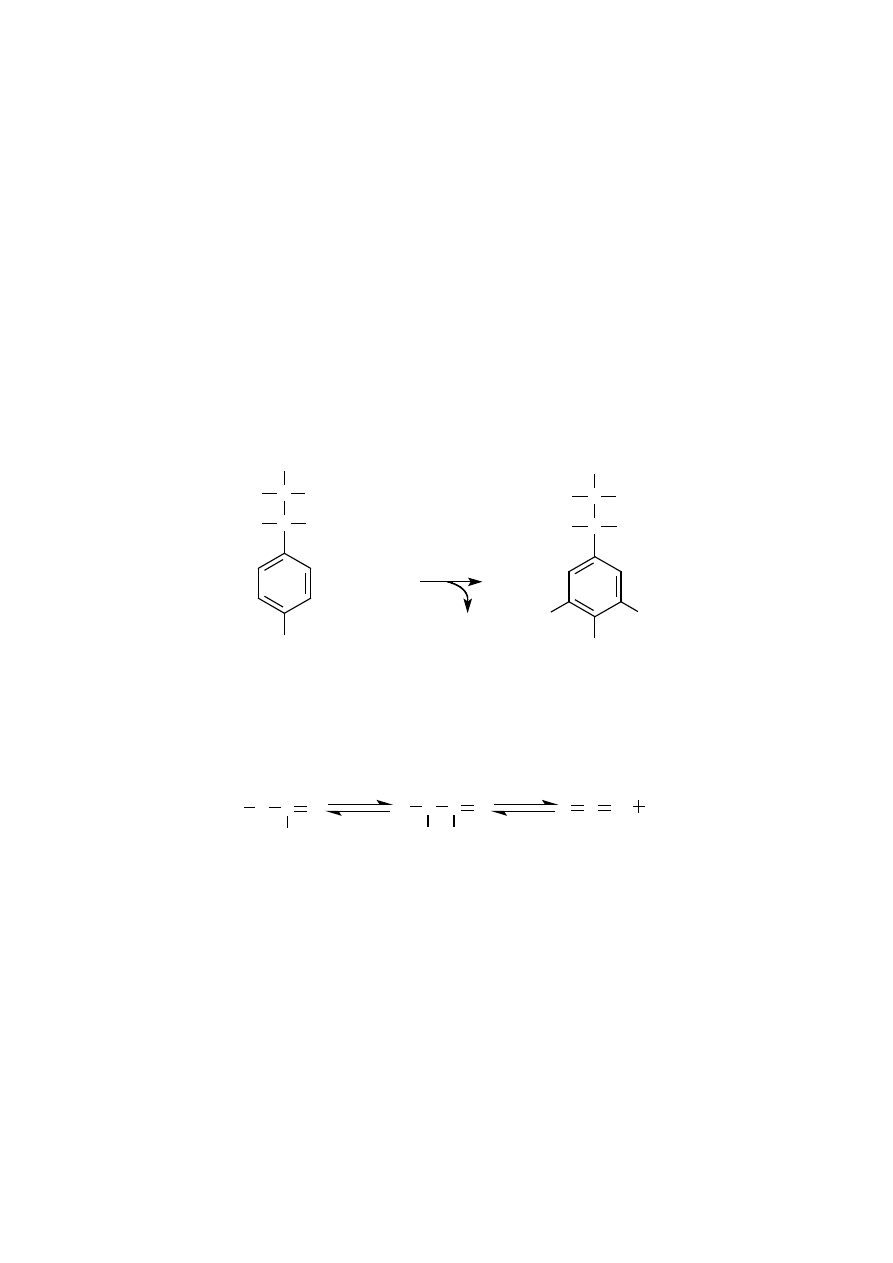
Aminokwasy aromatyczne – zarówno wolne, jak i związane w białku – ulegają
nitrowaniu, tworząc nitrowe pochodne o barwie żółtej. Tylko sporadycznie
można nitrować związki aromatyczne samym stężonym kwasem azotowym (V).
Udaje się to w przypadku związków o skondensowanych pierścieniach, np. an-
tracenu, oraz w przypadku dwóch aminokwasów, tyrozyny i tryptofanu. Reak-
cja z tyrozyną przebiega według następującego schematu:
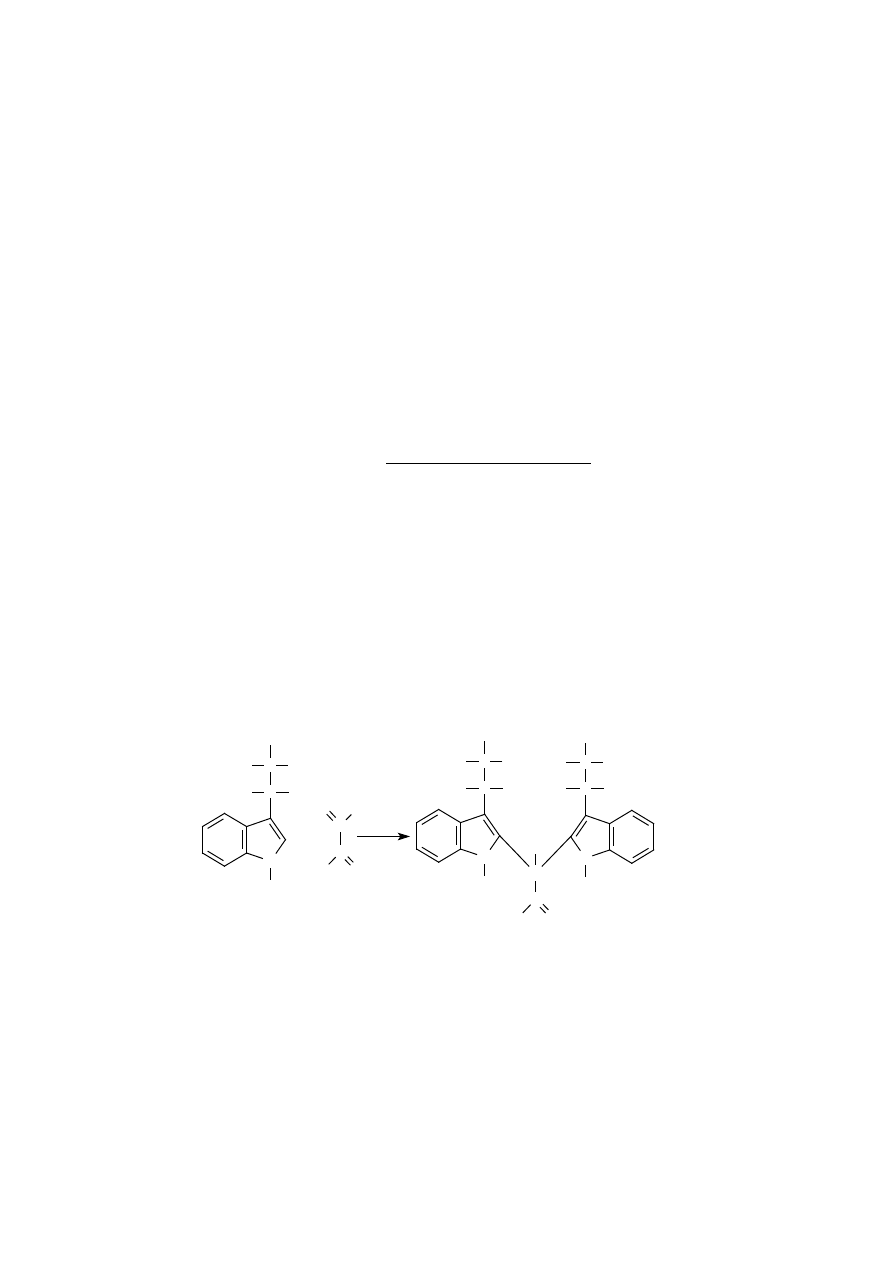
W reakcjach nitrowania innych związków aromatycznych, w tym również feny-
loalaniny, najczęściej wykorzystywanym azotowym elektrofilem jest kation ni-
troniowy, NO
2
+
. Jon nitroniowy powstaje z kwasu azotowego (V) pod wpły-
wem katalizującego protonu, dostarczanego przez kwas siarkowy, zgodnie z re-
akcją:
Uprotonowany kwas azotowy po odłączeniu cząsteczki wody przechodzi w jon
nitroniowy. W praktyce podczas reakcji nitrowania stosuje się tzw. mieszaninę
nitrującą, która składa się ze stężonego kwasu azotowego (V) oraz ze stężonego
kwasu siarkowego (w stosunku 1:3 v/v). W środowisku zasadowym barwa ni-
trowych pochodnych aminokwasów pogłębia się do żółtopomarańczowej, skut-
kiem utworzenia soli.
OH
C
C
COOH
H
H
NH
3
+
H
HNO
3
OH
C
C
COOH
H
H
NH
3
+
H
O
2
N
NO
2
2
+
H
2
O
2
O
H
+
+
HSO
4
-
H O
+
N
O
-
H O
+
N
O
-
H
+
O
O
O
+
N
H
2
O
kwas azotowy
uprotonowany
nitroniowy
jon
kwas azotowy (V)
3
Wykonanie:
•
Przygotować trzy probówki, do których należy odmierzyć po 1 ml:
– 1% roztworu tyrozyny – do pierwszej,
– 1% roztworu glicyny – do drugiej probówki,
– 1% roztworu białka (albuminy, owoalbuminy, żelatyny lub rozcieńczonej su-
rowicy) – do trzeciej.
•
Do wszystkich probówek dodać po 1 ml stężonego kwasu azotowego (V)
i ogrzewać 5 minut we wrzącej łaźni wodnej.
•
Zaobserwować, w których probówkach roztwór zabarwił się na żółto.
•
Następnie wszystkie probówki należy oziębić pod bieżącą wodą i dodać po
4 ml 20% roztworu NaOH (reakcja silnie egzotermiczna!).
•
Zaobserwować, w których probówkach roztwór zabarwi się na kolor
ż
ółtopomarańczowy. Zinterpretować uzyskane wyniki.
3. Wykrywanie pierścienia indolowego w tryptofanie
Zasada:
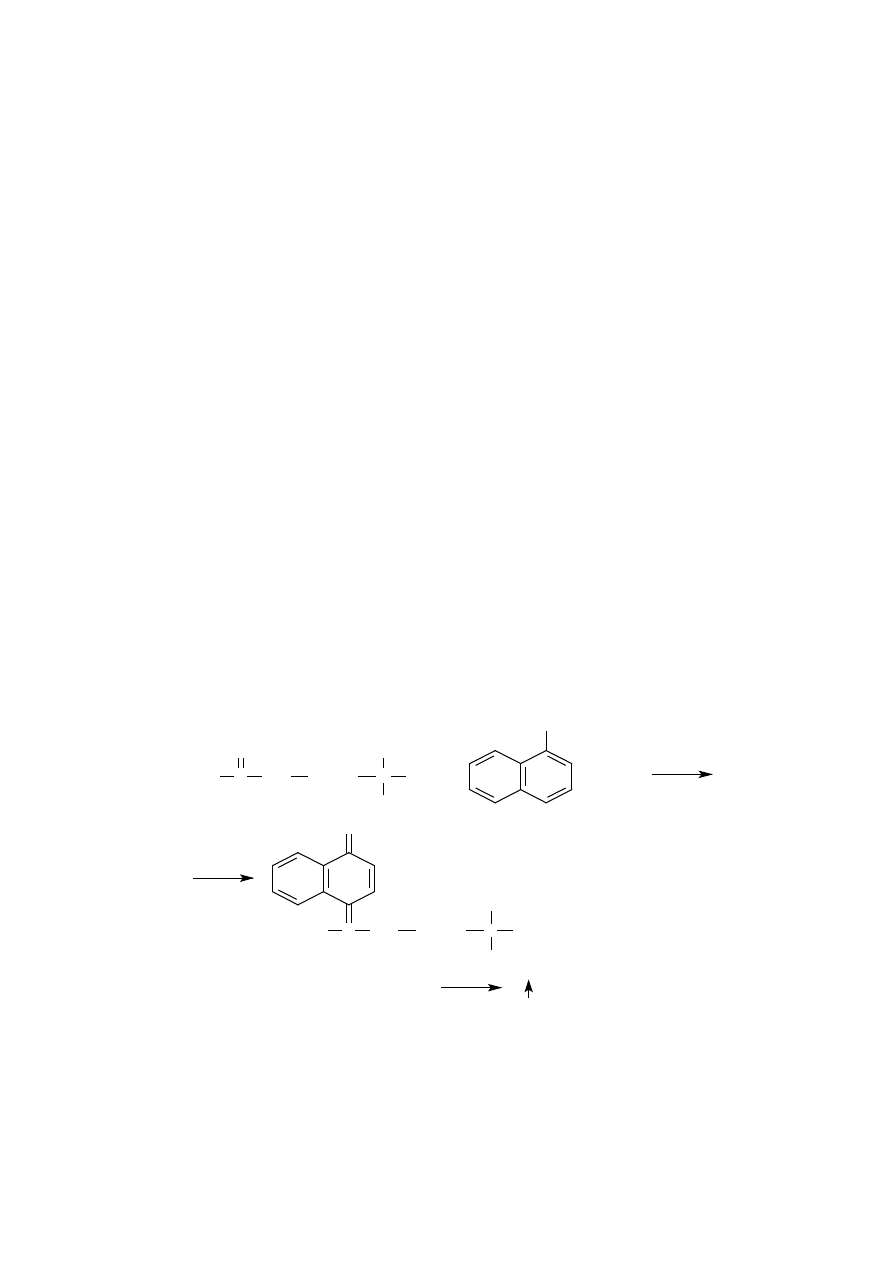
W środowisku kwaśnym tryptofan reaguje z aldehydami, między innymi z kwa-
sem glioksalowym (reakcja Adamkiewicza-Hopkinsa) lub aldehydem mrów-
kowym (reakcja Voisseneta), dając barwne produkty kondensacji. W kwaśnych
hydrolizatach peptydów lub białek wynik tej reakcji jest ujemny, ponieważ
tryptofan podczas kwaśnej hydrolizy ulega zniszczeniu.
Wykonanie:
•
Przygotować trzy probówki, do których należy odmierzyć po 1 ml:
– 1% roztworu tryptofanu – do pierwszej,
N
C
C
COOH
H
H
NH
3
+
H
H
C
C
H
HO
O
O
N
C
C
COOH
H
H
NH
3
+
H
H
C
C
HO
O
H
N
C
C
COOH
H
H
H
NH
3
+
H
H
2
O
+
+
2
4
– 1% roztworu glicyny – do drugiej,
– 2% roztworu białka (jaja kurzego, albuminy, żelatyny lub rozcieńczonej su-
rowicy) – do trzeciej.
•
Do wszystkich probówek dodać 0,5 ml kwasu glioksalowego (lub formaliny)
i wymieszać.
•
W każdej próbie podwarstwić 1 ml stężonego kwasu siarkowego – dodając
kwas powoli, po ściance lekko przechylonej probówki, której nie należy
wstrząsać. Ogrzewać we wrzącej łaźni do 2 minut.
•
Pojawienie się czerwonofioletowego pierścienia na granicy faz oznacza do-
datni wynik na obecność tryptofanu.
•
Zinterpretować uzyskane wyniki.
4. Wykrywanie układu guanidynowego w argininie, reakcja
Sakaguchiego
Zasada:
Grupa guanidynowa argininy w obecności utleniacza bromianu (I) w środowi-
sku zasadowym tworzy z
α
-naftolem barwny, pomarańczowoczerwony produkt
i uwalnia się amoniak. W razie dłuższego działania NaBrO następuje odbarwie-
nie roztworu, ponieważ barwny produkt utlenia się dalej. Dodanie roztworu
mocznika (40%) stabilizuje utworzony barwnik. Reakcja ta wykorzystywana
jest do ilościowego oznaczenia argininy w białkach, szczególnie bogatych w ten
aminokwas.
H
2
N
C
N H
N H
(C H
2
)
3
C
N H
2
C O O
-
H
O H
N aBrO
O
C
H
2
N
N H
(C H
2
)
3
C
H
N H
2
C O O
-
N aBr
N H
3
+
+
+
+
2 N H
3
+ 3 N aBrO
N
2
+ 3H
2
O + 3N aBr
5
Wykonanie:
•
Przygotować trzy probówki, do których należy odmierzyć po 1 ml:
– 0,1% roztworu argininy – do pierwszej,
– 1% roztworu glicyny – do drugiej,
– 1% roztworu białka (jaja kurzego, albuminy, żelatyny lub rozcieńczonej su-
rowicy) – do trzeciej.
•
Do wszystkich probówek dodać po:
– 1 ml 10% roztworu NaOH, a następnie po 2–3 krople 0,2% alkoholowego
roztworu
α
-naftolu (odczynnik Molischa), każdą próbę dokładnie wymieszać.
•
Do wszystkich prób dodać po 0,25 ml bromianu (I) sodowego, dokładnie
wymieszać i dodać po: 0,5 ml 40% roztworu mocznika w celu stabilizacji po-
jawiającego się pomarańczowoczerwonego barwnika.
•
Zinterpretować uzyskane wyniki.
5. Wykrywanie pierścienia imidazolowego w histydynie,
reakcja Pauly’ego
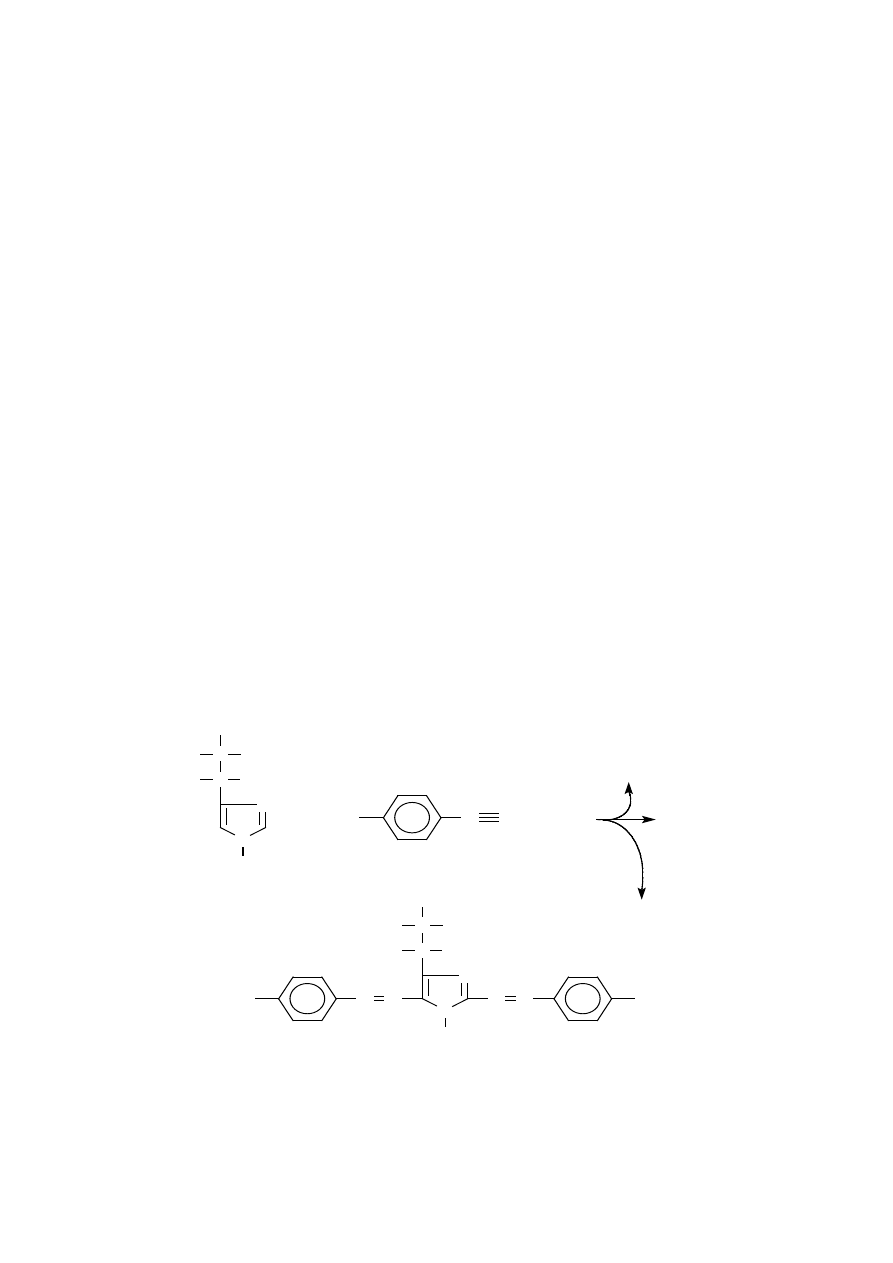
Zasada:
Pierścień imidazolowy histydyny w środowisku zasadowym ulega reakcji
sprzęgania z jonem p-sulfobenzenodiazoniowym, której produktem jest poma-
rańczowy barwnik azowy, powstający zgodnie z przedstawionym schematem:
N
N
C
C
C O O
-
N H
2
H
H
H
H
-
O
3
S
N
+
N
N aC O
3
C O
2
H
2
O
N
N
C
C
C O O
-
N H
2
N
N
N
N
N aO
3
S
SO
3
N a
H
H
H
H
-
+ 2
+

6
Wykonanie:
•
Przygotować trzy probówki, do których należy odmierzyć po 0,5 ml:
– 0,5% roztworu histydyny – do pierwszej,
– 1% roztworu glicyny – do drugiej,
– 1% roztworu białka (jaja kurzego, albuminy, żelatyny lub rozcieńczonej su-
rowicy) – do trzeciej.
Otrzymywanie roztworu soli diazoniowej:
5 ml 0,5% roztworu kwasu sulfanilowego odmierzyć do probówki, umieścić ją
w zlewce z zimną wodą, następnie do próby dodać: 0,5 ml 0,5% roztworu
NaNO
2
i wymieszać. Otrzymany roztwór zalkalizować za pomocą Na
2
CO
3
in
subst., sprawdzając pH roztworu papierkiem wskaźnikowym.
•
Do trzech probówek z wcześniej przygotowanymi roztworami aminokwasów
lub białka dodać zalkalizowany roztwór soli diazoniowej i wymieszać.
•
Pojawienie się pomarańczowego zabarwienia oznacza dodatni wynik na obec-
ność histydyny.
•
Zinterpretować uzyskane wyniki.
6. Reakcja ninhydrynowa
Zasada:
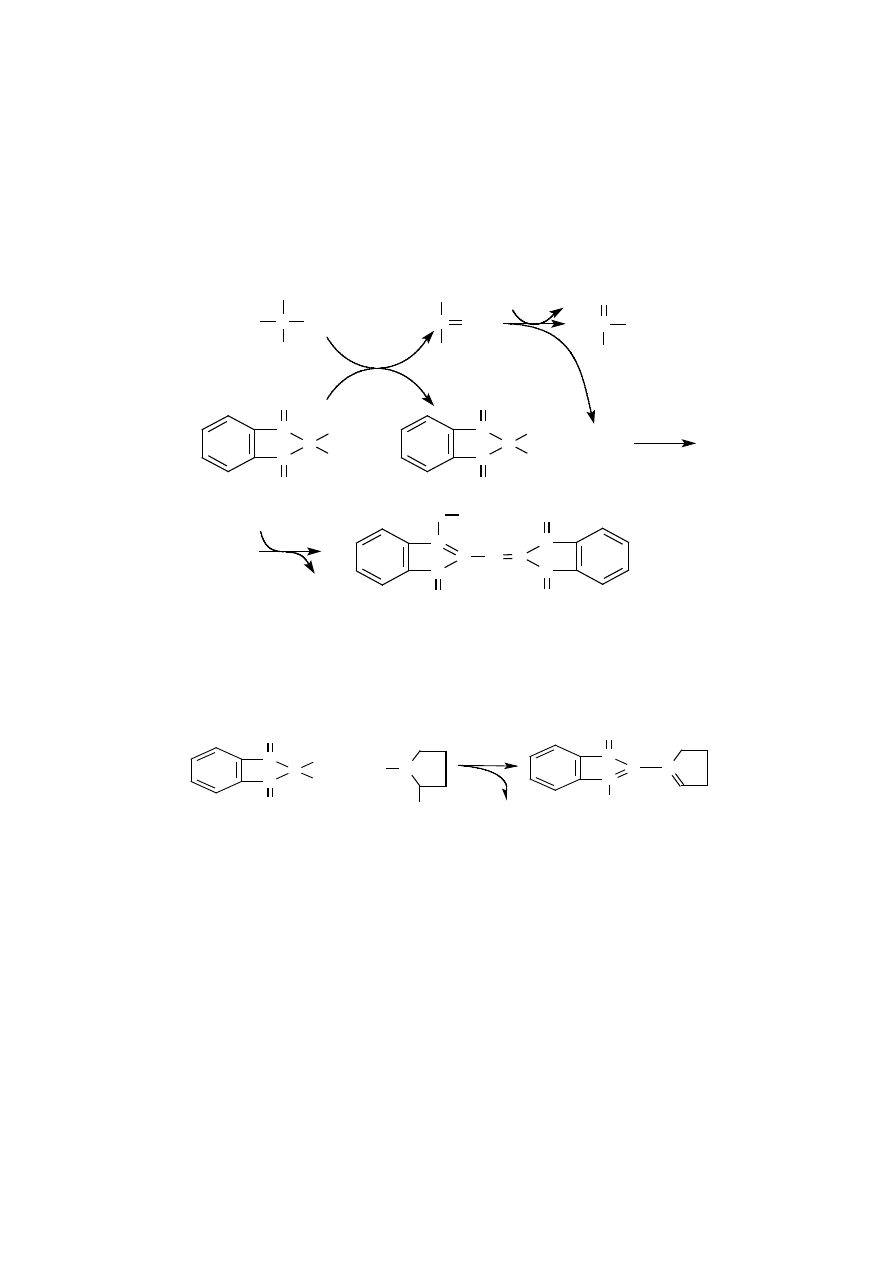
Aminokwasy pod wpływem ninhydryny ulegają utlenieniu, dekarboksylacji,
a później deaminacji. Przejściowo powstaje iminokwas i zredukowana ninhy-
dryna. Następnie iminokwas przekształca się w aldehyd uboższy o jeden atom
węgla, uwalnia się CO
2
oraz amoniak. W obecności powstałego amoniaku zre-
dukowana cząsteczka ninhydryny ulega reakcji kondensacji z utlenioną czą-
steczką ninhydryny i powstaje fioletowoniebieski produkt kondensacji zwany
purpurą Ruhemanna. Zależnie od rodzaju aminokwasu różna jest intensywność
i odcień powstającego zabarwienia. Reakcja ninhydrynowa jest czuła i dokład-
na. Dodatni jej wynik dają wszystkie wolne aminokwasy w środowisku o pH>4,
dlatego reakcja ta jest powszechnie stosowana do wykazania rozdzielanych
aminokwasów metodą chromatograficzną (patrz ćwiczenie: chromatografia
cienkowarstwowa). Natężenie zabarwienia jest proporcjonalne do stężenia
α
-
-aminokwasów, dlatego reakcja ninhydrynowa stanowi podstawę metody kolo-
rymetrycznej, ilościowego oznaczania wolnych
α
-aminokwasów. Dodatni od-
czyn ninhydrynowy dają również inne związki, które zawierają grupę
α
-ami-
nową, czyli sole amonowe, aminocukry, amoniak. Peptydy i białka również mo-
gą dawać dodatni odczyn ninhydrynowy, jednak tylko w nieznacznym stopniu;
7
zastanów się dlaczego? Reakcja aminokwasów z ninhydryną stanowi podstawę
metod gazometrycznych ilościowego oznaczania aminokwasów na podstawie
ilości wydzielonego CO
2
lub NH
3
.
Iminokwasy, prolina i hydroksyprolina, które nie zawierają grupy
α
-aminowej,
dają w reakcji z ninhydryną produkt o barwie żółtej.
Wykonanie:
•
Przygotować trzy probówki, do których należy odmierzyć po 1 ml:
– 0,1% roztworu
α
-aminokwasu (leucyny) do pierwszej,
– 1% roztworu proliny do drugiej,
– 1% roztworu peptydu lub białka (glutationu, albuminy, żelatyny lub rozcień-
czonej surowicy) do trzeciej.
•
Zakwaszone roztwory aminokwasów zobojętnić roztworem NaOH.
C
COOH
H
NH
2
R
C
C
O
O
C
OH
OH
C
C
O
O
C
H
OH
C
COOH
R
NH
C
R
H
O
H
2
O
CO
2
NH
3
H
2
O
C
C
O
C
N
O
NH
4
+
C
C
O
O
C
3
+
purpura Ruhemanna
+
NH
3
C
C
O
O
C
O H
O H
N
C O O H
H
C
C
O
O
-
C
+
N
C O
2
+

8
•
Do wszystkich probówek dodać po: 0,5 ml 0,1% roztworu ninhydryny w 50%
etanolu.
•
Próby ogrzać do wrzenia we wrzącej łaźni wodnej.
•
Zaobserwować pojawienie się charakterystycznego zabarwienia. Porównać
i zinterpretować uzyskane wyniki w poszczególnych próbach.
7. Wykrywanie siarki cysteiny i cystyny
Zasada:
Aminokwasy siarkowe z grupami –SH lub –S-S- (zarówno w stanie wolnym lub
związanym w białkach), podczas ogrzewania w środowisku silnie alkalicznym,
przekształcając się w kwas pirogronowy, uwalniają siarkę w postaci jonów
siarczkowych. Jony siarczkowe reagują z jonami ołowiu (II), dając czarny osad
PbS. Dodatkowym produktem jest amoniak. Metionina nie daje dodatniego wy-
niku tej reakcji.
Wykonanie:
•
Przygotować trzy probówki, do których należy odmierzyć po 0,5 ml:
– 1% roztworu cysteiny lub cystyny do pierwszej,
– 1% roztworu metioniny do drugiej,
– 1% roztworu białka: (jaja kurzego, albuminy, żelatyny lub rozcieńczonej su-
rowicy) do trzeciej.
•
Do wszystkich probówek dodać po: 1 kropli 0,25 M roztworu octanu ołowiu
(II), wymieszać i dodać
2 ml 20% roztworu NaOH.
•
Wstawić do wrzącej łaźni wodnej na 2–3 minuty.
•
Porównać i zinterpretować wyniki w poszczególnych próbach.
HS
CH
2
C
H
NH
2
COO
-
OH
-
C
CH
3
COO
-
O
NH
3
H
2
O
S
2-
Pb
2+
S
2-
PbS
+ 2
+
+
+
+

9
8. Wykrywanie grup tiolowych
Zasada:
Grupy tiolowe –SH tworzą z nitroprusydkiem sodu związek kompleksowy o za-
barwieniu czerwonofiołkowym, według przedstawionej reakcji:
Wykonanie:
•
Przygotować trzy probówki, do których należy odmierzyć po 1 ml:
– 0,1% świeżego roztworu cysteiny do pierwszej,
– 0,1% świeżego roztworu cystyny do drugiej,
– 1% roztworu białka (jaja kurzego, albuminy, żelatyny lub rozcieńczonej su-
rowicy) do trzeciej.
•
Do wszystkich probówek dodać po: 1 ml 1% wodnego roztworu nitroprusyd-
ku sodu, następnie siarczanu amonu in subst. do nasycenia roztworu, po czym
próby zalkalizować amoniakiem pod dygestorium.
•
Pojawienie się czerwonofiołkowego zabarwienia prób oznacza dodatni wynik
na obecność grup tiolowych.
•
Porównać i zinterpretować wyniki w poszczególnych próbach.
ODCZYNNIKI
10% roztwór NaNO
2
; 2 M roztwór CH
3
COOH; 1% wodny roztwór glicyny; 1%
wodny roztwór lizyny; 0,1% wodny roztwór argininy; 0,5% wodny roztwór hi-
stydyny; 1% wodny roztwór proliny; 1% roztwór tyrozyny w 0,1 M HCl; 1%
roztwór fenyloalaniny w 0,1 M HCl; 1% roztwór tryptofanu w 0,1 M HCl; 0,1%
roztwór leucyny w 0,05 M HCl; 1% roztwór cysteiny w 0,1M HCl; 1% roztwór
cystyny w 0,1 M HCl; 1% roztwór metioniny; 1% wodny roztwór białka;
20-krotnie rozcieńczone białko jaja kurzego (białko jaja roztrzepywać bagietką
szklaną, dodać dwudziestokrotną objętość wody, po maksymalnym roztrzepa-
[
Fe
+3
(CN )
5
N O
]
-2
N H
3
HS
CH
2
C
CO O H
H
N H
2
[
Fe
+2
(CN )
5
N
O
S
CH
2
C
N H
2
H
CO O H
]
-3
N H
4
+
+
+
+

10
niu, przesączyć); 2% roztwór albuminy w 0,9% NaCl; 2% roztwór żelatyny
w 0,9% NaCl; surowica bydlęca 10-krotnie rozcieńczona 0,9% NaCl; 1% roz-
twór glutationu; stężony HNO
3
; stężony H
2
SO
4
; 20% NaOH; 10% NaOH; stę-
ż
ony NH
3
aq.; aldehyd mrówkowy (formalina) lub kwas glioksalowy (sporzą-
dzony w następujący sposób: a) przygotować zawiesinę magnezową: 10 g pyłu
magnezowego dodać do 200 ml H
2
O w 2-litrowej zlewce; b) osobno przygoto-
wać nasycony roztwór kwasu szczawiowego – 25 g kwasu szczawiowego do
250 ml H
2
O; roztwór „b” wlać do zawiesiny „a” mieszaninę szybko schłodzić,
przesączyć przez sączek z bibuły i odrzucić osad szczawianu magnezu); 0,2%
etanolowy roztwór
α
-naftolu; roztwór NaOBr (sporządzony następująco: do
100 ml 5% NaOH dodać 0,62 ml bromu – przed użyciem roztwór ten rozcień-
czać 10-krotnie 5% NaOH); 40% roztwór mocznika; 0,5% roztwór kwasu sul-
fanilowego w 2 M HCl; 0,5% roztwór NaNO
2
; Na
2
CO
3
in subst.; papierki
wskaźnikowe; 0,1% roztwór ninhydryny w 50% etanolu; 0,25 M roztwór octa-
nu ołowiu (II); 1% wodny roztwór nitroprusydku sodu; (NH
4
)
2
SO
4
in subst.
NOTATKI
Wyszukiwarka
Podobne podstrony:
Aminokwasy i białka Reakcje charakterystyczne białek reakcja biuretowa
Aminokwasy i białka Reakcje charakterystyczne białek reakcja ksantoproteinowa
BIAŁEK I KWASÓW NUKLEINOWYCH REAKCJE CHARAKTERYSTYCZNE
Właściwości białek i kwasów nukleinowych Reakcje charakterystyczne
Reakcje charakterystyczne kationĂlw, STUDIA IŚ, semestr II, Chemia
biochemia VI a, Temat: Reakcje charakterystyczne sacharydów
8) Reakcje charakterystyczne sa Nieznany (2)
reakcje charakterystyczne
Lab 2 - Reakcje charakterystyczne cukrowców - instrukcja, BIOCHEMIA
3ta - ogólna charakterystyka białek, dydaktyka, konspekty
Reakcje charakterystyczne kationów I grupy
Reakcje charakterystyczne kationów, PWR, chemia
WŁAŚCIWOŚCI CUKRÓW I TŁUSZCZÓW REAKCJE CHARAKTERYSTYCZNE
Aminokwasy i białka Reakcje charakterystyczne aminokwasów II
reakcje charakterystyczne cukrów, ochrona środowiska UJ, IV semestr, chemia ograniczna, sprawozdania
Reakcje charakterystyczne alkoholi i fenoli
reakcje charakterystyczne
więcej podobnych podstron