
REAKCJE
CHARAKTERYSTYCZNE GRUP
FUNKCYJNYCH .
Reakcje grupowe alkoholi i
fenoli
ALKOHOLE
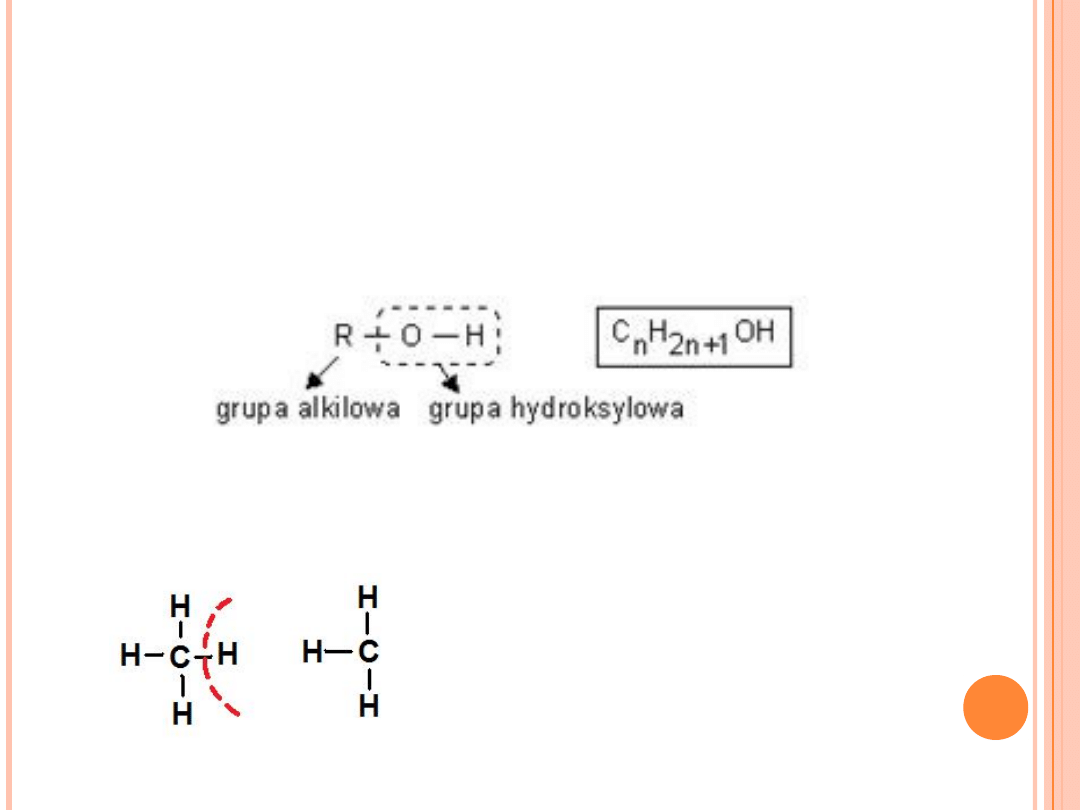
Alkohole są pochodnymi węglowodorów, w których atom lub atomy
został zastąpiony grupą hydroksylową -OH (hydroksylową). Grupa -OH
zawsze jest połączona z atomem węgla przy którym występują
wiązania pojedyncze.
Ogólny wzór alkoholi:
Grupa alkilowa - to grupa węglowodorowa, uzyskana z cząsteczki
węglowodoru,
po oderwaniu od niej jednego atomu wodoru,
Grupa metylowa
metyl
-CH
3
PODZIAŁ ALKOHOLI
Alkohole można podzielić ze względu na:
1.Liczbę grup hydroksylowych. Dzielimy na:
- monohydroksylowe (jednowodorotlenowe), np. CH
3
-OH
- polihydroksylowe (wielowodorotlenowe) np. glikol etylowy, glicerol
2. Rodzaj grupy węglowodorowej. Na:
-Alifatyczne, np. C2H5-OH
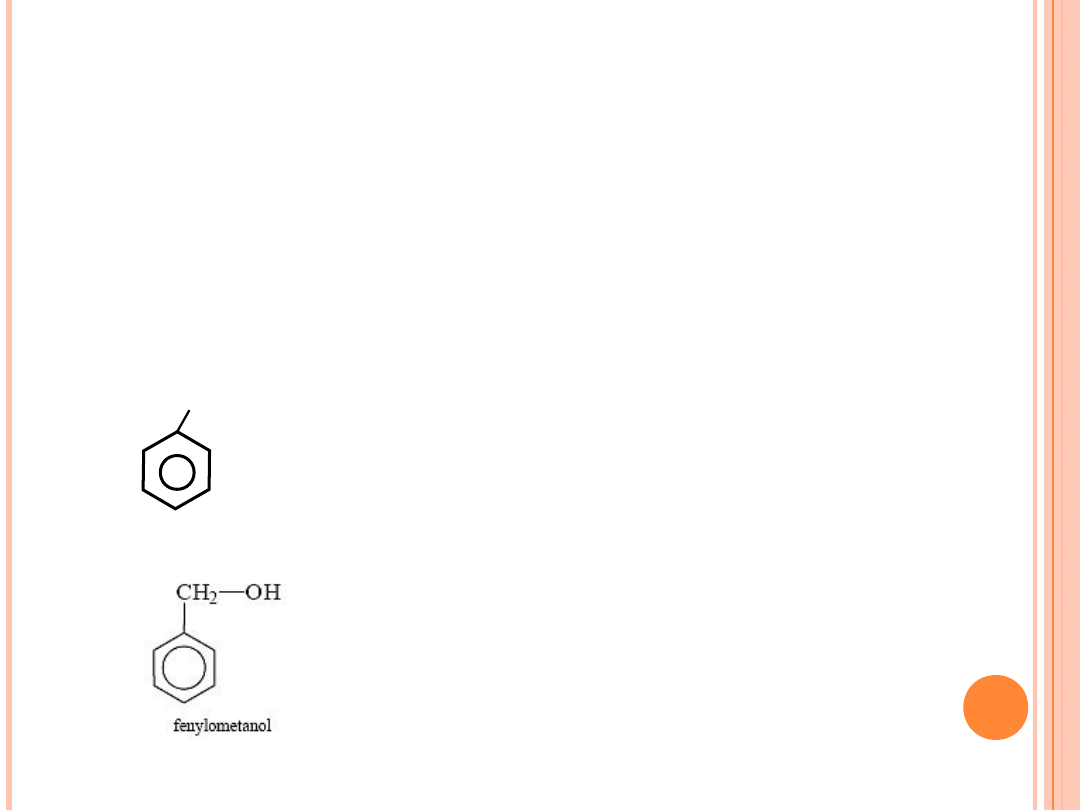
-Cykliczne , np. cykloheksan
OH
-Aromatyczne, np. fenylometanol (alkohol benzylowy)
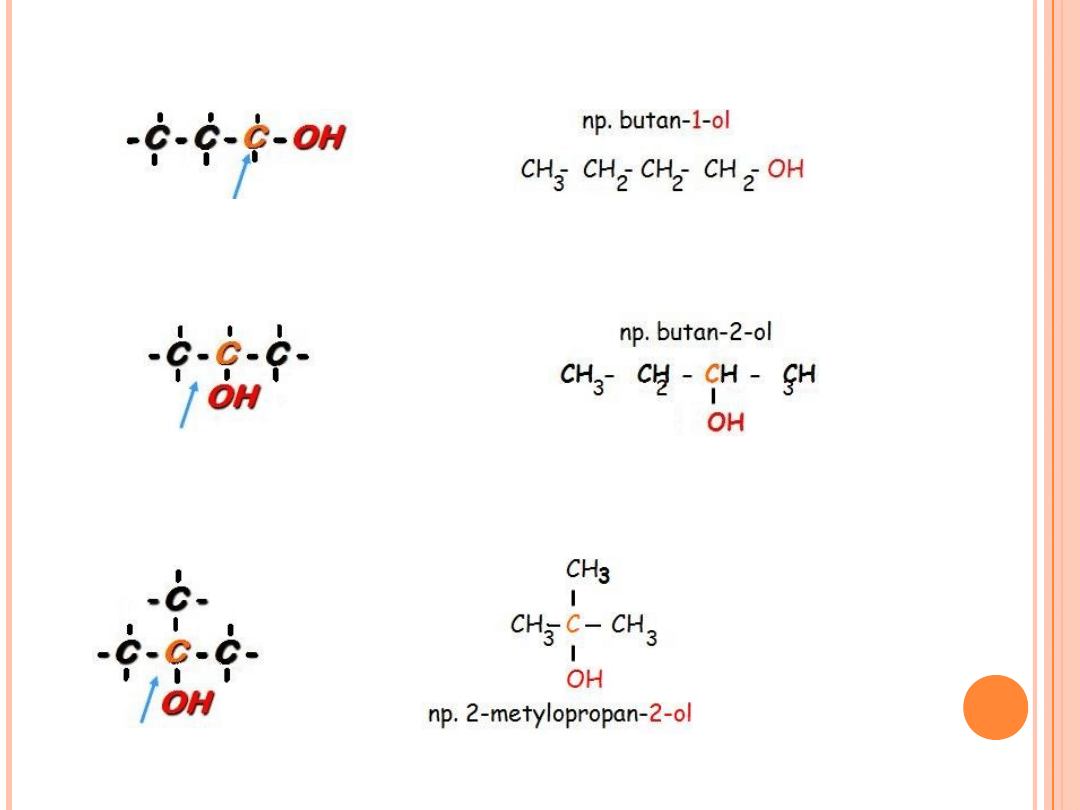
3. Rzędowość atomu węgla, przy którym znajduje się grupa hydroksylowa,
na:
•I-rzędowe: grupa –OH związana jest z pierwszorzędowym atomem węgla,
np.:
Węgiel I rzędowy (połączony tylko z jednym atomem
węgla)
• II- rzędowe: grupa –OH związana jest z drugorzędowym atomem
węgla, np.:
Węgiel II rzędowy (połączony z dwoma atomami węgla)
• III- rzędowe: grupa –OH związana jest z trzeciorzędowym atomem
węgla, np.:
Węgiel III rzędowy (połączony z trzema atomami węgla)
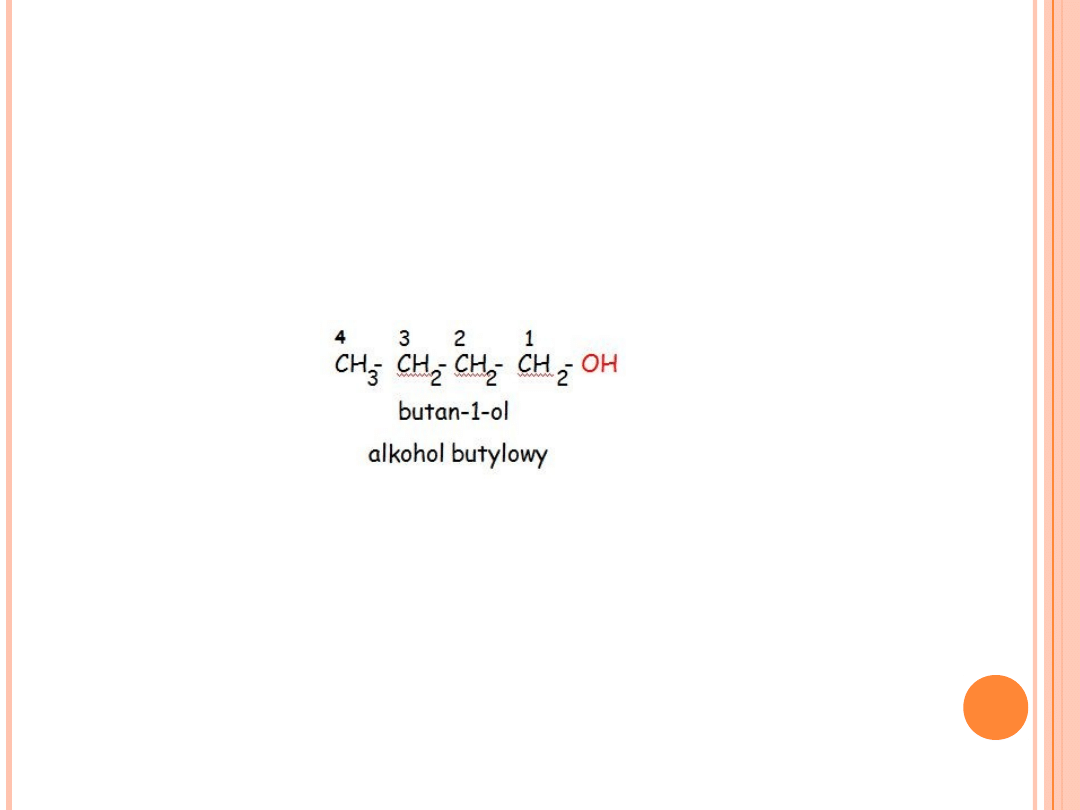
NAZEWNICTWO ALKOHOLI
Stosowane są trzy sposoby nazywania alkoholi.
1. Nazwę alkoholu tworzymy przez dodanie końcówki –ol do nazwy
macierzystego węglowodoru. Do utworzenia nazwy wybieramy
najdłuższy łańcuch węglowy, przy którym jest grupa OH.
2. Nazwy tworzy się używając słowa „alkohol” i przymiotnika,
określającego rodnik, z którym połączona jest grupa OH. Np. CH
3
OH
alkohol
metylowy.
3. Nazwy tworzy się używając przedrostka hydroksy- . Np.
hydroksymetyl
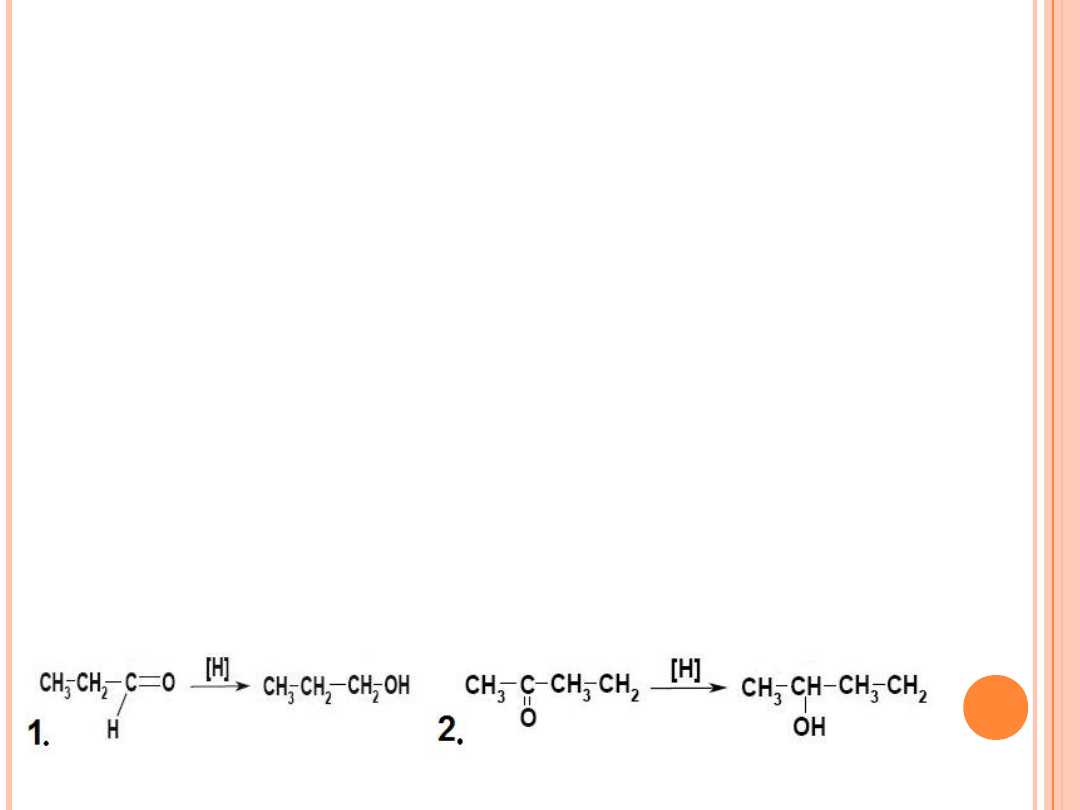
OTRZYMYWANIE ALKOHOLI
1. przez addycje wody do alkenów w środowisku kwaśnym
CH
2
=CH
2
+ H
2
O →CH
3
-CH
2
-OH
2. zastąpienie atomu chlorowca grupą –OH (reakcja substytucji)
CH
3
– CH
2
-Cl + H
2
O → CH
3
-CH
2
-OH + HCl
3. reakcja fluorowcoalkanów z mocnymi zasadami
CH
3
-CH
2
–Cl + NaOH → CH
3
-CH
2
-OH + NaCl
4. hydroliza estrów w środowisku kwaśnym
R
1
-COO-R
2
+ H
2
O –[H+ ]→ R
1
-COOH + R
2
-OH
5. Redukcja aldechydów (1) (alkohole pierwszorzędowe) i ketonów (2)
(alkohole drugorzędowe )
REAKCJE CHARAKTERYSTYCZNE
1. reakcja z metalami aktywnymi(K, Na na gorąco również Ca i Mg).
W wyniku reakcji powstają alkoholany.
2 CH
3
CH
2
-OH + 2Na → 2 CH
3
CH
2
-ONa
Powstał etanolan sodu
2. reakcja odwadniania(reakcja eliminacji cząsteczki wody).
Kataliator: Al2O3 i temperatura.
CH
3
CH
2
-OH→ CH
2
=CH
2
+H
2
O
3. Działając fluorowcowodorem otrzymuje się fluorowcoalkany.
Najłatwiej reakcja zachodzi dla alkoholi IIIrzędowych.
R-OH + HBr →R-Br + H2O
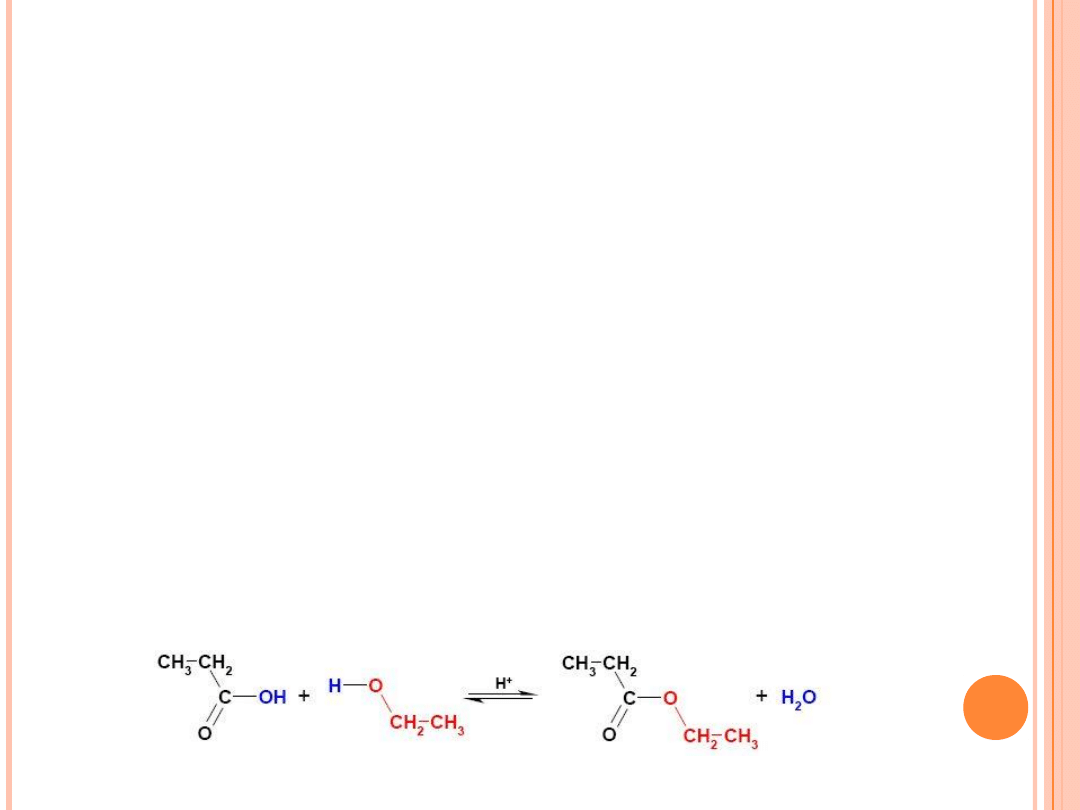
4. Tworzenie estrów. Estry to produkty reakcji alkoholi z kwasami
organicznymi i nieorganicznymi.
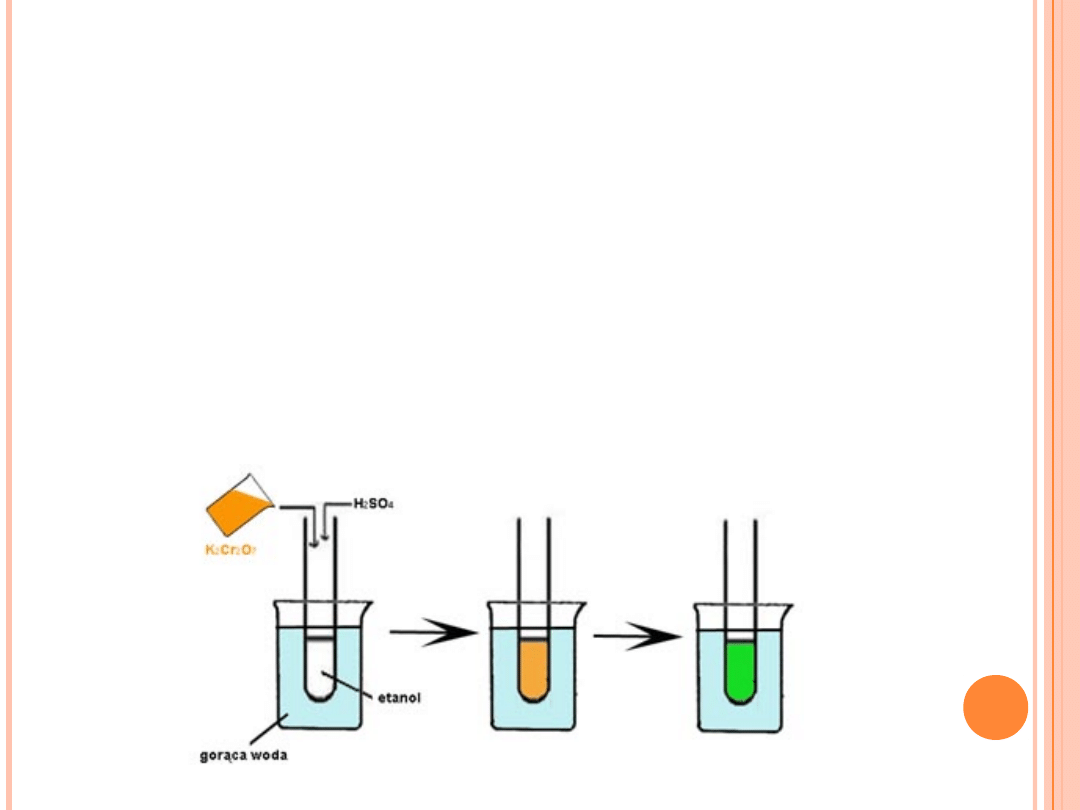
WYKRYWANIE OBECNOŚCI
ETANOLU
Do probówki z etanolem dodaje sie 2 krople roztworu
dichromianu(VI) potasu (K2Cr2O7) i krople stężonego kwasu
siarkowego (H2SO4). Całość należy łagodnie podgrzać np. w zlewce
z gorącą wodą.
Obserwacje:
Roztwór zmienił zabarwienie z pomarańczowej na zieloną.
K
2
Cr
2
O
7
+ 3CH
3
OH + 4H
2
SO
4
→ Cr
2
(SO
4
)
3
+ 3HCHO + K
2
SO
4
+
7H
2
O
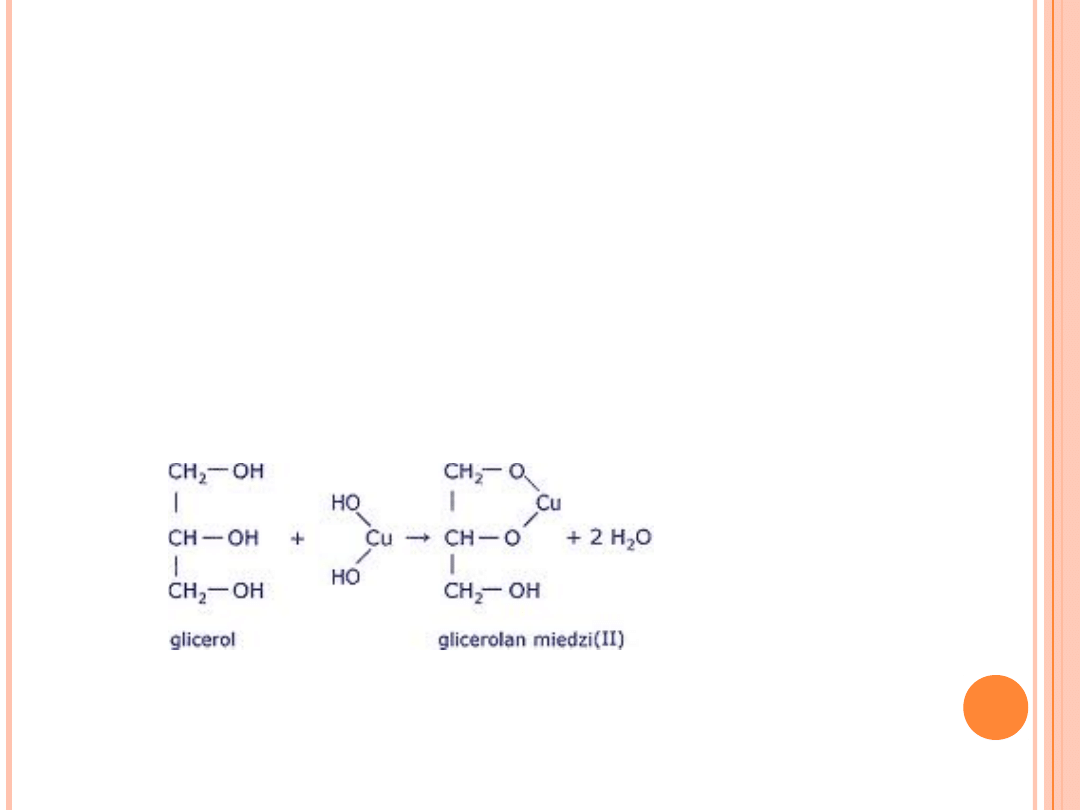
ODRÓŻNIANIE ALKOHOLI
MONOHYDROKSYLOWYCH OD
POLIHYDROKSYLOWYCH
Do próbówki dodajemy świeżo wytrącony wodorotlenek miedzi(II)
Cu(OH)
2 .
Reakcja zachodzi na zimno
Obserwacje:
Zabarwienie się roztworu na szafirowo świadczy o obecności
alkoholu polihydroksylowego.
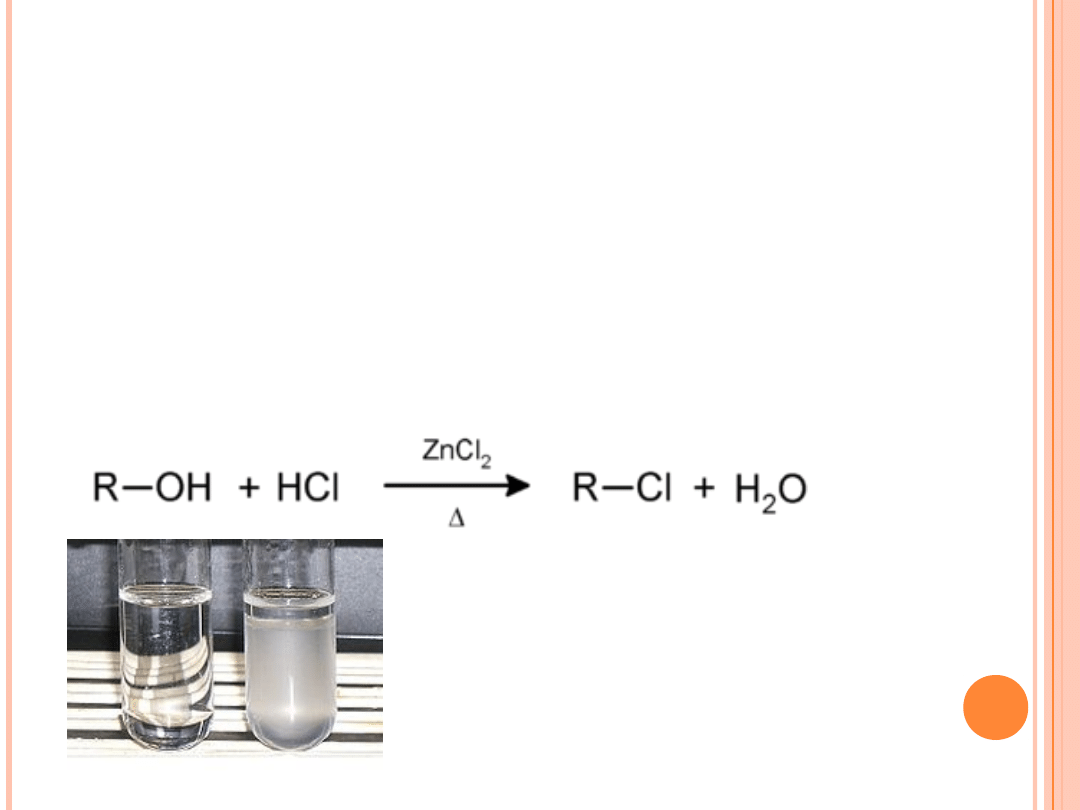
PRÓBA LUCASA
Do probówki z badanym alkoholem dodajemy odczynnik
Lucasa (mieszanina stężonego HCl i ZnCl
2
).
Obserwacje:
Zmętnienie pojawia się najszybciej w przypadku alkoholi
trzeciorzędowych, dla alkoholi drugorzędowych reakcja
zachodzi dopiero po kilku minutach.
Próba Lusaca. Wynik
negatywny dla
pierwszorzędowego etanolu (po
lewej); wynik pozytywny dla
trzeciorzędowego tert-butanolu
(po prawej - widoczne
zmętnienie i rozdzielenie faz)

REAKCJA JODOFORMOWA
Próba jodoformowa pozwala na jednoznaczne wykrycie etanolu lub
alkohou drugorzędowego o wzorze ogólnym RCHOHCH
3
z alkoholi
takich może powstać jodoform, ponieważ jod w zasadowym utlenia
drugorzędowe alkohole do ketonów. RCHCH
3
WYKONANIE:
Do próbówki z alkoholem dodać ok. wody i 1-2 cm³ 5% NaOH, a
następnie
kroplami dodawać odczynnik do chwili utrzymania się ciemnej
barwy jodu. Jeśli po chwili nie pojawi się osad wstawić probówkę do
gorącej wody na kilka minut. Następnie oziębić.
Obserwację:
powstaje żółty krystaliczny osad.
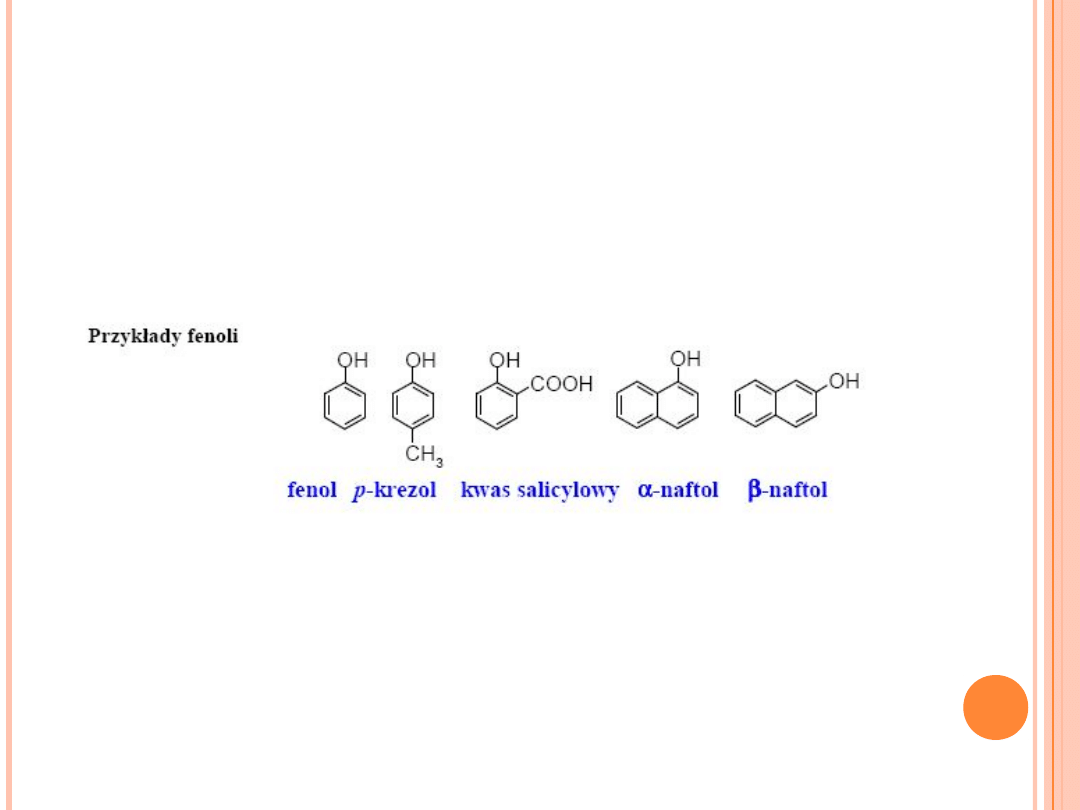
FENOLE
Fenolami nazywane są areny zawierające grupę hydroksylową -OH
związaną bezpośrednio z pierścieniem aromatycznym.
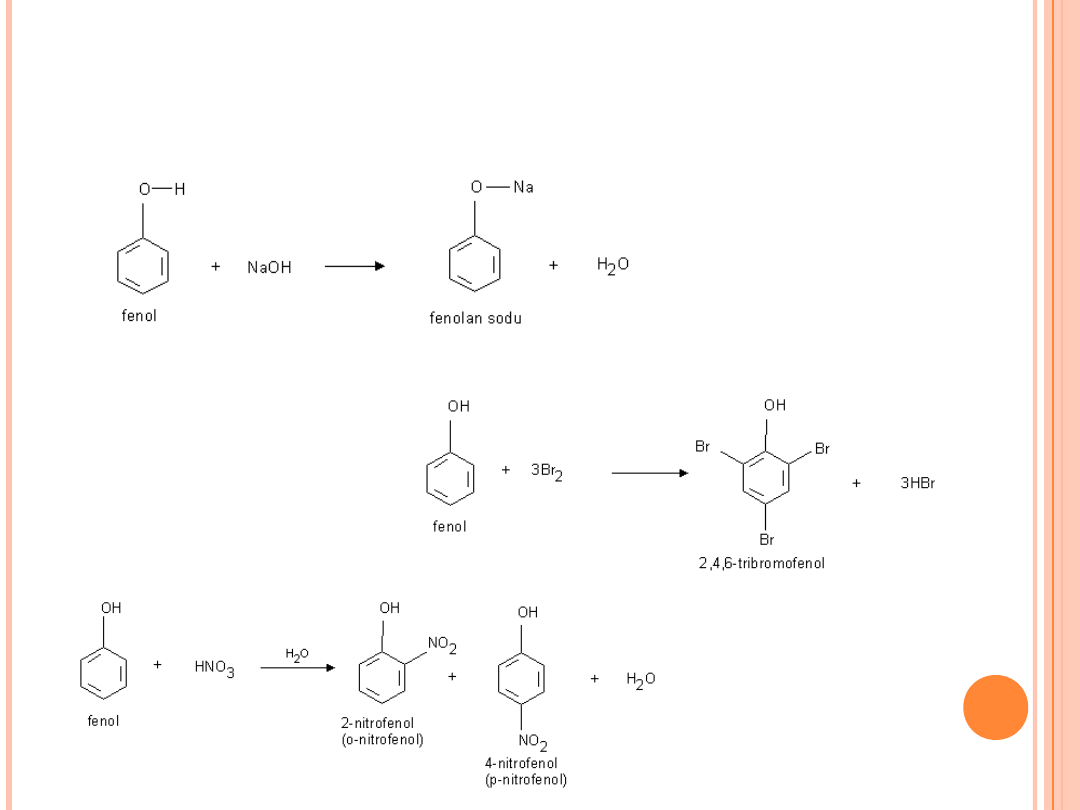
REAKCJE CHARAKTERYSTYCZNE
FENOLI
1. reakcja fenolu z NaOH. Powstał fenolan sodu
2. reakcja fenolu z woda bromową . Pomarańczowy roztwór wody
bromowej odbarwia się po dodaniu fenolu.
3. Reakcja nitrowania
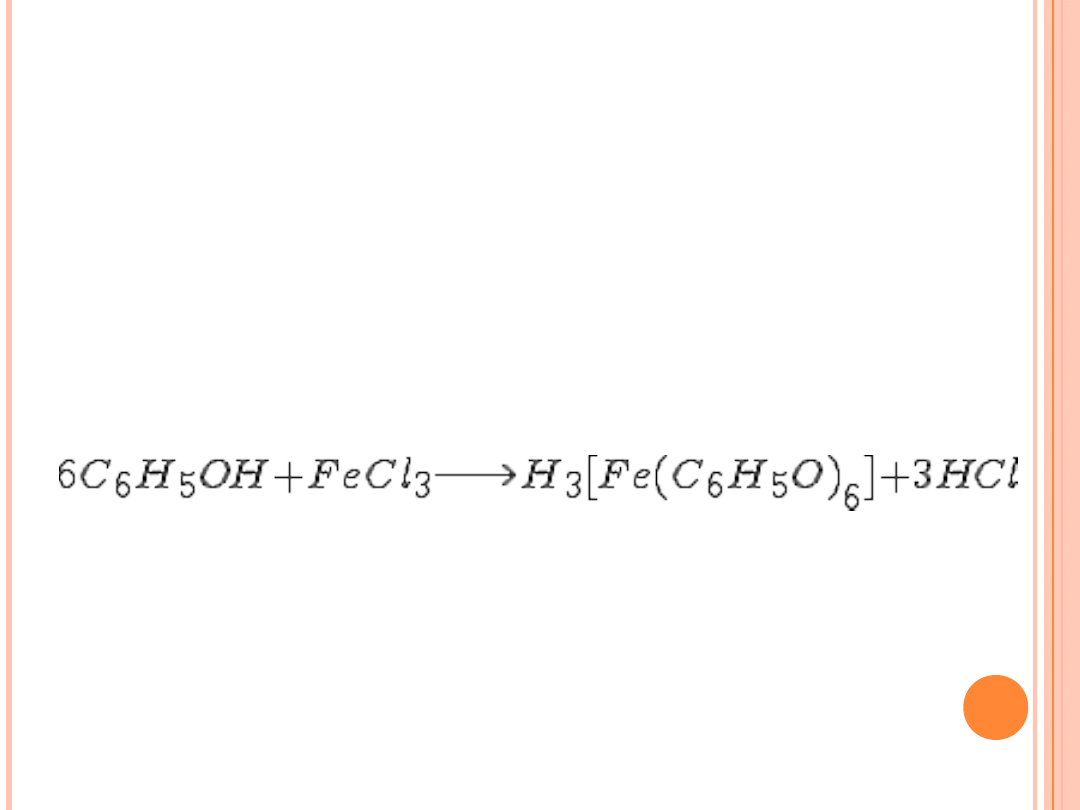
WYKRYWANIE FENOLU
Do próbówki z fenolem dodajemy chlorek żelaza(III) FeCl
3
Obserwacje:
Powstaje niebieskofioletowy roztwór. Reakcja ta jest bardzo
czuła - pozwala wykryć nawet śladowe ilości fenolu.
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
Wyszukiwarka
Podobne podstrony:
Aminokwasy i białka Reakcje charakterystyczne białek reakcja biuretowa
Reakcje charakterystyczne kationĂlw, STUDIA IŚ, semestr II, Chemia
biochemia VI a, Temat: Reakcje charakterystyczne sacharydów
BIAŁEK I KWASÓW NUKLEINOWYCH REAKCJE CHARAKTERYSTYCZNE
8) Reakcje charakterystyczne sa Nieznany (2)
reakcje charakterystyczne
Lab 2 - Reakcje charakterystyczne cukrowców - instrukcja, BIOCHEMIA
Reakcje charakterystyczne kationów I grupy
Reakcje charakterystyczne kationów, PWR, chemia
WŁAŚCIWOŚCI CUKRÓW I TŁUSZCZÓW REAKCJE CHARAKTERYSTYCZNE
Aminokwasy i białka Reakcje charakterystyczne białek reakcja ksantoproteinowa
Aminokwasy i białka Reakcje charakterystyczne aminokwasów II
reakcje charakterystyczne cukrów, ochrona środowiska UJ, IV semestr, chemia ograniczna, sprawozdania
reakcje charakterystyczne
Reakcje charakterystyczne2
biochemia VI, Temat: Reakcje charakterystyczne sacharydów
Aminokwasy i białka Reakcje charakterystyczne aminokwasów
Estry produkty reakcji kwasów z alkoholami
więcej podobnych podstron