
1
Historia
promieniotwórczości
• 1895 r. - odkrycie promieniowania X
• 1896 r. - odkrycie promieniotwórczości
niektórych pierwiastków
• 1896 r.- opisanie zespołu popromiennego
• 1897 r.- pierwsze osłony przed promieniowaniem
• 1912 r.- śmiertelne skutki napromieniowania radem
• 1950 r. – próbne wstrzyknięcie strontu
• 1954 r. – powstanie Amerykańskiego
Towarzystwa Medycyny Nuklearnej
2
MEDYCYNA NUKLEARNA
• Zastosowanie izotopów promieniotwórczych w:
– diagnostyce
• in vivo,
– Możliwość zbadania morfologii i czynności narządów
– Rozmieszczenie podanych wewnętrznie izotopów określa się za
pomocą gamma-kamer
• in vitro (RIA)
– terapii (np. 131-jod, 89-stront, 153-samar, 32-fosfor)
– jest to samodzielna specjalizacja lekarska
• specjalizacja diagnostyczno – terapeutyczna
• szczególnie pomocna dla:
– endokrynologów, kardiologów, onkologów, neurologów

3
Zastosowanie izotopów
promieniotwórczych
w endokrynologii

4
Tarczyca
• Scyntygrafia tarczycy
– Z użyciem 99m-Tc (technet)
– Z użyciem 131-I (jod)
• jodochwytność
– Z użyciem MIBI – 99m-Tc

5
Scyntygrafia tarczycy
– Wykonuje się w celu zobrazowania czyli
oceny morfologicznej:
• wola zamostkowego,
• kontroli i ewentualnego odrostu po zabiegu
operacyjnym,
• zaburzeń rozwojowych tarczycy,
• wola guzowatego
• Nie wymaga wykonania scyntygrafii –
– wole miąższowe i proste

6
• Scyntygrafia Tc 99 m
– metabolizm technetu jest różny od jodowego
• ulega czynnemu wychwytowi przez komórki pęcherzykowe
(pompa jodowa)
• nie podlega innym przemianom
– bierze udział w nieorganicznej przemianie jodu nie ulegając
wbudowaniu w cząsteczkę tyrozyny.
– Zalety:
• dawka pochłonięta niższa niż przy scyntygrafii
jodowej
• metoda tania
– Wady:
• technet wychwytywany jest także przez m.in.
ślinianki (znacznik nieswoisty dla tarczycy)
– Sposób badania:
• odczytu radioaktywności dokonuje się:
– po 1 godz. od podania doustnego,
– 20-30 min od podania dożylnego

7
• Wole guzowate
– Scyntygrafia tarczycy może pomóc w rozróżnieniu
charakteru guzka:
• zimne - słabo gromadzące znacznik - np. torbiel, rak, krwiak,
ograniczone zmiany zapalne
• ciepłe - wysycone w podobnym stopniu znacznikiem jak pozostała
tkanka gruczołowa
• gorące - w obrazie scyntygraficznym widoczny jest tylko guzek
gorący; pozostały miąższ tarczycy może nie wychwytywać
radioznacznika
– z powodu hamowania wydzielania TSH poprzez wytwarzane w tym
guzku hormony tarczycy
• Uwaga:
– przy każdym podejrzeniu nowotworu tarczycy na
podstawie wyniku pojedynczego badania (badanie
kliniczne lub usg lub scyntygrafii) należy dążyć do
wykluczenia rozpoznania nowotworu za pomocą
wykonania następujących badań: scyntygrafii, usg i
biopsji cienkoigłowej.

8
Scyntygrafia 131-I
– Jod 131 bierze udział we wszystkich
przemianach jodu w tarczycy
– Konieczne wykonanie scyntygrafii jodowej w
podejrzeniu:
• wola zamostkowego,
• zaburzeniach rozwojowych tarczycy,
• lokalizacji przerzutów nowotworowych tarczycy
– Wada:
• przy scyntygrafii jodowej dawka pochłonięta
jest 60 razy wyższa niż przy scyntygrafii
technetowej
– Sposób badania:
» Po 24 godzinach od podania doustnego
9
Wskazania do wykonania
scyntygrafii tarczycy przy
podejrzeniu:
• wola
zamostkowego,
• zaburzeń
rozwojowych
tarczycy
• kontroli i
ewentualnego
odrostu po zabiegu
operacyjnym,
• wola guzowatego
•
wola zamostkowego,
wola zamostkowego,
•
zaburzeniach
zaburzeniach
rozwojowych
rozwojowych
tarczycy,
tarczycy,
•
lokalizacji
lokalizacji
przerzutów
przerzutów
nowotworowych
nowotworowych
tarczycy
tarczycy
konieczne użycie
konieczne użycie
131-I
131-I

10
• Uwaga:
– wykonanie scyntygrafii tarczycy z użyciem MIBI - Tc
99 m - pozwala na uwidocznienie
• gruczolaków
• wysoko zróżnicowanych raków tarczycy.
– wychwyt tego radiofarmaceutyku nie zależy od TSH
• można wykonywać u pacjentów stosujących lewotyroksynę
• Uwaga:
– substancje blokujące tarczycę - wpływają na wynik
badania scyntygraficznego
• Uwaga:
– W diagnostyce chorób tarczycy scyntygrafia i usg to
badania wzajemnie się uzupełniające

11
• Jodochwytność tarczycy
– ustalenie dawki 131-I przy planowanej terapii 131-I
nadczynności tarczycy
– polega na wyliczeniu frakcji 131-I wychwyconego przez
tarczycę w 6 i 24 godz. po doustnym podaniu dawki
diagnostycznej 4 MBq 131-I
– wynik podaje się w % uprzednio podanej aktywności izotopu
– średni zakres norm
• po 6 godz - 15-30%,
• po 24 godz - 40-55%.
• Na terenach gdzie istnieje niedobór jodu jodochwytność w populacji
jest zazwyczaj wyższa.
• Sposób wykonywania:
– kapsułkę diagnostyczną umieszcza się ok. 20 cm od sondy
– mierzy się jej radioaktywność przez 2 min.
– bezpośrednio po pomiarze chory połyka kapsułkę
– po 24 godz. (chętniej 6 i 24 godz.) mierzy się u pacjenta radioaktywność
w rzucie szyi w odległości 20 cm od sondy (gamma kamery) przez 2
minuty
12
Leki zaburzające
jodochwytność
Typ leku
mechanizm działania
wymagany czas odstawienia
Tyreostatyki
zaburzają procesy jodowania
3-7 dni
(propylotiouracyl, karbimazol)
w tarczycy
Preparaty tarczycy
blokowanie wychwytu
2 (trójjodotyronina) –
4 (tyroksyna) tygodnie
Leki wykrztuśne, witaminy
Wysoka zawartość jodu, 1- 2 tygodnie
blokada kompetycyjna
Leki zawierające jod
kompetycyjna blokada
1- 6 miesięcy
(np. amiodaron)
wychwytu jodu
Środki jodowe stosowane zewnętrznie
kompetycyjne hamowanie 1 – 2 tygodni
przez blokadę tarczycy
Środki kontrastowe
kompetycyjna blokada
Dożylne
wychwytu jodu
1 miesiąc
Doustne
3-4 miesiące
Olejowe – bronchorafia
6-12 miesięcy
Mielografia
2-10 lat
13
Leki zaburzające
jodochwytność
Typ leku
wymagany czas odstawienia
Fenylobutazon
1 – 2 tygodnie
Salicylany
1 tydzień
Steroidy
1 tydzień
Nitroprusydek sodu
1 tydzień
Beznodiazepiny
4 tygodnie
Inne leki:
Antykoagulanty
1 tydzień
Antyhistaminiki
1 tydzień
Leki przeciwrobacze
1 tydzień
Penicyliny
1 tydzień
Sulfonamidy
1 tydzień
Tolbutamid
1 tydzień
Tiopental
1 tydzień

14
• w organizmie człowieka jest 30-40 g jodu,
–
z tego 15-17 g w tarczycy
–
dobowe zapotrzebowanie na jod - 50-200 g
(1-4 mikrog/kg ciała)
–
spożycie < 10 g dziennie - zaburzenie funkcji tarczycy
• wchłaniany jest szybko w górnym odcinku
przewodu pokarmowego (90% w ciągu 60
minut)
• ze krwi jest transportowany do tarczycy
• w nerkach jest akumulowany
Biodystrybucja
15
Leczenie 131-I
łagodnych chorób tarczycy
• tyreotoksykoza,
hipertyreoza
skąpoobjawowa i
utajona
– choroba Gravesa
– wole wieloguzkowe
– ognisko autonomiczne
• eutyreoza
– wole rozlane
– wole wieloguzkowe
• bezwzględne
– ciąża
– okres karmienia piersią
• względne (już nie są to
przeciwwskazania)
– młody wiek
– duże wole
– orbitopatia
WSKAZANIA
WSKAZANIA
PRZECIWWSKAZANIA
PRZECIWWSKAZANIA

16
• Jod
–
Jedyny znany izotop trwały – A = 127
–
20 sztucznych izotopów
– od A =117-140
– Praktyczne znaczenie – I – 125, 131, 132
–
Sposób otrzymywania
• mieszanina produktów rozszczepienia
uranu i plutonu
– uzyskuje się poprzez napromienienie prętów uranowych w reaktorach
• akceleratory
•
125
- I
–
emituje promieniowanie gamma
•
131 -
I
– promieniowanie – fotony o energii 364 keV
– promieniowanie– elektrony o energii 606 keV
• wolne rodniki – uszkodzenie DNA - śmierć komórki albo utrata wzrostu i
podziału - obliteracja błony wewnętrznej naczyń krwionośnych –
atrofia
narządu
– fizyczny czas półtrwania 8,02 dnia
• W tarczycy – ok. 5-10 tygodni

17
Przygotowanie do leczenia
131-I
• Wywiad
– leczony uprzednio tyreostatykami ?
– obecna orbitopatia ?
• Badanie lekarskie
• Badania dodatkowe
– Badania hormonalne
– Usg
– Scyntygrafia z jodochwytnością

18
Leczenie nadczynności tarczycy
131-I
-
czy przygotować tyreostatykami ?
• ZA
-
możliwość
zaostrzenia
hipertyreozy po
131-I
• PRZECIW
– zmniejszenie skuteczności
131-I
– brak „przełomów”
– brak pogorszenia stanu
kardiologicznego
– odstawienie tyreostatyków
przyczyną wzrostu
poziomu HT
we krwi
Włączenie tyreostatyków przed .... czy ... po podaniu I 131
- I-131 –
96% wyleczeń
- włączenie
do 5-
7 dni
po podaniu 131- - I-131 + M –
83 %
I
Metizolu zmniejsza skuteczność
- I-131 + PP – 77%
- I-131 + C – 49%
- lit w przypadku bardzo
dużego wola,
- beta blokery

19
- Progresja
- po podaniu 131-I
15 - 35 %
- w trakcie leczenia tyreostatykami
10 - 15 %
- po tyreoidektomii subtotalnej
11 - 16 %
- po tyreoidektomii totalnej
0 - 6 %
pacjentów
UWAGA –
- SN, wysokie ATPO, niski TRAK + podanie 131- I –
oftalmopatia !!
Leczenie nadczynności tarczycy 131-I
- orbitopatia w przebiegu choroby Gravesa
• czas leczenia
– rozpoczęcie 0 - 21 dni po 131-I
– zakończenie ?
• dawka: 0,4 - 0,5 mg / kg mc
Glikokortykoidy
20
-
wielkość dawki zależy od przepisów obowiązujących w danym Państwie
do 185 MBq (5 mCi) Holandia, Austria, Szwajcaria
do 370 MBq (10 mCi) Anglia
do 1110 MBq (30 mCi) USA
• dawki stałe
– 111-185 MBq (3 - 5 mCi)
dawka pochłonięta
• dawka pochłonięta - modyfikacja
M Bq =
K x V x 25
T
eff
x U
24
K – w zależności od
rozpoznania:
- ch. Gravesa – 80 - 150
mikroCi/g
- wole wieloguzkowe – 100-150
mikroC/g
- ognisko – 150 mikroCi/g
mCi =
V x K
U
24
Obliczanie dawki 131-I
K - w zależności od
rozpoznania:
- ch. Gravesa kobiety – 20
- ch. Gravesa mężczyźni – 30
- wole wieloguzkowe – 10
- ognisko – 10
V – objętość
V – objętość
U
U
24
24
– jodochwytność po 24 godz
– jodochwytność po 24 godz

21
Wyższe dawki stosujemy:
• U dzieci
• U mężczyzn
• Przy drugiej (kolejnej) dawce
• Po przygotowywaniu pacjenta
tyreostatykami

22
Skuteczność leczenia
• ZALEŻY OD DAWKI POCHŁONIĘTEJ
– masa tarczycy
– jodochwytność
– obrót jodu w tarczycy
– promienioczułość
•
ZALEŻY OD DOSTĘPNOŚCI 131-I

23
niska jodochwytność
• bo niska aktywność TSH zależnego
symportera sodowo-jodowego (NIS)
– w badaniach immunohistochemicznych
wykazano, że zawartość NIS jest
• MGBasedow >prawidłowa tarczyca>= wole
guzowate
– aktywność NIS
• (+) TSH
• (-) zwiększona podaż jodu
» Fiddes 1979, Saito 1997

24
Rekombinowany ludzki TSH
• Hodowla ludzkich komórek
embrionalnych
• Komórki jajnika chomika chińskiego

25
Potencjalne zastosowanie rh
TSH
•
Zatwierdzone
Zatwierdzone
– w raku zróżnicowanym tarczycy
• Scyntygrafia całego ciała 131-I
•
Stymulacja tyreoglobuliny
Stymulacja tyreoglobuliny
•
Niezatwierdzone
Niezatwierdzone
– Diagnostyka wrodzonej niedoczynności tarczycy
– Rozpoznanie zróżnicowanego raka tarczycy
• Diagnostyka PET
– Leczenie zróżnicowanego raka tarczycy
• Ablacja pooperacyjnych resztek tarczycy
• Leczenie uzupełniające do chemioterapii w zaawansowanym
słabozróznicowanym raku tarczycy
– Leczenie wola obojętnego tarczycy
» Woodmansee 2004

26
Zastosowanie rh TSH
(w łagodnych chorobach tarczycy)
• Badania trwają od kilku lat
•
Zwiększa niską jodochwytność
Zwiększa niską jodochwytność
– Blokada farmakologiczna
•
Zmienia dystrybucję radiojodu w tarczycy
Zmienia dystrybucję radiojodu w tarczycy
– Zwiększając ją w w miejscach słabego gromadzenia
» Nieuwlaat 2001
• W efekcie
powoduje większy odsetek wyzdrowień
powoduje większy odsetek wyzdrowień
– Niższa podana aktywność 131-I
– Wyższa dawka pochłonięta = Większa redukcja wola
– Większy odsetek niedoczynności = rzadziej kolejna dawka 131-I
• Brak rejestracji do ww działań
27
0
2
4
6
8
10
12
14
16
18
0
5-8 godz
0
0,5
1
1,5
2
2,5
3
3,5
0
5-96 godz
0
5
10
15
20
25
30
35
0
8-96 godz
TSH (mU/l)
TSH (mU/l)
T3 (pmol/l)
T3 (pmol/l)
fT4 (pmol/l)
fT4 (pmol/l)
0,01 mg rh
TSH (Huysmans 2000)
0,03 mg rh
TSH (Huysmans 2000)
0,01 mg
0,03 mg
0,01 mg
0,03 mg
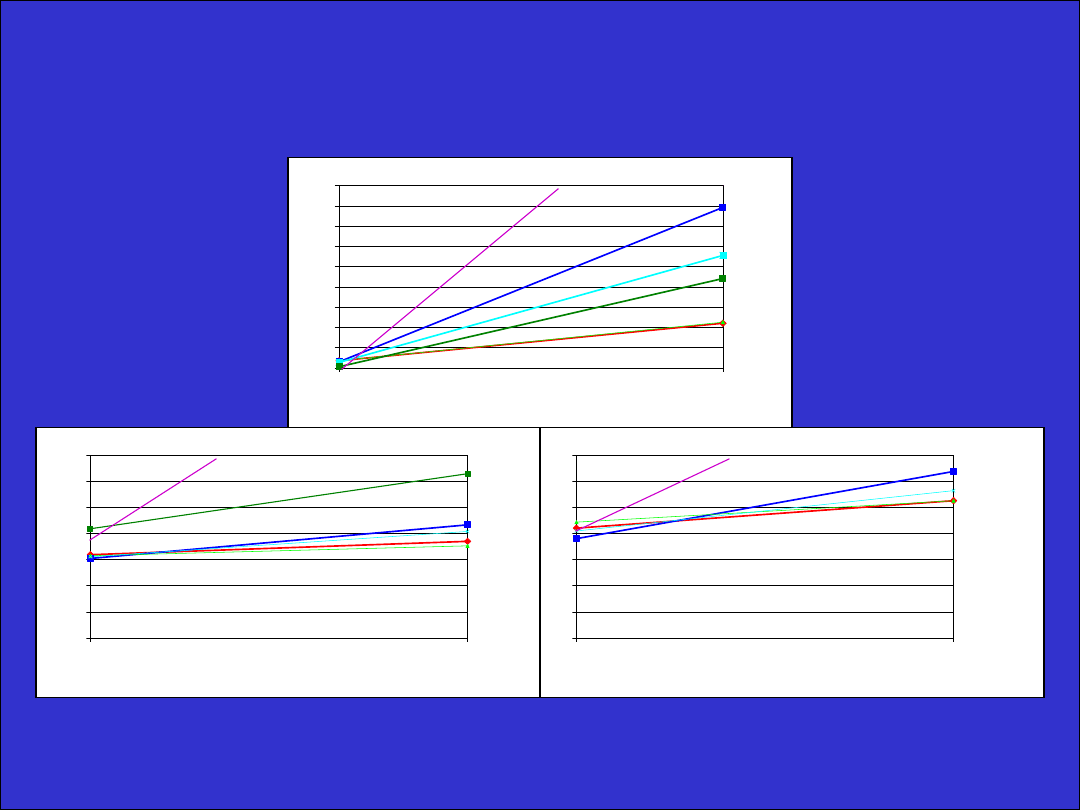
Wpływ na stężenie TSH, fT4, fT3
Wpływ na stężenie TSH, fT4, fT3
0,03 mg rh
TSH (Nieuwlaat 2003)
0,01 mg rh
TSH (Nieuwlaat 2003)
0,05 mg rh
TSH (Gietka-Czernel 2004)
0,05 mg rh TSH (Gietka-Czernel 2004)
0,05 mg rh TSH (Gietka-Czernel 2004)
(45,9) 0,45 mg rhTSH, (Silva 2004)
(45,9) 0,45 mg rhTSH, (Silva 2004)
(49,1) 0,45 mg rh TSH (Silva 2004)
(49,1) 0,45 mg rh TSH (Silva 2004)
(6,3) 0,45 mg rh TSH (Silva 2004)
(6,3) 0,45 mg rh TSH (Silva 2004)
28
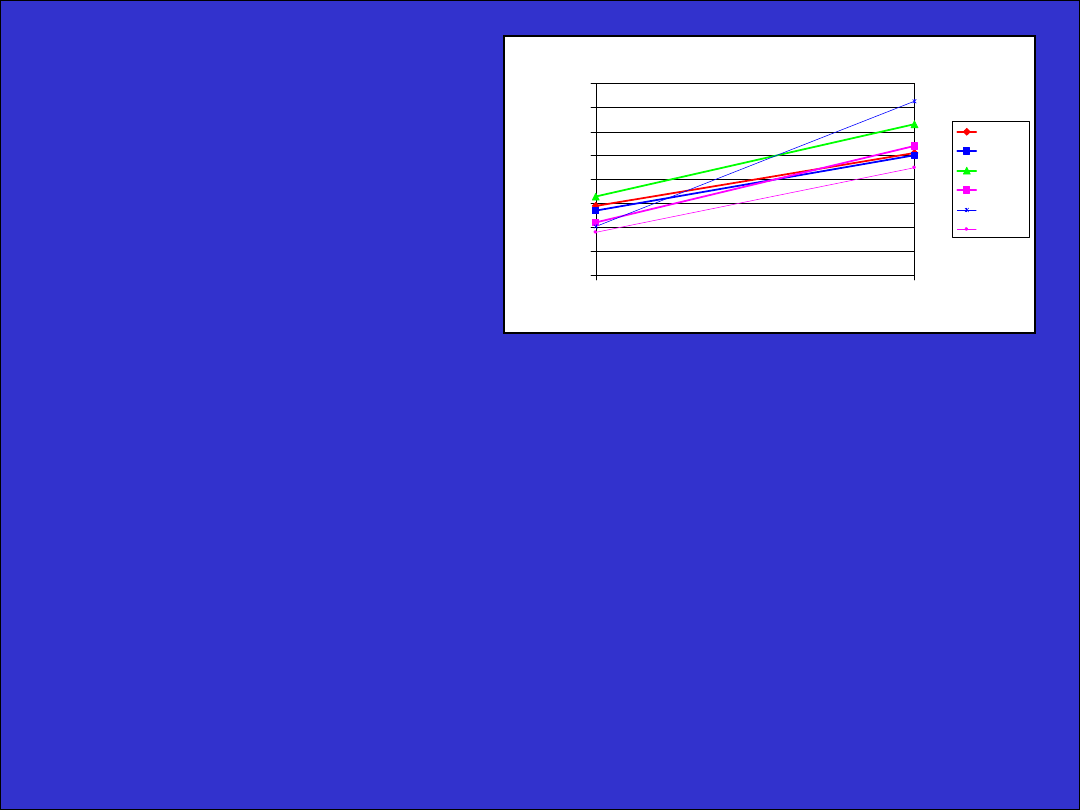
Wpływ
na jodochwytność
•
0,01 mg rh TSH
0,01 mg rh TSH
– z 29 do 51 % (po 24 godz) - Huysmans 2000
– z 27 do 50 % (po 24 godz) – Nieuwlaat 2003
•
0,03 mg rh TSH
0,03 mg rh TSH
– z 33 do 63 % (po 24 godz) - Huysmans 2000
– z 22 do 54% (po 24 godz) – Nieuwlaat 2003
•
0,05 mg rh TSH
0,05 mg rh TSH
– z 20,4 do 72,58 (po 24 godz) – Gietka Czernel 2004
•
0,45 mg rh TSH
0,45 mg rh TSH
– z 18 do 45% (po 24 godz) – Silva 2004
Czyli zwiększenie 1,7–1,8 ; 1,9- 2,4 do 3,6 krotnie
Czyli zwiększenie 1,7–1,8 ; 1,9- 2,4 do 3,6 krotnie
0
10
20
30
40
50
60
70
80
przed
po rhTSH
0,01 mg
0,01 mg
0,03 mg
0,03 mg
0,05 mg
0,45 mg
%
29
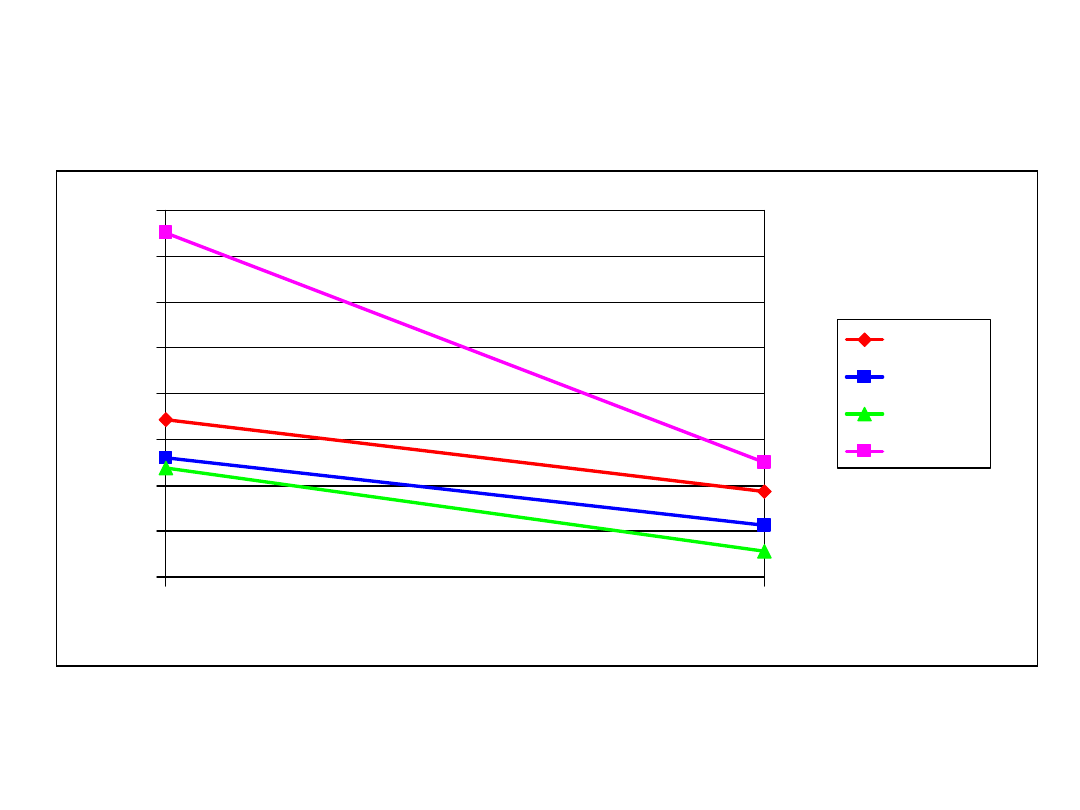
0
20
40
60
80
100
120
140
160
przed
po rhTSH
0,01 mg
0,03 mg
0,05 mg
0,45 mg
Nieuwlaat 2003, Silva 2004,
Gietka - Czernel 2004
mCi
Wpływ na redukcję dawki podanej
Wpływ na redukcję dawki podanej

30
Wskazania dla pacjenta przed i po
podaniu 131-I
• wykluczyć ciążę !
– po podaniu 131-I
• nie zachodzić w ciążę 3 - 6 miesięcy,
• mężczyźni nie starać się o potomstwo do 4 miesięcy
– karmienie piersią:
– Tc 99m – 12 godz.
– 123 - I – 2 dni
– 131-I – 3 tygodnie
• przed - 4 godziny na czczo,
po - 2 godziny nic nie jeść i nie pić

31
Wskazania dla pacjenta przed i po
podaniu 131-I
• unikać bliskich kontaktów
– nie karmić piersią
– troszczyć się o higienę osobistą (pot)
– pić duże ilości płynów
– nie przygotowywać samodzielnie
posiłków
– uwaga
• pamiętać o zaświadczeniu lekarskim przy
przekraczaniu granic Państwa

32
Monitorowanie pacjenta po
podaniu 131-I
• Wizyty u lekarza
– po 3 - 4 tygodniach, następne wg zaleceń
endokrynologa
• Badania
– po 3 - 4 tygodniach ocena czynności tarczycy
– po 3 - 4 miesiącach usg tarczycy
• Leczenie farmakologiczne
– tyreostatyki i LT 4 - zależnie od stanu pacjenta i funkcji
tarczycy (unikać bezpośrednio po podaniu 131-I
)
• Ewentualna następna dawka 131-I
– po około 6 miesiącach

33
NASTĘPSTWA LECZENIA 131-I
• WCZESNE
– podwyższenie stężenia HT
– przełom tarczycowy ?
– popromienne zapalenie tarczycy
– wymioty, nudności, jadłowstręt
• PÓŹNE
– nasilenie orbitopatii
– zapalenie ślinianek
– niedoczynność tarczycy
• NIEDOCZYNNOŚĆ TARCZYCY JEST
OCZEKIWANYM NASTĘPSTWEM
LECZENIA 131-I

34
Niedoczynność tarczycy po leczeniu
131-I
• wczesna
• późna
• KUMULUJE SIĘ
– po roku od podania 131-I
• hipotyreoza - 7 - 47,4 %
• wzrost od 2 - 5 roku o 4,8 %
• wzrost od 6 roku o 1 %
» Clarke 1991, Aizawa 1997,
Tarintharan 1997

35
KANCERO - i TERATOGENNOŚĆ
131-I
• brak wpływu na częstość występowania raków
tarczycy
– po 131-I - 0,15% (jak w całej populacji)
» Angusti 2000
• białaczki -
– bardzo rzadko, częściej po podaniu 131-I w
leczeniu raka tarczycy (800mCi - 1Ci)
» Laurenti 1998
• brak dowodów na zwiększenie częstości
występowania wad płodu
• zwiększona śmiertelność po podaniu 131-I (RR –
1,47) związana jest z objawami wcześniej trwającej
nadczynności, a nie bezpośrednio z leczeniem 131-I

36
WADY I ZALETY
• stosunkowo późno
stabilna eutyreoza
• zwiększenie
częstości
orbitopatii
• skuteczny i
bezpieczny
• komfort leczenia
• dobry efekt
• rzadkie nawroty
• niski koszt 131-I
• możliwość leczenia
chorych w złym
stanie ogólnym

37
Rak tarczycy
- scyntygrafia całego ciała
(przerzuty)
- leczenie 131-I
• Nie:
– anaplastyczny, rdzeniasty, chłoniak, mięsak
• Tak:
– pęcherzykowaty i brodawkowaty
(przerzuty)
• Kiedy:
– Po operacji
• Dawka:
– 60-150-300mCi
• Scyntygrafia tarczycy – 50 microCi

38
PRZYTARCZYCE
– wykrywanie obecności gruczolaka przytarczyc
– znacznik - MIBI - Tc 99m
• kompleks ten wymywany jest z gruczolaków przytarczyc
wolniej niż z dobrze unaczynionej tarczycy.
– Sposób badania:
• Po podaniu iv MIBI TC 99m i akwizycji po 15min. i 3
godzinach , nie zmieniając pozycji chorego podaje się
Tc 99 i po 20 minutach rejestruje się obraz.
• Po 15 min. widoczna jest tarczyca i ew. słabo widoczne są
gruczolaki przytarczyc, po 3 godz. - ukazują się one jako
wyraźne ogniska silniejszego gromadzenia znacznika. Dla
ułatwienia uwidocznienia patologicznie zmienionych
przytarczyc wykonuje się scyntygrafię subtrakcyjną tj
porównanie wysycenia poszczególnych regionów obrazów
zarejestrowanych po podaniu Tc 99m i 99 m Tc - MIBI.

39
• Uwaga:
– należy pamiętać o takim dobraniu pola widzenia aby widoczna
była nie tylko okolica tarczycy lecz również śródpiersia (częsta
ektopowa lokalizacja dla przytarczyc).
– projekcje nie tylko przednie i ukośne lecz także SPECT
• Pierwotna nadczynność przytarczyc:
– Czułość scyntygrafii - 75-100%.
• W porównaniu z usg: czułość - 93% vs 68%, swoistość - 93% vs 68%.
– Rzadko wyniki fałszywie dodatnie - swoistość badania 95%.
Na 5% składają się:
• gruczolaki tarczycy
• raki sutka
• raki płuc
• raki wywodzące się z tkanek głowy i szyi
– Uwidocznienie się gruczolaka zależy od:
• rozmiarów
• ilorazu wychwytu radioznacznika w obrębie gruczolaka do
wychwytu w tkankach otaczających
• umiejscowienia (trudniej gdy zlokalizowane są w tylnej części
śródpiersia lub gdy są przesłonięte przez kości bądź naczynia

40
– Uwaga:
• Dla diagnostyki zawsze powinny być wykonane dwa badania
wizualizacyjne w tym na pewno scyntygrafia i usg (o wysokiej
rozdzielczości) lub MRI (gdy istnieje podejrzenie gruczolaków w
śródpiersiu)
– Wtórna nadczynność przytarczyc:
• Wykonywanie scyntygrafii przytarczycy może być niemiarodajne,
czułość zarówno dla usg jak i dla scyntygrafii 50%.
– Uwaga:
• W związku z tym, że wyszkolony chirurg podczas operacji potrafi
ustalić położenie zmienionych patologicznie gruczołów (gruczolak
czy rozrost) dąży się do tego, żeby metody wizualizacyjne
wykonywać u chorych, którzy mają być poddani reoperacji z
powodu nawrotu lub utrzymywania się nadczynności przytarczyc
pomimo przeprowadzonego leczenia chirurgicznego lub u chorych
w złym stanie ogólnym. Wykonywanie badań wizualizacyjnych
przed pierwszą operacją jest wciąż przyjęte i wykonuje się je
z powodu:
– skrócenia czasu operacji
– zmniejszenia rozległości zabiegu
– zmniejszenia prawdopodobieństwa reoperacji

41
RDZEŃ NADNERCZY
• Scyntygrafia rdzenia nadnerczy - MIBG - 131 I lub
123 I
– metajodobenzylguanidyna –
» fizjologiczny analog noradrenaliny i guanetydyny,
» gromadzi się w pęcherzykach chromofilnych,
» nie jest metabolizowany przez MAO czy COMT
» mechanizm gromadzenia - dyfuzja do wnętrza komórki
(bierny) oraz pompa sodowa (aktywny)
» może być blokowana przez m.in. pochodne rezerpiny i
trójcykliczne leki antydepresyjne (konieczne odstawienie
leków)
» prawidłowo MIBG może gromadzić się w wątrobie i
śledzionie (szczyt po 24 godz.), nerkach (po 24 godz.
radioaktywność znad nerek jest śladowa), śliniankach,
sercu, jelitach
• Sposób badania:
– Obrazuje się po 24 i 48 godz. od podania i.v.

42
OBRAZOWANIE Z UŻYCIEM MIBG –
meta-jodobenzylguanidyna
• obrazowanie m.in. guzów pochodzenia
neuroektodermalnego:
– Pheochromocytoma
– Rak rdzeniasty tarczycy
– Karcinoidy
– Neuroblastoma
– Paraganglioma
– Gangliocytoma
• oraz przerzuty tych guzów wychwytujące MIBG
– Hiperplazja rdzenia nadnerczy

43
MIBG jest wychwytywany fizjologicznie
również przez:
– wątrobę,
– śledzionę
– mięsień sercowy (szczególnie wysoki wychwyt u
dzieci <1 roku życia)
– ślinianki
– prawidłowe nadnercza
• A także:
– mięśnie szkieletowe
– śluzówkę nosa
– płuca
– układ moczowy
– jelita
– pęcherz moczowy
– tarczycę
– Wychwyt ten odzwierciedla bogate unerwienie adrenergiczne
lub/i wydzielanie katecholamin

44
• Brak wychwytu MIBG
– Kościec
• Kończyny na scyntygrafii powinny wykazywać niewielką
aktywność związaną z mięśniami, kości winny być widoczne jako
obszary fotopeniczne
• Wychwyt MIBG w tkankach miękkich:
– Guzy pierwotne
– Przerzuty:
• Węzły chłonne
• Wątroba
• Kości
• Szpik kostny
• Intensywność wychwytu podobna w przypadku
łagodnych i złośliwych guzów (także dojrzałość
guzów nie ma znaczenia)
• Zwiększenie wychwytu w kościach może być
związane z przerzutami w kości lub/i infiltracji
szpiku

45
Wyniki fałszywie ujemne
– guzy leżące blisko tkanek miękkich
fizjologicznie gromadzących MIBG
– brak wychwytu albo niski wychwyt w guzie
z wysoką heterogenicznością, martwicą,
– mała objętość guza,
– brak wychwytu z powodu stosowania leków

46
Leczenie 131 – I
meta-
jodobenzylguanidyną
• Wskazania:
– Guzy wychwytujące 131-I MIBG
• Nieoperacyjne lub złośliwe przypadki
– Pheochromocytoma
– Rakowiaki
– Rak rdzeniasty tarczycy
– Paraganglioma
– III lub IV stopień neuroblastoma

47
Przeciwwskazania do
terapii
• Bezwzględne
– Ciąża
– Karmienie piersią
– Przewidywany okres przeżycia < 1 m-c
– Mielosupresja:
• Hb < 9 g%
• Leukocytoza < 4 tys.
• Płytki < 100 tys.
– Szybko postępujące upośledzenie funkcji nerek < 30 ml/min
• Względne
– Ryzyko medyczne wynikające z izolacji po podaniu
radiofarmaceutyku
– Nietrzymanie moczu

48
Przygotowanie pacjenta
• Potwierdzenie
obecności
nieoperacyjnego guza neuroendokrynnego
poprzez wykazanie go w scyntygrafii z
131-I MIBG, TK lub MRI oraz przy użyciu
badań biochemicznych
• Odstawienie
przed planowanym
leczeniem na ok. 1-2 tygodnie leków
konkurujących w wychwycie lub
gromadzeniu 131-I MIBG

49
• Leki konkurujące
– Labetalol
– Rezerpina
– Blokery kanału
wapniowego
• werapamil
– Trójcykliczne
antydepresyjne
• Amitryptylina
• Imipramina
– Sympatykomimetyk
i
• Efedryna
– Kokaina
• Leki konkurujące
(potencjalnie)
– Blokery
adrenergiczne
• Bretylium
• Guanetydyna
– Sympatykomimetyki
• Amfetamina
• Dopamina
• Izoprenalina
• terbutalina
– Fenotiazyny
• Chlorpromazyna
• Prometazyna
– Butyrofenony
• Droperidol
• haloperidol
– Tioxantyny

50
Leczenie 131-I MIBG
• Podanie dożylne
• Wskazane podanie profilaktyczne leków
przeciwwymiotnych
(w dniu podania oraz
do 72 godz. po leczeniu)
• Dawka podana –
100-300 mCi
– Niższa –
• u pacjentów z upośledzoną funkcją nerek
• z mielosupresją
• Następna dawka 131-I MIBG w zależności
od ilości płytek krwi
– U dzieci - nie wcześniej niż po 4 tygodniach
– U dorosłych – nie wcześniej niż po 6 tygodniach

51
Po leczeniu
• Bezpośrednio po podaniu –
pić
duże ilości
płynów
• Do
3-4 dni
po zabiegu powinno się
utrzymywać cewnik u pacjentów z
nietrzymaniem moczu i możliwie często
opróżniać zbiornik
• Do
5 dni
po leczeniu możliwe wydalanie
radiofarmaceutyku z moczem
• Przez
4 –6 miesięcy
po podaniu leku– nie
zachodzić w ciążę

52
Objawy uboczne
• Wczesne:
–
Okresowe
nudności i wymioty
mogą się pojawić
podczas pierwszych 2 dni po leczeniu
–
Przejściowa
mielosupresja
pojawia się 4-6 tygodni po
leczeniu
• Częściej występują u dzieci z neuroblastomą po chemioterapii
jako izolowana trombocytopenia
–
Upośledzenie funkcji nerek
(szczególnie u
pacjentów wcześniej leczonych cisplatyną lub
fosfamidem)
–
Rzadko u pacjentów dorosłych z pheochromocytomą
lub paragangliomą, a u dzieci z neuroblastomą pojawia
się
kryza nadciśnieniowa
wywołana przez wyrzut
katecholamin wymagająca leczenia alfa-blokerami
–
U pacjentów z rakowiakiem mogą pojawić się
uderzenia gorąca
(wyrzut serotoniny)

53
Objawy uboczne
• Późne:
– Niedoczynność tarczycy
(po
niewystarczającej blokadzie tarczycy)
– Trwała
trombocytopenia,
mielosupresja
– Białaczki
(do tej pory nigdy nie
zaobserwowano lecz nie można
wykluczyć)

54
Po leczeniu dziecka
• Po leczeniu dziecka dorosły pozostaje z nim w
izolacji. Powinien zachować odstęp tak daleki
jak to tylko możliwe, unikać spożywania
pokarmów i picia płynów w pokoju
• Ewentualne narażenie na zewnętrzne
promieniowanie winno być monitorowane
stale przez indywidualną dozymetrię a
wewnętrzne poprzez pomiary próbki moczu w
liczniku gamma

55
KORA NADNERCZY
• Uwaga:
– badania kory nadnerczy wykonywane są
obecnie rzadko z powodu:
– wykorzystania dokładniejszych metod
wizualizacyjnych (TK, MRI)
– wysokiego narażenia pacjenta na promieniowanie
– Wskazania
• zespół Cushinga i pierwotny
hiperaldosteronizm
• Scyntygrafia z użyciem pochodnych cholesterolu
znakowanych 131 I
– jodo - metyl – norcholesterol
– Uwaga: fizjologicznie związki te wychwytywane są
przez wątrobę i nadnercza

56
• Zespół Cushinga:
– Sposób badania
• Obrazuje się
po 7 dniach od podania iv
(wcześniej
może być obecna aktywność znad wątroby)
• Objawy scyntygraficzne:
– jednostronne uwidocznienie się nadnercza lub
asymetria:
» gruczolak
» rak wysoko zróżnicowany
» przerzut do nadnercza
» stan po operacyjnym usunięciu nadnercza
– obustronne gromadzenie
» obustronny przerost kory
– brak gromadzenia radiofarmacutyku
» rak nandercza
» leczenie kortykosteroidami
» hiperlipidemia

57
Hiperaldosteronizm
pierwotny:
• Sposób badania:
– Badanie wykonuje się po zahamowaniu wychwytu
radioznacznika przez prawidłową tkankę
nadnerczy (
deksametazon 3 razy dziennie 2 mg 2
dni przed i 7 dni po podaniu radioznacznika
).
Akwizycje przeprowadza się do
5 dnia
po iniekcji
i.v. radioznacznika.
– uwidocznienie się nadnerczy do 5 dnia
• obustronne - hiperplazja idiopatyczna
• jednostronne - gruczolak
– uwidocznienie się nadnerczy powyżej 5 dnia
• gruczolakowaty przerost warstwy kłębkowatej kory
nadnerczy

58
Guzy neuroendokrynne
przewodu pokarmowego
• Nowotwory rzadkie, wolno rosnące
• Średnica < 1 cm
• Zazwyczaj złośliwe
• Przerzuty wcześniej niż objawy kliniczne
– wątroba, węzły chłonne
• Nieme klinicznie przez lata
• Brak charakterystycznych objawów
• Diagnostyka wymaga skomplikowanych
metod laboratoryjnych i obrazowania

59
Guzy neuroendokrynne
przewodu pokarmowego
• Rodzaj guza
• Rakowiak
• Insulinoma
• Gastrinoma
• VIP-oma
• Glukagonoma
• Somatostatinoma
• Guzy nieczynnie
hormonalnie
częstość (%)
złośliwość (%)
50
90
15
10
5
55
1
80
2
80
1
50
30
70

60
• Diagnostyka
– Scyntygrafia z użyciem 131-I – MIBG
– Scyntygrafia z użyciem ligandów
receptora somatostatynowego
• Za wyjątkiem insulinoma (brak wystarczającej
ekspresji receptora dla SST)
• 111 In – DTPA – Octreotyd
• 99 m Tc – HYNIC – Tektreotyd
• 111 In – DOTA – Lanreotyd
• 99 m Tc – Depreotyd
• Leczenie izotopowe
– 90 Y – DOTA – Lanreotyd
– 177 Lu – DOTA Lanreotyd

61
Blokowanie tarczycy przy
wykonywaniu innych
badań
– 131- I fizjologicznie gromadzi się w tarczycy
podczas badań tarczycy
– ale również podczas wykonywania scyntygrafii
innych narządów z użyciem 131-I
• Blokowanie tarczycy ma na celu:
– uzyskanie wyższej jakości wyników badań,
– uzyskanie rzetelnej informacji o czynności danego
narządu
– ochronę przed napromieniowaniem narządów nie
podlegających badaniu
– blokowanie tarczycy należy bezwzględnie
wykonać zawsze przed planowaną diagnostyką i
leczeniem z użyciem 131-I
62
Blokowanie tarczycy przy
wykonywaniu innych
badań
• płyn Lugola
– stosowany od dawna,
tani
– p.o.
– 1 kropla = 7-8 mg jodu,
• dzień przed badaniem
3x3 krople,
• w dniu badania - 3
krople przed aplikacją
blokowanie utrzymuje się
> 72 godziny.
• nadchloran
potasowy
• nowość, nieco droższy
• p.o.
• krople, 6 mg/kg masy ciała
– 30-40 minut przed
aplikacją
blokowanie utrzymuje się
< 72 godziny

63
Blokowanie tarczycy przy
leczeniu MIBG - 131-I
• Dorośli:
– 24 godz. przed planowaną terapią
– 10 dni po terapii
• Dzieci
– dzień przed, w dniu terapii i dzień po:
– Noworodki 16 mg KJ dziennie
– Od 1m-ca - 3 lat
32 mg KJ dziennie
– Od 3-13 lat 56 mg KJ dziennie
– > 13 lat
130 mg KJ dziennie
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
- Slide 34
- Slide 35
- Slide 36
- Slide 37
- Slide 38
- Slide 39
- Slide 40
- Slide 41
- Slide 42
- Slide 43
- Slide 44
- Slide 45
- Slide 46
- Slide 47
- Slide 48
- Slide 49
- Slide 50
- Slide 51
- Slide 52
- Slide 53
- Slide 54
- Slide 55
- Slide 56
- Slide 57
- Slide 58
- Slide 59
- Slide 60
- Slide 61
- Slide 62
- Slide 63
Wyszukiwarka
Podobne podstrony:
zastosowanie izotopow w endokrynologii
Najważniejsze zastosowania izotopów promieniotwórczych w medycynie
ćw 3 zastosowanie izotopów
ćw 1 zastosowanie izotopów
Zastosowanie izotopów w medycynie, DOZYMETRIA
Zastosowanie izotopów promieniotwórczych, Fizyka jądrowa
ZASTOSOWANIE IZOTOPÓW PROMIENIOTWÓRCZYCH 2, Fizyka
Zastosowanie izotopów promieniotwórczych
chemia - zastosowanie izotopów, Sprawdziany kl 1 gim, Chemia
Zastosowanie izotopów promieniotwórczych
Zastosowanie izotopów promieniotwórczych 2
Lokalizacja wezła wartownika przy zastosowaniu technik izotopowych w czerniaku skóry
Izotopy i ich zastosowanie
9 Zastosowanie norm żywienia i wyżywienia w pracy dietetyka
Zmiany endokrynne narządo we
Zastosowanie SEM
Metodologia SPSS Zastosowanie komputerów Golański Standaryzacja
więcej podobnych podstron