Ilości substancji
Masa atomowa - określa, ile razy masa danego atomu jest większa od 1/12 masy izotopu węgla 12C (jednostka masy atomowej - u)
![]()
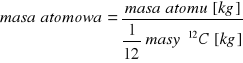
Masa cząsteczkowa - jest suma mas atomów wchodzących w jej skład z uwzględnieniem liczby tych atomów w cząsteczce
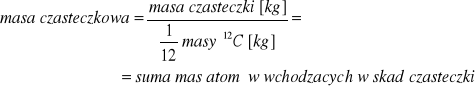
Masę cząsteczkową związku o wzorze AaBbCc obiczyć można znając masy atomowe poszczególnych pierwiastków A, B, C.
![]()
Mol - określa liczbę drobin (atomów, cząsteczek, jonów, wolnych rodników itd.) równą liczbie atomów zawartych w 0,012 kg czystego izotopu 12C. W 0,012 kg 12C znajduje się
![]()
![]()
- liczba Avogadra
Mol jest zatem jednostką ilości materii. Masa jednego mola drobin (atomów, cząsteczek, jonów, wolnych rodników itd.) nosi nazwę masy molowej (g/mol)
Wyszukiwarka
Podobne podstrony:
Mechanika techniczna(12)
Mechanika Semest I pytania egz
wykl 8 Mechanizmy
mechanizm mycia i prania
MECHANIKA II DYN
METODY KOMPUTEROWE W MECHANICE 2
08 BIOCHEMIA mechanizmy adaptac mikroor ANG 2id 7389 ppt
Mechanizm obrzęków
Mechanizmy swoistej immunoterapii alergii 3
mechanika kwantowa
Mechanizmy nadwrażliwości
Mechanika górotworu cz 3
Szkol Uszkodzenie ciała przez czynniki mechaniczne
więcej podobnych podstron