Piotr Jankowiak gr. C 14. 05. 2000 r.
WM sem. IV ( mgr )
Ćwiczenie nr 18.
Temat: Pomiar ciepła właściwego cieczy w stałym ciśnieniu metodą elektryczną.
Ciepło właściwe c (J/kgK) jest to liczbowo ilość ciepła Q pobierana lub oddawana przez jednostkę masy m danej substancji przy zmianie temperatury Δt o jeden stopień Kelwina lub Celcjusza (ściślej
). Zależne jest ono od rodzaju substancji, stanu skupienia, temperatury, ciśnienia, a także od sposobu ogrzewania. Rozróżnia się ciepło właściwe cV w stałej objętości oraz ciepło właściwe cP pod stałym ciśnieniem. Konieczne jest to w przypadku gazów, ponieważ cP - cV = R, gdzie R odpowiada stałej gazowej w równaniu stanu. Wartość tych wielkości zależy od rodzaju gazu, ściślej z ilu składa się atomów (czyli, ile posiada stopni swobody). Przyjęto, że:
dla gazu jednoatomowego (liczba stopni swobody n=3)
cV = 3/2R
cP = 5/2R
dla gazu dwuatomowego (liczba stopni swobody n=5)
cV = 5/2R
cP = 7/2R
dla gazu wieloatomowego (liczba stopni swobody n=6)
cV = 3R
cP = 4R.
Ciepło właściwe gazu przy stałej ciśnieniu jest większe niż przy stałej objętości o różnicę równą pracy jaką wykonuje gaz zmieniając swą objętość przy ogrzewaniu go pod stałym ciśnieniem.
Przedmiotem kalorymetrii jest badanie ciepła właściwego i ciepła przemiany, przedmiotem służącym do powyższego celu jest kalorymetr.
Kalorymetr ten zwany kalorymetrem wodnym składa się z dwu cylindrycznych naczyń metalowych umieszczonych jedno w drugim. Naczynie wewnętrzne spoczywające na korkach lub innych izolatorach termicznych ze względu na swe dobre przewodnictwo cieplne bierze udział w wymianie ciepła w całej swej masie.
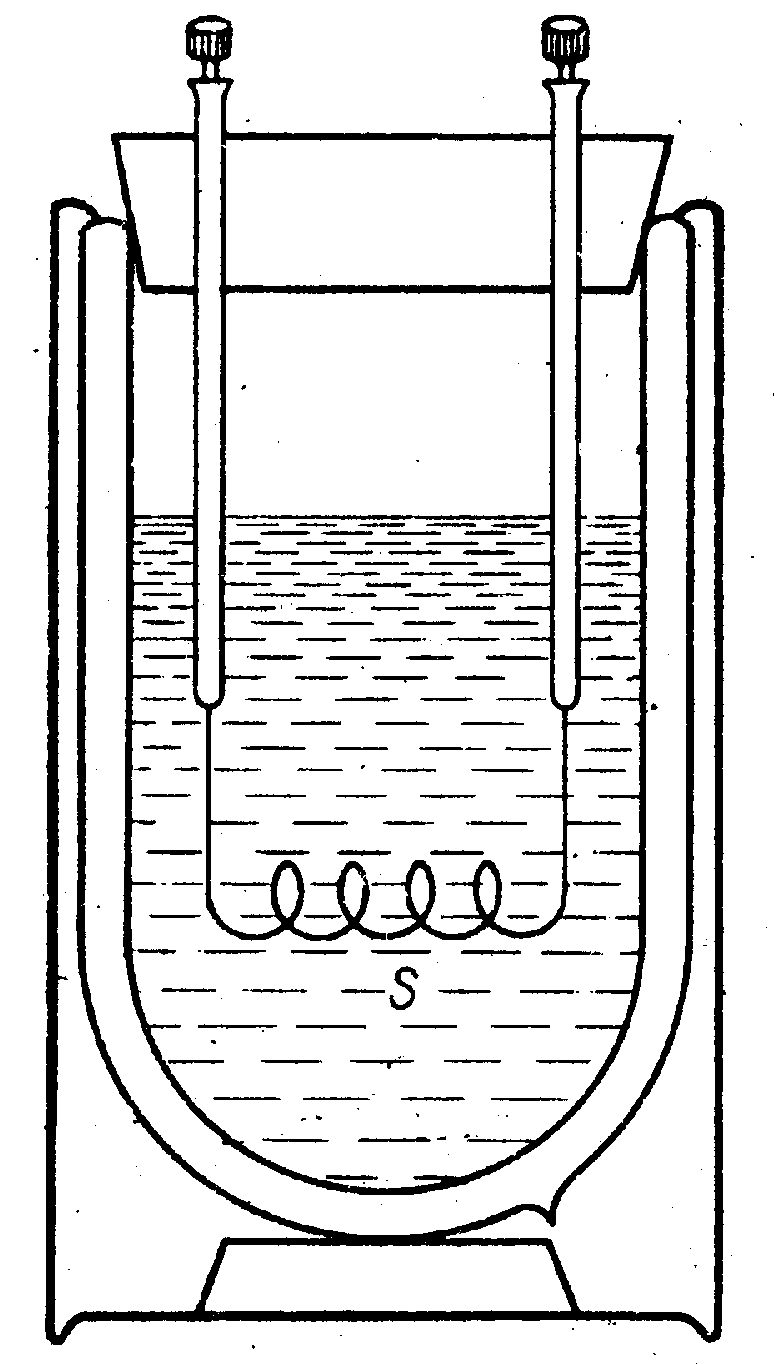
Rys. kalorymetru do pomiaru ciepła Joule'a.
Zasada działania elektrokalorymetru opiera się na zasadzie procesu zmiany pracy prądu elektrycznego na energię wewnętrzną zgodnie z prawem Joule'a. Prosty kalorymetr elektryczny otrzymuje się z kalorymetru o ściankach metalowych do, którego wprowadza się spiralę grzejną z drutu oporowego (konstantanu). Wzór na ciepło Joule'a wytworzone podczas przepływu prądu elektrycznego ma postać:
Jeżeli spirala grzejna zanurzona jest w badanej cieczy to ciepło Joule'a przekazane zostaje tej cieczy oraz naczyniu kalorymetru o pojemności cieplnej W. Zaobserwujemy wzrost temperatury od początkowej t1 do końcowej t2. Ciepło pochłonięte Q2 przez dwie substancje jest równe:
Ponieważ Q1 = Q2 z zasady zachowania, czyli wzór ostateczny ma postać:
Schemat układu pomiarowego.
+
-
Oszacowanie błędów metodą różniczki zupełnej.
V
A
Wyszukiwarka
Podobne podstrony:
chemia fizyczna wykłady, sprawozdania, opracowane zagadnienia do egzaminu Sprawozdanie ćw 3 Ciepł
Cieplolecznictwo
Ciepło i zimno
FB Cieplo
Prezentacja Ciepło I
Badanie wyplywu cieczy ze zbior Nieznany (2)
Ciepło, cieplej, gorąco wprowadzenie do zagadnień zmian klimatu
Czujniki temperatury cieczy chłodzącej
cieplownictwo 5
Kanapka na ciepło z tuńczykiem i boczkiem
Omron Przewodnościowy regulator poziomu cieczy 61F D21T V1
lepkość cieczy edwqed, Technologia chemiczna, Fizyka, semestr 2, Laborki, Sprawozdania
Pomiar natężenia przepływu cieczy roboczej w układach hydrauliki siłowej - sprawko, Uczelnia, Hydrau
Mech- Badanie zależności współczynnika lepkości cieczy od te, Sprawozdania - Fizyka
2.12 molowe ciepło właściwe, materiały, Fizyka
Ciepło topnienia - Metoda różniczki zupełnej, Sprawozdania
więcej podobnych podstron