Egzamin 2005-02-03
Struktura elektronowa atomów (4 pkt)
Struktura elektronowa ![]()
przedstawia się następująco ...................................................................................................................................... .
rom leży w grupie ......... , okresie .........., w bloku ........ układu okresowego pierwiastków.
Orbitale molekularne (2 pkt)
Elektron, którego położenie opisane jest następującymi liczbami kwantowymi: n=4, l=1 ml=0 znajduje się na powłoce elektronowej..............na jednym z orbitali............
Reakcje dysocjacji (4 pkt)
Dysocjacja kwasu siarkowego (VI) H2SO4 w roztworze wodnym zachodzi w dwóch następujących etapach
1......................................................................................................................................
2......................................................................................................................................
Na przykładzie pierwszej reakcji zgodnie z teorią Brönsteda-Lowry'ego można stwierdzić, iż.....................................jest kwasem, ponieważ .................................... proton, czyli jest ................................... .
Hydroliza (4 pkt)
W wyniku reakcji hydrolizy NH4Cl ....................................................................... (napisz reakcję) w roztworze stężenie jonów ............. jest większe niż stężenie jonów ................. . Odczyn roztworu po hydrolizie chlorku amonu będzie ............................
Procesy redoks (6 pkt)
Uzgodnij współczynniki stechiometryczne równania. Napisz równania połówkowe.
H2S + HNO3 → H2SO4 + NO + H2O
Procesowi utleniania towarzyszy ................... elektronów przez reagent ulegający utlenieniu nazywany ........................... , którym w przypadku powyższej reakcji jest................................ . Natomiast w reakcji redukcji elektrony są ................... przez reagent ulegający redukcji nazywany .........................., którym w przypadku powyższej reakcji jest.................................. .
Związki organiczne (4pkt)
W grupie karbonylowej, będącej grupą funkcyjną w cząsteczkach ....................... , atom węgla jest połączony wiązaniami ................. z ................. innymi atomami. Do utworzenia tych wiązań zostały wykorzystane zhybrydyzowane orbitale ................. Pozostały(e) orbital(e) ........ atomu węgla nakłada(ją) się z orbitalem(i) ............ atomu tlenu, tworząc ................................................ . Wiązanie(a) występuje(ą) między atomami o różnej elektroujemności i dlatego chmura elektronowa nie jest centralnie rozmieszczona, lecz przesunięta w kierunku bardziej elektroujemnego atomu .................
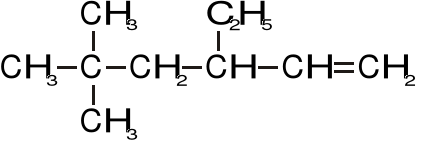
Nazewnictwo węglowodorów (4 pkt)
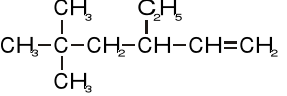
Proszę podać poprawną nazwę związku........................................................................
Właściwości jonitów (2 pkt)
Zdolność wymienna robocza (użytkowa) wyraża liczbę ................................................ przeciwjonów, które są wymieniane przez jednostkową ilość jonitu, aż do chwili ............................ złoża jonowymiennego.
Iloczyn rozpuszczalności (4 pkt)
![]()
Proszę napisać wzór na iloczyn rozpuszczalności soli dysocjującej według reakcji:
Zapobieganie korozji metali (4 pkt)
Wymień podstawowe sposoby zapobiegania korozji metali:
1. .............................................................................
2. .............................................................................
3. .............................................................................
4. .............................................................................
5. .............................................................................
![]()
Wyszukiwarka
Podobne podstrony:
egzamin test v3, Inżynieria Środowiska PW semestr I, chemia, sesja
16. egzamin test 1rok, Inżynieria Środowiska PW semestr I, chemia, sesja
7. egzamin test v1, Inżynieria Środowiska PW semestr I, chemia, sesja
13. egzamin 17 09 04, Inżynieria Środowiska PW semestr I, chemia, sesja
egzamin 2004sciaga, Inżynieria Środowiska PW semestr I, chemia, sesja
3. egzamin 22 01 2007, Inżynieria Środowiska PW semestr I, chemia, sesja
2. egzamin 9 2 2006, Inżynieria Środowiska PW semestr I, chemia, sesja
Chemia egzamin 2004(2005-06), Inżynieria Środowiska PW semestr I, chemia, sesja
1. egzamin 2 2 2006, Inżynieria Środowiska PW semestr I, chemia, sesja
SESJA ZIMOWA 2006, Inżynieria Środowiska PW semestr I, chemia, sesja
zestawy 28 pyt Ai B mini, Inżynieria Środowiska PW semestr I, chemia, sesja
testy 1rok egz2, Inżynieria Środowiska PW semestr I, chemia, sesja
11. testy 1rok v4, Inżynieria Środowiska PW semestr I, chemia, sesja
wszystkie pytania - ciąg - sciąga - długopisy, Inżynieria Środowiska PW semestr I, chemia, sesja
sciaga chemia, Inżynieria Środowiska PW semestr I, chemia, sesja
więcej podobnych podstron