Wykład 35
Lasery
Emisja spontaniczna
Jeden z postulatów Bohra mówił, że promieniowanie elektromagnetyczne zostaje wysłane tylko wtedy gdy elektron poruszający się po orbicie o całkowitej energii Ej zmienia swój ruch skokowo, tak że porusza się następnie po orbicie o energii Ek. W języku mechaniki kwantowej mówimy, że cząstka (elektron) przechodzi ze stanu wzbudzonego (o wyższej energii) do stanu podstawowego emitując foton. Częstotliwość emitowanego promieniowania jest równa
![]()
Jak już widzieliśmy źródłem takiego promieniowania jest na przykład jednoatomowy gaz pobudzony do świecenia metodą wyładowania elektrycznego (widmo liniowe).
Teoria kwantowa przewiduje, że elektron znajdujący się w stanie wzbudzonym samoistnie przejdzie do stanu podstawowego emitując foton. Zjawisko takie jest nazywane emisją spontaniczną.
Jeżeli różnica energii wynosi kilka elektronowoltów (jak w atomie wodoru, gdzie E1 = -13.6 eV) to czas charakterystyczny dla procesu emisji spontanicznej ma wartość rzędu 10-8 s.
Absorpcja
Na gruncie modelu Bohra można łatwo zrozumieć własności widm emisyjnych atomów jednoelektronowych. Można również zrozumieć widma absorpcyjne.
Ponieważ elektron musi mieć w atomie energię całkowitą równą jednej z energii dozwolonych (stanu stacjonarnego) więc z padającego promieniowania może on absorbować tylko określone porcje (kwanty) energii. Energia absorbowanych kwantów hν musi być równa różnicy pomiędzy energiami dozwolonych stanów tak więc linie widma absorpcyjnego mają te same częstotliwości (długości fal) co linie widma emisyjnego.
Doświadczenie pokazuje, że w chłodnym gazie atomy są w stanie podstawowym n = 1 więc procesy absorpcji odpowiadają serii Lymana. W bardzo wysokich temperaturach atomy będą już w stanie n = 2 i możemy obserwować linie absorpcyjne serii Balmera (widzialne).
Procesy wzbudzania atomów na wyższe poziomy energetyczne przez ich oświetlanie nosi nazwę pompowania optycznego.
Emisja wymuszona
Teoria kwantowa mówi także, że oprócz emisji spontanicznej oraz procesów absorpcji występuje także inny proces, nazywany emisją wymuszoną.
Przypuśćmy, że atom znajduje się w stanie wzbudzonym Ej i może emitować foton o energii (Ej - Ek). Jeżeli taki atom zostanie oświetlony promieniowaniem, które zawiera fotony o energii właśnie równej (Ej - Ek) to prawdopodobieństwo wypromieniowania przez atom energii wzrośnie.
Takie zjawisko przyspieszenia wypromieniowania energii przez oświetlenie atomów wzbudzonych odpowiednim promieniowaniem nazywane jest emisją wymuszoną.
Uwaga: Foton wysyłany w procesie emisji wymuszonej ma taką samą fazę oraz taki sam kierunek ruchu jak foton wymuszający.
W emisji spontanicznej mamy do czynienia z fotonami, których fazy i kierunki są rozłożone przypadkowo. Emisja wymuszona stwarza szansę uzyskania promieniowania spójnego.
Żeby móc przeanalizować możliwość takiej emisji musi wiedzieć jak atomy (cząsteczki) układu obsadzają różne stany energetyczne tzn. ile jest w stanie podstawowym a ile w stanach wzbudzonych.
Rozkład Boltzmana
Opis szczegółowy układu fizycznego złożonego z bardzo dużej liczby elementów jest bardzo skomplikowany np. próba opisu ruchu jednej cząstki gazu w układzie zawierającym 1023 cząstek (1 mol).
Na szczęście do wyznaczenia podstawowych własności układu (wielkości mierzalnych) takich jak temperatura, ciśnienie - informacje szczegółowe są na ogół niepotrzebne.
Jeśli do układu wielu cząstek zastosujemy ogólne zasady mechaniki (takie jak prawa zachowania) to możemy zaniedbać szczegóły ruchu czy oddziaływań pojedynczych cząstek i podstawowe własności układu wyprowadzić z samych rozważań statystycznych.
Taki przykład już poznaliśmy. Jest nim związek pomiędzy własnościami gazu klasycznego i rozkładem Maxwella prędkości cząsteczek gazu.
Funkcja rozkładu N(v) daje informację o prawdopodobieństwie, że cząsteczka ma prędkość w przedziale v, v + d v. Znając funkcję N(v) możemy obliczyć takie wielkości jak średnia prędkość (pęd niesiony przez cząsteczki), średni kwadrat prędkości (energia kinetyczna) itp. a na ich podstawie obliczyć takie wielkości mierzalne jak ciśnienie (związane z pędem) czy temperaturę (związaną z energią).
Spróbujemy teraz znaleźć rozkład prawdopodobieństwa z jakim cząstki układu zajmują różne stany energetyczne.
W tym celu rozpatrzymy układ zawierający dużą liczbę cząstek, które znajdują się w równowadze w temperaturze T. By osiągnąć ten stan równowagi cząstki muszą wymieniać energię ze sobą (poprzez zderzenia). Podczas tej wymiany ich energie będą fluktuować, przyjmując wartości raz mniejsze raz większe od średniej.
Żeby to zilustrować rozważmy układ, w którym cząstki mogą przyjmować jedną z następujących wartości energii E = 0, ΔE, 2ΔE, 3ΔE, 4ΔE..... .
Celem uproszczenia przyjmijmy, że układ ma zawiera tylko 4 cząstki oraz, że energia całkowita układu ma wartość 3ΔE.
Ponieważ te cztery cząstki mogą wymieniać energię między sobą, więc realizowany może być każdy możliwy podział energii całkowitej 3ΔE pomiędzy te obiekty. Na rysunku poniżej pokazane są wszystkie możliwe podziały, które numerujemy indeksem i.
Uwaga: Obliczając ilość sposobów realizacji danego podziału traktujemy jako rozróżnialny podział, który można otrzymać z danego w drodze przestawiania cząstek pomiędzy różnymi stanami. Przestawienia cząstek w tym samym stanie energetycznym nie prowadzą do nowych sposobów realizacji podziałów, bo nie można eksperymentalnie odróżnić od siebie takich samych cząstek o tej samej energii. Wreszcie ostatnie założenie: wszystkie sposoby podziału energii mogą wydarzyć się z tym samym prawdopodobieństwem.
i |
E=0 |
E=ΔE |
E=2ΔE |
E=3ΔE |
E=4ΔE |
liczba sposobów realizacji podziału |
Pi |
|||||||
1 |
1,2,3 |
|
|
4 |
|
|
|
|||||||
1 |
1,2,4 |
|
|
3 |
|
4 |
4/20 |
|||||||
1 |
1,3,4 |
|
|
2 |
|
|
|
|||||||
1 |
2,3,4 |
|
|
1 |
|
|
|
|||||||
2 |
1,2 |
3 |
4 |
|
|
|
|
|||||||
2 |
1,2 |
4 |
3 |
|
|
|
|
|||||||
2 |
1,3 |
2 |
4 |
|
|
|
|
|||||||
2 |
1,3 |
4 |
2 |
|
|
|
|
|||||||
2 |
1,4 |
2 |
3 |
|
|
|
|
|||||||
2 |
1,4 |
3 |
2 |
|
|
12 |
12/20 |
|||||||
2 |
2,3 |
1 |
4 |
|
|
|
|
|||||||
2 |
2,3 |
4 |
1 |
|
|
|
|
|||||||
2 |
2,4 |
1 |
3 |
|
|
|
|
|||||||
2 |
2,4 |
3 |
1 |
|
|
|
|
|||||||
2 |
3,4 |
1 |
2 |
|
|
|
|
|||||||
2 |
3,4 |
2 |
1 |
|
|
|
|
|||||||
3 |
1 |
2,3,4 |
|
|
|
|
|
|||||||
3 |
2 |
1,3,4 |
|
|
|
4 |
4/20 |
|||||||
3 |
3 |
1,2,4 |
|
|
|
|
|
|||||||
3 |
4 |
1,2,3 |
|
|
|
|
|
|||||||
n(E) |
40/20 |
24/20 |
12/20 |
4/20 |
0/20 |
|||||||||
Obliczamy następnie n(E) czyli prawdopodobną ilość cząstek w danym stanie energetycznym E.
Weźmy stan E = 0.
Dla podziału i = 1 mamy 3 cząstki a prawdopodobieństwo, że taki podział ma miejsce wynosi 4/20.
Dla podziału i = 2 mamy 2 cząstki a prawdopodobieństwo, że taki podział ma miejsce wynosi 12/20.
Wreszcie dla podziału i = 3 mamy 1 cząstkę a prawdopodobieństwo, że taki podział ma miejsce wynosi 4/20.
Zatem prawdopodobna ilość obiektów w stanie E = 0 wynosi:
n(E) = 3 (4/20) + 2 (12/20) + 1 (4/20) = 40/20 = 2
Analogicznie obliczamy n(E) dla pozostałych wartości E (patrz ostatni wiersz tabeli).
Zauważmy, że suma tych liczb wynosi cztery, tak że jest równa całkowitej liczbie cząstek we wszystkich stanach energetycznych.
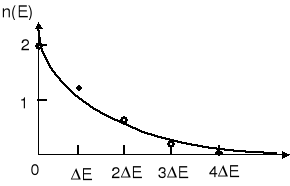
Wykres zależności n(E) jest pokazany na rysunku poniżej.
Ciągła krzywa na rysunku jest wykresem malejącej wykładniczo funkcji
|
(35.1) |
Możemy teraz brać ΔE coraz mniejsze (zwiększając ilość dozwolonych stanów) przy tej samej co poprzednio wartości całkowitej energii. Oznacza to, że będziemy dodawać coraz więcej punktów do naszego wykresu, aż w granicy gdy ΔE → 0 przejdziemy do funkcji ciągłej danej powyższym równaniem.
Potrzebujemy jeszcze znaleźć E0. Obliczenia te choć proste wykraczają poza ramy tego wykładu. Wystarczy więc zapamiętać, że E0 = kT, tzn. jest równa średniej energii układu cząstek w temperaturze T.
Ostatecznie więc
|
(35.2) |
Jest to rozkład Boltzmana, który mówi, że prawdopodobna ilość cząstek układu w równowadze w temperaturze T, znajdujących się w stanie o energii E jest proporcjonalna do ![]()
. Sposób wyboru stałej proporcjonalności A zależy od tego jaki układ rozważamy. Poniżej pokazana jest zależność n(E) dla trzech różnych temperatur i trzech odpowiednich wartości stałej A.
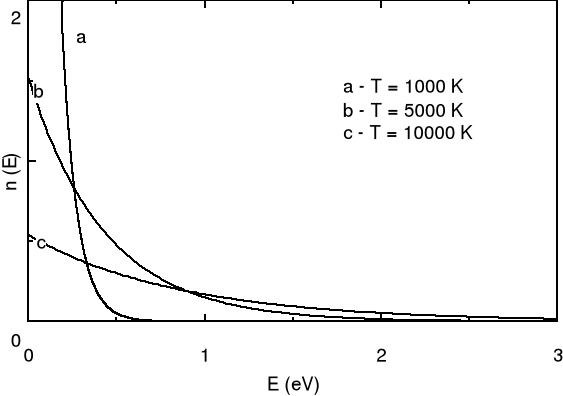
Widzimy, że stany o niższej energii są obsadzane z większym prawdopodobieństwem niż stany o wyższym E.
Laser
Jeżeli więc układ będący w stanie równowagi oświetlimy odpowiednim promieniowaniem to w takim układzie absorpcja będzie przeważała nad emisją wymuszoną.
Żeby przeważała emisja wymuszona, to w wyższym stanie energetycznym musi się znajdować więcej atomów (cząsteczek) niż w stanie niższym. Mówimy, że rozkład musi być antyboltzmanowski.
Taki układ można przygotować na kilka sposobów min. za pomocą zderzeń z innymi atomami lub za pomocą pompowania optycznego.
Ten pierwszy sposób jest wykorzystywany w laserze helowo-neonowym.
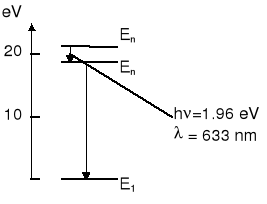
Schemat poziomów energetycznych dla tego lasera jest pokazany na rysunku obok.
W tym laserze atomy neonu są wzbudzane do na poziom En' w trakcie zderzeń ze wzbudzonymi atomami helu. Przejście na poziom En zachodzi wskutek emisji wymuszonej. Następnie atomy neonu przechodzą szybko do stanu podstawowego oddając energię w wyniku zderzeń ze ściankami.
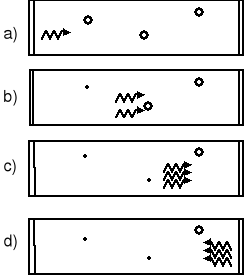
Emisja wymuszona w laserze przedstawiona została na rysunkach poniżej.
Na rysunku (a) foton zostaje „wprowadzony” do gazu. Foton wymusza emisję drugiego fotonu przez wzbudzony atom (b). Przez układ poruszają się dwa fotony. Wymuszona zostaje kolejna emisja i już trzy fotony o tej samej fazie poruszają się przez układ (c). Jeżeli na końcach zbiornika znajdują się lustra to ten proces będzie trwał aż wszystkie atomy wypromieniują nadmiar energii.
Jeżeli jedno z tych zwierciadeł będzie częściowo przepuszczające to układ będzie opuszczała wiązka spójna - wszystkie fotony będą miały tę samą fazę.
Inny sposób „odwrócenia” rozkładu boltzmanowskiego jest wykorzystany w laserze rubinowym. Laser zbudowany na ciele stałym składa się z pręta wykonanego z kryształu Al2O3, w którym jonami czynnymi są jony z grupy ziem rzadkich. Na końcach pręta są naniesione zwierciadła odbijające. Promieniowanie pompujące jest wytwarzane przez lampę błyskową umieszczoną wokół kryształu tak jak pokazano na rysunku poniżej.
Od czasu uruchomienia pierwszego lasera tj. od 1960 roku technologia tych urządzeń bardzo się rozwinęła. Obecnie działają zarówno lasery impulsowe jak i lasery o pracy ciągłej. Ośrodkami czynnymi w laserach są gazy, ciała stałe i ciecze, a zakres długości fal jest bardzo szeroki; od podczerwieni przez obszar widzialny aż do nadfioletu (ostatnio !!!).
Zastosowania laserów są wszechstronne. Przykładowo:
w odtwarzaczach i nagrywarkach (CD),
w dalmierzach, celownikach
przy obróbce mechanicznej
holografia
Z. Kąkol-Notatki do Wykładu z Fizyki
34-8
35-1
Wyszukiwarka
Podobne podstrony:
PATOMORFOLOGIA wykład 35 9, PATOMORFOLOGIA wykład 9 (35) (7 XII 01)
wyklad 35
wykłady 35
Wyklad 35 Atom w polu zewnętrznym
35 Wykłady z Zarządzania Strategicznego
31-35, EIT, FPGA, Opracowane pytania do zaliczenia wykładu
Integracja Europejska - Wykłady - 2007 - Mucha-Leszko (35), Nowy folder
Logistyka i Zarządzanie Łańcuchem dostaw Wykłady str 35
Prawo bankowe - wykład dziennych, zchomikowane, 35 000 edukacyjnych plików z każdej branży
10 Leszek Kołakowski O tolerancji, w Mini wykład o maxi sprawach (s 35 41)
35 Wykłady z Zarządzania Strategicznego
Napęd Elektryczny wykład
wykład5
więcej podobnych podstron