Chemia organiczna - konspekt
(materiały do wykładów i do zajęć laboratoryjnych).
Związki organiczne
Szczególne właściwości - tworzenie połączeń łańcuchowych i pierścieniowych
Najprostsze związki organiczne składają się z dwóch pierwiastków — węgla i wodoru,
ważną rolę spełniają także pochodne węglowodorów, zawierające w cząsteczce takie pierwiastki, jak tlen, azot, siarka i chlorowce.
Wiązania między atomami węgla mogą mieć charakter:
pojedynczy (hybrydyzacja sp3),
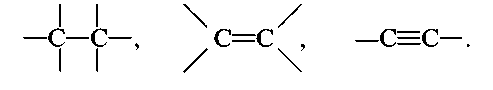
podwójny (sp2 )potrójny (sp1)
Energia wiązania kJ/mol
343 615 802
Pojedyncze
są bardzo trwałe,
związki charakteryzują się małą reaktywnością.
Wiązania węgla z innymi pierwiastkami - powstają związki - pochodne węglowodorów
- mają charakter polarny, a niekiedy nawet jonowy,
- grupy funkcyjne w pochodnych węglowodorów są przyczyną zwiększonej reaktywności.
Nazewnictwo: W technice dla związków organicznych stosuje się raczej nazwy popularne, przyjęte w handlu. Nazewnictwo zgodne z nomenklaturą genewską lub przyjętą w CAS (Chemical Abstracts Service Registry Number) występuje dodatkowo.
Węglowodory nasycone - alkany CnH2n+2:
Metan, etan propan, butan, pentan, heksan itd.
Nazwy grup alkilowych CnH2n+1, metylowa, etylowa itd. , grupy arylowe np. fenolowa C6H5-
Alkeny (olefiny)
Węglowodory nienasycone np. z jednym wiązaniem podwójnym CnH2n :
Eten ( nazwa zwyczajowa - etylen), propen, buten, penten, itd.
Występuje izomeria, w zależności od miejsca wiązania podwójnego w łańcuchu.
Alkiny (acetyleny)
Węglowodory nienasycone np. z jednym wiązaniem potrójnym: CnH2n-2
etyn (nazwa zwyczajowa - acetylen), propyn, butyn, pentyn.
Rodzaje związków organicznych z grupą funkcyjną
ALKOHOLE: R - OH,
ETERY: R - O - R liniowe oraz cykliczne,
ALDEHYDY: R C=O
H
KETONY: R C=O
R
KWASY KARBOKSYLOWE: R C=O
OH
AMINY : CH3NH2 metyloamina (pierwszorzędowa), CH3NHCH3 dimetyloamina (drugorzędowa), N(CH3)3, trimetyloamina (trzeciorzędowa),
Podstawowe rodzaje reakcji chemicznych związków organicznych:
Podstawianie, przyłączanie, odszczepianie.
WĘGLOWODORY AROMATYCZNE
Najprostszy związek: benzen (pierścień) C6H6
Podstawniki w pierścieniu aromatycznym: orto, meta, para.
Strukturotwórcze pierwiastki materiałów budowlanych:
Węgiel C jako podstawowy składnik wszystkich materiałów organicznych (naturalnych i syntetycznych),
TWORZYWA SZTUCZNE
ZALETY : stosunkowo łatwe przetwórstwo, trwałość, odporność na korozję, gładkość powierzchni, właściwości hydrofobowe i nie nasiąkliwość wodą, możliwość uzyskiwania ładnych kolorów, niski ciężar właściwy, łatwe łączenie (spawanie, zgrzewanie, klejenie)
i montaż.
CECHY OGRANICZAJĄCE ZAKRES ZASTOSOWAŃ.
ograniczona odporność mechaniczna, są na ogół palne.
Krzem Si jako składnik większości materiałów mineralnych, związki krzemoorganiczne jako wzmacniacze i środki hydrofobowe.
Krzemowodory, inaczej silany, ogólny wzór: SinH2n+2,
SiH4 - silan, H3Si-SiH3 - disilan, H3Si-SiH2-SiH3 - trisilan, H3Si-SiH2-SiH2-SiH3 - tetrasilan itd.
Łańcuchowe i pierścieniowe związki krzemoorganiczne zbudowane naprzemiennie z atomów krzemu i tlenu nazywamy siloksanami związki krzemoorganiczne:
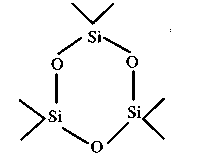
Nazwa techniczna: silikony
Nazwa precyzyjna, używana dla celów naukowych: monomery - pochodne silanu,
polimerowe związki - poliorganosiloksany.
Zastosowanie w budownictwie :
siloksany i silikony, silikoniany sodu lub potasu, żywice polisiloksanowe:
jako składniki materiałów powłokowych (np. do hydrofobizacji mineralnych materiałów porowatych), jako środki impregnujące i zabezpieczające materiały budowlane przed działaniem wody, środki antyadhezyjne ( przeciwprzyczepne),
środki do smarowania form itp.
Polimery siloksanowe: oleje silikonowe, kauczuki silikonowe, żywice silikonowe, gumy,
farby i lakiery.
Polimery - wielkocząsteczkowe związki organiczne
Substancje małocząsteczkowe, z których otrzymuje się polimery, nazywa się monomerami.
nA (monomer) Ⴎ A-A-A-A-A..... (polimer)
nA+ mC (dwa różne monomery) Ⴎ A-A-C-A-A-C-A..... (kopolimer)
Jednakowe, powtarzające się jednostki proste w polimerze nazywane są merami.
(Liczba merów w makrocząsteczce jest zwykle większa od 100).
Opracowała dr inż. Teresa Szymura
Wyszukiwarka
Podobne podstrony:
Chemia organiczna czesc I poprawiona
chemia organiczna wykład 6
Wykład 9 CHEMIA ORGANICZNA
Chemia Organiczna 4
Chemia organiczna IV
CHEMIA- CHEMIA ORGANICZNA, CHEMIA
bromoacetanilid, Studia, Sprawozdania, Chemia organiczna
kationy, Polibuda, II semestr, fizyka, FIZA, lab, Chemia laborki, chemia ogolna nie organiczna
Przykladowy egzamin chemia organiczna - ICiP - 2010-zima. , Egzamin
I POPRAWKA EGZAMINU Z CHEMII ORGANICZNEJ, Technologia chemiczna, Chemia organiczna, 4 semestr, organ
chemia organiczna 2003 cała PDF(1)
więcej podobnych podstron