Michał Murawski WM-32
Grzegorz Boguszewski P-5
Zadanie 1.36.
Powietrze traktowane tak jak gaz doskonały zajmuje zasób objętości ![]()
i osiąga następujące parametry stanu: ciśnienie ![]()
i temperaturę ![]()
. Następnie w przemianie izotermicznej odwracalnej powietrze zostaje rozgęszczone osiągając ciśnienie ![]()
. Obliczyć przyrosty zasobów energii wewnętrznej ![]()
, antalpii ![]()
, entropii ![]()
oraz prace bezwzględną objętościową ![]()
, pracę techniczną ![]()
i przyrost ilości ciepła przemiany izotermicznej odwracalnej ![]()
.
Dane: Szukane:
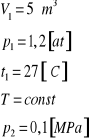
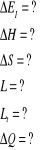
1. Ilustracja układu oraz wykresy przemiany izotermicznej odwracalnej we współrzędnych p,V oraz T,S.
![]()
![]()
ps - ciśnienie statyczne powietrza w układzie
p=psa=ps+po - ciśnienie statyczne absolutne powietrza w układzie
po - ciśnienie otoczenia
T(p,V) = const
2. Bilans zasobu energii wewnętrznej dla przemiany odwracalnej.
Pierwsza postać pierwszej zasady termodynamiki:
![]()
gdzie praca bezwzględna objętościowa określona jest zależnością
![]()
3. Bilans zasobu entalpii dla przemiany odwracalnej
Druga postać pierwszej zasady termodynamiki:
![]()
gdzie praca techniczna określona jest zależnością
![]()
4. Bilans zasobu energii wewnętrznej dla odwracalnej przemiany izotermicznej.
Pierwsza postać pierwszej zasady termodynamiki:
![]()
Zasób energii wewnętrznej gazu doskonałego w układzie substancjalnym wyrażony jest zależnością:
![]()
gdzie:
dla gazu doskonałego: ![]()
dla układu substancjalnego: ![]()
dla przemiany izotermicznej: ![]()
i elementarny przyrost zasobu energii wewnętrznej jest równy:
![]()
zaś bilans zasobu energii wewnętrznej przyjmie postać:
![]()
5. Bilans entalpii dla odwracalnej przemiany izotermicznej.
Druga postać pierwszej zasady termodynamiki:
![]()
Zasób entalpii gazu doskonałego w układzie substancjalnym określony jest zależnością:
![]()
gdzie:
dla gazu doskonałego: ![]()
dla układu substancjalnego: ![]()
dla przemiany izotermicznej: ![]()
i elementarny przyrost zasobu entalpii jest równy:
![]()
zaś bilans entalpii przyjmie postać:
![]()
6. Relacja między przyrostem ilości ciepła pracy bezwzględnej objętościowej i pracy technicznej w przemianie izotermicznej odwracalnej.
Uwzględniając wyniki rozwiązań w punkcie 4 i 5 otrzymano:
![]()
7. Wyznaczenie pracy bezwzględnej objętościowej.
Uwzględniając definicję pracy bezwzględnej objętościowej:
![]()
oraz równanie izotermy:
![]()
otrzymano:
![]()
całkując powyższe równanie w granicach:
![]()
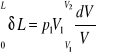
i uwzględniając równanie izotermy postaci:
![]()
uzyskano zależność określającą pracę bezwzględną objętościową wykonaną przez układ w przemianie izotermicznej:
![]()
8. Wyznaczenie przyrostu zasobu energii wewnętrznej.
Elementarny przyrost zasobu energii wewnętrznej w układzie substancjalnym w przemianie izotermicznej jest równy:
![]()
całkując powyższe równanie w granicach:
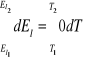
otrzymano:
![]()
9. Wyznaczenie przyrostu zasobu entalpii.
Elementarny przyrost zasobu entalpii w układzie substancjalnym w przemianie izotermicznej jest równy:
![]()
całkując powyższe równanie w granicach:
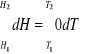
otrzymano:
![]()
10. Wyznaczenie przyrostu ilości ciepła i pracy technicznej w przemianie izotermicznej odwracalnej.
Uwzględniając, że dla przemiany izotermicznej zachodzi poniższe równanie:
![]()
otrzymano:
![]()
11. Wyznaczenie przyrostu zasobu entropii w przemianie izotermicznej odwracalnej.
Uwzględniając zależność definiującą elementarny przyrost zasobu entropii dla przemiany odwracalnej:
![]()
i całkując ją w granicach przy uwzględnieniu uwarunkowania przemiany izotermicznej
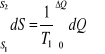
otrzymano:
![]()
12. Obliczenie wartości pracy bezwzględnej objętościowej, technicznej oraz przyrostu ilości ciepła.
![]()
13. Obliczenie wartości przyrostu zasobu entropii.
![]()
P(V,T=const)
p1
p2
V1
V2
p
V
L
Lt
V1 T2
p=pS1+p0
FS1
L
p2 V2 T2
FS2
p0
T
ΔQ
p2=pS2+p0
ΔQ
S1
S2
S
Wyszukiwarka
Podobne podstrony:
zad. I.27, MiBM WIP PW, inżynierskie, 4 semestr, TERTE, I kolokwium
zad. I.29, MiBM WIP PW, inżynierskie, 4 semestr, TERTE, I kolokwium
zad. I.18, MiBM WIP PW, inżynierskie, 4 semestr, TERTE, I kolokwium
Zad. I.25, MiBM WIP PW, inżynierskie, 4 semestr, TERTE, I kolokwium
Zad. I.09, MiBM WIP PW, inżynierskie, 4 semestr, TERTE, I kolokwium
zad. I.06, MiBM WIP PW, inżynierskie, 4 semestr, TERTE, I kolokwium
zad. I.10, MiBM WIP PW, inżynierskie, 4 semestr, TERTE, I kolokwium
Zad. I.20, MiBM WIP PW, inżynierskie, 4 semestr, TERTE, I kolokwium
zad. I.21, MiBM WIP PW, inżynierskie, 4 semestr, TERTE, I kolokwium
zad. I.30, MiBM WIP PW, inżynierskie, 4 semestr, TERTE, I kolokwium
Zad. I.35, MiBM WIP PW, inżynierskie, 4 semestr, TERTE, I kolokwium
zad. I.16, MiBM WIP PW, inżynierskie, 4 semestr, TERTE, I kolokwium
zad. I.19, MiBM WIP PW, inżynierskie, 4 semestr, TERTE, I kolokwium
zad. I.17, MiBM WIP PW, inżynierskie, 4 semestr, TERTE, I kolokwium
zad. I.14, MiBM WIP PW, inżynierskie, 4 semestr, TERTE, I kolokwium
zad. I.28, MiBM WIP PW, inżynierskie, 4 semestr, TERTE, I kolokwium
Zad. I.04, MiBM WIP PW, inżynierskie, 4 semestr, TERTE, I kolokwium
zad. I.07, MiBM WIP PW, inżynierskie, 4 semestr, TERTE, I kolokwium
zad. I.26, MiBM WIP PW, inżynierskie, 4 semestr, TERTE, I kolokwium
więcej podobnych podstron