Gr. 3
Technologia Żywności i Żywienie Człowieka
Środa 1415 -1800
Laboratorium chemii żywności
Barwniki naturalne:
Barwniki roślinne ze szpinaku
Wstęp:
Barwniki roślinne, barwne związki organiczne zawarte w roślinach, nadające im barwę. Znajdują się w soku komórkowym (cytoplazmie) (np. antocyjany i flawonoidy w owocach i kwiatach) lub w plastydach, jak chlorofil. Niektóre z barwników biorą udział w fotosyntezie (barwniki asymilacyjne).
Najbardziej znamienne dla roślin zabarwienie zielone pochodzi od chlorofilu, który odbija promienie podczerwone i zielone.
Żółte i pomarańczowe zabarwienie powodują barwniki bezpostaciowe lub krystaliczne tj. flawonoidy i karotenoidy, które odbijają promienie żółte i czerwone, zlokalizowane są w plastydach lub soku komórkowym. Nadają barwę korzeniom marchwi, kwiatom jaskra żółtego, pierwiosnka.
Czerwone zabarwienie pochodzi najczęściej od antocyjan, barwników ropuszczonych w soku komórkowym. Ich barwa i kolor zależą od pH soku komórkowego i w środowisku zasadowym jest niebieska. Kwiaty niektórych roślin (np. groszku, niezapominajki), zawierające te barwniki zmieniają barwę z czerwonej na niebieską i odwrotnie w zależności od stanu podłoża i metabolizmu.
Antocujany i barwniki flawonowe mają bardzo podobną budowę chemiczną, dlatego nieznaczne zmiany w metabolizmie powodują, że blisko spokrewnione rośliny, posiadające te barwniki, mają kwiaty żółte, czerwone lub niebieskie. Różne barwy i ich odcienie zależą nie tylko od ilości barwników, ale także od jakości podłoża, w tym szczególnie od stopnia pochłaniania i odbijania promieni świetlnych przez struktury, w których barwniki są zawarte.
Białe zabarwienie jest związane z całkowitym odbiciem światła przez pęcherzyki powietrza znajdujące się w przestworach międzykomórkowych żywych tkanek, np. w płatkach płatków.
Barwniki roślinne od wieków użytkowane są przez człowieka (barwierskie rośliny).
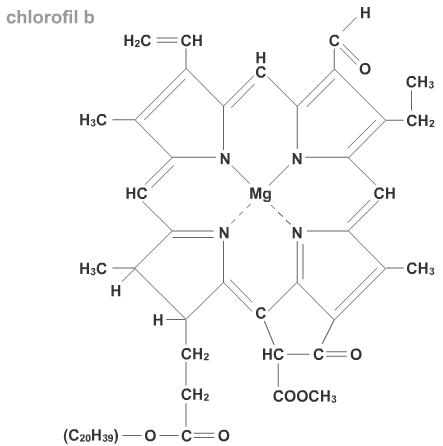
Chlorofile
Zielone barwniki roślinne zwane chlorofilami, występują w chloroplastach komórek odpornych w żywej tkance na działanie kwasów organicznych, tlenu i światła. Jest bardzo trwałym barwnikiem. Nie rozpuszcza się w wodzie, lecz w alkoholu.
Zawartość chlorofilu w zielonych owocach i warzywach wynosi najczęściej od kilku do kilkudziesięciu mg w 100 g świeżego produktu. Najwięcej zawierają go: jarmuż, brokuły, szpinak, groch zielony, liście selera i pietruszki, jabłka oraz agrest.
Chlorofil występujący w żywej tkance jest odporny na działanie czynników środowiskowych.
Podczas obróbki cieplnej owoców i warzyw w środowisku kwaśnym chlorofil przekształca się w oliwkowozieloną feofitynę. Reakcja ta ma charakter nieodwracalny i jest tym intensywniejsza, im niższe jest pH, wyższa temperatura i dłuższy czas obróbki cieplnej. Także gotowanie warzyw w naczyniach pod zwiększonym ciśnieniem powoduje prawie całkowite przejście chlorofilu w feofitynę.
Blanszowanie zielonych warzyw przed zamrażaniem sprzyja zachowaniu barwy.
Silnie kwaśne środowisko, np. w marynatach i kiszonkach, powoduje po dłuższym czasie przejście feofityny, chlorofilidu i chlorofiliny w ciemnozabarwione feoforbidy.
Pod wpływem wysokiej temperatury, np. w czasie sterylizacji szpinaku czy fasolki szparagowej, obok feofityny tworzy się oliwkowobrązowa pirofeofityna.
Barwi preparaty na różne odcienie zieleni. Służy do barwienia past do zębów, płynów do ust, niektórych mydeł i kremów. Ma właściwości dezynfekcyjne. Przyspiesza regenerację naskórka i gojenie drobnych podrażnień skóry. Wykorzystywany w kosmetykach do pielęgnacji cery przetłuszczającej się, szarej i zmęczonej. Poprawia ukrwienie skóry, a więc wpływa na lepsze jej dotlenienie i odżywienie. Ma budowę zbliżoną do hemoglobiny.
Karotenoidy
Karotenoidy są to żółte lub czerwone barwniki. Dzieli się je na:
karoteny,
ksantofile.
Ksantofile odznaczają się jaśniejszym, żółtym zabarwieniem (brzoskwinie, kukurydza) lub też intensywnie czerwonym (papryka). Z ważniejszych ksantofili można wymienić zeaksantynę w kukurydzy, kapsantynę w papryce i wiolaksantynę w soku pomarańczowym.
Spośród owoców najwięcej karotenoidów zawierają morele, brzoskwinie, śliwki. Dobrym źródłem karotenoidów są warzywa: marchew, papryka, dynia, zielona pietruszka, szpinak.
W żywych komórkach roślinnych barwniki te są trwałe. Procesy rozdrabniania i obróbki cieplnej zapoczątkowują destrukcyjne procesy chemiczne zachodzące pod wpływem światła, z udziałem tlenu, jonów metali i enzymów.
Zasadniczymi przemianami, jakim ulegają karotenoidy, są procesy utleniania i zmiany konfiguracji przestrzennej. Procesy utleniania prowadzą do pojaśnienia barwy produktów.
Karotenoidy w stanie naturalnym występują głównie w formie trans. Pod wpływem działania światła, temperatury, kwasów następuje częściowa zmiana konfiguracji do formy cis, co prowadzi do rozjaśnienia barwy i obniżenia wartości prowitaminowej.
Barwniki karotenoidowe w porównaniu z pozostałymi są najbardziej odporne na działanie różnych czynników w procesie sporządzania potraw. Ich stabilności sprzyja blanszowanie, unikanie działania światła, wysokich temperatur, tlenu i niektórych metali.
Karotenoidy są nierozpuszczalne w wodzie. Dodatek tłuszczu do gotowania marchwi powoduje rozpuszczenie kryształków karotenu stąd barwa jest bardziej jaskrawa.
Karoten to barwnik o kolorze pomarańczowym. Na największą uwagę zasługuje tzw. beta - karoten, który stanowi przeciętnie 80% wszystkich karotenów roślin wyższych. Szczególnie obficie występuje on w korzeniu marchwi. Od marchwi pochodzi zresztą nazwa karotenu, bo Daucus carota to łacińska nazwa tej rośliny. Dla zwierząt wyższych zasadnicze znaczenie ma tylko beta - karoten. To właśnie z niego produkują one witaminę A - retinol, którego dalsze produkty przemiany mają istotne znaczenie w procesie widzenia (wchodzą w skład barwnika wzrokowego - rodopsyny). Dlatego beta - karoten nazywany jest prowitaminą A.
Ksantofile to pochodne tlenowe karotenów (hydroksylowe, ketonowe, aldehydowe, karboksylowe). Mają barwę żółtą lub brązową (gr. ksanthos - żółty). Powstają one przy utlenianiu karotenów przy pomocy enzymów - tzw. oksydaz mieszanych. Najbardziej popularne są pochodne hydroksylowe, których najbardziej rozpowszechnionym przedstawicielem jest luteina.
Wśród jesiennych liści spotykamy też barwę intensywnie czerwoną. Odpowiedzialne za nią są jednak inne barwniki - antocyjany, które w przeciwieństwie do karotenoidów, nie występują w liściach cały czas, ale są jesienią specjalnie syntetyzowane.
Antocjyany
Antocyjany nadają owocom i warzywom barwę o odcieniu czerwonym, fioletowym lub niebieskim. Najwięcej antocyjanów zawierają jeżyny, maliny, czarne porzeczki, żurawiny, aronia, a z warzyw - czerwona kapusta i bakłażany.
Antocyjany są związkami nietrwałymi, szybko ulegają rozkładowi, przy czym najtrwalsza jest forma występująca w środowisku kwaśnym. Ulegają odwracalnym i nieodwracalnym przemianom, a przebieg tych procesów zależy przede wszystkim od pH środowiska. Na przykład barwa cyjanidy zmienia się od czerwonej w środowisku kwaśnym, przez fioletową w środowisku obojętnym, do niebieskiej, a nawet zielonej, w środowisku alkalicznym.
Antocyjany łatwo ulegają przemianom w trakcie zabiegów technologicznych, zwłaszcza przy zastosowaniu wyższej temperatury, wydłużaniu czasu obróbki cieplnej i w środowisku o podwyższonym pH oraz w czasie przechowywania.
Antocyjany najczęściej występują w owocach, kwiatach i liściach.
W grupie antocyjanów wyróżniono 15 typów budowy części aglikonowych (tych po odjęciu części cukrowej), z których 6 spotykamy w naturze najczęściej. Są to: cyjanidyna (aronia, wiśnie, czerwona kapusta, żurawina), delfinidyna (winogrona, czarne jagody, czarny bez, żurawina), pelargonidyna (pelargonia, truskawka), peonidyna (czarny bez, peonia), malwidyna (winogrona, malwa), petunidyna (petunia). Najbogatszym surowcem antocyjanowym są owoce aronii, które obfitują w różne glikozydy cyjanidyny.
Antocyjany są związkami o niezwykle niskiej toksyczności. Nic dziwnego, skoro występują one w dużych stężeniach w wielu owocach, "przygotowywanych" przez rośliny specjalnie do zjedzenia przez zwierzę, w celu przeniesienia nasion. Jasne więc, że ewolucja selekcjonowała takie rośliny, które nie truły tych, od których zależał ich własny sukces ewolucyjny.
Antoksantyny
Antoksantyny są to bezbarwne lub jasnożółte pochodne flawonowe. Występują w owocach i warzywach o jasnej barwie (jabłkach, gruszkach, ziemniakach, kalafiorach, selerach, cebuli). Ich znaczenie jako czynników naturalnej barwy jest mniejsze niż antocjanów. Są trudniej rozpuszczalne w wodzie i mniej wrażliwe na podwyższoną temperaturę, tlen i enzymy. W środowisku kwaśnym barwa antoksantyn nie ulega zmianie, natomiast w środowisku alkalicznym przyjmują one barwę żółtą do pomarańczowobrązowej.
W owocach i warzywach występują znaczne ilości związków, które mogą ulegać enzymatycznemu utlenianiu do ciemno zabarwionych substancji. Enzymatyczne brunatnienie surowca owocowo-warzywnego jest następstwem mechanicznego zniszczenia struktur komórkowych w czasie obróbki wstępnej i kontaktu z enzymem. Proces ten szczególnie intensywnie zachodzi, powodując niepożądane zmiany barwy, w jabłkach, gruszkach, morelach, czereśniach, brzoskwiniach oraz w ziemniakach. Korzystnym następstwem enzymatycznego brunatnienia jest natomiast powstanie właściwej barwy podczas fermentacji herbaty oraz ziarn kakaowych, a także w czasie dojrzewania daktyli.
Likopen
Sok pomidorowy jest bardziej wartościowy niż świeże pomidory.
W trakcie badań przeprowadzonych w Stanach Zjednoczonych i Europie odkryto, że likopen -barwnik nadający pomidorom czerwony kolor, mający właściwości przeciwutleniające, przez co ma działanie przeciwnowotworowe i, co ciekawe, nie tylko te spożywane w postaci świeżych warzyw, ale przede wszystkim przetworzone termicznie i podane w formie ketchupu, soku pomidorowego, sosu do pizzy czy zupy pomidorowej. Pod wpływem gotowania, zwłaszcza z dodatkiem niewielkiej ilości tłuszczu, dochodzi do uwalniania likopenu zawartego w skórce pomidorów, dzięki czemu jest on dużo łatwiej przyswajalny.
Poniższe zestawienie przedstawia średnią zawartość likopenu w niektórych produktach spożywczych:
|
||
|
w 100 g produktu |
w porcji |
Ketchup pomidorowy |
15mg |
2mg (10ml) |
Zupa pomidorowa |
4mg |
9mg (200g) |
Sos do makaronu |
22mg |
28mg (125ml) |
Sok pomidorowy |
8mg |
10mg (szklanka 120ml) |
Sos do pizzy |
12mg |
7mg (60ml) |
Świeże pomidory |
3mg |
2mg (85g) |
Wykonanie ćwiczenia:
Mrożone liście szpinaku (10 g) odcisnęłyśmy z wody przy pomocy bibuły i umieściłyśmy w kolbie Erlenmeyera. Dodałyśmy 12 ml metanolu, zakorkowałyśmy kolbę i mocno wstrząsałyśmy przez ok. 4 minuty. Odcisnęłyśmy roztwór metanolowy. Surowiec wrzuciłyśmy powrotem do kolby Erlenmeyera, dodałyśmy 15 ml heksanu, 5 ml metanolu i ponownie mocno wytrząsałyśmy przez ok. 6 minut. Ekstrakt przesączyłyśmy na lejku Buchnera i przelałyśmy do rozdzielacza. Oddzieliłyśmy warstwę metanolowo-wodną, a ekstrakt heksanowi przemyłyśmy 5 ml wody i wysuszyłyśmy bezwodnym siarczanem sodowym (ok. 15 minut). Przesączyłyśmy ekstrakt i przeprowadziłyśmy analizę metodą chromatografii cienkowarstwowej. Potem roztwór, który pozostał zatężyłyśmy na wyparce obrotowej i przeprowadziłyśmy analizę metodą chromatografii cienkowarstwowej jeszcze raz.
Rf dla poszczególnych barwników:
![]()
|
przed zatężaniem |
po zatężeniu |
Barwnik |
Odległość: start-meta: 7,4 cm |
Odległość: start-meta: 8,1 cm |
Karoteny -plama żółto-pomarańczowa |
Odległość: start-plama: 7,1 cm
Rf = 0,959 |
Odległość: start-plama: 8 cm
Rf = 0,988 |
Feofityna a -plama szara |
Odległość: start-plama: 2,2 cm
Rf = 0,297 |
Odległość: start-plama: 3 cm
Rf = 0,370 |
Feofityna b -plama jasnoszara |
- |
- |
Chlorofil a -plama niebieskozielona |
- |
Odległość: start-plama: 0,9 cm
Rf = 0,111 |
Chlorofil b -plama żółtozielona |
Odległość: start-plama: 0,2 cm
Rf = 0,027 |
Odległość: start-plama: 0,5 cm
Rf = 0,062 |
Ksantofile -plama żółta |
- |
Odległość: start-plama: 0,1 cm
Rf = 0,012 |
Wnioski:
Z doświadczenia wynika, że po zatężeniu plamy na płytce były intensywniejsze i bardziej widoczne niż przed zatężeniem roztworu. Im dalej substancja podniosła się do góry tym większy jest współczynnik retencji Rf. Metoda chromatograficzna oparta jest na wykorzystaniu różnic prędkości migracji rozdzielanych składników względem dwóch faz: fazy stacjonarnej i fazy ruchomej. Substancje o największym stosunku podziału poruszają się jako ostatnie, natomiast substancje o najmniejszych stosunkach podziału poruszają się razem z czołem rozpuszczalnika.
Odległość analizowanej substancji zależy od polarności fazy ruchomej. Im polarność cząsteczek fazy ruchomej jest większa od polarności cząsteczek analizowanej substancji, tym łatwiej cząsteczki analizowanej substancji są wypierane ze startu do góry. Jeżeli faza ruchoma jest znacznie mniej polarna od analizowanej substancji to cząsteczki analizowanej substancji pozostają na starcie.
Wyszukiwarka
Podobne podstrony:
Typy połączeń nieorganicznych, Studia, Technologia żywności i żywienia człowieka, Chemia ogólna i ni
chem, Studia, Technologia żywności i żywienia człowieka, Chemia ogólna i nieorganiczna, Notatki
technologia pytania, żywienie człowieka i ocena żywności, semestr 4, technologia gastronomiczna
gewiś sprawko nastepne, Technologia Żywności
moje sprawko woda 1, Technologia Żywności, 2 i 3 rok TŻ
gewiś sprawko mikroskop, Technologia Żywności
sprawko15, POLITECHNIKA ŁÓDZKA, Technologia Żywności i Żywienia Człowieka, semestr 4, Chemia fizyczn
7[1].1(2), Technologia żywnosci i Żywienie człowieka, 2 semestr, chemia fizyczna, chemia fizyczna, s
SPRAWOZDANIE-4-1-1, Technologia żywnosci i Żywienie człowieka, 2 semestr, chemia fizyczna, chemia fi
10-1-gr-11-A, Technologia żywnosci i Żywienie człowieka, 2 semestr, chemia fizyczna, chemia fizyczna
127d879b364443a7c898e032e415ed88, Technologia żywnosci i Żywienie człowieka, 2 semestr, chemia organ
2015 pyt tren do wykł VII, Technologia żywnosci i Żywienie człowieka, 2 semestr, chemia fizyczna, ch
Zasady nazewnictwa wybranych klas zwi-zk-w organicznych, STUDIA PŁ, TECHNOLOGIA ŻYWNOŚCI I ŻYWIENIA
CHEMIA-ŻYWNOŚCI-sem.-IV, STUDIA PŁ, TECHNOLOGIA ŻYWNOŚCI I ŻYWIENIA CZŁOWIEKA, ROK II, SEM 4, Chemia
octan cykloheksylu, STUDIA PŁ, TECHNOLOGIA ŻYWNOŚCI I ŻYWIENIA CZŁOWIEKA, ROK II, SEM 4, Chemia orga
Numer i tytuł ćwiczenia, Technologia żywnosci i Żywienie człowieka, 2 semestr, chemia fizyczna, chem
ch fizyczna 13, POLITECHNIKA ŁÓDZKA, Technologia Żywności i Żywienia Człowieka, semestr 4, Chemia fi
FARMACJA2, STUDIA PŁ, TECHNOLOGIA ŻYWNOŚCI I ŻYWIENIA CZŁOWIEKA, ROK I, SEM 2, CHEMIA ANALITYCZNA I
więcej podobnych podstron