003 (53)
—J2L —
strukturalnym Ca3 [ Si04]0. Niektórzy badacze traktują krzemian trójwapniowy jako roztwór stały CaO w krzemianie^wuwapniowym Ca2 [ Si04] i przypisują mu wzór: Ca2 [ Si04]CaO lub Ca2 [ Si04(CaO)]
Niesymetryczne otoczenie atomów wapnia przez atomy tlenu (o czym świadczy rn.in. różna długość wiązania Ca - O, która waha się w przedziale 2,54 -r 3,24 A) powoduje, że z jednej strony atomy wapnia są odsłonięte.
Niesymetryczna koordynacja atomów tlenu wokół atomów wapnia, oraz obecność w strukturze krzemianu trójwapniowego luźniej wypełnionej atomami przestrzeni (swoistego rodzaju „pustki") przylegającej do odsłoniętej strony atomów wapnia, determinują jego właściwości (np. duża reaktywność do wody - dużej zdolności do reakcji z wodą).
BELIT - symbol - C2S - jest zmodyfikowanym przez szereg podstawień izomorficznych (3 (betta) - krzemianem dwu wapniowym.
Rodzaj i ilość obcych atomów w strukturze 2Ca0 Si02, z jednej strony, oraz sposób obróbki termicznej, a zwłaszcza sposób schładzania klinkieru, z drugiej strony, decyduje o formie krystalicznej belitu w klinkierze.
Krzemian dwuwapniowy będący wzorem krystalochemicznym dla fazy belitowej, występuje w czterech odmianach: a, a', P i y. p i y są odmianami niskotemperaturowymi występującymi w temperaturach naturalnych.
Wg Brediga diagram przemian polimorficznych C2S przedstawia się następująco:
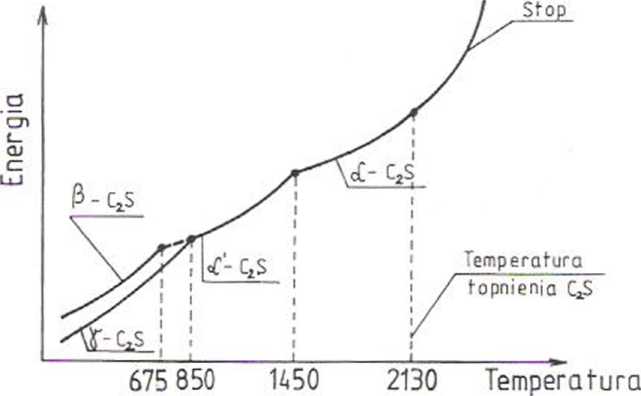
Z diagramu przemian polimorficznych wynika, że przy schładzaniu stopu następują następujące reakcje:
=> w temperaturze 2130°C krystalizuje ze stopu odmiana a , która w temperaturze 1450°C przechodzi łatwo i szybko w odmianę a';
=> w wyniku dalszego schładzania (powolnego) modyfikacja a' C2S przechodzi w temperaturze 850°C w niskotemperaturową trwałą odmianę y C2S;
Wyszukiwarka
Podobne podstrony:
strukturalnym Ca3 [ Si04]0. Niektórzy badacze traktują krzemian trójwapniowy jako roztwór stały CaO
IMG#25 Ponadto, niektórzy badacze skłonni są różnic oceniać wpływ nawet tego samego zespołu przyczyn
IMGt95 (3) Stary i notty świat niektórych badaczy, wzięła ona również udział w wydarzeniach odnotowa
wstęp do teorii polityki img 113 121 wellyna15. Niektórzy badacze dowodzili nawet, że Albert Einstei
le jest w dziejach utopii tematów trwałych. Tak wiele, że niektórzy badacze skłonni są mówić, że
CCF20120519�018 W preferowanym przez niektórych badaczy ekologiczny model klasy, zakładającym, że je
53 (289) Wprowadzenie teoretyczne 53 Inflacja strukturalna występuje wtedy, gdy producenci nie
Niektórzy badacze rozpoznali w tej ekspresyjnie przedstawionej postaci 7. okrytą płaszczem i hieraty
DSC02800 692 SCHIZOFRENIA I ZABURZENIE UROJENIOWE ści chorego. Zdaniem niektórych badaczy (Stem, Sil
71980 skanowanie0004 44 45 przetwarzania odebranego z zewnątrz sygnału, niektórzy badacz nazywają je
więcej podobnych podstron