Alkohole iюnole

2.6. Alkohole i fenole
benzenol. nie jest 3. Nazwy pochodni owej:
Otrzymywanie fenolu
Fenol na skalДҷ przemysЕӮowД… wydziela siДҷ ze smoЕӮy pogazowej lub otrzymuje z chlorobenzenu:
H;В°
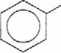
+ 2 NaOH
ci
p.l
ONa
+ Na Cl + 2 H,0
OH
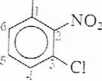
iloro-2-nitrofeno!
chlorobenzen fenolan sodu
Fenolan sodu przechodzi w fenol po ЕӮagodnym zakwaszeniu jego roztworu za pomocД… CO,: -ONa ^\^OH
-i- CO, + H,0 вҖ” f()l + NaHCO,

fenolan sodu
fenol
nej fenolu wyma-la pierЕӣcienia aro-rwiazanego z gru

вҖ”CHвҖ”CH-
! I вҖҳ
OH OH
|
PorГіwnywana cecha |
Alkohole |
Fenol |
|
Stan skupienia |
ciecze i ciaЕӮa staЕӮe |
ciaЕӮa staЕӮe |
|
RozpuszczalnoЕӣДҮ w wodzie |
metanol, etanol, glicerol i etanodiol mieszajД… siДҷ z w'odД… w kaЕјdych proporcjach; alkohole 0 wiДҷkszych i mniej polarnych czД…steczkach rozpuszczajД… siДҷ coraz sЕӮabiej |
w zimnej wodzie rozpuszcza siДҷ sЕӮabo, w gorД…cej nieco lepiej |
|
Dysocjacja w wodzie |
nie dysocjujД… |
dysocjuje, jest sЕӮabym kwasem Q,H5OH = CfiH50" + H+ |
|
Reakcja z zasadami |
nie reagujД… |
reaguje C(lHjOH + NaOH вҖ” CfiH5ONa + H20 |
|
Reakcja z sodem |
reagujД… 2 CHjOH + 2 Na вҖ” 2 CH,ONa + H- |
reaguje 2 C6H5OH + 2 Na вҖ” 2 C6H5ONa + H; |
|
Nitrowanie |
nie ulega |
ulega CH, OH OH 2O + 2HNO; - O +2H:0 NO, |
|
Eliminacja wody |
zachodzi A1,0; CHjвҖ”CH:OH вҖ” CH2=CH2 + H:0 |
nie zachodzi |
Alkoholany i fenolany
Alkoholany i fenolany sД… zwiД…zkami zaliczanymi do soli. Jako sole sЕӮabych kwasГіw ulegajД… w wodzie hydrolizie. Alkoholany sodowre lub potasowe powodujД… alkalizacjДҷ roztworu, gdyЕј sД… solami sЕӮabych kwasГіw' i mocnych zasad:
CH3ONa + H20 вҖ” CH3OH + NaOH CH3O- + H,0 вҖ” CH3OH + OH-

O
Wyszukiwarka
Podobne podstrony:
Picture 0 1X1 cd. tabeli Z.4 1 2 3 4 5 Alkohole i fenole silne pasma absorpcyjne dla wiД…zan
Uniwersytet JagielloЕ„ski, Collegium Medicum, Katedra Chemii Organicznej Grupa OH (alkohole, fenole,
Alkohole i fenole Cni pa funkcyjna Oli Alkohole zwiД…zki posiadajД…ce grupДҷ funkcyjna "z prawdziw
5 (1502) 4.3. Alkohole i fenole 97 maskujД…ca i neutralizujД…ca zapach potu i krwi, ktГіre dziaЕӮajД… na
6 (1368) 4.3. Alkohole i fenole 934.2.3. WДҷglowodory aromatyczne WДҷglowodory aromatyczne w przewaЕјaj
7 (1257) 4.3. Alkohole i fenole 99 mentol H,C OH CH3 or-terpineol a-Terpineol, trzeciorzДҷdowy alkoho
9 (1053) 4.3. Alkohole i fenole 101 Lanosterol wystДҷpuje w tЕӮuszczopocie weЕӮny owczej, okreЕӣlanym na
DSC05961 Absorpcja w podczerwieni tlenowych zwiД…zkГіw organicznych Alkohole I fenole Nowe pasma na wi
ВЈQ&QlVIMmВЈ-VЕӮAЕҡ.Cm.QЕҡC] ALKOHOLI 1 FENOLI Alkohole i fenole wykazujД… wiele podobieЕ„stw, np. sД…
Pochodne wДҷglowodorГіwZWIД„ZKI JEDNOFUNKCYJNE alkohole 1 fenole chlorowco pochodne R вҖ” OH
4-20 kj/mol Alkohole, fenole, aminy OddziaЕӮywania typu n - В« 4 - 40 kJ/mol ZwiД…zki
Alkohole i fenole Opracowanie: BartЕӮomiej SIEPSIAK klasa 3d Opiekun: p. Teresa GДҷbicka
PORГ“WNANIE WЕҒAЕҡCIWOЕҡCI ALKOHOLI I FENOLI Alkohole i fenole wykazujД… wiele podobieЕ„stw, np. sД…
PorГіwnanie wЕӮaЕӣciwoЕӣci alkoholi i?noli PorГіwnanie wЕӮaЕӣciwoЕӣci alkoholi i fenoli OgГіlna nazwa zwiД…z
wiДҷcej podobnych podstron