skanuj0013

Produktami rozpuszczania siarczków podgrupy B w alkaliach są głównie: siarkosole (tiosole) i "zwykłe" tlenosole. Jeżeli na Ą52S3 (lub SfoSO podziałamy roztworem silnej zasady (NaOH lub KOH), otrzymamy:
ĄS2S3 + 6 HO* Tt AsS33‘ + As033* + 3 H20
sUfkoanion
analogicznie dla Sn$?:
3 SnS2 + 6 HO' £ 2 SnS32' + Sn032- + 3 H20 (zamiast: Sn032“ + 3 H20 możemy zapisać hydroksokompleks [Sn(OH)6]2")
Rozpuszczając As?S< (lub §^§3) otrzymujemy:
As,S< + 6 HO' £ AsS43" + AsO,S3'+ 3 H20
sUrioanion tlenosiarkoanion
Pojawiają się tu dwa rodzaje siarkoanionów: siarkoarsenian(V) oraz arsenian(V), w którym dokonało się podstawienie jednego jonu O2' jonem S2". Zauważmy, że 4 jony As03S3 możemy traktować formalnie jako równoważne sumie : 3 As043 + AsS43‘.
Możemy zatem zapisać produkty- rozpuszczania jako sumę siarko- i „zwykłych’' tlenoanionów (bez udziału tlenosiarkoanionów).
Pod wpływem lekko zasadowego (NH^S, siarczki kwasowe tworzą siarkosole:
Ąs2Sj+3Sj- 2 2AsS,3'
ĄS2S5 + 3 S2“ H 2 AsS43'
Sn§2 + S2" SnS32"
Reakcją podobną, ale znacznie bardziej selektywną, jest działanie roztworem (NH^CO*
Ąs,St + 3 CO,2- ^ AsS,3" + AsOj3" + 3 C02t A&S, + 3 COj2- ^ AsS^ + AsOjS3' + 3 C02t
(NH4)2COj jest tak słabo zasadowy, że reaguje jedynie z siarczkami najsilniej kwasowymi czyli As(V) i As(III).
Zasadowość siarczku cyny (II) zmusza nas do użycia utleniacza, który upodobni zachowanie się SnS do pozostałych siarczków podgrupy B. Efektem ogrzewania w roztworze KOH z dodatkiem H202 jest reakcja:
3 SnS + 3 H202 + 6 HO' — SnS32' + 2 SnO,2" + 6 H20
3 SnS+12 HO" 2 SnSj2" + 2 Sn032" + 6 H20 + 6 e 1
H202 + 2 e 2
2 HO”
3
Przypominamy - w roztworach zasadowych, ale pozbawionych utleniacza, rozpuszczanie SnS nie zachodzi.
Inną drogą prowadzącą do rozdzielenia podgrup 2 grupy kationów, jest działanie nadmiarem roztworu (NH*)^ czyli disiarczku amonu. Odczynnik ten powstaje w reakcji wolnej siarki ze stężonym roztworem (NH4)2S:
T
(NH^S + S0 £ (NH4)2S2
Di-(lub dwu-)siarczek amonu, jest utleniaczem zdolnym do przeprowadzenia osadów: As?Si Sb?S>3 i SnS w odpowiednio As>Ss Sb?S< i SnS> Ponieważ w roztworach (NH,)2S2 znajduje się nadmiar (NH4)2S, utlenione siarczki podgrupy 2B przechodzą do roztworu jako siarkoaniony:
AsII!?Si + 2 S2”“ —* Asv?S< + 2 S2~ (redox)
ĄsjSj + ZS2" S
As->S< + 4 e
1
2
S22" + 2e 2 2S:
2
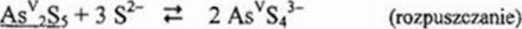
25
Wyszukiwarka
Podobne podstrony:
skanuj0013 (36) Produktami rozpuszczania siarczków podgrupy B w alkaliach są głównie: siarkosole (ti
skanuj0070 144 Resocjalizacja przestępców seksualnyclfl rodzinnej stosowane są głównie w dwóch przyp
skanuj0041 (Kopiowanie) rozpuszczalne w wodzie. Od reguły tej istnieją jednak odstępstwa, np. główny
skanuj0007 (41) 54 5.4. WPŁYW ŚRODOWISKA NA WYTRĄCANIE I ROZPUSZCZALNOŚĆ SIARCZKÓW METALI Odczy
41025 skanuj0011 mogą stanowić zagrożenie dla jakości produktu. Takimi punktami krytycznymi w drożdż
zdj 1 DIETETYKA WERSJA III 1. Źródłem węglowodanów w diecie są: y?h głównie produkty
KONCENTRATY KOLOROWE Koncentraty kolorowe POLI-CH® produkowane są głównie na nośnikach takich jak: P
r:KONCENTRATY KOLOROWE Koncentraty kolorowe POLI-CH® produkowane są głównie na nośnikach takich jak:
Nowy 3 a Zatrucia, pokarmowe wywołane przez rodzaj Salmonella przenoszone są głównie przez: a. produ
więcej podobnych podstron