Chemia pH str 8

45
[H4J = 0,0045

’kw
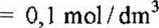
Ciw = 0,1 mol/dm3
PRZYKŁAD 10
Ile gramów NaOH należ}' użyć do sporządzenia 2 dmJ roztworu o pH=13?
pH = 13, to znaczy, że [H+] = 1013, czyli [OH-] = 10"1 =0,1 mol/dm3
NaOH jest mocną zasadą jednowodorotlenową, a więc zakładając całkowitą dysocjację, stężenie zasady w tym roztworze wynosi 0,1 mol/dm3
NaOH-> Na+ + OH'
0,1 mola 0,1 mola
1 dm3 roztworu zawiera 0,1 mola
2 dm3 roztworu zawierają 0,2 mola
1 mol NaOH--40 g
0,2 mola NaOH-x
x = 8 g NaOH
PRZYKŁAD 11
Obliczyć, ile gramów łŁS04 znajduje się w 300 cm3 roztworu o pH = 2, zakładając całkowitą dysocjację elektrolitu
pH = 2 to znaczy', że [H+] - 10'2 = 0,01 mol/dm3 kwas siarkowy jest kwasem dwuprotonowym
h2so.
» 2 H+ + SO4-
1 mol
x
2 mole 0,01 mola
x = 0,005 mol/dm3 H2S04
0,005 mola - 1 dm3
- 0,3 dm
x
Wyszukiwarka
Podobne podstrony:
Zadanie 101/YII Ile gramów NaOH należy dodać do 500 cm 31.2 N roztworu H3PO4, aby pH roztworu wynosi
Chemia pH str 1 38 a = n wynika, że stąd [OH ] = [NH4 ] = a • [NH4OH] = 0,0415 • 0,1 = 0,00415 b)(nr
Chemia pH str 2 39 Stała dysocjacji wody= IH*] [OH l = Przekształcając równanie i przyjmując, że stę
Chemia pH str 4 41 0,001 mol/dm HC1, który jest całkowicie zdysocjowany (a = 1, czyli HC1 -> H1
Chemia pH str 6 43 PRZYKŁAD 5 Obliczyć pH 0.02 mol/dni roztworu NaOH, przyjmując jego całkowitą dys
Chemia pH str 7 44 Dla zasad jednowodorotlenowych stężenie molowe anionów wodorotlenowycl jest równe
Chemia pH str 9 46 x = 0.0015 mola H2S04 znajduje się w 300 cm3 roztworu 1 mol H2S04 - 98 g 0,0015 m
Chemia pH str 3 40 Tabela 7 Skala pH pH [Hi [OH ] pOH Odczyn 0 10°=
Chemia pH str 5 1 42 W powyższym roztworze: :? [HI =0,042 pH = - (log 4,2 • lO 4) = - (log 4,2 /log
więcej podobnych podstron