skan0162 (2)
Roztwory i równowagi fazowe 165
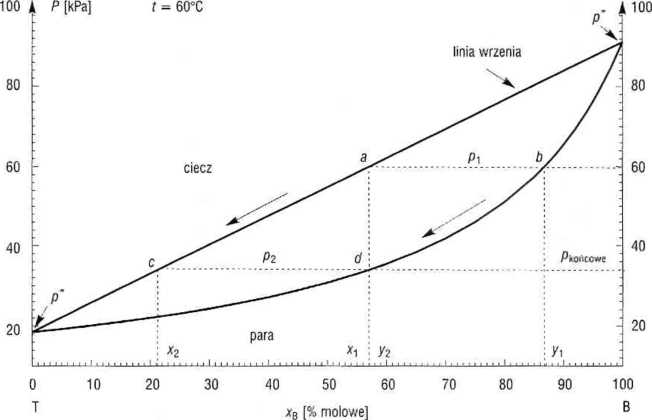
Rys. 4.17. Równowaga ciecz-para dla układu benzen (B) - toluen (T)
Skład roztworu wrzącego pod ciśnieniem p\ = 60 kPa w 60°C (punkt a na rys. 4.17) można wyznaczyć graficznie lub obliczyć z równania linii wrzenia:
Pi -Pt * * Pb ~Pt
60-18,52 91,23 - 18,52
= 0,5705 (57,05% molowych).
Ułamek molowy benzenu V| w parze, będącej w równowadze z tym roztworem (punkt b), można łatwo obliczyć:
= 0,8674.
91,23 • 0,5705 60
Para jest bogatsza w bardziej lotny składnik niż roztwór, będący z nią w równowadze, toteż, podczas odparowywania, roztwór wzbogaca się w składnik cięższy. Jego skład zmienia się wzdłuż linii a-c, natomiast para zmienia swńj skład wrzdłuż linii b-d (rys. 4.17). Układ jest zamknięty, jego skład sumaryczny nie ulega zmianie, toteż w momencie osiągnięcia przez parę takiego składu (punkt d), jaki miał roztwór wyjściowy, znika ostatnia kropla roztworu. Ciśnienie końcowe możemy obliczyć z równania linii skraplania, gdyż wówczas y2 = ,x1:
Pi =
_18,52_
1 -0,5705 • (1 - 18,52/91,23)
= 33,96 kPa.
Wyszukiwarka
Podobne podstrony:
Wykres równowagi ciecz- para dla układu toluen- heksan 0 punkty no krzywej cioczy
skan0144 (2) Roztwory i równowagi fazowe 147 Zależność przedstawiona na rys. 4.9,
skan0136 Roztwory i równowagi fazowe 139 Rys. 4.5. Wyznaczanie współczynnika aktywności metodą krios
skan0138 Roztwory i równowagi fazowe 141 Rys. 4.6. Dopasowanie wyników doświadczalnych metodą najmni
52643 skan0146 Roztwory i równowagi fazowe 149 Rys. 4.10. Cząstkowe objętości molowe NaCl (V2) i H20
skan0130 (2) Roztwory i równowagi fazowe 133 Dla roztworu o jc2 = 0,6 Gf1 = -3272,5 J • mol-1, G™ =
skan0164 (2) Roztwory i równowagi fazowe 167 wykreślić diagram destylacyjny mieszaniny benzenu i tol
skan0166 Roztwory i równowagi fazowe 169 x2 - dx2 = x2n —y2dn n - dn Zaniedbując iloczyn dx2dn ~ 0,
skan0170 (2) Roztwory i równowagi fazowe 173 mamy MC* AH° = AH°opni + (T- 7t więc otrzymane wyrażeni
skan0178 Roztwory i równowagi fazowe 181 v - 0 x-0 8-0 10-0=*y = 0,8 • *. Linia Sb przechodzi przez
skan0123 4. Roztwory i równowagi fazowe Roztworem nazywamy homogeniczną mieszaninę dwu lub więcej su
więcej podobnych podstron